|
|
(21), (22) Заявка: 2008129560/04, 17.07.2008
(24) Дата начала отсчета срока действия патента:
17.07.2008
(43) Дата публикации заявки: 27.01.2010
(46) Опубликовано: 27.06.2010
(56) Список документов, цитированных в отчете о
поиске:
HONDA T. et al. J. Med. Chem. 2004, v 47, p.4923-4932. SUH N. еt al. Cancer Res. 1999, v 59, p.336-341. ТОЛСТИКОВ Г.А., БАЛТИНА Л.А. и др. Солодка: биоразнообразие, химия, применение в медицине.: изд. «ГЕО», 2007, с.312.
Адрес для переписки:
630090, г.Новосибирск-90, пр. Ак. Лаврентьева, 9, НИОХ СО РАН, патентный отдел, Е.И. Витяевой
|
(72) Автор(ы):
Саломатина Оксана Владимировна (RU),
Салахутдинов Нариман Фаридович (RU),
Толстиков Генрих Александрович (RU),
Логашенко Евгения Борисовна (RU),
Зенкова Марина Аркадьевна (RU),
Власов Валентин Викторович (RU)
(73) Патентообладатель(и):
Новосибирский институт органической химии им. Н.Н. Ворожцова Сибирского отделения Российской академии наук (НИОХ СО РАН) (статус государственного учреждения) (RU),
Институт химической биологии и фундаментальной медицины Сибирского отделения Российской академии наук (ИХБиФМ СО РАН) (статус государственного учреждения) (RU)
|
(54) ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ТРИТЕРПЕНОВОЙ ПРИРОДЫ
(57) Реферат:
Изобретение относится к новому химическому соединению, а именно к метиловому эфиру 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты формулы (I):
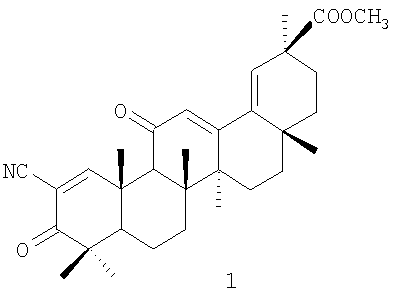
которое может быть использовано в медицине в качестве лекарственного средства, обладающего противоопухолевым действием. 1 табл., 3 ил.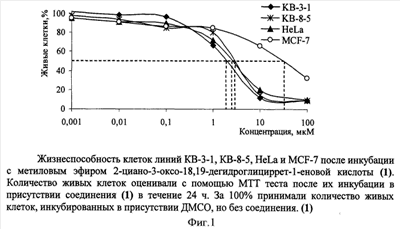
Изобретение относится к новому химическому соединению, а именно к метиловому эфиру 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты формулы (I):
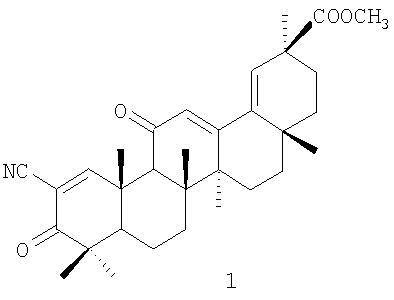
которое может быть использовано в медицине в качестве лекарственного средства, обладающего противоопухолевым действием.
Онкологические заболевания являются одной из основных проблем современной медицины, поскольку даже при благоприятном течении заболевания в большинстве случаев не удается достичь полного выздоровления пациента, существенно увеличить продолжительность и улучшить качество его жизни. Предлагаемые на данный момент схемы лечения различного типа злокачественных опухолей используют хирургические методы в комплексе в высокодозной агрессивной терапией, серьезным недостатком которой является высокая токсичность современных противоопухолевых препаратов в отношении жизненно-важных органов и систем организма. Сопутствующие побочные эффекты снижают эффективность, а в ряде случаев ограничивают применение противоопухолевых средств. Другой проблемой в лечении онкологических заболеваний является проблема остаточного опухолевого клона. Опухолевые клетки, пережившие химиотерапию, обычно проявляют лекарственную устойчивость к широкому кругу препаратов и вызывают рецидив заболевания в более тяжелой форме. В связи со всем вышесказанным, актуальной задачей является поиск новых противоопухолевых препаратов, обеспечивающих высокую избирательность и эффективность лечения.
Одним из важных направлений медицинской химии, позволяющим получать новые, эффективные противоопухолевые препараты, является использование синтетических трансформаций растительных метаболитов. Наиболее приемлемым считается исследование растительных метаболитов, о биологической активности которых имеются достоверные сведения и которые являются доступными в настоящее время или станут доступными в ближайшем будущем по мере формирования сырьевой базы. К данному классу соединений относятся тритерпеновые кислоты, широкий спектр биологической активности которых (противовоспалительная, противовирусная, противоопухолевая, иммуностимулирующая и т.д.) приковывает к ним пристальный интерес исследователей.
Задачей изобретения является создание нового эффективного, низкотоксичного лекарственного средства, обладающего противоопухолевым действием и получаемого из доступного растительного сырья.
Поставленная задача решается новым соединением тритерпеновой природы, а именно метиловым эфиром 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты формулы (1), которое может использоваться в качестве противоопухолевого средства.
50 10-6-10-950 ~10-650 1.1-3.0×10-6
Одним из таких доступных соединений с ярко выраженными физиологическими свойствами является 18 Н-глицирретовая кислота формулы (2) – агликон глицирризиновой кислоты – преобладающего гликозида корня солодки (~90% от общего количества тритерпеновых гликозидов). Н-глицирретовая кислота формулы (2) – агликон глицирризиновой кислоты – преобладающего гликозида корня солодки (~90% от общего количества тритерпеновых гликозидов).
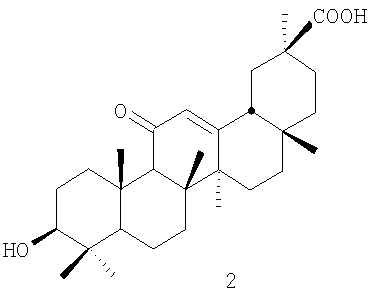
С химической точки зрения 18 Н-глицирретовая кислота необычна тем, что является единственным природным тритерпеном, содержащим карбонильную группу в 11-м положении [Толстиков Г.А., Балтина Л.А., Гранкина В.П., Кондратенко P.M., Толстикова Т.Г. Солодка: биоразнообразие, химия, применение в медицине. Новосибирск, Академическое издание «ГЕО», 2007, 312 с.]. Н-глицирретовая кислота необычна тем, что является единственным природным тритерпеном, содержащим карбонильную группу в 11-м положении [Толстиков Г.А., Балтина Л.А., Гранкина В.П., Кондратенко P.M., Толстикова Т.Г. Солодка: биоразнообразие, химия, применение в медицине. Новосибирск, Академическое издание «ГЕО», 2007, 312 с.].
Метиловый эфир 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты [метиловый эфир 11-циано-2,4а,6а,6b,9,9,12а-гептаметил-10,13-диоксо-2,3,4,4а,5,6,6а,6b,7,8,8а,9,10,12а,12b,13-гексадекагидропицен-2-оловой кислоты] формулы (1) был получен нами в результате комбинированной модификации колец А и Е 18 Н-глицирретовой кислоты формулы (2): Н-глицирретовой кислоты формулы (2):
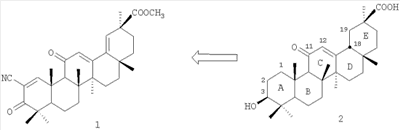
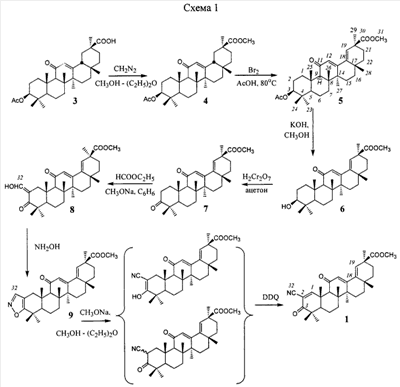
Модификацию проводили согласно схеме 1. В качестве исходного соединения был взят ацетат 18 Н-глицирретовой кислоты (3), полученный в результате дегликолизации глицирризиновой кислоты в уксусной кислоте [Толстиков Г.А. Синтетические исследования в области физиологически-активных высших терпеноидов и стероидов. Дис. работа д-ра хим. наук. Уфа. 1969]. Метиловый эфир ацетата 18 Н-глицирретовой кислоты (3), полученный в результате дегликолизации глицирризиновой кислоты в уксусной кислоте [Толстиков Г.А. Синтетические исследования в области физиологически-активных высших терпеноидов и стероидов. Дис. работа д-ра хим. наук. Уфа. 1969]. Метиловый эфир ацетата 18 Н-глицирретовой кислоты (4) получали взаимодействием соединения (3) с диазометаном. Первоначально при взаимодействии соединения (4) с бромом в уксусной кислоте при 80°С и в результате реакции бромирования – дегидробромирования получено соединение (5), содержащее 18,19-двойную связь в кольце Е. Таким образом, был сохранен 11-он-12-еновый фрагмент (уникальный для глицирретовой кислоты), а также удлинена система сопряжения кратных связей. Н-глицирретовой кислоты (4) получали взаимодействием соединения (3) с диазометаном. Первоначально при взаимодействии соединения (4) с бромом в уксусной кислоте при 80°С и в результате реакции бромирования – дегидробромирования получено соединение (5), содержащее 18,19-двойную связь в кольце Е. Таким образом, был сохранен 11-он-12-еновый фрагмент (уникальный для глицирретовой кислоты), а также удлинена система сопряжения кратных связей.
Следующим этапом являлось получение 2-циано-3-оксо-1-енового фрагмента в кольце А (схема 1). Гидроксильную группу окисляли в кетонную с образованием соединения (7). Производное изоксазола (9) получали формилированием соединения (7) с дальнейшей конденсацией с гидроксиламином. Расщепление изоксазольного кольца метилатом натрия с последующим окислением дихлоро-дицианохиноном (DDQ) приводит к соединению (1).
Элементный состав полученных веществ определяли из масс-спектров высокого разрешения, записанных на приборе DFS (Double Focusing Sector) фирмы Thermo Electron Corporation.
В работе использовался ацетат метилового эфира глицирретовой кислоты (3) 94%-ной чистоты (ВЭЖХ).
Спектры ЯМР 1Н и 13С регистрировали на спектрометрах АМ-400 (рабочие частоты 400.13 MHz для 1Н и 100.61 MHz для 13С) и DRX-500 (500.13 MHz и 125.76 MHz соответственно) фирмы Bruker для растворов веществ в CDCl3. В качестве внутреннего стандарта использовали сигналы растворителя ( H 7.24 и H 7.24 и  C 76.9 м.д). Строение полученных соединений устанавливали на основании анализа спектров ЯМР 1Н с привлечением спектров двойного резонанса 1Н-1Н, а также анализа спектров ЯМР 13С с использованием стандартных методик записи спектров в режиме J-модуляции (JMOD), с внерезонансным и селективным подавлением протонов, двумерных спектров гетероядерной 13С-1Н корреляции на прямых константах спин-спинового взаимодействия (С-Н COSY, 1JC,H 135 Гц) и двумерных и одномерных спектров гетероядерной 13С-1Н корреляции на дальних константах спин-спинового взаимодействия (COLOC, LRJMD, 2,3JC,H C 76.9 м.д). Строение полученных соединений устанавливали на основании анализа спектров ЯМР 1Н с привлечением спектров двойного резонанса 1Н-1Н, а также анализа спектров ЯМР 13С с использованием стандартных методик записи спектров в режиме J-модуляции (JMOD), с внерезонансным и селективным подавлением протонов, двумерных спектров гетероядерной 13С-1Н корреляции на прямых константах спин-спинового взаимодействия (С-Н COSY, 1JC,H 135 Гц) и двумерных и одномерных спектров гетероядерной 13С-1Н корреляции на дальних константах спин-спинового взаимодействия (COLOC, LRJMD, 2,3JC,H
Было исследовано влияние заявляемого метилового эфира 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1) на жизнеспособность клеток карциномных линий человека, клеток нейробластомы человека и опухолевых клеток почки эмбриона человека.
В результате было показано, что заявляемое соединение (1) проявляет высокую противоопухолевую активность по отношению ко всем использованным опухолевым клеточным культурам, включая карциномную линию клеток КВ-8-5, обладающую фенотипом множественной лекарственной устойчивости. При исследовании цитотоксичности соединения (1) по отношению к использованным опухолевым клеткам были получены значения IC50, концентрации соединения, при котором наблюдается гибель 50% клеток. Показано, что значения IC50 для соединения (1) имеют сходный порядок величины для всех опухолевых клеток и лежат в диапазоне от 50×10-6 (для линии клеток MCF-7) до 3×10-6 (для линии клеток КВ-3-1). Полученные данные по противоопухолевой активности соединения (1) позволяют рассматривать его как перспективный лекарственный агент.
Кроме того, при сравнении заявляемого соединения (1) с известным и широко испытываемым противоопухолевым агентом CDDO можно отметить следующее. При практически одинаковой противоопухолевой эффективности заявляемое соединение дешевле агента CDDO, так как 18 Н-глицерретовая кислота – исходный продукт при синтезе соединения (1) – является гораздо более доступным и более дешевым соединением по сравнению с олеанолорой кислотой, исходным соединением для синтеза CDDO (стоимость олеаноловой кислоты более чем в 60 раз превышает стоимость 18 Н-глицерретовая кислота – исходный продукт при синтезе соединения (1) – является гораздо более доступным и более дешевым соединением по сравнению с олеанолорой кислотой, исходным соединением для синтеза CDDO (стоимость олеаноловой кислоты более чем в 60 раз превышает стоимость 18 Н-глицерретовой кислоты). Н-глицерретовой кислоты).
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение ацетата метилового эфира 18 Н-глицирретовой кислоты (4) Н-глицирретовой кислоты (4)
К смеси ацетата 18рН-глицерретовой кислоты (3) (10 г, 19.0 ммоль) в 200 мл метанола при перемешивании прибавили эфирный раствор диазометана до тех пор, пока раствор не окрасился в бледно-желтый цвет. После полного разложения диазометана (исчезновения характерной окраски) растворитель отогнали на ротационном испарителе и полученный осадок перекристаллизовали из смеси метанол-хлороформ.
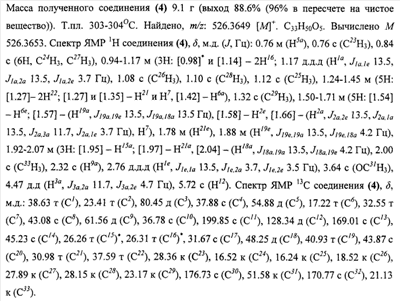
(*Здесь и далее: химические сдвиги (центры мультиплетов) атомов водорода, заключенные в квадратные скобки, получены из двумерных спектров 13С – 1Н корреляции на прямых константах ССВ
* Химические сдвиги, возможно, следует поменять местами.)
Пример 2. Получение ацетата метилового эфира 18,19-дегидроглицирретовой кислоты (5)
К раствору ацетата метилового эфира глицирретовой кислоты (4) (10.0 г, 19.0 ммоль) в ледяной уксусной кислоты (400 мл) при 80°С в течение 1 часа по каплям прибавляли 5%-ный раствор брома в ледяной уксусной кислоте (70.0 мл, 21,8 ммоль). Реакционную смесь выдерживали 1 час при той же температуре, охладили и вылили в 1.5 л холодной воды. Полученный осадок отфильтровали, промыли водой и сушили на воздухе. Перекристаллизацией из смеси метанол-хлороформ был получено 6.5 г продукта (5) (выход 65.3%). Т.пл. 244-247°С. Найдено, m/z: 524.3490 [М]+. C33H48O5.

Пример 3. Получение метилового эфира 18,19-дегидроглицирретовой кислоты (6)
Раствор ацетата метилового эфира 18,19-дегидроглицерретовой кислоты (5) (6.5 г, 12.4 ммоль) и КОН (45 г, 775.8 ммоль) в метаноле (650 мл) кипятили в течение 1 часа. Реакционную смесь охладили и отогнали большую часть метилового спирта на вакууме, затем добавили этилацетат (100 мл) и 5%-ный раствор соляной кислоты. Экстрагировали смесью хлороформ – этилацетат (1:4) (3×750 мл). Объединенный экстракт промывали раствором гидрокарбоната натрия (3х25 мл) и насыщенным раствором хлорида натрия (3×25 мл). Сушили сульфатом магния. Масса полученного продукта (6) 5.9 г (выход 98.7%). Для получения аналитически чистого образца 100 мг продукта перекристаллизовали из смеси метанол-хлороформ. Для дальнейших превращений продукт использовали без дополнительной очистки. Т.пл. 208-210°С.

Пример 4. Получение метилового эфира 3-оксо-18,19-дегидроглицирретовой кислоты (7)
К раствору метилового эфира 18,19-дегидроглицерретовой кислоты (6) (5.8 г, 12.0 ммоль) в ацетоне (400 мл) по каплям прибавляли 6 мл реагента Джонса (бихромат натрия в 33%-ой серной кислоте). Перемешивали 2.5 часа, затем добавили 50 мл этилового спирта и перемешивали еще 30 минут для разложения хромовой кислоты. Реакционную смесь упарили в вакууме до объема ~100-150 мл и вылили в воду (700 мл). Выпавший осадок отфильтровали и высушили на воздухе. Для очистки вещество растворяли в хлороформе и фильтровали через слой окиси алюминия. Масса полученного соединения (7) 5.2 г (выход 90.3%). Для получения аналитически чистого образца 100 мг продукта перекристаллизовали из смеси метанол-хлороформ. Для дальнейших превращений продукт использовали без дополнительной очистки. Т. пл.
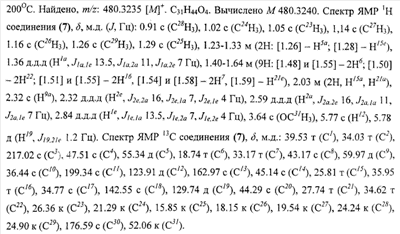
Пример 5. Получение метилового эфира 2-гидроксиметилен-3-оксо-18,19-дегидроглицерретовой кислоты (8)
К перемешиваемому раствору метилового эфира 3-оксо-18,19-дегидроглицерретовой кислоты (4.2 г, 8.8 ммоль), этилформиата (4 мл, 50.5 ммоль) в бензоле (32 мл) порциями прибавляли метилат натрия (3.0 г, 55.5 ммоль). Перемешивали 2 часа при комнатной температуре. Затем к реакционной смеси добавили бензол (50 мл) и 5%-ный раствор соляной кислоты. Экстрагировали этилацетатом (3×75 мл). Объединенный экстракт промывали раствором гидрокарбоната натрия (3×25 мл) и насыщенным раствором хлорида натрия (3×25 мл). Сушили сульфатом магния. Масса полученного продукта (8) 4.3 г (выход 96.7%). Для получения аналитически чистого образца 150 мг очищали колоночной хроматографией на силикагеле (элюент – гексан с градиентом этилацетата 10-15%). Для дальнейших превращений продукт использовали без дополнительной очистки.

Пример 6. Получение метилового эфира изоксазоло[4,5-b]-18,19-дегидроглицерретовой кислоты (9)
Смесь метилового эфира 2-гидроксиметилен-3-оксо-18,19-глицерретовой кислоты (4.2 г, 8.3 ммоль), этилового спирта (110 мл) и гидрохлорида гидроксиламина (5,8 г, 83.5 ммоль) в воде (11 мл) кипятили с обратным холодильником 2 часа. Реакционную смесь охладили, спирт удалили на ротационном испарителе, добавили воды, экстрагировали этилацетатом (2×100 мл). Объединенный экстракт промыли раствором гидрокарбоната натрия (3×25 мл) и насыщенным раствором хлорида натрия (3×25 мл), сушили сульфатом магния. Получили 4.0 г (выход 95.4%) производного изоксазола (9). Для получения аналитически чистого образца 100 мг очищали колоночной хроматографией на силикагеле (элюент – гексан с градиентом этилацетата 10-20%). Для дальнейших превращений продукт использовали без дополнительной очистки. Найдено, m/z:

Пример 7. Расщепление изоксазольного кольца в соединении (9)
К перемешиваемому раствору соединения (9) (3.9 г, 7.7 ммоль), диэтилового эфира (250 мл) и метанола (120 мл) при охлаждении на ледяной бане порциями прибавляли метилат натрия (15 г). Смесь перемешивали 1 ч при комнатной температуре. Затем добавили этилацетат и 5%-ный раствор соляной кислоты. Экстрагировали этилацетатом (2×50 мл). Объединенный экстракт промыли раствором гидрокарбоната натрия (3×25 мл) и насыщенным раствором хлорида натрия (3×25 мл), сушили сульфатом магния. Масса реакционной смеси (смесь таутомеров) 3.8 г (выход 97%). Для получения аналитически чистого образца 100 мг очищали колоночной хроматографией на силикагеле (элюент гексан с градиентом этилацетата 10-20%). Для дальнейших превращений продукт использовали без дополнительной очистки. Найдено, m/z:

Пример 8. Получение метилового эфира 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1)
Раствор смеси таутомеров (3.7 г, 7.3 ммоль) и 2,3-дихлоро-5,6-дициано-1,4-бензохинона (DDQ) (1.91 г, 8.4 ммоль) в бензоле (200 мл) кипятили с обратным холодильником 4 ч. Отфильтровали, фильтрат упарили. Колоночной хроматографией на силикагеле (элюент бензол с градиентом ацетона 0-10%) был получен кристаллический осадок. Перекристаллизацией последнего из смеси метанол-хлороформ был получен целевой продукт (1) массой 3.0 г (выход 84%). Т. пл. 214-217°С. Найдено, m/z 503.3025 [M]+. C32H43NO4. Вычислено М505.3181.

Пример 9. Влияние метилового эфира 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1) на жизнеспособность клеток карциномных линий человека
Клетки линии КВ-3-1 (эпидермоидная карцинома ротовой полости), КВ-8-5 (линия, производная КВ-3-1, обладающая фенотипом множественной лекарственной устойчивости), HeLa (эпителоидная карцинома шейки матки) и MCF-7 (аденокарцинома молочной железы) культивировали в среде IMDM, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина) и антимикотик амфотерицин (0.25 мкг/мл), в атмосфере 5%-ного CO2 при 37°С. Клетки линии КВ-8-5 культивировали в тех же условиях в присутствии 200 нМ винбластина.
Жизнеспособность клеток после инкубации с соединением (1) определяли с помощью МТТ теста, который основан на способности живых клеток превращать соединения на основе тетразола (МТТ) в ярко окрашенные кристаллы формазана, что позволяет спектрофотометрически оценивать количество живых клеток в препарате. Для этого клетки высаживали в 96-луночные планшеты (15000 клеток на лунку для линий КВ-3-1, КВ-8-5 и MCF-7, 7000 клеток на лунку для линии HeLa). Через 24 ч в лунках меняли среду и к клеткам добавляли 0.1 М раствор соединения (1) в ДМСО до конечной концентрации в среде от 10-4 до 10-9 М. Клетки инкубировали в присутствии соединения (1) еще в течение суток в тех же условиях. По окончании инкубации, без смены среды, к клеткам добавляли раствор МТТ (5 мг/мл) в фосфатно-солевом буфере до концентрации 0.5 мг/мл и инкубировали в течение 3 ч в тех же условиях. Среду удаляли, к клеткам добавляли по 100 мкл ДМСО, в котором происходит растворение образовавшихся в клетках кристаллов формазана и измеряли оптическую плотность на многоканальном спектрофотометре на длинах волн 570 и 630 нм, где А570 – поглощение формазана, а А630 – фон клеток.
Данные представляли в виде количества живых клеток относительно контроля. За 100% принимали количество клеток в контроле, где клетки инкубировали в течение 24 ч в отсутствие соединения, но в присутствии растворителя ДМСО (фиг.1). Из данных, приведенных на фиг.1 видно, что обработка клеток различных карциномных линий соединением (1) вызывает их эффективную гибель уже при концентрации соединения 10-6 М. Значения IC50 – концентрация соединения (1), при которой наблюдается гибель 50% клеток – приведены в таблице.
| Значения IC50 метилового эфира 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1) для различных карциномных линий клеток человека |
| Линия клеток |
IC50(1) |
| KB-3-1 |
3×10-6 М |
| KB-8-5 |
5×10-6 М |
| HeLa |
4.8×10-6 М |
| MCF-7 |
50×10-6M |
Пример 10. Влияние инкубации с метиловым эфиром 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1) на жизнеспособность клеток нейробластомы человека
Клетки линии SK-N-MC (нейробластома) культивировали в среде IMDM, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина) и антимикотик амфотерицин (0.25 мкг/мл), в атмосфере 5%-ного CO2 при 37°С.
Жизнеспособность клеток после инкубации с соединением определяли с помощью МТТ теста, как описано в примере 9. Для этого клетки высаживали в 96-луночные планшеты (30000 клеток на лунку). Далее, как в примере 9.
Данные представляли в виде количества живых клеток относительно контроля после их инкубации в присутствии соединения (1) в течение 24 ч. За 100% принимали количество клеток в контроле, где клетки инкубировали в отсутствие соединения, но в присутствии растворителя ДМСО (фиг.2). Из данных, приведенных на фиг.2 видно, что обработка клеток линии SK-N-MC соединением (1) вызывает их эффективную гибель уже при концентрации соединения 10-6 М, что подтверждает высокий противоопухолевый потенциал соединения (1). Значение IC50, полученное для данной клеточной линии, составило 5×10-6 М.
Пример 11. Влияние инкубации опухолевых клеток почки эмбриона человека с метиловым эфиром 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой кислоты (1) на их жизнеспособность
Клетки линии НЕК293 (почка эмбриона человека) культивировали в среде IMDM, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина) и антимикотик амфотерицин (0.25 мкг/мл), в атмосфере 5%-ного CO2 при 37°С.
Жизнеспособность клеток после инкубации с соединением определяли с помощью МТТ теста, как описано в примере 9. Для этого клетки высаживали в 96-луночные планшеты (20000 клеток на лунку). Далее как в примере 9.
Данные представляли в виде количества живых клеток относительно контроля после их инкубации в присутствии соединения (1) в течение 24 ч. За 100% принимали количество клеток в контроле, где клетки инкубировали в отсутствие соединения, но в присутствии растворителя ДМСО (фиг.3). Из данных, приведенных на фиг.3 видно, что обработка клеток линии НЕК293 соединением (1) вызывает их эффективную гибель при концентрации соединения выше 1×10-6 М, что свидетельствует о высоком противоопухолевом потенциале соединения (1). Значение IC50, полученное для данной клеточной линии, составило 5×10-6 М.
Формула изобретения
Метиловый эфир 2-циано-3-оксо-18,19-дегидроглициррет-1-еновой-кислоты формулы (1):
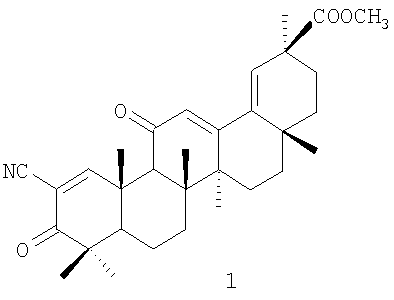
обладающий противоопухолевой активностью.
РИСУНКИ
|
|