|
|
(21), (22) Заявка: 2008136831/04, 12.09.2008
(24) Дата начала отсчета срока действия патента:
12.09.2008
(43) Дата публикации заявки: 20.03.2010
(46) Опубликовано: 27.06.2010
(56) Список документов, цитированных в отчете о
поиске:
Н.Takahana et al. Org. Biomol. Chem., 2006, v.4, p.1587-1595. RU 2167877 C2, 27.05.2001. RU 200334630 A, 27.05.2005. RU 2006100034 A, 27.08.2006. WO 0187886 A1, 22.11.2001.
Адрес для переписки:
197376, Санкт-Петербург, ул. Профессора Попова, 14, Санкт-Петербургская гос.химико-фармацевтическая академия (ГОУ ВПО СПХФА Росздрава), патентно-лицензионный отдел
|
(72) Автор(ы):
Петина Ольга Андреевна (RU),
Яковлев Игорь Павлович (RU),
Препьялов Александр Васильевич (RU),
Лалаев Борис Юрьевич (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования САНКТ-ПЕТЕРБУРГСКАЯ ГОСУДАРСТВЕННАЯ ХИМИКО-ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ (ГОУ ВПО СПХФА Росздрава) (RU)
|
(54) ЗАМЕЩЕННЫЕ 2Н,8Н-1,4-ДИОКСА-9b-АЗАФЕНАЛЕН-2,8-ДИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
Изобретение относится к новым индивидуальным соединениям класса периконденсированных гетероциклических систем – замещенным 2Н,8Н-1,4-диокса-9b-азафенален-2,8-дионам общей формулы I
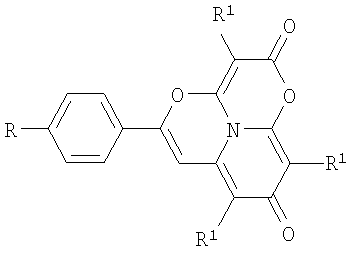
(I),где: R=H, R1=Me (Ia); Bu (1б); cHex (Iв); R=Cl, R1 – Me (Ir); R=Br, R1=Me (Iд), и способу их получения путем взаимодействия амидов арилпропиоловых кислот моноалкилзамещенных малонилдихлоридов в среде безводного неполярного органического растворителя при кипячении с последующим выделением целевого продукта. Соединения формулы 1 обладают противомикробной активностью, а также могут быть использованы для синтеза новых биологически активных производных. Минимальная ингибирующая концентрация соединения Iб на Е. coli и C.albicans составляет 1000 мкг/мл, а на St. aureus составляет 1 мкг/мл. 2 н.п. ф-лы,7 табл., 1 ил.
Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса периконденсированных гетероциклических систем – замещенным 2H,8H-1,4-диокса-9b-азафенален-2,8-дионам общей формулы I и способу их получения, которые могут быть использованы для синтеза новых биологически активных производных, а также в медицине.
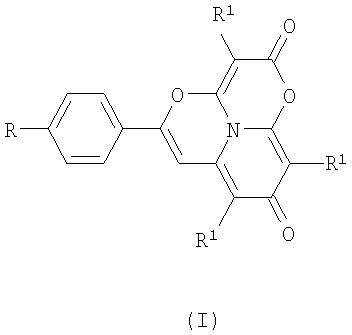 , ,
где
R=Н, R1=Me (Ia); Bu (Iб); сНех (Iв);
R=Cl, R1=Me (Iг);
R=Br, Rl=Me(Iд).
Известны соединения общей формулы II, включая их стереоизомеры, пролекарства и фармацевтически приемлемые соли или сольваты, с пери-конденсированной структурой, содержащие только азот в качестве гетероатома (не менее трех в системе) [Заявка  2003134630 на патент РФ, 7 МПК C07D 487/06. Антагонисты рецептора CRF]. 2003134630 на патент РФ, 7 МПК C07D 487/06. Антагонисты рецептора CRF].
Известны соединения формулы III или их фармацевтически приемлемые соли или эфиры [Заявка  2006100034 на патент РФ, 8 МПК C07D 487/06. Производные 1,3,4-триазафеналена и 1,3,4,6-тетраазафеналена]. 2006100034 на патент РФ, 8 МПК C07D 487/06. Производные 1,3,4-триазафеналена и 1,3,4,6-тетраазафеналена].
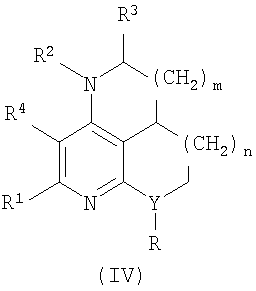
Известны соединения формулы IV, включая их стереоизомеры, пролекарства и фармацевтически приемлемые соли и сольваты, имеющие в периконденсированной системе не менее двух гетероатомов (только азот) [Заявка  2004104464 на патент РФ, 7 МПК C07D 471/16. Химические соединения]. 2004104464 на патент РФ, 7 МПК C07D 471/16. Химические соединения].
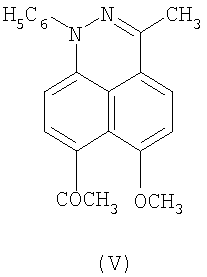
Известен диазафенален V [Пат.  2049090РФ, 6 МПК C07D 237/36. 7-ацетил-6-метокси-3-метил-1-фенил-1Н-1,2-диазафенален, обладающий гипотензивной активностью]. 2049090РФ, 6 МПК C07D 237/36. 7-ацетил-6-метокси-3-метил-1-фенил-1Н-1,2-диазафенален, обладающий гипотензивной активностью].
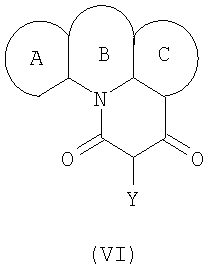
Известны дионы периконденсированных гетероциклических систем, обладающие низкой токсичностью и высокой противоопухолевой активностью VI [Пат  2167877, 7 МПК C07D 471/06, 2167877, 7 МПК C07D 471/06,  , 498/16. Производные конденсированных полициклических гетероциклических соединений и способ их получения; Pat. 5952335 US, Int. Cl. C07D 471/06, , 498/16. Производные конденсированных полициклических гетероциклических соединений и способ их получения; Pat. 5952335 US, Int. Cl. C07D 471/06,  , 498/06. Fused polycyclic heterocycle derivatives]. , 498/06. Fused polycyclic heterocycle derivatives].
Известны оксаазафеналены, содержащие кетогруппу VII [Pat. 6500839 US (WO 0187886). CRF receptor antagonists and methods relating thereto].
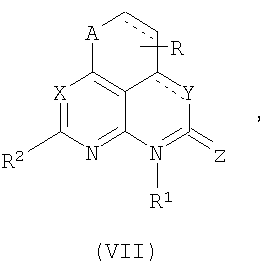 , ,
где может быть A=Y=O, Z=O.
Известны тетраазафеналены с центральным атомом азота и способы их получения VIII [Pat. 966251 GB. Novel Polycyclic Nitrogen-Containing Compounds; Pat. 3112314 US. Certain 1,4,7,9b-tetraazaphenalenes and preparation thereof; Pat. 3112315 US. Production of dodecahydro-1,4,7,9b-tetraazaphenalenes].
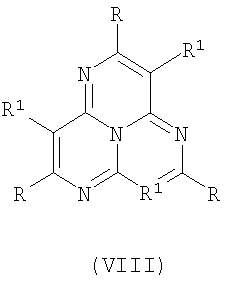
Известно, что вещества с азафеналеновой структурой представляют собой обширный класс алкалоидов, которые обладают самой разнообразной физиологической активностью [Eberhard Breitmaier. Alkaloide. Vieweg+Teubner Verlag, 2002, 192 с.].
Изучение способов синтеза структур, близких по строению к алкалоидам, представляет большой интерес вследствие их высокой биологической активности, сложности строения, а также в связи с тем, что эти соединения могут быть исходными продуктами для получения лекарственных препаратов.
Наиболее близкой по строению к синтезированному нами веществу является структура (-)-порантеридина, алкалоида, выделенного из растения Poranthera corymbosa семейства Молочайные (Euphorbiaceae).
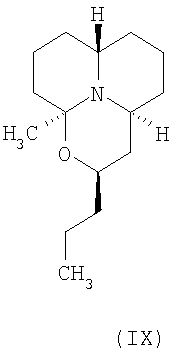
Описан способ получения данного алкалоида [Takahana, H. A new route to trans-2,6-disubtituted piperidine-related alkaloids using a novel С22-симметричного 2,6-диаллилпиридинкарбоновой кислоты по общей схеме:
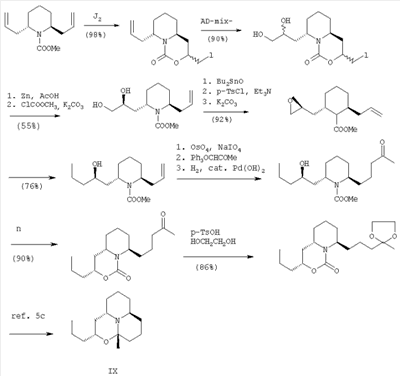
К недостаткам данного способа относятся сложность, многостадийность и вообще невозможность получения замещенных 2H,8H-1,4-диокса-9b-азафенален-2,8-дионов.
Задачей предполагаемой группы изобретений является синтез новых неописанных в литературе соединений, близких к алкалоидам с периконденсированными гетероциклическими структурами, потенциально обладающих биологической активностью, раскрытие технологических возможностей получения таких соединений.
Техническими результатами, на решение которых направлена группа изобретений, являются получение нового класса соединений – замещенных 2H,8H-1,4-диокса-9b-азафенален-2,8-дионов общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например, в качестве антимикробных средств; разработка простого способа их получения.
Поставленная задача осуществляется путем взаимодействия амида арилпропиоловой кислоты с моноалкилзамещенным малонилдихлоридом в соотношении 1:3 при температуре кипения в среде безводного неполярного органического растворителя с последующим выделением целевого продукта по схеме:
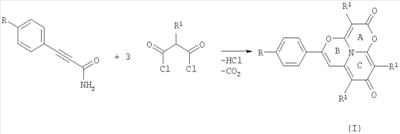 , ,
где
R=H, R1=Me (a); Bu (б); сНех(в);
R=n-Cl, R1=Me (г);
R=n-Вr, R1=Ме (д).
Из патентной и научно-технической литературы не выявлены способы синтеза новых заявляемых авторами соединений, и сами соединения.
Способ получения замещенных 2H,8H-1,4-диокса-9b-азафенален-2,8-дионов изучен и проведен в лабораторных условиях на стандартном товарном сырье.
Данные элементного анализа приведены в табл.1, выходы продуктов реакций, температуры плавления и величины Rf приведены в табл.2, спектральные характеристики полученных соединений сведены в табл.3 и 4.
Предполагаемая группа изобретений иллюстрирована чертежом и примерами практического осуществления.
На чертеже – общий вид молекулы 3,7,9-триметил-5-фенил-2H,8H-1,4-диокса-9b-азафенален-2,8-диона (Iа).
Пример 1. 3,7,9-триметил-5-фенил-2H,8H-1,4-диокса-9b-азафенален-2,8-дион (Iа).
В круглодонную колбу емкостью 100 мл загружают 1,0 г (0,007 моль) амида фенилпропиоловой кислоты и 40 мл безводного дихлорэтана в качестве среды (амид фенилпропиоловой кислоты растворяется полностью), а затем добавляют 2,3 мл (0,021 моль) метилмалонилдихлорида.
Реакционную смесь нагревают, через 30 минут в осадок выпадает кристаллический продукт. После 4-часового кипячения (84°С) реакционную массу охлаждают и выпавший твердый осадок отфильтровывают. Продукт представляет собой сухой остаток ярко-желтого цвета.
Затем осадок дважды перекристаллизовывают из ДМФА, промывают диэтиловым эфиром и сушат при комнатной температуре.
Перекристаллизованный продукт бледно-желтого цвета составляет 2 г, 90,5% от теоретического из расчета на амид фенилпропиоловой кислоты. Температура плавления >300°С. Хроматографическая однородность целевого продукта подтверждалась хроматографированием раствора его в ацетоне в системе этилацетата. Rf=0,57. Состав синтезированного соединения подтвержден элементным анализом. Брутто-формула: C19H154
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С, УФ-, ИК-масс-спектроскопией, а также с помощью рентгеноструктурного анализа.
В ИК спектрах вещества (таблетки КВr) наиболее характеристической является область 1800-1650 см-1, где наблюдаются полосы поглощения, соответствующие валентным колебаниям циклической сложноэфирной карбонильной группы (1750 см-1) и циклической карбонильной группы (1660 см-1). Полосы поглощения в области 1980-2780 см-1 относятся к колебаниям связей С-Н метильных групп, деформационные колебания этих связей находятся в диапазоне 1400-1380 см-1. В области 1620-1500 см-1 присутствуют полосы валентных колебаний ароматической системы, колебания С-Н связей бензольного кольца и азафеналенового цикла находятся в диапазоне 3100-3000 см-1.
УФ-спектр 3,7,9-триметил-5-фенил-2H,8H-1,4-диокса-9b-азафенален-2,8-диона в ацетонитриле имеет 2 максимума поглощения в области длин волн 251 и 316 нм.
В спектре ЯМР 1Н полученного соединения в дейтерированном ДМСО присутствуют сигналы протонов бензольного кольца ( 7.95 2Н; 7.95 2Н;  7.54 3Н), протона азафеналенового цикла при углероде С6 ( 7.54 3Н), протона азафеналенового цикла при углероде С6 ( 7.12 1Н) и протонов трех метильных групп ( 7.12 1Н) и протонов трех метильных групп ( 2.07 3Н; 2.07 3Н;  1.94 3Н; 1.94 3Н;  1.86 3Н). 1.86 3Н).
Спектр ЯМР 13С этого соединения характеризуется сигналами атомов углерода бензольного кольца ( 125,38-130,84 м.д.), азафеналенового цикла ( 125,38-130,84 м.д.), азафеналенового цикла ( 95,96; 108,5; 110,57; 133,82; 140,03; 145,75; 153,85; 157,92; 167,26 м.д.) и метильных групп ( 95,96; 108,5; 110,57; 133,82; 140,03; 145,75; 153,85; 157,92; 167,26 м.д.) и метильных групп ( 9,10-11,09 м.д.). 9,10-11,09 м.д.).
Также строение полученного вещества было доказано с помощью масс-спектра. Рассчитанная молекулярная масса полностью совпала с экспериментально найденной (M+=321).
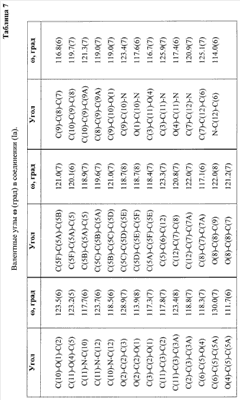
Гетероциклический скелет был однозначно установлен на основании данных рентгеноструктурного анализа. На чертеже видно, что трициклическая азафеналеновая система почти планарна. Двугранный угол между плоскостями А и В циклов составляет 2,0 град., циклов В и С – 2,8 град., а А и С – 3,6 град. Все заместители находятся практически в плоскости цикла – их отклонения не превышают 0,06 град. Бензольное кольцо также находится фактически в плоскости азафеналенового цикла – двугранный угол между плоскостями азафеналенового цикла и бензольного кольца равен 7,0 град. Координаты базисных атомов приведены в таблице 5, длины связей и валентные углы – в таблице 6 и 7 соответственно.
Пример 2. 3,7,9-трициклогексил-5-фенил-2H,8H-1,4-диокса-9b-азафенален-2,8-дион (Iв).
В круглодонную колбу емкостью 100 мл загружают 1,0 г (0,007 моль) амида фенилпропиоловой кислоты, 4,1 мл (0,021 моль) циклогексилмалонилдихлорида и 40 мл безводного дихлорэтана в качестве среды. Реакционную смесь нагревают при температуре кипения растворителя в течение 3 часов. При этом амид фенилпропиоловой кислоты растворяется полностью даже без нагревания. После 3-часового нагревания реакционную смесь охлаждают и растворитель отгоняют. Затем осадок дважды перекристаллизовывают из ацетонитрила, промывают диэтиловым эфиром и сушат при комнатной температуре.
Перекристаллизованный продукт бледно-желтого цвета составляет 2,8 г, 78,4% от теоретического из расчета на амид фенилпропиоловой кислоты.
Пример 3. 3,7,9-триметил-5-(n-хлорфенил)-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион (Iг).
В круглодонную колбу емкостью 100 мл загружают 1,0 г (0,006 моль) амида n-хлорфенилпропиоловой кислоты, 2,1 мл (0,018 моль) метилмалонилдихлорида и 40 мл безводного бензола в качестве среды. Реакционную смесь кипятят. При этом амид n-хлорфенилпропиоловой кислоты растворяется полностью даже без нагревания, затем через 20 минут в осадок выпадает кристаллический продукт. Осадок отфильтровывают. Сухой остаток ярко-желтого цвета составляет 1,0 г. Затем осадок дважды перекристаллизовывают из ДМФА, промывают диэтиловым эфиром и сушат при комнатной температуре. Перекристаллизованный продукт бледно-желтого цвета составляет 0,85 г, 42,7% от теоретического из расчета на амид n-хлорфенилпропиоловой кислоты.
Пример 4. 3,7,9-триметил-5-(n-хлорфенил)-2H,8H-1,4-диокса-9b-азафенален-2,8-дион (Iг).
В круглодонную колбу емкостью 100 мл загружают 1,0 г (0,006 моль) амида n-хлорфенилпропиоловой кислоты, 2,1 мл (0,018 моль) метилмалонилдихлорида и 40 мл безводного бензола в качестве среды. После 4-часового кипячения реакционную смесь охлаждают и выпавший твердый осадок отфильтровывают. Сухой остаток ярко-желтого цвета составляет 1,8 г. Затем осадок дважды перекристаллизовывают из ДМФА, промывают диэтиловым эфиром и сушат при комнатной температуре. Перекристаллизованный продукт бледно-желтого цвета составляет 1,6 г, 81,6% от теоретического из расчета на амид n-хлорфенилпропиоловой кислоты.
Пример 5. 3,7,9-триметил-5-(n-бромфенил)-2H,8H-1,4-диокса-9b-азафенален-2,8-дион (Iд).
В круглодонную колбу емкостью 100 мл загружают 1,0 г (0,0045 моль) амида n-бромфенилпропиоловой кислоты, 1,5 мл (0,014 моль) метилмалонилдихлорида и 40 мл безводного хлороформа в качестве среды. Реакционную смесь кипятят течение 4 часов. Затем реакционную массу охлаждают и выпавший твердый осадок отфильтровывают. Сухой остаток оранжевого цвета составляет 1,7 г. Затем осадок дважды перекристаллизовывают из ДМФА, промывают диэтиловым эфиром и сушат при комнатной температуре. Перекристаллизованный продукт желтого цвета составляет 1,4 г, 75,4% от теоретического из расчета на амид n-бромфенилпропиоловой кислоты.
Пример 6. На примере соединения Iб проверена антимикробная активность. Определение минимально ингибирующих концентраций (МИК) проводили методом серийных разведений в мясопептонном бульоне в отношении тест-культур микроорганизмов Staphylococcus aureus (штамм 209-Р), Escherichia coli (штамм 1257), Candida albicans (штамм АТСС 885-635), рекомендованных Государственной Фармакопеей [Государственная Фармакопея СССР. Вып.2. Общие методы анализа. Лекарственное растительное сырье / МЗ СССР – 11 изд. доп. – М.: Медицина, 1989. 400 с.]. Исследуемые соединения не растворяются в воде, поэтому в качестве растворителя использовали 20%-ный раствор ДМСО, не подавляющий роста ни одной из использованных тест-культур в условиях эксперимента. Минимальная ингибирующая концентрация соединения 16 на Е. coli и С.albicans составляет 1000 мкг/мл, а на St. aureus составляет 1 мкг/мл, что находится на уровне широко используемых на практике антибиотиков (эдицин – 10-20 мкг/мл, ванкомицин и тейкопланин – 0,3-12,5 мкг/мл).
Получены новые соединения – замещенные 2Н,8Н-1,4-диокса-9b-азафенален-2,8-дионы общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например, в качестве антимикробных средств. Разработан простой одноэтапный способ их синтеза с высоким выходом. Способ занимает мало времени, не требует дорогого оборудования, основан на использовании доступного дешевого сырья.
| Таблица 1 |
| Данные элементного анализа соединений (Iа-д) |
 |
Найдено, % |
Формула |
Вычислено, % |
 |
С |
Н |
N |
0 |
другие |
 |
С |
Н |
N |
0 |
другие |
| Iа |
72,3 |
4,65 |
4,57 |
18,75 |
– |
C19H15NO4 |
71,02 |
4,71 |
4,36 |
19,92 |
– |
| Iб |
74,93 |
7,58 |
3,50 |
13,99 |
– |
С28Н33NO4 |
75,14 |
7,43 |
3,13 |
14,30 |
– |
| Iв |
78,50 |
7,09 |
2,96 |
11,45 |
– |
С34Н39NO4 |
77,68 |
7,48 |
2,66 |
12,17 |
– |
| Iг |
63,78 |
4,01 |
3,63 |
18,56 |
10,7(Сl) |
C19H14ClNO4 |
64,14 |
3,97 |
3,94 |
17,99 |
9,97 (Сl) |
| Iд |
57,53 |
3,23 |
3,40 |
16,17 |
19,67(Br) |
C19H14BrNO4 |
57,02 |
3,53 |
3,50 |
15,99 |
19,96(Br) |
| Таблица 2 |
| Температуры плавления, выходы, значения Rf соединений (Iа-д) |
 |
R |
R1 |
Т.пл., °С |
Выход, % |
Rf a a |
| Iа |
Н |
Me |
>300 |
90,5 |
0,57 |
| Iб |
Н |
Bu |
154-156 с разл. |
80,5 |
0,18 |
| Iв |
Н |
cHex |
148-150 |
78,4 |
0,90 |
| Iг |
Сl |
Me |
>300 |
81,6 |
0,50 |
| Iд |
Вr |
Me |
>300 |
75,4 |
0,55 |
| Таблица 3 |
| ЯМР 1Н, УФ, ИК спектры соединений (Iа-д) |
 |
Спектр ЯМР 1Н (ДМСО-d6),  , м.д. , м.д. |
УФ спектр,  макс, нм макс, нм |
ИК спектр,  , см-1 , см-1 |
| Н6 |
Ph |
R1 |
C8=O |
C2=O |
R1 |
| Iа |
7.12(1Н) |
7.54(3Н); 7.95(2Н) |
2.07 (3Н); 1.94(3Н); 1.86(3Н) |
251 и 316 |
1750 |
1660 |
2940-2780 |
| Iб |
6.99(1Н) |
7.50(3Н); 7.90(2Н) |
0.75-2.72 (27Н) |
225,251 и 393 |
1760 |
1670 |
2820-3000 |
| Iв |
7.08(1Н) |
7.63(3Н); 7.96(2Н) |
1.25-2.06 (33Н) |
269 и 348 |
1750 |
1665 |
2830-3050 |
| Iг1 |
6.88(1Н) |
7.42(2Н); 7.65(2Н) |
2.09(3Н): 2.22(3Н): 2.30(3Н) |
259,5 и 317 |
1755 |
1660 |
2840-3000 |
| Iд1 |
6.89(1Н) |
7.60-7.61 (4Н) |
2.13(3Н); 2.20(3Н); 2.26(3Н) |
262,5 и 317 |
1765 |
1665 |
2900-3050 |
| 1СF3СООD |
| Таблица 4 |
Спектры ЯМР 13С ( C, м. д.) растворов соединений (Iа-д) в ДМСО-d6. C, м. д.) растворов соединений (Iа-д) в ДМСО-d6. |
 |
Азафеналеновый цикл |
R1 |
Ph |
| 1а |
95,96; 108,5; 110,57; 133,82; 140,03; 145,75; 153,85; 157,92; 167,26 |
9,10-11,09 |
125,38-130,84 |
| 16 |
95,73; 113,09; 115,73; 134,27; 140,09; 145,16; 154,16; 157,58; 167,07 |
13,82-32,04 |
125,29-130,95 |
| 1в |
95,65; 105,51; 118,15; 133,03; 141,10; 145,27; 155,13; 157,69; 166,34 |
25,76-34,79 |
126,34-131,90 |
| 1 г2 |
95,83; 106,34; 112,30; 133,52; 140,05; 145,59; 154,02; 157,83; 167,15 |
9,15-11,59 |
125,25-130,78 |
| 1д1 |
95,83; 110,03; 115,36; 133,28; 140,11; 145,84; 154,13; 157,94; 167,96 |
9,20-11,21 |
125,37-130,59 |
| 2CF3COOD |
| Таблица 5 |
| Координаты базисных атомов (*104) в структуре 3,7,9-триметил-5-фенил-2H,8H-1,4-диокса-9b-азафенален-2,8-диона (Iа) |
| Атом |
x |
у |
z |
U(eq) |
| O(1) |
9158(6) |
2452(5) |
-687(3) |
48(2) |
| O(4) |
6540(5) |
5445(5) |
-567(3) |
48(2) |
| O(8) |
11915(6) |
2894(6) |
2307(3) |
63(2) |
| O(2) |
7802(7) |
2040(6) |
-2048(3) |
75(2) |
| N |
8575(6) |
4126(5) |
139(3) |
33(2) |
| С(2) |
7942(8) |
2753(9) |
-1435(4) |
50(2) |
| С(3) |
7059(9) |
3806(8) |
-1374(4) |
45(2) |
| С(3А) |
5769(9) |
4172(8) |
-2161(4) |
64(3) |
| С(5) |
6706(8) |
6120(7) |
201(4) |
36(2) |
| С(5А) |
5514(8) |
7104(7) |
75(4) |
35(2) |
| С(5В) |
4370(8) |
7144(7) |
-717(4) |
39(2) |
| С(5С) |
3254(9) |
8023(8) |
-838(4) |
48(2) |
| C(5D) |
3246(8) |
8858(7) |
-178(5) |
47(2) |
| С(5Е) |
4406(9) |
8808(8) |
611(5) |
53(2) |
| C(5F) |
5554(9) |
7935(7) |
744(4) |
44(2) |
| С(6) |
7823(8) |
5797(7) |
920(4) |
36(2) |
| С(7) |
9968(8) |
4377(7) |
1668(4) |
40(2) |
| С(7А) |
10265(9) |
5022(7) |
2554(5) |
57(3) |
| С(8) |
10899(8) |
3278(8) |
1635(4) |
44(2) |
| С(9) |
10584(8) |
2649(7) |
797(5) |
42(2) |
| С(9А) |
11521(9) |
1512(8) |
723(5) |
55(2) |
| С(10) |
9471(8) |
3085(7) |
102(4) |
37(2) |
| С(11) |
7416(8) |
4431(7) |
-610(4) |
36(2) |
| С(12) |
8842(8) |
4754(7) |
948(4) |
31(2) |
| Таблица 6 |
| Длины связей d (Å) в молекуле соединения (Iа) |
| Связь |
d, Å |
Связь |
d, Å |
| O(1)-С(10) |
1.378(8) |
C(5A)-C(5F) |
1.375(9) |
| O(1)-С(2) |
1.406(8) |
C(5A)-C(5B) |
1.382(9) |
| O(4)-С(11) |
1.360(8) |
C(5B)-C(5C) |
1.371(10) |
| O(4)-С(5) |
1.391(8) |
C(5C)-C(5D) |
1.376(10) |
| O(8)-С(8) |
1.257(8) |
C(5D)-C(5E) |
1.388(10) |
| O(2)-С(2) |
1.207(8) |
C(5E)-C(5F) |
1.387(10) |
| N-C(11) |
1.380(8) |
C(6)-C(12) |
1.447(10) |
| N-C(I0) |
1.391(9) |
C(7)-C(12) |
1.353(9) |
| N-C(12) |
1.408(8) |
C(7)-C(8) |
1.457(10) |
| С(2)-С(3) |
1.403(10) |
C(7)-C(7A) |
1.522(9) |
| С(3)-С(11) |
1.334(9) |
C(8)-C(9) |
1.444(10) |
| С(3)-С(3А) |
1.497(10) |
C(9)-C(10) |
1.343(10) |
| С(5)-С(6) |
1.334(9) |
C(9)-C(9A) |
1.509(10) |
| С(5)-С(5А) |
1.495(10) |
 |
 |
Формула изобретения
1. Замещенные 2Н,8Н-1,4-диокса-9b-азафенален-2,8-дионы общей формулы I

(I),
где R=H, R1=Me (Ia – 3,7,9-триметил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=H, R1=Bu (Iб – 3,7,9-трибутил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=H, R1=cHex (Iв – 3,7,9-трициклогексил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=Cl, R1=Me (Iг – 3,7,9-триметил-5-(n-хлорфенил)-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=Br, R1=Me (Iд – 3,7,9-триметил-5-(n-бромфенил)-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион).
2. Способ получения замещенных 2Н,8Н-1,4-диокса-9b-азафенален-2,8-дионов общей формулы I

(I),
где R=H, R1=Me (Ia – 3,7,9-триметил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=H, R1=Bu (Iб – 3,7,9-трибутил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=H, R1=cHex (Iв – 3,7,9-трициклогексил-5-фенил-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=Cl, R1=Me (Iг – 3,7,9-триметил-5-(n-хлорфенил)-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион);
R=Br, R1=Me (Iд – 3,7,9-триметил-5-(n-бромфенил)-2Н,8Н-1,4-диокса-9b-азафенален-2,8-дион),
заключающийся в том, что амид арилпропиоловой кислоты подвергают взаимодействию с моноалкилзамещенным малонилдихлоридом, взятыми в соотношении 1:3, при кипячении в среде безводного неполярного органического растворителя с последующим выделением целевого продукта.
РИСУНКИ
|
|