|
|
(21), (22) Заявка: 2008144678/14, 13.11.2008
(24) Дата начала отсчета срока действия патента:
13.11.2008
(46) Опубликовано: 27.06.2010
(56) Список документов, цитированных в отчете о
поиске:
RU 2234318 C2, 20.08.2004. RU 2166947 C1, 20.05.2001. WO 0173132 A1, 04.10.2001. ВИНСКАЯ Е.П. Полирадиомодификация, метронидазол и гипертермия при радиотерапии местнораспространенных форм рака прямой кишки. VIII Съезд онкологов УССР. 1990, с.421-422. MACDONALD J.S. et al. Chemoradiotherapy after surgery compared with surgery alone foradenocarcinoma of the stomach or gastroesophageal junction. N. Engi. J. Med. 2001, Sep 6; 345(10), pp.725-730.
Адрес для переписки:
123001, Москва, а/я 66, А.К. Кирбаю
|
(72) Автор(ы):
Кожушков Андрей Иванович (RU),
Вёрткин Аркадий Львович (RU),
Барсуков Юрий Андреевич (RU),
Малихов Андрей Геннадьевич (RU)
(73) Патентообладатель(и):
Кожушков Андрей Иванович (RU)
|
(54) СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ РЕЦИДИВИРОВАНИЯ И МЕТАСТАЗИРОВАНИЯ РАКА
(57) Реферат:
Изобретение относится к медицине, в частности к онкологии, и касается лечения и профилактики рецидивирования и метастазирования опухолей, содержащих рецепторы половых гормонов. Для этого осуществляют забор биопсийного материала опухоли и определяют наличие андрогенных и эстрогенных рецепторов. Затем определяют уровень половых гормонов, на основании чего добиваются развития гиперандрогении путем введения в организм гормонального препарата. После этого осуществляют воздействие на опухоль путем проведения дистанционной гамма-терапии РОД-25 Гр или РОД-40 Гр. Далее при наличии в предварительно взятом биопсийном материале опухоли эстрогенных рецепторов добиваются достижения в организме больного постоянной андрогенизации, а при наличии в биопсийном материале опухоли андрогенных рецепторов – эстрогенизации. Способ обеспечивает увеличение лечебного эффекта при подавлении роста и метастазирования опухоли, вплоть до ее регрессии, при снижении побочных явлений и противопоказаний к лечению. 2 з.п. ф-лы, 2 табл., 1 ил.
Изобретение относится к области медицины, а более конкретно к способам комбинированной терапии злокачественных опухолей, и может быть использовано при лечении и профилактике онкологических заболеваний.
Известен способ комбинированного лечения рака, включающий локальную радиомодификацию клеток опухоли с последующей лучевой терапией и проведением радикальной операции, характеризующийся тем, что локальную радиомодификацию осуществляют путем эндоваскулярной перфузии ее ткани 5%-ным раствором метронидазола через верхнюю ректальную артерию при верхнеампулярном раке прямой кишки, верхнюю ректальную и одну из внутренних подвздошных артерий при средне- и нижнеампулярном раке прямой кишки с окклюзией указанных сосудов нелизирующимися рентгеноконтрастными эмболами, см. патент RU  2269341, кл. A61N 5/10, опубл. 2006 02.10. Способ позволяет усилить повреждающий эффект лучевого воздействия на радиорезистентные формы рака. 2269341, кл. A61N 5/10, опубл. 2006 02.10. Способ позволяет усилить повреждающий эффект лучевого воздействия на радиорезистентные формы рака.
Известен способ лечения рака, путем воздействия на опухоль в предоперационном периоде дистанционного гамма-облучения, перорального приема капецитабина, введения внутриректально в прямую кишку метронидазола в виде композитной смеси метронидазола, альгината натрия и диметилсульфоксида с последующим оперативным вмешательством, при этом больному проводят сеанс дистанционной гамма-терапии РОД-5 Гр на фоне двукратного приема капецитабина, см патент RU,  2311909, кл A61N 5/10, опубл. 2007.12.10. Изобретение позволяет снизить частоту локорегионарных рецидивов и метастазов и удлиняет безрецидивный период. 2311909, кл A61N 5/10, опубл. 2007.12.10. Изобретение позволяет снизить частоту локорегионарных рецидивов и метастазов и удлиняет безрецидивный период.
Недостатком указанных известных способов лечения рака является их недостаточная эффективность, связанная с опасностью возникновения рецидивов и отдаленных метастазов, а также технические трудности, возникающие при обращении с метронидазолом.
Известен способ лечения рака прямой кишки путем воздействия на опухоль в предоперационном периоде дистанционного гамма-облучения, локальной СВЧ-гипертермии и вводимого в кишку метронидазола в виде композитной смеси, преимущественно при следующих соотношениях ингредиентов, мас.%: метронидазол 12-22, альгинат натрия 4-6, диметилсульфоксид 2, вода дистиллированная до 100, при осуществлении способа больному проводят 5-дневный курс сеансов дистанционной гамма-терапии РОД – 5 Гр с введением внутриректально композитной смеси и проведением сеансов локальной СВЧ-гипертермии, см. патент RU,  2234318, кл. A61N 5/10, опубл. 2004 08 20. Данный способ позволяет эффективного осуществлять комбинированное лечения больных первично-операбельными формами рака прямой кишки, снизить частоту возникновения локорегионарных рецидивов и увеличить среднюю продолжительность жизни и 5-летнюю выживаемость пациентов. Указанный известный объект изобретения – способ принят в качестве прототипа как наиболее близкий по технической сущности и достигаемому результату аналог. 2234318, кл. A61N 5/10, опубл. 2004 08 20. Данный способ позволяет эффективного осуществлять комбинированное лечения больных первично-операбельными формами рака прямой кишки, снизить частоту возникновения локорегионарных рецидивов и увеличить среднюю продолжительность жизни и 5-летнюю выживаемость пациентов. Указанный известный объект изобретения – способ принят в качестве прототипа как наиболее близкий по технической сущности и достигаемому результату аналог.
Недостатком прототипа и всех перечисленных известных способов лечения рака прямой кишки является невысокая степень радиомодификации тканей опухоли, достигаемая при его реализации, что является следствием использования метронидазола в качестве основного радиомодификатора, обладающего невысокой степенью избирательного накопления в ткани опухоли. Кроме того, способ лечения рака прямой кишки согласно прототипу обладает выраженными побочными явлениями, связанными с органолептическими свойствами, раздражающим действием химического препарата на слизистую оболочку желудочно-кишечного тракта и нейротоксичностью.
Достигаемым в предлагаемом способе техническим результатом является:
– увеличение лечебного эффекта,
– подавление роста и метастазирования опухоли вплоть до ее регрессии,
– снижение количества побочных явлений и противопоказаний.
Таким образом, предлагаемый способ позволяет повысить эффективность лечения и профилактики онкологических заболеваний, расширить область применения способа. В предлагаемом способе максимально сохранены все положительные свойства прототипа, а именно комплексный подход, свойственный, например, комбинированному методу лечения рака прямой кишки.
В основу изобретения положено оригинальное техническое решение использования гиперандрогенемии (состояний устойчивого повышенного содержания андрогенов) в качестве радиомодифицирующего агента, повышающего чувствительность опухоли к ионизирующему излучению, вместо химического соединения, а также контроль и стимулирование гормонального фона пациента в предоперативном периоде. Авторами изобретения установлена уникальная зависимость между склонностью к рецидивированию и метастазированию раковых новообразований и изменениями гормонального фона пациента.
Способ осуществляется следующим образом.
На первой стадии лечения выполняют забор биопсийного материала опухоли и определяют наличие андрогенных и эстрогенных рецепторов. Кроме того, определяют уровень половых гормонов, на основании чего добиваются развития гиперандрогенемии.
На второй стадии лечения создают устойчивое повышенное содержание андрогенов в организме больного путем введения гормональных препаратов. В качестве гормонального препарата используют половые гормоны тестостерон или синэстрол. Тестостерон является основным мужским половым гормоном, который секретируется мужскими половыми железами – яичками, а в небольших количествах – корой надпочечников у обоих полов. Биологическое действие тестостерона наиболее специфично проявляется в тканях-мишенях, где происходит его избирательное накопление, преимущественно к таким тканям относятся клетки органов половой системы. В медицинской практике применяют синтетические препараты тестостерона – пропионат, метилтестостерон Синэстрол, синтетический аналог женских половых гормонов, белый или белый со слегка желтоватым оттенком порошок без запаха, практически нерастворим в воде, легко растворим в спирте, трудно – в персиковом масле, по химическому строению отличается от стероидных эстрогенных гормонов, но по биологическим и лечебным свойствам близок к ним. Для ускоренного проникновения препаратов в организм применяют их втирание в кожу. Параллельно препараты водят внутримышечно. Препараты на данной стадии используют в виде геля, преимущественно в масляных растворах (синэстрол применяют в виде 2% масляного раствора). Препараты таким образом вводят ежедневно по 3-4 мл. Общая доза и продолжительность лечения зависит от изменений в составе крови и длится до достижения устойчивого повышенного содержания гормона. Необходимая и предельная концентрация гормона в крови определяется индивидуально для каждого пациента исходя из параметров его роста, веса и первоначальной концентрации. Препараты хорошо переносятся, быстро усваиваются и желаемый эффект, как правило, достигается за 7-10 сеансов.
Повышенное содержание в организме уровня полового гормона оказывает эффективное радиомодифицирующее действие на опухолевые клетки. Дополнительно после введения андрогенных или эстрогенных препаратов и до проведения дистанционной гамма-терапии выполняют локальную СВЧ-гипертермию при температуре 42,5-43° в течение 60 минут.
Кроме того, по истечении 6-8 часов после гормонотерапии проводят сеанс дистанционной гамма-терапии РОД-25 Гр или РОД-40 Гр. На основании оценки результатов облучения принимают решение о дальнейшем лечении. В случае необходимости курсы гормонотерапии проводят повторно. Через 24-48 часов после завершения курса предоперационного облучения при необходимости выполняют радикальное оперативное вмешательство, характер и объем которого определяется уровнем локализации опухоли и степенью ее местного распространения.
На завершающей стадии при наличии в предварительно взятом биопсийном материале опухоли эстрогенных рецепторов добиваются достижения в организме больного постоянной андрогенизации, а при наличии в биопсийном материале опухоли андрогенных рецепторов – эстрогенизации. При этом постоянно осуществляют контроль гормонального фона в крови пациента.
Исследование влияния созданной гиперадрогенемии на чувствительность опухоли к дистанционной гамма-терапии с предшествующим сеансом локальной СВЧ-гипертермии проводилось на лабораторных животных с привитой солидной карциномой Эрлиха линии ELD. Животные – мыши линии BALB/C, самцы весом 20-22 г. Клетки карциномы Эрлиха линии ELD привили мышам в мышцу голени за 7 дней до облучения. За день до облучения животным введены тестостерон (Тестостерон пропионат 5%) или синэстрол (Синэстрол, раствор в масле 0,1%). Локальную СВЧ-гипертермию проводили путем прогрева конечности с растущей опухолью при температуре 43°С в течение 60 минут. В день облучения диаметр голени с растущей опухолью варьировался в пределах 7-9 мм (диаметр голени мышей без привитой опухоли составляет в середине примерно 4 мм). Каждая экспериментальная группа состояла из 6-8 животных. Облучение происходило на кобальтовой гамма-усталовке АГАТ-Р, снабженной дополнительным устройством для увеличения перепада мощности дозы между облучаемой опухолью и экранируемым телом животного. Доза облучения равнялась 5 Гр.
Животные с привитыми опухолями в день облучения были разделены на следующие группы
– контрольная группа, никаких воздействий;
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли;
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли в комбинации с предшествующей локальной СВЧ-гипертермией (ГТ) (Обл + ГТ);
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли на фоне введения радиомодифицирующего гормонального препарата тестостерона (Тестостерон + Обл);
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли в комбинации с предшествующей локальной СВЧ-гипертермией (ГТ) на фоне введения радиомодифицирующего гормонального препарата тестостерона (Тестостерон + Обл + ГТ);
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли на фоне введения радиомодифицирующего гормонального препарата синэстрола (Синэстрол + Обл);
– дистанционная гамма-терапия РОД-5 Гр (Обл) опухоли в комбинации с предшествующей локальной СВЧ-гипертермией (ГТ) на фоне введения радиомодифицирующего гормонального препарата синэстрола (Синэстрол + Обл + ГТ).
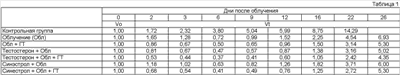
Оценку эффекта воздействия проводили путем измерения объема опухоли, т.е. максимальных размеров опухоли в трех перпендикулярных направлениях. Полученные числа перемножали. Данные, полученные в день облучения, рассматривали как исходный объем (Vo) новообразований, а данные в остальные дни измерений обозначали как (Vt). Динамику регрессии и рецидивироваяня опухоли отражает сотношение Vt и Vo. Определение величины Vt производили трижды в неделю в течение двадцати шести дней после воздействия. Результаты динамики изменения объема опухолей у контрольной группы животных, а также животных, опухоли которых были подвергнуты дистанционной гамма-терапии РОД-5 Гр (Обл) в комбинации с локальной СВЧ-гипертермией (ГТ), а также действия этих агентов на фоне введения тестостерона (Т) или синэстрола (С) приведены в Таблице 1.
На чертеже результаты Таблицы 1 представлены в графическом виде, при этом: гладкая кривая отображает динамику изменения объема опухолей у контрольной группы животных; кривая, отмеченная черными квадратами, – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр (Обл); кривая, отмеченная белыми квадратами, – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр опухоли в комбинации с предшествующей локальной СВЧ-гипертермией (Обл + ГТ); кривая, отмеченная знаками плюс (+), – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр опухоли на фоне введения радиомодифицирующего гормонального препарата тестостерона (Тестостерон+Обл); кривая, отмеченная черными ромбами, – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр опухоли в комбинации с предшествующей локальной СВЧ-гипертермией (ГТ) на фоне введения радиомодифицирующего гормонального препарата тестостерона (Тестостерон + Обл + ГТ); кривая, отмеченная крестиками, – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр опухоли на фоне введения радиомодифицирующего гормонального препарата синэстрола (Синэстрол + Обл); кривая, отмеченная черными треугольниками, – группа животных, подвергнутых дистанционной гамма-терапии РОД-5 Гр опухоли в комбинации с предшествующей локальной СВЧ-гипертермией на фоне введения радиомодифицирующего гормонального препарата синэстрола (Синэстрол + Обл + ГТ).
В таблице 2 представлены результаты замеров времени (в сутках) дорастания до исходного объема опухолей всех групп, а также время удвоения объема опухолей.
Из представленных в таблицах 1, 2 и на графиках (см. чертеж) материалов видно, что дистанционная гамма-терапия РОД-5 Гр приводит к значительному торможению роста опухоли, а при воздействии локальной СВЧ-гипертермии этот эффект несколько усиливается. Оба гормональных препарата и тестостерон, и синэстрол увеличивают глубину регрессии опухолей как после дистанционной гамма-терапии РОД-5 Гр, так и после дистанционной гамма-терапии РОД-5 Гр опухоли в комбинации с предшествующей локальной СВЧ-гипертермией. Глубина регрессии является наиболее выраженной на шестой день после дистанционной гамма-терапии, причем тестостерон увеличивает глубину регрессии сильнее, чем синэстрол. Эффект модификации поражения опухолей гормональными препаратами в представленных экспериментах выражен вполне определенно. При этом модифицирующий эффект тестостерона и синэстрола примерно одинаков для дистанционной гамма-терапии РОД-5 Гр и для дистанционной гамма-терапии РОД-5 Гр опухоли в комбинации с предшествующей локальной СВЧ-гипертермией, из чего следует, что усиление эффекта гормональными препаратами происходит в основном за счет модификации действия лучевого компонента.
Пример 1
Больной 3. Возраст 60 лет. Диагноз – рак прямой кишки IV ст., наличие отдаленных метастазов. Результаты оценки гормонального статуса: Тестостерон 5,4 нмоль/л (норма 7,0-30 нмоль/л).
Больному проведено лечение заявленным способом.
Выполнили забор биопсийного материала опухоли. Исследование материала выявило наличие эстрогенных рецепторов. На основании выявленного уровня тестостерона выполнили введение гормональных препаратов в организм больного, что позволило добиться развития гиперандрогенемии. На фоне развившейся гиперандрогенемии осуществили воздействие на опухоль путем проведения дистанционной гамма-терапии РОД-25 Гр. Вследствие того, что во взятом биопсийном материале были выявлены эстрогенные рецепторы, после воздействия провели мероприятия, позволившие добиться достижения в организме больного постоянной андрогенизации.
В результате проведенного лечения отмечена регрессия опухоли, что позволило выполнить пациенту радикальное хирургическое лечение (брюшно-промежностную экстирпацию прямой кишки).
Больной находился под наблюдением в течение 2 лет. За этот период рецидивирования и метастазирования выявлено не было.
В настоящее время у нас получены результаты 2-летнего наблюдения за 12 пациентами (с рецепторсодержащими опухолями), у которых был применен предлагаемый способ. У всех больных за этот период не было отмечено рецидивирования и метастазирования.

Формула изобретения
1. Способ лечения и профилактики рецидивирования и метастазирования опухолей, содержащих рецепторы половых гормонов, путем воздействия на опухоль дистанционной гамма-терапии, отличающийся тем, что предварительно осуществляют забор биопсийного материала опухоли и определяют наличие андрогенных и эстрогенных рецепторов, затем определяют уровень половых гормонов, на основании чего добиваются развития гиперандрогении путем введения в организм гормонального препарата, после чего осуществляют на фоне гиперандрогенемии воздействие на опухоль путем проведения дистанционной гамма-терапии РОД-25 Гр или РОД-40 Гр, далее при наличии в предварительно взятом биопсийном материале опухоли эстрогенных рецепторов добиваются достижения в организме больного постоянной андрогенизации, а при наличии в биопсийном материале опухоли андрогенных рецепторов – эстрогенизации.
2. Способ по п.1, отличающийся тем, что дополнительно через 24-48 ч после проведения дистанционной гамма-терапии выполняют радикальное оперативное вмешательство.
3. Способ по п.1, отличающийся тем, что дополнительно после введения андрогенных или эстрогенных препаратов и до проведения дистанционной гамма-терапии выполняют локальную СВЧ-гипертермию при температуре 42,5-43° в течение 60 мин.
РИСУНКИ
|
|