|
|
(21), (22) Заявка: 2009112919/04, 06.04.2009
(24) Дата начала отсчета срока действия патента:
06.04.2009
(46) Опубликовано: 10.06.2010
(56) Список документов, цитированных в отчете о
поиске:
MURKOVIC S.I., MILARDOVIC S. Talanta. 2007. v.71, p.1782-1787. RU 2238563 C1, 20.10.2004. RU 2282851 C2, 10.10.2005. ZAPOROZHETS O.A., KRUSHYNSKA O.A., LIPKOVSKA N.A., BARVIN-CHENKO V.N. Agricultural and food chemistry. 2004.  52. p.21-25. 52. p.21-25.
Адрес для переписки:
634050, г.Томск, пр. Ленина, 36, ТГУ, отдел трансфера технологий, Л.Н. Борило
|
(72) Автор(ы):
Гавриленко Наталия Айратовна (RU),
Саранчина Надежда Васильевна (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение Высшего профессионального образования “Томский государственный университет” (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕГРАЛЬНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ
(57) Реферат:
Изобретение относится к определению интегральной антиоксидантной активности растительного сырья и продуктов питания на его основе. Способ включает взаимодействие реагента, иммобилизованного в оптическую мембрану, с аналитом, последующее ее отделение от раствора и оценку величины антиоксидантной активности, причем в качестве мембраны применяют полиметакрилатную матрицу с иммобилизованной индикаторной системой железо (III) – о-фенантролин, аналитический сигнал представляют в виде светопоглощения при (510±20) нм, координаты цвета или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и/или цветовой шкале, построенных для аскорбиновой кислоты, используемой в качестве вещества-стандарта. Достигается повышение надежности и информативности определения. 4 табл., 2 ил.
Изобретение относится к области аналитической химии и может быть использовано для определения интегральной антиоксидантной активности (АОА) растительного сырья и продуктов питания на его основе.
Известен способ спектрофотометрического определения суммарной АОА растительного сырья и пищевых продуктов на его основе (Патент 2282851, Россия, МПК G01N 33/02. Способ определения суммарной антиоксидантной активности. Цюпко Т.Г., Темердашев З.Ф., Воронова О.Б., Храпко Н.В. – 2004138188/13, заявл 27.12.2004; опубл. 27.08.2006). Способ основан на взаимодействии аналита с реагентом 0,06 М Fe(III) – 0,01 М о-фенантролин и аскорбиновой кислоты (АК) с таким же реагентом, который добавляют в соотношении 1:100, инкубировании не менее 90 мин, фотометрировании при (510±20) нм, с последующим установлением зависимости величины аналитического сигнала от количества вещества и расчетом величины суммарной АОА. Недостатком данного способа можно считать низкую оперативность.
Повысить оперативность определения можно путем иммобилизации аналитических реагентов на твердых матрицах. Иммобилизация аналитических реагентов на твердых матрицах представляет большой практический интерес ввиду возможности их использования для изготовления чувствительных элементов, которые являются основной частью оптических сенсоров и тест-методов, позволяющих проводить экспрессное определение.
 52. P. 21-25). Определение АОА основано на восстановлении комплекса тетрабензо[b,f,j,n]-[l,5,9,13] тетраазациклогексадецинмедь (II) нитрат, адсорбированного на силикагеле до его Cu(1)-аналога при воздействии восстановителей органической природы, присутствующих в анализируемом объекте с последующим фотометрированием мембраны при 712 нм. 52. P. 21-25). Определение АОА основано на восстановлении комплекса тетрабензо[b,f,j,n]-[l,5,9,13] тетраазациклогексадецинмедь (II) нитрат, адсорбированного на силикагеле до его Cu(1)-аналога при воздействии восстановителей органической природы, присутствующих в анализируемом объекте с последующим фотометрированием мембраны при 712 нм.
 11. С.3005-3010], что ограничивает ее применение для определения широкого круга восстановителей. 11. С.3005-3010], что ограничивает ее применение для определения широкого круга восстановителей.
Задачей настоящего изобретения является разработка способа определения интегральной антиоксидантной активности с использованием иммобилизованной индикаторной окислительно-восстановительной системы.
Решение указанной задачи достигается тем, что в способе определения интегральной антиоксидантной активности, включающем взаимодействие реагента, иммобилизованного в оптическую мембрану, с аналитом, последующее ее отделение от раствора и оценку величины антиоксидантной активности, отличающемся тем, что в качестве мембраны применяют полиметакрилатную матрицу с иммобилизованной индикаторной системой железо (III) – о-фенантролин, аналитический сигнал представляют в виде светопоглощения при (510±20) нм, координаты цвета или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и/или цветовой шкале, построенных для аскорбиновой кислоты, используемой в качестве вещества-стандарта.
Сущность заявляемого способа заключается во взаимодействии восстановителей органической природы с индикаторной системой железо (III) – о-фенантролин, иммобилизованной в полиметакрилатную матрицу. При этом железо (III) восстанавливается до железа (II), которое образует с о-фенантролином прочный, окрашенный в оранжевый цвет комплекс, имеющий в спектре поглощения максимум при  =510 нм. =510 нм.
Иммобилизацию индикаторной системы железо (III) – о-фенантролин в полиметакрилатную матрицу проводили ее сорбцией из раствора в статическом режиме в две стадии. Для этого полиметакрилатную матрицу перемешивали в 0,5% водном растворе о-фенантролина в течение 5 мин, затем в водном растворе железа (III) в течение 5 мин.
Условия взаимодействия восстановителей с индикаторной системой железо (III) – о-фенантролин, иммобилизованной в полиметакрилатную матрицу, были определены в результате изучения изменения поглощения (A510) от рН раствора и концентрации аскорбиновой кислоты при различном времени контакта оптической мембраны с раствором аскорбиновой кислоты объемом 50 мл. Было установлено, что оптимальное pH раствора аскорбиновой кислоты для восстановления железа в полиметакрилатной матрице и образования окрашенного комплекса соответствует 3-6. С увеличением времени контакта диапазон линейности зависимости A510=f(casc) падает, но при этом возрастает чувствительность определения. Поэтому в качестве условий исследования взаимодействия восстановителей с иммобилизованными индикаторными системами были выбраны время контакта 45 мин и pH растворов, равный 3.
Для исследования влияния восстановителей органической природы на изучаемые индикаторные системы были выбраны наиболее часто встречающиеся в реальных объектах антиоксиданты: рутин, танин, кверцетин, галловая кислота, цистеин. Зависимости A510 от содержания восстановителя в растворе и их параметры представлены на фиг.1 и в таблице 1.
 11. С.15-19). Для этого изучено влияние модельных смесей, в состав которых входили восстановители танин, рутин, кверцетин и АК в различных соотношениях, на индикаторную систему железо (III) – о-фенантролин, иммобилизованную в полиметакрилатную матрицу. Расчет теоретической величины интегральной АОА проводили по уравнениям количественного соответствия, характеризующим антиоксидантную способность исследуемого восстановителя по отношению к аскорбиновой кислоте как вещества-стандарта (таблица 2). Экспериментальные значения АОА рассчитывали по усредненному уравнению регрессии для зависимости A510 от количества аскорбиновой кислоты. Из результатов, представленных в таблице 3, видно, что экспериментально полученные величины АОА удовлетворительно согласуются с теоретически рассчитанными. Полученные данные показывают, что определяемая величина АОА является результатом совместного действия всех присутствующих в модельной смеси восстановителей. Таким образом, определяемый показатель является интегральным, и оптическая мембрана на основе полиметакрилатной матрицы с иммобилизованной системой железо (III) – о-фенантролин может быть использована при разработке способа оценки интегральной АОА. 11. С.15-19). Для этого изучено влияние модельных смесей, в состав которых входили восстановители танин, рутин, кверцетин и АК в различных соотношениях, на индикаторную систему железо (III) – о-фенантролин, иммобилизованную в полиметакрилатную матрицу. Расчет теоретической величины интегральной АОА проводили по уравнениям количественного соответствия, характеризующим антиоксидантную способность исследуемого восстановителя по отношению к аскорбиновой кислоте как вещества-стандарта (таблица 2). Экспериментальные значения АОА рассчитывали по усредненному уравнению регрессии для зависимости A510 от количества аскорбиновой кислоты. Из результатов, представленных в таблице 3, видно, что экспериментально полученные величины АОА удовлетворительно согласуются с теоретически рассчитанными. Полученные данные показывают, что определяемая величина АОА является результатом совместного действия всех присутствующих в модельной смеси восстановителей. Таким образом, определяемый показатель является интегральным, и оптическая мембрана на основе полиметакрилатной матрицы с иммобилизованной системой железо (III) – о-фенантролин может быть использована при разработке способа оценки интегральной АОА.
Пример 1. Измерение поглощения оптической мембраны и определение интегральной АОА по градуировочному графику.
В 50 мл анализируемого раствора с суммарным содержанием антиоксидантов не более 1,5 мг с pH 3 (цитратный буфер, контроль pH-метром) помещали пластинку полиметакрилатной матрицы с иммобилизованной индикаторной системой и перемешивали в течение 45 минут, затем вынимали, подсушивали фильтровальной бумагой и измеряли поглощение при 510 нм. Содержание интегральной АОА находили по градуировочной зависимости, построенной для АК в аналогичных условиях, с последующим расчетом величины суммарной АОА в виде количества вещества-стандарта (аскорбиновой кислоты), производящего антиоксидантный эффект, эквивалентный действию суммы восстановителей в аналите. Уравнение градуировочной зависимости имеет вид: A510=0,12+19,61·cАK (r=0,999), где cАK – концентрация AK, мг/мл. Диапазон линейности градуировочной зависимости составляет 0-0,03 мг/мл.
Пример 2. Измерение координаты цвета В оптической мембраны и определение интегральной АОА по градуировочному графику.
В 50 мл анализируемого раствора с суммарным содержанием антиоксидантов не более 1,5 мг с pH 3 (цитратный буфер, контроль pH-метром) помещали пластинку полиметакрилатной матрицы с иммобилизованной индикаторной системой и перемешивали в течение 45 минут, затем вынимали, подсушивали фильтровальной бумагой. Мембраны сканировали с применением настольного офисного сканера, обрабатывали полученные изображения с помощью компьютерной программы цифровой обработки изображений «Adobe Photoshop» по светлоте в координатах R, G, В. В качестве аналитического сигнала выбран голубой канал В. Содержание суммарной АОА находили по градуировочной зависимости, построенной для АК в аналогичных условиях с последующим расчетом величины суммарной АОА в виде количества вещества-стандарта (аскорбиновой кислоты), производящего антиоксидантный эффект, эквивалентный действию суммы восстановителей в аналите. Уравнение градуировочной зависимости имеет вид: В=145,9-2969,7 cАK (r=0,9880), где cАK – концентрация аскорбиновой кислоты, мг/мл. Диапазон линейности градуировочной зависимости составляет 0-0,03 мг/мл.
Пример 3. Визуально-тестовое определение интегральной АОА.
Для визуально-тестового определения АОА получены цветовые шкалы путем сканирования образцов, полученных при построении градуировочных зависимостей для АК. Визуальное тест-определение выполняли аналогично методике, описанной в примере 1, с тем отличием, что после контакта с аналитом поглощение полиметакрилатных матриц не измеряли, а проводили сравнение их окраски с цветовой шкалой (фиг.2) и полуколичественно определяли концентрацию восстановителей.
Пример 4. Определение интегральной АОА чая.
Подготовку чая к анализу проводили по ГОСТу (ГОСТ 19885-74. Чай. Методы определения содержания танина и кофеина). Далее поступали, как указано в примере 1, 2. Для подтверждения правильности предлагаемого способа определения АОА использовали метод разбавления анализируемой пробы. Показатель правильности в виде относительной систематической погрешности (± , %) определяли в соответствии с требованиями РМГ 61 – 2003. , %) определяли в соответствии с требованиями РМГ 61 – 2003.
Результаты определения интегральной АОА заявляемым способом представлены в таблице 4. Как видно, границы относительной систематической погрешности (правильности) не более 10%.
Преимуществом заявленного изобретения является возможность использования нескольких вариантов измерения аналитического сигнала оптической мембраны на основе полиметакрилатной матрицы с иммобилизованной индикаторной системой железо (III) – о-фенантролин для качественной и/или количественной оценки АОА.
Таблица 1
Зависимость A510 от концентрации-восстановителя |
| Восстановитель |
Уравнение зависимости A510=f(cвосст), cвосст в г/л |
r |
Диапазон линейности, г/л |
| Аскорбиновая кислота |
A510=0,12+19,61·cАК |
0,999 |
0-0,03 |
| Танин |
A510=0,10+8,23·cT |
0,997 |
0-0,05 |
| Рутин |
A510=0,14+2,36·cP |
0,998 |
0-0,03 |
| Кверцетин |
A510=0,15+50,17·сK |
0,993 |
0-0,01 |
| Галловая кислота |
A510=0,13+95,38·сГ |
0,999 |
0-0,01 |
| Цистеин |
A510=0,14+0,98·сЦ |
0,997 |
0-0,03 |
Таблица 2
Уравнения количественного соответствия для восстановителей |
| Восстановитель |
Усредненные значения функции |
Уравнения количественного соответствия |
| Для вещества-стандарта (АК) |
Для данного восстановителя |
| Танин |
A510=0,12+19,61·cAK |
A510=0,10+8,23·cT |
cAK=0,42·cT-0,02 |
| Рутин |
A510=0,14+2,36·cP |
cAK=0,12·cP+0,02 |
| Кверцетин |
A510=0,15+50,17·cK |
cAK=2,56·cK+0,03 |
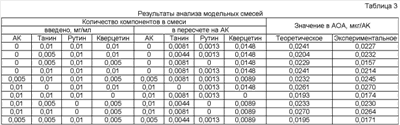
Таблица 4
Результаты определения интегральной АОА (n=4, P=0,95) |
| Марка чая |
АОА, г AK/100 г продукта |
sr, % |
X, мг/мл |
± ,% ,% |
| без разбавления |
с разбавлением  =2 =2 |
| Зеленый чай |
 |
 |
 |
 |
 |
| «Tess» |
7,5±0,7 |
6 |
0,023 |
0,011 |
7 |
| «Jaf Tea» |
9,1±0,5 |
3 |
0,027 |
0,014 |
10 |
| Черный чай |
 |
 |
 |
 |
 |
| «Беседа» |
3,0±0,3 |
6 |
0,009 |
0,005 |
7 |
| Примечание. X – результат анализа пробы |
Формула изобретения
Способ определения интегральной антиоксидантной активности с использованием полиметакрилатной матрицы, включающий взаимодействие реагента, иммобилизованного в оптическую мембрану, с аналитом, последующее ее отделение от раствора и оценку величины антиоксидантной активности, отличающийся тем, что в качестве мембраны применяют полиметакрилатную матрицу с иммобилизованной индикаторной системой железо (III) – о-фенантролин, аналитический сигнал представляют в виде светопоглощения при (510±20) нм, координаты цвета или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и/или цветовой шкале, построенных для аскорбиновой кислоты, используемой в качестве вещества-стандарта.
РИСУНКИ
|
|