Патент на изобретение №2167878
|
||||||||||||||||||||||||||
(54) СПОСОБ РАСЩЕПЛЕНИЯ ПОБОЧНЫХ ПРОДУКТОВ ПРЯМОГО СИНТЕЗА АЛКИЛХЛОРСИЛАНОВ
(57) Реферат: Описывается способ расщепления тяжелых побочных продуктов, поступающих с синтеза алкилхлорсиланов, путем обработки соляной кислотой в присутствии каталитической системы, заключающийся в том, что каталитическая система содержит по меньшей мере один фосфат металла. Техническим результатом является расщепление практически всех дисиланов, тяжелых побочных продуктов прямого синтеза типа Мех Cly Si СН2 Si Mez, Сlt или Меx Cly Si Si Mew Clu [Si Mez, Clt]n с n 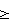 1, где x = 0-3, у = 0-3, x + y = 3, z = 0-3, t = 0-3, z + t = 3, w = 0-2, u = 0-2, w + u = 2, a также значительное увеличение в ходе процесса количества гидридсиланов. 18 з.п. ф-лы, 8 табл. 1, где x = 0-3, у = 0-3, x + y = 3, z = 0-3, t = 0-3, z + t = 3, w = 0-2, u = 0-2, w + u = 2, a также значительное увеличение в ходе процесса количества гидридсиланов. 18 з.п. ф-лы, 8 табл.
Настоящее изобретение относится к способу расщепления тяжелых побочных продуктов, являющихся результатом синтеза алкилхлорсиланов, таких как метилхлорсиланов, в частности к способу расщепления алкилхлордисиланов, в частности метилхлордисиланов, в том числе таких, которые имеют от одного до пяти атомов хлора, путем обработки соляной кислотой в присутствии каталитической системы. Метилхлорсиланы получают путем действия хлористого метила на металлический кремний (прямой синтез). Хотя этот синтез и дает удовлетворительные результаты, однако он приводит к образованию многочисленных тяжелых побочных продуктов, а именно силилметиленов, полисиланов, дисилоксанов, углеводородов и, в частности, метилхлорсиланов, которые составляют наибольшую фракцию (более 80%). Эти побочные продукты не имеют значительного промышленного применения, поэтому их пытаются утилизировать путем расщепления связи Si-Si. Так, некоторые из этих побочных продуктов могут быть интересны тем, что они превращаются в моносиланы путем их обработки с помощью HCl + амин: речь идет о дисиланах, имеющих, по крайней мере, два атома хлора на, по крайней мере, один атом кремния; они квалифицируются как “расщепляемые”. Другие дисиланы являются нерасщепляемыми: Me2ClSi-SiClMe2 (симметричный тетраметилдихлордисилан), пентаметилхлордисилан, силилметилены, полисиланы. Был проведен целый ряд исследований по расщеплению дисиланов, в частности, расщеплением соляной кислотой в присутствии каталитической системы. Так, описаны различные каталитические системы, такие как амины или третичные амины, в патентах FR-A-1119915 и FR-A-1447304 (вышеупомянутый способ, в котором использовались HCl + амии). Каталитическая система, описанная в этих патентах, позволяет эффективно преобразовывать тетрахлордиметилдисилан и трихлортриметилдисилан и некоторые тетраметилдихлордисиланы, однако эти системы имеют тот недостаток, что они не могут расщепить все дисиланы и, в частности, не могут преобразовать симметричный тетраметилдихлордисилан. Органометаллические комплексные соединения палладия могут решить эту проблему посредством использования более жестких реакционных условий. Кроме того, применение такой каталитической системы ограничено в промышленности из-за трудности рециркуляции гомогенного катализатора. При описанных условиях (Н. Матусомо и др., Bulletin of the chemical Society of Japan, том 51 (6), 1913-1914, 1978) обработанные объемы оказываются небольшими, а материальные балансы – плохими. В связи с этим в патенте US-A-3772347 предложено вести обработку галогенидом RCl в присутствии комплексных соединений переходных металлов, например комплексного соединения фосфин-палладий, возможно на угле или силикагеле, что приводит к получению примерно 25% по весу гидридсиланов. Этот процесс описывает расщепление тетраметилдихлордисилана с продолжительностью реакции 86 часов. Патент US-A-5210255 предлагает использовать при гетерогенном катализе металл подгруппы VIII периодической таблицы (стандарт IUPAC), такой как платина, палладий, родий и рутений, в частности, в виде катализатора с подложкой, например, из активированного угля. Предпочтительным является палладий. Целью, по всей видимости, является получение негидрированных метилхлорсиланов. Сравнение проводилось между палладием на угле и тетракис (трифенилфосфин) палладием. Первый катализатор, как оказалось, приводит к высокому выходу реакции превращения дисиланов в негидрированные моносиланы, тогда как второй катализатор приводит к получению значительного количества гидридсилана MeHSiCl2 и Me2HSiCl, но при низкой производительности. Кинетика расщепления протекает медленно: время контакта составляет несколько часов. Термическое расщепление в паровой фазе при 500oC, описанное в патентах US-A-5292912, US-A-5292902, US-A-5321147 и US-A-5326896, также позволяет в присутствии газа водорода, хлора и/или соляной кислоты расщеплять целый комплекс дисиланов на различных катализаторах, таких как активированный уголь, металлические окиси, цеолиты или металлы носителя. При этой температуре реакции являются, в основном, термическими и получается лишь немного гидрогеносиланов. Кроме того, известно, что используемые катализаторы претерпевают изменения при взаимодействии с хлорсиланами, что модифицирует их каталитические свойства. Следовательно, по-прежнему существует необходимость в процессе, позволяющем расщеплять побочные продукты прямого синтеза и, в частности, симметрического тетраметилдихлордисилана в условиях, наиболее выгодных для промышленности. Таким образом, задачей настоящего изобретения является устранение указанных недостатков известного уровня техники и обеспечение расщепления в мягких условиях при высокой скорости побочных продуктов прямого синтеза c обеспечением расщепления практически всех дисиланов, в частности метилхлордисиланов, имеющих от одного до пяти атомов хлора, и, в частности, симметрического тетраметилдихлордисилана, а также пентаметилхлордисилана, т.е. в условиях, применяемых для промышленности. Другой задачей изобретения является расщепление других тяжелых продуктов, в частности, типа (Me)xClySiCH2Si(Me)zClt или (Me)xClySiSi(Me)wClu [Si(Me)zClt]n с n больше или равным 1, в частности между 1 и 8, где x = 0-3, y = 0-3, причем x + y = 3, z = 0-3, t = 0-3, причем z + t = 3, w = 0-2, u = 0-2, причем w + u = 2, и, по крайней мере, y или t, или u равно по крайней мере 1. Следующей задачей изобретения является разработка такого процесса, который приводил бы к получению значительного количества гидрогеносиланов, применимых в промышленности. Для решения этих задач заявителем предложен способ расщепления тяжелых побочных продуктов, например алкилхлордисиланов, являющихся результатом прямого синтеза алкилхлорсиланов, содержащих, в частности, 1-6 атомов углерода, путем обработки соляной кислотой в присутствии каталитической системы, отличающийся тем, что каталитическая система включает, по крайней мере, один металлический фосфат. Настоящее изобретение, предпочтительно, применимо для расщепления тяжелых побочных продуктов, являющихся результатом синтеза метилхлорсиланов, и, в особом случае, для расщепления метилхлордисиланов, имеющих от одного до пяти атомов хлора. Предпочтительно, чтобы металлический фосфат включал пропитывающее соединение основного характера, выбранное, например, из группы щелочноземельных металлов, щелочных металлов и их смесей (путем определения смесей внутри и/или между группами), предпочтительно, соединенных с контранионом, чтобы обеспечить электрическую нейтральность. Одним или более первоначальным контранионом, выбранным перед термической обработкой, преимущественно может быть анион нитрата, сульфата, хлорида, фторида, гидрогенофосфата, фосфата, дигидрогенфосфата, гидрогеносульфата, оксалата, ацетата, бензоата и т.д. Анионы могут быть только одного вида или состоять из смеси нескольких видов; для простоты предпочитают выбирать только один вид или один класс анионов. Содержание в катализаторе пропитывающего соединения (или активизирующего агента), предпочтительно, такое, чтобы весовое процентное содержание пропиточного соединения основного характера в расчете, например, на щелочной и/или щелочноземельный элемент по отношению к металлическому сухому фосфату составляло 0-25%, преимущественно 3-15%. Предпочтительно, металлический фосфат включает металл, выбранный из группы, состоящей из одновалентных, двухвалентных, трехвалентных металлов, включая редкоземельные четырехвалентные и пятивалентные элементы. Более предпочтительно, чтобы металлический фосфат отвечал формуле M(XPO4)y, в которой M представляет металл, выбранный из: – одновалентных металлов, в случае которых X является 2H и y = 1 – двухвалентных металлов, в случае которых X является H и y =1 – трехвалентных металлов, таких, в частности, как Al:B, Fe, Ga и редкоземельные металлы (лантаниды, имеющие атомный номер 57-71, включая лантан, в частности лантаниды, упомянутые выше, а также иттрий, скандий), в случае которых X отсутствует, а y = 1 – четырехвалентных металлов, таких, в частности, как Zr, Ti, и т.д., в случае которых X является H, а y = 2 – пятивалентных металлов, таких, в частности, как Nb, Та и т.д., в случае которых X является О, а y = 1. В конкретном предпочтительном варианте изобретения предусматривается использовать металлический фосфат, основанный на применении трехвалентного редкоземельного элемента. В этом случае металлический фосфат отвечает формуле MPO4, в которой – M представляет: трехвалентный редкоземельный элемент M3 или смесь, по крайней мере, одного трехвалентного редкоземельного металла M3 и, по крайней мере, одного элемента, выбранного в группе, состоящей из щелочных металлов M1 и щелочноземельных металлов M2 при соотношении M = aM1 + bM2 + cM3 и a + 2b + 3c = 3 – a является коэффициентом от 0 до 3, преимущественно от 0,01 до 0,5, предпочтительно от 0,05 до 0,2, – b является коэффициентом от 0 до 3/2, преимущественно от 0 до 1/3 или 1  0,1, а 0,1, а– c является коэффициентом от 0 до 1, преимущественно больше или равным 1/3, предпочтительно составляет 1/2. В этом случае предпочитают, чтобы металлический фосфат включал, кроме того, пропитывающее соединение, тогда формула фосфата описывается в виде MPO4(Jm)p, в которой – Jm означает пропитывающее соединение основного характера, выбранное из щелочноземельных металлов, щелочных металлов и их смесей, объединенных, предпочтительно, с контранионом для обеспечения электрической нейтральности, и – p является меньше 0,5, в частности составляет 0,4-0,25. Предпочтительно, – M1 выбирается из элементов группы 1A периодической системы, предпочтительно, щелочные металлы, такие как литий, натрий, калий, рубидий, цезий и их смеси, – M2 выбирается из элементов группы 2A периодической системы, предпочтительно, щелочноземельные металлы, такие как бериллий, магний, кальций, стронций, барий и их смеси. – M3 выбирается из группы трехвалентных редкоземельных, выбранных среди лантанидов, иттрия и скандия и их смесей, причем лантаниды являются, предпочтительно, лантаном, церием, празеодимом, неодимом, самарием, европием, гадолинием, тербием, диспрозием, гольмием, эрбием, тулием, иттербием и лютенцием. При их определении использовалась классификация элементов, опубликованная в Бюллетене химического общества Франции (Bulletin de Ja.Societe chimigue de France) N 1, 1966. Как правило, M, предпочтительно, состоит самое большее из трех элементов, что диктуется соображениями удобства. По тем же причинам и с экономической точки зрения можно использовать смесь редкоземельных металлов, имеющихся в продаже, независимо от формы их выпуска при условии, что из них легко получить соединения согласно изобретению. Металлические фосфаты согласно изобретению могут приготавливаться путем пропитки фосфата, в частности соединения формулы MPO4, раствором или суспензией Jm в растворителе, предпочтительно в воде. Результаты получаются тем лучше, чем более растворим Jm и чем свежее приготовленный фосфат, в частности MPO4. Преимущественно, способ приготовления фосфатов формулы MPO4(Jm)p состоит в том, чтобы: а) осуществить синтез соединения MPO4, затем, предпочтительно, не выделяя MPO4 из реакционной среды, б) ввести пропитывающее соединение Jm в реакционную среду, в) отделить возможную остаточную жидкость от твердого продукта реакции, г) высушить и, в случае необходимости, прокалить. Ссылаясь на общие методики приготовления фосфатов (в частности, описанные в “PASCAL. Р., Nouveautraite dechimie minerale”, том X (1956), стр. 821-823, и в “G.MELNIS, Handbuchder anorganischen cheme”, 8-е издание, том 16 (С), стр. 201-206 (1965), можно различить два главных пути получения фосфатов. С одной стороны, осаждение растворимой соли металла (хлорида, нитрата) обработкой кислым фосфатом аммония или фосфорной кислотой и окончательной обработкой гидратом окиси аммония с последующей, в случае необходимости, нейтрализацией. С другой стороны, взаимодействием окиси металла с фосфорной кислотой при нагревании. В обоих случаях предусматривают окончательную обработку гидроокисью щелочного металла. Фосфаты указанных металлов могут также приготавливаться путем приготовления шамота реакции твердое – твердое солей этих металлов с солями фосфора и последующего обжига. Затем продукт высушивается по классической технологии, известной специалисту. Сушку преимущественно осуществляют при температуре между 50oC и 200oC в течение периода предпочтительно от 2 до 8 часов при нормальном атмосферном давлении или при пониженном давлении или путем вакуумной сушки. Высушенный продукт затем обжигается при температуре между 200oC и 1000oC, предпочтительно между 400oC и 700oC, в течение времени от 1 до 15 часов, предпочтительно от 3 до 6 часов. Для приготовления фосфатов с активными добавками, пропитанных согласно изобретению, можно сослаться на заявки на патент EP-A-0440555 и EP-A-0599688, которые даны здесь в виде ссылок. Процесс расщепления может вестись в паровой фазе (газ HCl и расщепляемые продукты в виде пара) в трехфазной системе газ-жидкость-твердое вещество (газ HCl, расщепляемые продукты в растворе), причем катализатор в обоих случаях находится, предпочтительно, в твердой форме, способ может осуществляться непрерывно или периодически с непрерывным сбором или отгонкой продуктов реакции. Используемый катализатор, если процесс осуществляют в паровой фазе, находится в неподвижном слое или в кипящем слое, в частности, в смеси с инертными веществами для того, чтобы увеличить поверхность контакта, а если процесс проводят в трехфазной системе, то он находится в виде суспензии (пульпы). Процесс расщепления обычно проводят при температуре от 100oC до 500oC. В случае дисиланов, включающих два атома хлора или более на атом кремния, температура может заключаться между 100oC и 300oC. Для других дисиланов или тяжелых продуктов температура реакции преимущественно заключена между 300, предпочтительно 350oC, и 500oC. Если используют смесь всех тяжелых продуктов, то можно также наблюдать реакции расщепления тяжелых продуктов или продуктов, не содержащих два атома хлора на атом кремния, даже при более низкой температуре, например 200oC. Во время применения паровой фазы время контакта, определяемое как соотношение между объемом катализатора и общим расходом газов (дисилан + соляная кислота + транспортирующий газ) при выбранной температуре, изменяется обычно от 0,01 сек до 50 сек и наиболее часто от 0,1 сек до 10 сек. Давление не является критическим. Оно, в основном, располагается в пределах от атмосферного давления до 10 МПа (100 бар) и, предпочтительно, от атмосферного давления до 1,5 МПа (15 бар). Молярное соотношение между соляной кислотой и всеми дисиланами может заключаться между 0,1 и 100, предпочтительно между 0,5 и 10. Можно также использовать инертный транспортирующий газ, парциальное давление которого составляет от 0 до 10% от всех газовых потоков. Инертный транспортирующий газ может представлять собой инертный газ или смесь инертных в реакционных условиях газов, например аргон, азот и т.д. Если катализатор используют в виде суспензии (пульпы), то это может быть суспензия катализатора в смеси дисиланов и других тяжелых продуктов, выходящих после прямого синтеза, но также и в инертном органическом растворителе с высокой точкой кипения, заключенной между 80oC и 300oC. Органический растворитель выбирают по его свойству растворять дисиланы. В качестве инертного растворителя можно назвать циклические карбоксамиды, алифатические или ароматические нитрилы, простые эфиры и т.д. Моносилановые продукты могут отгоняться непрерывно в процессе их образования или извлекаться в конце реакции. Осуществление процесса в паровой фазе с катализатором в виде неподвижного слоя является предпочтительным и приводит к успешному расщеплению симметрического тетраметилдихлордисилана при очень коротком времени контакта, порядка нескольких секунд, например около 2 секунд и даже меньше. Это приводит также к чрезвычайно эффективному расщеплению других метилхлордисиланов. Так, степень расщепления от 99 до 100% достигается при обработке смесей триметилтрихлордисилана + диметилтетрахлордисилана при очень коротком времени контакта, соответственно 3 и 0,6 секунд. Подобные степени превращения были получены со смесью промышленного типа, включающей три вышеуказанных дисилана. Очень короткие сроки реакции представляют большое преимущество в промышленном плане, особенно в том, что касается реактора, который может быть очень небольшого размера, обрабатывая значительный объем. Изобретение имеет другое явное преимущество, поскольку позволяет эффективно расщеплять симметрический тетраметилдихлордисилан с получением гидридсилана Me2HSiCl, который в настоящее время представляет собой большую коммерческую ценность. При применении катализатора в виде суспензии предпочитают, чтобы катализатор был пропитан. Длительность реакции составляет несколько минут до нескольких часов, в частности от 5 мин до 5 час, в особенности между 30 мин и 2 часами. Способ согласно изобретению имеет, кроме того, то преимущество, что обеспечивает получение гидридсиланов Me2HSiCl и MeHSiCl2. Следующие примеры иллюстрируют изобретение, не ограничивая, однако, область его применения. Приготовление фосфата лантана Пример 1 В реактор вводят 106 г H3PO4 (с концентрацией 85%, продаваемой фирмой Пролабо), или 0,92 моля, в 800 мл деионизированной воды. Перемешивают при 500-700 об/мин. Вводят 299 г La2(CO3)3  12H2O в холодном состоянии (или 0,8 моля лантана) в 736 мл воды медленно и при сильном перемешивании.
Затем реакционную среду нагревают при 80oC в течение 2 часов тридцати минут.
В течение получаса охлаждают до температуры окружающей среды без перемешивания и заканчивают охлаждение в ванне с холодной водой.
Суспензию фильтруют на фриттированном стекле N 3 до истощения маточных растворов.
Затем продукт снова диспергируют в двух литрах воды при сильном перемешивании и оставляют суспензию в течение получаса при перемешивании.
Суспензию фильтруют на фриттированном стекле N 3 до истощения маточных растворов. Продукт снова диспергируют в 900 мл деионизированной воды и нейтрализуют раствором аммиака до pH, равном 9.
Продукт фильтруют, промывают водой и центрифугируют перед тем, как подвергнуть сушке при 110oC.
Часть полученного продукта затем прокаливают 4 часа при 400oC.
Пример 2 12H2O в холодном состоянии (или 0,8 моля лантана) в 736 мл воды медленно и при сильном перемешивании.
Затем реакционную среду нагревают при 80oC в течение 2 часов тридцати минут.
В течение получаса охлаждают до температуры окружающей среды без перемешивания и заканчивают охлаждение в ванне с холодной водой.
Суспензию фильтруют на фриттированном стекле N 3 до истощения маточных растворов.
Затем продукт снова диспергируют в двух литрах воды при сильном перемешивании и оставляют суспензию в течение получаса при перемешивании.
Суспензию фильтруют на фриттированном стекле N 3 до истощения маточных растворов. Продукт снова диспергируют в 900 мл деионизированной воды и нейтрализуют раствором аммиака до pH, равном 9.
Продукт фильтруют, промывают водой и центрифугируют перед тем, как подвергнуть сушке при 110oC.
Часть полученного продукта затем прокаливают 4 часа при 400oC.
Пример 2Продукт, приготовленный в соответствии с примером 1, высушенный при 110oC, прокаливают 4 часа при 700oC. Приготовление фосфата лантана с активизирующей добавкой соли щелочного металла Пример 3 Отбирают 7,8 мл GM раствора CSOH, в который добавляют 23,5 мл 1 М раствора H3PO4. Затем добавляют количество воды, необходимое для доведения раствора до 50 мл. Берут 50 г продукта, приготовленного в примере 1, и помещают в химический стакан на 200 мл. Прикапывают туда 20 мл предварительно приготовленного высокогомогенного пропитывающего раствора. Оставляют продукт на один час. Его сушат всю ночь при 110oC и прокаливают 2 часа при 500oC. Содержание цезия в расчете на сухой продукт 5%. Пример 4 Действуют как в примере 2, но используют пропитывающий раствор, приготовленный из 15,7 мл 6 М раствора CSOH и 23,5 мл М раствора H3PO4. Содержание цезия в расчете на сухой вес 10%. Пример 5 Действуют как в примере 2, но используют пропитывающий раствор, приготовленный из 16,3 мл раствора 6 М CSOH и 24 мл раствора 4 М H3PO4. Содержание цезия в расчете на сухой вес 13%. Пример 6 Действуют как в примере 2, во используют пропитывающий раствор, приготовленный из 4,7 мл 6 М раствора КОН и 14,1 мл 1 М раствора H3PO4. Содержание калия в расчете на сухой вес 0,88%. Пример 7 Вводят в реактор 182,4 г H3PO4 (с концентрацией 85%, продаваемой фирмой Пролабо), или 1,6 моля, в 640 мл деионизировавной воды. Реакционную среду нагревают до 85oC и, когда температура достигнута, вводят 260,8 г La2O3 (или 0,8 моля лантана) равномерным образом (14 г каждые 5 минут). Реакционную смесь нагревают 1 час при 85oC, затем охлаждают до температуры окружающей среды при перемешивании. Затем добавляют при сильном перемешивании 1 М раствор CSOH до тех пор, пока не получат раствор с pH 9. Продукт извлекают путем центрифугирования (3600 об/мин), затем снова диспергируют в 400 мл деионизированной воды. Промытый таким образом продукт извлекается центрифугированием. Эта операция промывки повторяется четыре раза согласно одной и той же методике. Промытый таким образом продукт сушат при 110oC, затем прокаливают 4 часа при 500oC. Пример 8: приготовление гидрофосфата циркония В реактор, снабженный холодильником и якорной мешалкой, вводят 93 мл 10,33 М H3PO4. Затем с помощью масляной бани, помещенной на нагревающую плиту с регулированием температуры контактным термометром, доводят H3PO4 до кипения (перемешивание 300 об/мин). В этот момент туда вводят 0,064 моля сульфата циркония. Пастообразный продукт становится бледно-желтым (в течение 1/2 часа). Затем температуру понижают до 80oC и оставляют 48 часов. После охлаждения извлекают полученный продукт, который центрифугируют 25 минут. Продукт промывают один раз горячей водой (80oC), затем холодной водой до тех пор, пока промывочные воды не достигнут pH 4. Сушку под вакуумом проводят в течение 40 часов. Пример 9: приготовление гидрофосфата кальция В химическом стакане растворяют 106,6 г Ca(NO3)2 в 300 мл H2O (pH раствора около 7). Затем вводят при расходе 1,2 литра/час раствор (NH4)2HPO4 в пермутированной воде (m = 145,2 г в 300 мл H2O). Продукт осаждается. Заканчивают введение и добавляют 50 мл H2O (промывание труб насоса). Затем оставляют при перемешивании при температуре окружающей среды в течение 4 часов. Отбирают 413,7 г суспензии. Затем центрифугируют в течение 20 минут (pH маточных вод 6,7). Осуществляют промывку с помощью 500 мл H2O, затем перемешивают в течение 20 минут. Центрифугируют, промывают (pH промывочных вод 7,8). Сушат, затем прокаливают 3 часа при 500oC. A – примеры 10-13 иллюстрируют проведение процесса в трехфазной системе с реактором, работающим с партиями продуктов (периодически), при этом катализатор находится в виде суспензии (пульпы). Общая методика работы В трехгорлый реактор, снабженный вертикальным холодильником, вводом для газа и измерителем температуры, после продувания установки азотом в течение часа загружают дисилан и катализатор, затем начинают нагревать установку также в потоке азота. Когда достигнута температура кипения (145-150oC), подачу азота прекращают и начинают подавать соляную кислоту. Когда реакция закончена, подачу HCl прекращают, затем установку прочищают азотом. Анализ продуктов реакции проводится с помощью хроматографии в газовой фазе (ХГФ). Таким образом, рассчитывают для каждого опыта: – степень превращения (ТТ): % превращенного дисилана по отношению к введенному дисилану, – селективность по моносиланам, исходя из нормы 100. Примеры 10-13 Таблица 1 иллюстрирует степень преобразования, таблица 2 иллюстрирует образованные моносиланы (селективность, исходя из нормы 100). B – примеры 14-26, приведенные ниже, иллюстрируют использование процесса в паровой фазе с катализатором в неподвижном слое. Общий метод работы Катализаторы тестируют в соответствия со следующей методикой, если нет других указаний. В реактор, установленный вертикально (кварцевая труба длиной 15 см и диаметром 2 см), последовательно загружают 5 см3 кварца, катализатор, затем 5 см3 кварца. Катализатор доводится до кондиции при температуре, выбранной для реакции, в течение двух часов в потоке азота (2 литр/час при нормальных условиях давления и температуры). Затем хлордисиланы впрыскиваются посредством проталкивателя-шприца. Расход устанавливают таким, чтобы добиться времени контакта, выбранного для каждого эксперимента. После выхода на режим в течение около 15 минут опыт длится обычно 1 час. Продукты, выходящие из реактора, улавливаются в сборнике, охлаждаемом водяной баней с температурой 0oC. Анализ продуктов реакции производится хроматографией в газовой фазе (ХГФ). Так, для каждого опыта рассчитывают: – степень превращения (ТТ): % преобразованного дисилана относительно введенного дисилана, – селективность по моносиланам при норме 100. Примеры 14-20: опыт на расщепление Me2ClSi-SiClMe2 (85% в/в) Таблица 3: степень превращения, таблица 4: образованные моносиланы (селективность при норме 100). Примеры 21-25: опыт на расщепление Me2ClSi-SiCl2Me (27%) + MeCl2Si-SiCl2Me (61%) Таблица 5: степень превращения, таблица 6: образованные моносиланы (селективность при норме 100). Пример 26: опыт на расщепление смеси промышленного типа Me2ClSi-SiClMe2 (25% в/в + Me2ClSi-SiCl2Me (22% в/в) + MeCl2Si-SiCl2Me (49% в/в) Таблица 7: степень превращения, таблица 8: образованные моносиланы (селективность при норме 100). Формула изобретения
М(ХРО4)y в которой М означает металл, выбранный из: одновалентных металлов, в случае которых Х = 2Н, а у = 1 двухвалентных металлов, в случае которых Х является H, а у = 1 трехвалентных металлов, в случае которых Х отсутствует, а у = 1 четырехвалентных металлов, в случае которых Х является H, а у = 2 пятивалентных металлов, в случае которых Х является 0, а у = 1. 10. Способ по п.9, отличающийся тем, что фосфат металла соответствует формуле МРO4, в которой – М означает трехвалентный редкоземельный элемент М3 или смесь, по крайней мере, одного трехвалентного редкоземельного элемента М3 и, по крайней мере, одного элемента, выбранного в группе, состоящей из щелочных металлов M1 и щелочноземельных металлов М2 при соотношении: M = aM1 + bM2 + сМ3 и а + 2b + 3с = 3 – а является коэффициентом: заключенном межу 0 и 3, преимущественно между 0,01 и 0,5. – b является коэффициентом, включенном между 0 и 3/2, преимущественно, между 0 и 1/3 и – с является коэффициентом, заключенном между 0 и 1, преимущественно больше или равным 1/3. 11. Способ по п.10, отличающийся тем, что “а” заключено между 0,05 и 0,2 и/или b является 1  0,1 и/или с – больше или равно 1/2.
12. Способ по п.10 или 11, отличающийся тем, что фосфат металла включает пропитывающее соединение и отвечает формуле 0,1 и/или с – больше или равно 1/2.
12. Способ по п.10 или 11, отличающийся тем, что фосфат металла включает пропитывающее соединение и отвечает формулеMPO4(Jm)p в которой: Jm соответствует пропитывающему соединению основного характера, состоящему из металла, выбранного в группе, состоящей из щелочноземельных металлов, щелочных металлов и их смесей, соединенных, предпочтительно, с контр-анионом для обеспечения электрической нейтральности и – p- меньше 0,5, в частности, заключено между 0,04 и 0,25. 13. Способ по любому из пп.10-12 отличающийся тем, что: M1 выбран в группе, состоящей из лития, натрия, калия, рубидия, цезия и их смесей, М2 выбран в группе, состоящей из берилия, магния, кальция, стронция, бария и их смесей, М3 выбран в группе, состоящей из лантанидов, иттрия, скандия и их смесей. 14. Способ по любому из пп.1-13, отличающийся тем, что обработку ведут при температуре между 100 и 500°С, предпочтительно, между 350 и 500°С. 15. Способ по п.14, отличающийся тем, что обработку ведут при температуре между 100 и 300°С для расщепления дисиланов, имеющих два атома хлора или больше на атом кремния. 16. Способ по одному из пп.1-15, отличающийся тем, что обработку ведут в паровой фазе, с твердым катализатором в неподвижном или кипящем слое. 17. Способ по п.16, отличающийся тем, что обработку ведут при времени контакта 0,01 – 50 с, особенно 0,1 – 10 с. 18. Способ по любому из пп.1-17, отличающийся тем, что обработку проводят в трехфазной системе газ – жидкость – твердое с твердым катализатором в виде суспензии. 19. Способ по п. 18, отличающийся тем, что время контакта находится между 5 мин и 5 ч, особенно, между 30 мин и 2 ч. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 10.04.2004
Извещение опубликовано: 20.10.2005 БИ: 29/2005
|
||||||||||||||||||||||||||
