Патент на изобретение №2167857
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ ФЕНИЛАМИДИНА, ИХ ТАУТОМЕРЫ И СТЕРЕОИЗОМЕРЫ, ИХ СМЕСИ, ИХ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИТРОМБОТИЧЕСКИМ И АНТИАГРЕГАТОРНЫМ ДЕЙСТВИЕМ
(57) Реферат: Описываются новые производные фениламидина общей формулы I, где R означает атом водорода, алкил с 1 или 2 атомами углерода или циклогексил, Y – 1,4-пиперидил, их таутомеры и стереоизомеры, включая их смеси, и соли, которые могут представлять собой активное вещество фармацевтической композиции с антитромботическим и антиагрегаторным действием. Описывается фармацевтическая композиция на основе формулы I. 2 с.п.ф-лы, 1 табл. 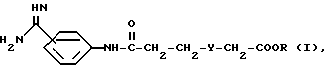
Изобретение относится к новым химическим соединениям с биологической активностью, в частности к новым производным фениламидина, их таутомерам и стереоизомерам, включая их смеси, их соли, фармацевтической композиции с антитромботическим и антиагрегаторным действием. Известны производные фениламидина с биологической активностью, которые могут представлять собой активное вещество фармацевтической композиции с многосторонним действием, в том числе с антитромботическим и антиагрегаторным действием (см. заявку ЕР N 0 381 033, кл. C 07 C 311/19, A 61 K 31/16, опуб. 08.08.1990 г.). Задачей изобретения является разработка новых производных фениламидина, которые могут представлять собой активное вещество фармацевтической композиции с антитромботическим и антиагрегаторным действием. Поставленная задача решается предлагаемыми производными фениламидина общей формулы (I) 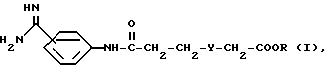 где R означает атом водорода, алкил с 1 или 2 атомами углерода или циклогексил; Y означает 1,4-пиперидинилен, их таутомерами и стереоизомерами, включая их смеси, и соли. Новые соединения общей формулы (I) можно получать известными способами, например, по следующему способу. Соединение формулы (II) 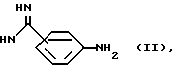 подвергают взаимодействию с соединением общей формулы (III) 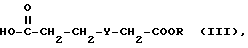 где R и Y имеет вышеуказанное значение, или его реакционноспособными производными, а затем в случае необходимости радикал R переводят в атом водорода. В качестве реакционноспособных производных соединения общей формулы (III) пригодны, например, его хлорангидриды, азидангидриды, смешанные ангидриды с алифатическими или ароматическими карбоновыми кислотами, или сложные моноэфиры угольной кислоты, их имидазолиды и их сложные эфиры, такие как, например, сложные алкиловые эфиры, сложные ариловые эфиры и сложные аралкиловые эфиры, такие как, например, сложный метиловый эфир, сложный этиловый эфир, сложный изопропиловый эфир, сложный пентиловый эфир, сложный фениловый эфир, сложный нитрофениловый эфир или сложный бензиловый эфир. Взаимодействие осуществляют целесообразно в среде растворителя или смеси растворителей, такого как, например, метиленхлорид, диметилформамид, диметилсульфоксид, бензол, толуол, хлорбензол, тетрагидрофуран, пиридин, смесь пиридина и диметилформамида, смесь бензола и тетрагидрофурана или диоксан, в случае необходимости в присутствии обезвоживающего агента, такого как, например, сложный изобутиловый эфир хлормуравьиной кислоты, тионилхлорид, триметилхлорсилан, серная кислота, метансульфокислота, п-толунилхлорид, триметилхлорсилан, серная кислота, метансульфокислота, п-толуолсульфокислота, трихлорид фосфора, фосфорный ангидрид, N,N’-дициклогексилкарбодиимид, смесь N, N’- дициклогексилкарбодиимида и N-гидроксисукцинимида, соль-2-(1H- бензтриазолил)-1,1,3,3-тетраметил-урония, N, N’-карбонилдиимидазол, N,N’-тионилдиимидазол или смесь трифенилфосфина и тетрахлоруглерода, в случае необходимости в присутствии диметиламинопиридина или 1-гидроксибензтриазола и/или основания, такого как, например, триэтиламин, N-этилдиизопропиламин, пиридин или N-метилморфолин, целесообразно при температурах между -10 и 180oC, предпочтительно при температурах между 0 и 120oC. Последующий перевод радикала R в атом водорода осуществляют целесообразно или в присутствии кислоты, такой как, например, соляная кислота, серная кислота, фосфорная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, или в присутствии смесей этих кислот, или в присутствии основания, такого как, например, гидроокись лития, гидроокись натрия или гидроокись калия в среде пригодного растворителя, такого как, например, вода, смесь воды и метанола, смесь воды и этанола, смесь воды и изопропанола, метанол, этанол, смесь воды и тетрагидрофурана или смесь воды и диоксана, при температурах между -10 и 120oC, например, при температурах между комнатной температурой и температурой кипения реакционной смеси. При вышеуказанных реакциях имеющиеся реакционноспособные группы, такие как карбоксил, амино- или амидиногруппы, во время реакции можно защищать обычными защитными группами, которые снимаются по завершении реакции. В качестве защитного остатка для карбоксильной группы можно применять, например, триметилсилил, метил, этил, трет.бутил, бензил или тетрагидропиранил, в качестве защитного остатка для амидиногруппы – бензилоксикарбонил и в качестве защитного остатка для аминогруппы – формил, ацетил, трифторацетил, этоксикарбонил, трет.бутоксикарбонил, бензилоксикарбонил, бензил, метоксибензил, 2,4-диметоксибензил или фталил. Возможное последующее снятие использованного защитного остатка осуществляют, например, путем гидролиза в среде водного растворителя, такого как, например, вода, смесь изопропанола и воды, смесь уксусной кислоты и воды, смесь тетрагидрофурана и воды или смесь диоксана и воды, в присутствии кислоты, такой как, например, трифторуксусная кислота, соляная кислота или серная кислота, или в присутствии щелочного основания, такого как, например, гидроокись натрия или калия, или путем расщепления простого эфира, например, в присутствии триметилсилана йода, при температурах между 0 и 120oC, предпочтительно при температурах между 10 и 100oC. Снятие бензилового, метоксибензилового или бензилоксикарбонилового остатка осуществляют, например, путем гидрогенолиза, например, водородом в присутствии катализатора, такого как палладия на угле в среде растворителя, такого как, например, метанол, этанол, сложный этиловый эфир уксусной кислоты или ледяная уксусная кислота, в случае необходимости с добавкой кислоты, как соляная кислота, при температурах между 0 и 100oC, предпочтительно при температурах между 20 и 60oC, при давлении водорода 1 – 7 бар, предпочтительно 3 – 5 бар. Снятие 2,4-диметоксибензилового остатка осуществляют предпочтительно в среде трифторуксусной кислоты в присутствии анизола. Снятие трет.бутилового или трет.бутилоксикарбонилового остатка осуществляют предпочтительно путем обработки кислотой, такой как, например, трифторуксусная кислота или соляная кислота, или путем обработки триметилсиланом йода, в случае необходимости при использовании растворителя, такого как, например, метиленхлорид, диоксан, метанол или простой эфир. Снятие трифторацетилового остатка предпочтительно осуществляют путем обработки кислотой, как соляной, в случае необходимости в присутствии растворителя, такого как, например, уксусная кислота или метанол, при температурах между 50 и 120oC или путем обработки натровым щелоком, в случае необходимости в присутствии растворителя, такого как, например, тетрагидрофуран или метанол, при температурах между 0 и 50oC. Снятие фталилового остатка предпочтительно осуществляют в присутствии гидразина или первичного амина, такого как, например, метиламин, этиламин или н-бутиламин, в среде растворителя, такого как, например, метанол, этанол, изопропанол, смесь толуола и воды или диоксан, при температурах между 20 и 50oC. Кроме того, полученные соединения общей формулы (I) можно разделять на их энантиомеры и/или диастереомеры. Так, например, смеси цис-/транс-изомеров можно разделять на отдельные цис- и транс-изомеры, а соединения по крайней мере с одним активным атомом углерода – на отдельные энантиомеры. Так, например, полученные смеси цис-/транс-изомеров можно разделять путем хроматографии на отдельные цис- и транс-изомеры, полученные соединения общей формулы (I), имеющиеся в виде рацематов, по общеизвестным методам (см. Аллингер Н. Л. и Эдиел Э.Л. в “Topics in Stereochemistry”, том 6, Вайли Интерсайенс, 1971) – на оптические антиподы, а соединения общей формулы (I) по крайней мере с двумя асимметричными атомами углерода на основе своих физико-химических различий по общеизвестным методам, например, путем хроматографии и/или фракционной кристаллизации – на диастереомеры, которые, если они имеются в виде рацематов, можно потом, как вышеуказано, разделять на энантиомеры. Разделение энантиомеров предпочтительно осуществляют путем колоночной хроматографии на хиральных фазах или путем перекристаллизации из оптически активного растворителя, или путем взаимодействия с образующим с рацемическим соединением соли или производные как, например, сложные эфиры или амиды, оптически активным веществом, в частности кислотой и их активированными производными или спиртами, и путем разделения получаемой таким образом диастереомерной смеси солей или производного, например на основе различной растворимости, причем из чистых диастереомерных солей или производных можно освобождать свободные антиподы путем воздействия подходящих средств. Особо применяемыми оптически активными кислотами являются, например, D- или L-формы винной кислоты или дибензоилвинной кислоты, диотолилвинная кислота, яблочная кислота, миндальная кислота, камфорная сульфокислота, глутаминовая кислота, аспарагиновая кислота или хинная кислота. В качестве оптически активного спирта можно назвать, например, (+)- или (-)-ментол, а в качестве оптически активного ацилового остатка в амидах – например, (+)- или (-)-ментилоксикарбонил. Кроме того, получаемые соединения формулы (I) могут переводить в их соли, в частности для фармацевтического применения в их физиологически переносимые соли с неорганическими или органическими кислотами. В качестве кислот можно применять такие как, например, соляная кислота, бромистоводородная кислота, серная кислота, фосфорная кислота, фумаровая кислота, янтарная кислота, молочная кислота, лимонная кислота, винная кислота или малеиновая кислота. Кроме того, получаемые таким образом новые соединения формулы (I), если последние содержат карбоксил, при желании затем переводят в их соли с неорганическими или органическими основаниями, в частности для фармацевтического применения в их физиологически переносимые соли. В качестве оснований можно применять, например, гидроокись натрия, гидроокись калия, аргинин, циклогексиламин, этаноламин, диэтаноламин и триэтаноламин. Применяемые в качестве исходных веществ соединения отчасти известны из литературы или их можно получать по общеизвестным из литературы методам (см. примеры). Вторым объектом изобретения является фармацевтическая композиция с антитромботическим и антиагрегаторным действием, которая помимо одного или нескольких инертных носителей и/или разбавителей содержит производное фениламидина вышеприведенной общей формулы (I) или его физиологически переносимую соль в эффективном количестве. Биологическое действие соединений общей формулы (I), которые относятся к категории малотоксичных веществ, исследовали, например, нижеописанным образом. 1. Торможение связывания 3H-BIBU 52 с тромбоцитами человека В суспензию тромбоцитов человека в плазме добавляют 3H-BIBU 52 [=(3S, 5S)-5-[(4′-амидино-4-бифенилил)оксиметил] -3- [(карбоксил)метил]-2-пирролидинон [3-3Н-4-бифенилил] ] , заменяющий известный из литературы лиганд 125J-фибриноген (см. заявку на патент ФРГ A-4214245), и инкубируют с разными концентрациями исследуемых соединений. Свободный и связанный лиганды разделяют путем центрифугирования и их количество определяют путем сцинтилляции. На основе результатов опыта определяют торможение связывания 3H-BIBU 52 исследуемым соединением. Для осуществления опыта путем прокола антикубитальной вены извлекают кровь, которую для задержки свертывания обрабатывают тринатрийцитратом (конечная концентрация: 13 ммоль). Кровь подвергают центрифугированию при 170 x g в течение 10 минут. Богатую тромбоцитами плазму удаляют, и остаточную кровь для получения плазмы еще раз подвергают центрифугированию. Богатую тромбоцитами плазму разбавляют аутогенной плазмой в соотношении 1:10, 750 мкл полученной жидкости вместе с 50 мкл физиологического раствора поваренной соли, 100 мкл раствора исследуемого соединения, 50 мкл 14C-сахарозы (3700 Бк) и 50 мкл 3H-BIBU 52 (конечная концентрация: 5 нмоль) инкубируют при комнатной температуре в течение 20 минут. Для определения неспецифического связывания вместо исследуемого соединения используют 5 мкл BIBU 52 (конечная концентрация: 30 мкмоль). Пробы подвергают центрифугированию при 10000 x g в течение 20 сек, надосадочную жидкость удаляют. 100 мкл данной жидкости подвергают измерению для определения свободного лиганда. Продукт центрифугирования растворяют в 500 мкл 0,2 н. гидроокиси натрия, к 450 мкл получаемого раствора добавляют 2 мл сцинтилляционной жидкости и 25 мкл 5 н. соляной кислоты и измеряют. Еще имеющуюся в продукте центрифугирования плазму определяют исходя из содержания 14C, а связанный лиганд – исходя из 3H. После вычитания неспецифического связывания сравнивают активность центрифугата с концентрацией исследуемого соединения и определяют ту концентрацию, при которой исследуемое соединение задерживает связывание 3H BIBU 52 на 50% (концентрацию торможения KT50). 2. Антитромбические действия Методика Агрегацию тромбоцитов определяют по методу Борн и Кросс (J. Physiol., 170, стр. 397, 1964 г.) на богатой тромбоцитами плазме здоровых людей. Для задержки свертывания к крови добавляют 3,14%-ный цитрат натрия в объемном соотношении 1:10. Индуцированная коллагеном агрегация Снижение оптической плотности суспензии тромбоцитов измеряют фотометрически и регистрируют после добавления вызывающего агрегацию вещества. Скорость агрегации определяют на основе угла наклона кривой плотности. Точка кривой, показывающая наибольшую светопроницаемость, служит для расчета оптической плотности. Количество коллагена выбирают как можно более маленьким, но достаточным для получения необратимой кривой реакции. Используют имеющийся в торговле коллаген фирмы Гормонхеми, г. Мюнхен/DE. Перед добавлением коллагена плазму вместе с исследуемым соединением инкубируют при температуре 37oC в течение 10 минут. На основе кривых по концентрациям и действию определяют эффективную дозу ЭД50 в нмоль, т.е., дозу, при которой достигается 50%-ное торможение изменения оптической плотности. Результаты опыта приведены в таблице. Благодаря тормозящему действию на взаимодействие между клетками или между клетками и матрицами новые соединения общей формулы (I) и их физиологически переносимые соли пригодны для лечения и профилактики болезней, при которых возникают агрегации клеток разного размера, или при которых некоторую роль играет взаимодействие между клетками и матрицами, например, для борьбы и профилактики венозных и артериальных тромбозов, церебрососудистых болезней, эмболии легочной артерии или ее ветвей, инфаркта миокарда, артериосклероза, остеопороза и метастазирования опухолей или лечения генетически обусловленных или приобретенных нарушений взаимодействия между клетками или между клетками и твердыми структурами. Кроме того, данные соединения пригодны для сопутствующего лечения при тромболизе при использовании фибринолитических лекарств или при вмешательстве в сосуды, например, при чрезкожной баллоной ангиопластике коронарных артерий, а также для лечения в случае состояния шока, псориаза, диабета и воспалений. Для лечения и профилактики вышеуказанных болезней новые соединения применяют в дозах между 0,1 мкг и 30 мг на кг веса тела, предпочтительно 1 мкг – 15 мг на кг веса тела, при 1 – 4 дозах в день. Для этого новые соединения общей формулы (I) можно переводить в известные препараты, например, таблетки, драже, капсулы, порошки, суспензии, растворы, аэрозоли или суппозитории, в случае необходимости, в сочетании с другими активными веществами, например, антагонистами рецептора тромбоксана или задерживающими синтез тромбоксана веществами или их смесью, антагонистами серотонина, антагонистами  -рецепторов, алкилнитратами, например, тринитратом глицерина, веществами, задерживающими фосфодиэстеразу, простациклином и их аналогами, фибринолитическими лекарствами, например, активатором плазминогена ткани, проурокиназой, урокиназой, стрептокиназой или тормозящими свертывание лекарствами, например, гепарином, сульфатом дерматана, активированным белком C, антагонистами витамина K, гирудином, ингибиторами тромбина или других активированных факторов свертывания, вместе с одним или некоторыми известными инертными носителями и/или разбавителями, например, кукурузным крахмалом, лактозой, сахарозой, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, смесью воды и этанола, смесью воды и глицерина, смесью воды и сорбита, смесью воды и полиэтиленгликоля, пропиленгликолем, стеариловым спиртом, карбоксиметилцеллюлозой или содержащими жир веществами, например, отверженным жиром, или их пригодными смесями.
Нижеследующие примеры поясняют получение соединений формулы (I).
Пример 1 -рецепторов, алкилнитратами, например, тринитратом глицерина, веществами, задерживающими фосфодиэстеразу, простациклином и их аналогами, фибринолитическими лекарствами, например, активатором плазминогена ткани, проурокиназой, урокиназой, стрептокиназой или тормозящими свертывание лекарствами, например, гепарином, сульфатом дерматана, активированным белком C, антагонистами витамина K, гирудином, ингибиторами тромбина или других активированных факторов свертывания, вместе с одним или некоторыми известными инертными носителями и/или разбавителями, например, кукурузным крахмалом, лактозой, сахарозой, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, смесью воды и этанола, смесью воды и глицерина, смесью воды и сорбита, смесью воды и полиэтиленгликоля, пропиленгликолем, стеариловым спиртом, карбоксиметилцеллюлозой или содержащими жир веществами, например, отверженным жиром, или их пригодными смесями.
Нижеследующие примеры поясняют получение соединений формулы (I).
Пример 14-[2-[(Амидинофенил)аминокарбонил] этил]-1-[(карбоксиметил]- пиперидин х 0,2 H2O К 420 мг 4-аминобензамидин-дигидрохлорида и 20 мг 4- диметиламинопиридина в смеси 1,5 мл диметилформамида и 1,5 мл пиридина добавляют 720 мг гидрохлорида 4-[2-(хлоркарбонил)этил]-1- этоксикарбонил)метил]пиперидина и перемешивают при 100oC в течение 80 минут. Реакционную смесь охлаждают, смешивают с ледяной водой, подщелачивают натровым щелоком и экстрагируют простым трет.бутил- метиловым эфиром и метиленхлоридом. Водную фазу подщелачивают соляной кислотой до значения pH 3 – 4 и упаривают досуха при температуре бани 70oC. Остаток в 100 мл этанола нагревают до кипения, а после охлаждения фильтруют, после чего фильтрат сгущают. Остаток упаривания нагревают с 30 мл этанола, затем охлаждают, и твердое вещество отсасывают. Твердое вещество перемешивают с 15 мл тетрагидрофурана и 4,5 мл 1 н. натрового щелока. К смеси прибавляют 2,75 мл 1 н. соляной кислоты, затем перемешивают в ледяной бане. Осадок промывают водой и тетрагидрофураном и сушат в вакууме. Выход: 144 мг (21% теории) Точка плавления: 283oC (разл.) Значение Rf: 0,76 (силикагель для обратнофазной хроматографии; элюент: смесь метанола и 5%-ного раствора поваренной соли в соотношении 6:4) Рассч.: C 60,77 H 7,32 N 16,67 Найд.: 60,55 7,26 16,83 Масс-спектр: (M+H)+ = 333. Исходный гидрохлорид 4-[2-(хлоркарбонил)этил]-1 – [(этоксикарбонил)метил]-пиперидина получают следующим образом. К 1,46 г 4-(2-карбоксиэтил)-1-[(этоксикарбонил)метил]- пиперидина в 10 мл метиленхлорида добавляют при перемешивании 1 мл насыщенной эфирной соляной кислоты. Прибавляют 1,2 г тионилхлорида и перемешивают при комнатной температуре в течение 3 часов. Реакционную смесь сгущают, к остатку два раза добавляют толуол, причем каждый раз снова сгущают. Аналогично примеру 1 получают следующее соединение: (1) 1 -[2-[(4-амидинофенил)аминокарбонил] этил]-4- карбоксиметил-пиперидин x 2H2O Точка плавления: 192 – 200oC (при спекании и разложении) Значение Rf: 0,77 (силикагель для обратнофазной хроматографии; элюент: смесь метанола и 5%-ного раствора поваренной соли в соотношении 6:4) Рассч.: C 55,42 H 7,66 N 15,21 Найд.: 55,02 7,38 14,95. Пример 2 4-[2-[(Амидинофенил)аминокарбонил] этил] -1- [(этоксикарбонил)метил]-пиперидин x 2,15 HCl x 0,7 H2O К 625 мг 4-аминобензамидина и 30 мг 4-диметиламинопиридина в 5 мл пиридина добавляют 950 мг гидрохлорида 4-[2- (хлоркарбонил)этил]-1-этоксикарбонил)метил]пиперидина и перемешивают при 100oC в течение часа. Добавляют 2 мл диметилформамида и перемешивают при 100oC в течение дальнейших 72 минут. Реакционную смесь сгущают, остаток перемешивают два раза с простым трет. бутил-метиловым эфиром, причем каждый раз растворитель декантируют и удаляют. Остаток очищают путем хроматографии на окиси алюминия этанолом. Продукт растворяют в этаноле, слегка подщелачивают эфирной соляной кислотой и сгущают. Остаток растирают с ацетоном, твердое вещество отсасывают и сушат. Выход: 335 мг (25% теории) Значение Rf: 0,35 (окись алюминия; элюент: смесь этанола и концентрированного водного аммиака в соотношении 99:1) Рассч.: C 50,55 H 7,04 N 12,41 Cl 16,88 Найд.: 50,02 6,96 12,51 17,27 Масс-спектр: (M+H)+ = 361. Аналогично примеру 2 получают следующее соединение: (1) 4-[2-[(4-амидинофенил)аминокарбонил]этил]-1- [(циклогексилоксикарбонил)метил]-пиперидин x 2,3 HCl x 2 H2O Точка плавления: начиная с 170oC (разл.) Значение Rf: 0,58 (силикагель для обратнофазной хроматографии; элюент: смесь метанола и 5%-ного раствора поваренной соли в соотношении 6:4) Рассч.: C 51,69 H 7,60 N 10,48 Cl 15,26 Найд.: 51,69 7,46 10,44 15,17. Нижеследующие примеры иллюстрируют возможные препараты предлагаемой фармацевтической композиции. Пример 3 Ампула с сухим стерильным веществом, содержащим 2,5 мг активного вещества на мл Состав: Активное вещество примера 1 – 2,5 мг Маннитол – 50,0 мг Вода для инъекции – До 1,0 мл Получение: Активное вещество и маннитол растворяют в воде. После розлива сушат путем вымораживания. Растворение до получения готового к применению раствора осуществляют с использованием воды для инъекции. Пример 4 Ампула с сухим стерильным веществом, содержащим 35 мг активного вещества на мл Состав: Активное вещество примера 1(1) – 35,0 мг Маннитол – 100,0 мг Вода для инъекции – До 2,0 мл Получение: Активное вещество и маннитол растворяют в воде. После розлива сушат путем вымораживания. Растворение до получения готового к применению раствора осуществляют с использованием воды для инъекции. Пример 5 Таблетка, содержащая 50 мг активного вещества Состав: (1) Активное вещество примера 1 – 50,0 мг (2) Лактоза – 98,0 мг (3) Кукурузный крахмал – 50,0 мг (4) Поливинилпирролидон – 15,0 мг (5) Стеарат магния – 2,0 мг – 215,0 мг Получение: (1), (2) и (3) смешивают и гранулируют вместе с водным раствором (4). После сушки гранулята примешивают (5). Из этой смеси прессуют таблетки с плоской поверхностью и фаской с обеих сторон и делительной засечкой с одной стороны. Диаметр таблетки 9 мм. Пример 6 Таблетка, содержащая 350 мг активного вещества Состав: (1) Активное вещество примера 2 – 350,0 мг (2) Лактоза – 136,0 мг (3) Кукурузный крахмал – 80,0 мг (4) Поливинилпирролидон – 30,0 мг (5) Стеарат магния – 4,0 мг – 600,0 мг Получение: (1), (2) и (3) смешивают и гранулируют вместе с водным раствором (4). После сушки гранулята примешивают (5). Из этой смеси прессуют таблетки с плоской поверхностью и фаской с обеих сторон и делительной засечкой с одной стороны. Диаметр таблетки 12 мм. Пример 7 Капсулы, содержащие 50 мг активного вещества Состав: (1) Активное вещество примера 2 (1) – 50,0 мг (2) Кукурузный крахмал, сушеный – 58,0 мг (3) Лактоза, распыленная – 50,0 мг (4) Стеарат магния – 2,0 мг – 160,0 мг Получение: (1) растирают вместе с (3). Эту смесь при интенсивном перемешивании добавляют к смеси из (2) и (4). Получаемую порошкообразную смесь с помощью дозировочной машины разливают во вставные капсулы размера 3 из твердой желатины. Пример 8 Капсулы, содержащие 350 мг активного вещества Состав: (1) Активное вещество примера 2 (1) – 350,0 мг (2) Кукурузный крахмал, сушеный – 46,0 мг (3) Лактоза, распыленная – 30,0 мг (4) Стеарат магния – 4,0 м – 430,0 мг Получение: (1) растирают вместе с (3). Эту смесь при интенсивном перемешивании добавляют к смеси из (2) и (4). Получаемую порошкообразную смесь с помощью дозировочной машины разливают во вставные капсулы размера 0 из твердой желатины. Формула изобретения
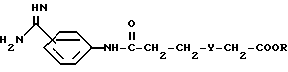 где R означает атом водорода, алкил с 1 или 2 атомами углерода или циклогексил; Y означает 1,4-пиперидинил, их таутомеры и стереоизомеры, включая их смеси, и соли. 2. Фармацевтическая композиция с антитромботическим и антиагрегаторным действием, содержащая активное вещество на основе производных фениламидина и один или несколько инертных носителей и/или разбавителей, отличающаяся тем, что в качестве производного фениламидина она содержит соединение по п.1 или его физиологически переносимую соль в эффективном количестве. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.04.2003
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
