Патент на изобретение №2167856
|
||||||||||||||||||||||||||
(54) СОЛИ ПРОИЗВОДНЫХ АМИДИНА И ИНГИБИТОРА ЦИКЛООКСИГЕНАЗЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ
(57) Реферат: Соли производных амидина и ингибитора циклооксигеназы общей формулы А  В, в которой А – ингибитор циклооксигеназы с карбоксильной функцией; В – соединение общей формулы Iв, в которой R1 – атом водорода, нитро- или фенильный радикал, возможно замещенный одним или несколькими заместителями, выбранными из радикалов галогена, циано, нитро, CF3, низший алкил или низший алкокси; R2 – низший алкил, алкил-тиоалкил, фенил, возможно замещенный одним или несколькими атомами галогена, цикл, содержащий гетероатом, выбранный из атомов серы и кислорода; или амино, который возможно замещен амино или низшим алкилом. Соединения по изобретению обладают двойной биологической активностью, они ингибируют одновременно процесс L-аргинина/окиси азота и процесс циклооксигеназы. 3 с. и 5 з.п.ф-лы, 4 табл. В, в которой А – ингибитор циклооксигеназы с карбоксильной функцией; В – соединение общей формулы Iв, в которой R1 – атом водорода, нитро- или фенильный радикал, возможно замещенный одним или несколькими заместителями, выбранными из радикалов галогена, циано, нитро, CF3, низший алкил или низший алкокси; R2 – низший алкил, алкил-тиоалкил, фенил, возможно замещенный одним или несколькими атомами галогена, цикл, содержащий гетероатом, выбранный из атомов серы и кислорода; или амино, который возможно замещен амино или низшим алкилом. Соединения по изобретению обладают двойной биологической активностью, они ингибируют одновременно процесс L-аргинина/окиси азота и процесс циклооксигеназы. 3 с. и 5 з.п.ф-лы, 4 табл.
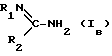
Настоящее изобретение касается новых соединений с двойным биологическим эффектом, при котором они одновременно ингибируют образование окиси азота (NO) и активность циклооксигеназ, способа их получения, фармацевтических композиций на их основе и их использования, в частности в качестве ингибиторов NO-синтазы и циклооксигеназы. Ингибиторы циклооксигеназы или медикаменты, аналогичные аспирину, т.е. ацетилсалициловой и салициловой кислотам, производные метилированного индола, такие как индометацин (DCl уксусной кислоты [1-(4-хлорбензоил)-5-метокси-2-метил-1H-индол-3-ил] ) и сулиндак (DCl уксусной кислоты [5-фтор-2-метил-1-[[4- (метилсульфинил) фенил] метилен]-1H-инден-3-ил]), производные N- фенилантраниловых кислот (меклофенамат, фенаматы), производные пропионовой кислоты, такие как ибупрофен (DCl p-изобутилгидратроповой кислоты), напроксен, фенопрофен, находят широкое применение в качестве эффективных медикаментов при терапии воспалений, которое, правда, сопровождается при повышенных дозах некоторыми побочными нежелательными явлениями (R. Flower, S.Moncada и J. Vane, Mechanism of action of aspirinlike drugs (Механизм воздействия лекарств, аналогичных аспирину). In the pharmacological basis of therapeutics Goodman and Gilman (Фармакологические основы терапии Гудмана и Джильмана), 1985 г., 29 с. 674-715). Кроме того, указанные соединения одновременно применялись при неотложном и профилактическом лечении мигрени. Эффективность данных медикаментов неоспорима, несмотря на то что часто их терапевтические результаты остаются неполными и что для некоторых больных лечение такими соединениями не удавалось. Ввиду своих противовоспалительных свойств и способности предупреждать скопление тромбоцитов указанные соединения применялись, кроме того, при лечении тромбоза и, для заметного снижения отеков, в моделях ишемии мозга, в результате они были предложены для лечения и предупреждения инфарктов, сотрясений и церебрососудистых заболеваний (W. Armstrong Recent trends in research and treatment of stroke, SCRIP, PJB publications (Современные направления в исследовании и терапии инсульта), публикации SCRIP, PJB, 1991 г.). Биологическая активность ингибиторов NO-синтазы была обнаружена лишь недавно и их потенциальное применение в терапевтических целях пока исследуется. Данные вещества, структуры которых представлены аналогами L-аргинина и описаны в патенте Дании 3041/90, являются ингибиторами образования окиси азота (NO). Современные знания об NO подвергались ревизии в 1991 г. со стороны Moncada и др. (S.Monkada, R.M.J. Palmer, E.A. Higgs: Nitric oxide (окись азота): physiology, pathophysiology and pharmacology (физиология, патофизиология и фармакология), Pharmacological Reviews 43,2, с. 109-142), а еще раньше со стороны Kerwin и др. (Kerwin J., Lancaster J., Feidman P., Nitric oxide (окись азота): a new paradigm for second messengers (новый пример вторичных посредников), J. Med. Chem., 1995 г., т.38, 22, с.4343-4362). В сущности, представляется, что NO служит механизмом трансдукции растворимой гуанилатциклазы в тромбоцитах, в нервной системе, а также эффекторной молекулой при иммунологических реакциях в большинстве клеток и тканей, включая макрофаги и нейрофилы. Окись азота производится ферментативно из L-аргинина ферментом под названием “NO-синтаза”. Этот фермент существует в двух формах: конститутивной (эндотелиальной и нейтрональной) и индуктивной. При некоторых патологиях происходит избыточное выделение окиси азота, как это было доказано на примере шока, описанного в упомянутом патенте. В таком контексте ингибиторы NO-синтазы являются эффективными медикаментами, используемыми для предупреждения сосудистых осложнений и смертельного исхода вследствие болезни, в частности, в том случае, когда их применяют в сочетании с ингибиторами циклооксигеназы, такими как аспирин, индометацин и меклофенамат. Благотворное воздействие такой комбинации обоих активных веществ, присутствующих в одной и той же молекуле, может быть достигнуто в отношении пациентов, страдающих другими патологиями, например: сердечно-сосудистые и церебрососудистые нарушения, например, атеросклероз, мигрень, повышение артериального давления, септический шок, инфаркты миокарда и церебральные инфаркты ишемического и геморрагического происхождения, ишемии и тромбозы; расстройства центральной и периферической нервной системы, например, нейродегенеративные болезни, к которым можно отнести, в частности, церебральные инфаркты, старческое слабоумие, в том числе болезнь Альцгеймера, хорея Гентингтона, болезнь Паркинсона, болезнь Крейтцфельда Якоба, амиотрофический боковой склероз, а также ревматические невралгические боли, церебральные травмы или травмы спинного мозга, влечение к содержащим опий веществам, к алкоголю и веществам, вызывающим привыкание, нарушения эрекции и размножения, нарушения познавательной способности, заболевания головного мозга; пролиферативные и воспалительные заболевания, например, атеросклероз, легочная гипертензия, гломерулонефрит, портальная гипертензия, псориаз, артроз и ревматоидный артрит, фиброзы, амилоидозы, воспаления желудочно-кишечной системы (колит, болезнь Крона) или системы легких и дыхательных путей (астма, синуситы); трансплантация органов; аутоиммунные и вирусные заболевания, например, волчанка, СПИД, инфекции, вызываемые паразитами и вирусами, диабет, образование склеротических бляшек; злокачественная опухоль; или любые виды патологии, характеризующиеся образованием или дисфункцией NO и/или циклооксигеназ. Таким образом, объектом изобретения являются соли производных амидина и ингибитора циклооксигеназы общей формулы I: A.B (I) в которой A – ингибитор циклооксигеказы с карбоксильной функцией; B – соединение общей формулы Iв 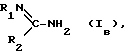 в которой R1 – атом водорода, нитро- или фенильный радикал, при этом фенильный радикал может быть замещен одним или несколькими заместителями, выбранными из радикалов галоген, циано, нитро, трифторметил, низший алкил или низший алкокси; R2 – низший алкил, низший алкилтиоалкил, фенил, который может быть замещен одним или несколькими атомами галогена, цикл, содержащий гетероатом, выбранный из атомов серы и кислорода; или амино, который может быть замещен радикалом, выбранным из радикалов амино или низшего алкила при условии, что: когда A означает ацетилсалициловую кислоту, a R1 – атом водорода, то R2 не является ни фенилом, замещенным или незамещенным, ни циклом, содержащим гетероатом. В приведенных выше определениях термин “галоген” означает радикал фтора, брома или иода, предпочтительно фтора или хлора. Выражение “низший алкил” преимущественно означает алкильный, линейный или разветвленный радикал с 1-6 атомами углерода, в частности, алкильный радикал с 1-4 атомами углерода, такой как метиловый, этиловый, пропиловый, изопропиловый, бутиловый, изобутиловый, втор.-бутиловый и трет.-бутиловый радикал. Низшие алкоксильные радикалы могут соответствовать приведенным выше алкильным радикалам. Предпочтительными радикалами являются метокси, этокси и изопропилокси. Объектом изобретения являются, в частности, продукты приведенной выше общей формулы I, отличающиеся тем, что соединение A выбрано из салицилатов, таких как салициловая кислота и ее производные, индометацин, сулиндак, фенаматы и производные пропионовой кислоты. Из производных салициловой кислоты можно указать на соединения, получаемые этерификацией карбоксильной функции салициловой кислоты, например, салицилат метила, соединения, получаемые замещением гидроксильного радикала салициловой кислоты, например, ацетилсалициловая кислота, или же соединения, получаемые введением заместителя (заместителей) в свободные сайты фенильного радикала салициловой кислоты, например, дифлунизала. Из фенаматов можно указать на мефенаминовую, меклофенаминовую, флуфенаминовую и толфенаминовую кислоты. В качестве примеров производных пропионовой кислоты можно назвать такие соединения, как ибупрофен, напроксен, фенопрофен, фенбуфен, флурбипрофен, индопрофен, кетопрофен и супрофен. Объектом изобретения являются также, в частности, соединения приведенной выше общей формулы I, отличающиеся тем, что – A означает салициловую кислоту, метилсалицилат, ацетилсалициловую кислоту, индометацин, сулиндак, мефенаминовую кислоту, меклофенаминовую кислоту или ибупрофен; – B означает соединение приведенной выше общей формулы (Iв), в которой R1 – атом водорода, нитро- или фенильный радикал, при этом фенильный радикал может быть замещен одним или несколькими заместителями, выбранными из хлора, фтора, циано, нитро, трифторметила, метила, этила, метокси, этокси и изопропилокси; R2 – радикал амино, гидразино, метиламино, этиламино, метил, этил, метилтиометил, фенил, который может быть замещен одним или несколькими атомами галогена. В частности, целью изобретения являются продукты, приводимые ниже в примерах, а именно продукты, отвечающие следующим формулам: – салицилат аминогуанидина; – ибупрофенат аминогуанидина; – индометацинат аминогуанидина; – ацетилсалицилат метилгуанидина; – салицилат метилгуанидина; – ибупрофенат метилгуанидина; – мефенамат метилгуанидина. Объектом изобретения является также способ получения продуктов указанной выше общей формулы I, отличающийся тем, что соединение формулы A подвергают взаимодействию с соединением формулы B в воде при температуре от комнатной до 70oC. При осуществлении способа соединение формулы A может использоваться в том виде, в каком оно есть, или в виде соли, например, натриевой. Также соединение формулы В может использоваться, как оно есть, или в виде, например, его бикapбoнaтa или гидрохлорида. Продукты формулы A являются известными и могут быть получены методами, известными среднему специалисту. Продукты формулы В могут быть получены посредством способов получения амидинов, известных специалисту. (Schwan T.J. и сотр. , J. Pharm.Sci., 1975, N 64, стр. 337-338; Roger R. и сотр., Chem. Rev. , 61, 179, 1961 г.; Tetrahedron, 29(14), 2147-2151, 1973 ” Patai S., Chem. Amidines Imidates, т.I, стр. 283-348, 1975 г., Patai S., Chem.Amidines Imidates, т. 2, стр. 339-366, 1990 г.). Соединения согласно изобретению характеризуются интересными фармакологическими свойствами. Они обладают двойной биологической активностью, а именно они ингибируют одновременно процесс L-аргинина/окиси азота (NO) и процесс циклооксигеназы. Соединения согласно данному изобретению могут найти применение в различных областях терапии. Учитывая потенциальную роль NO-синтазы и циклооксигеназы в физиопатологии, соединения согласно изобретению могут вызывать положительное, благотворное влияние при лечении: – сердечно-сосудистых и церебрососудистых нарушений, например, мигрени, гиперемии мозга, инфарктов, ишемической болезни, септических, эндотоксических и геморрагических шоков, боли; – разных форм воспаления, например, острой ревматической атаки, ревматоидного артрита и других видов артрита, остеоартрита, астмы; – расстройств иммунной системы, включающих инфекции вирусного и не вирусного происхождения, аутоиммунных заболеваний и любых патологий, характеризующихся избыточной выработкой окиси азота и/или метаболитов арахидоновой кислоты. Ниже, в экспериментальной части, приводится иллюстрация фармакологических свойств соединений согласно изобретению. Упомянутые свойства обеспечивают продуктам формулы I пригодность для применения в фармации. Настоящая заявка касается также соединений приведенной выше формулы I в качестве медикаментов, а также фармацевтических композиций, содержащих в качестве активного начала, по меньшей мере, один из медикаментов, описанных выше. Изобретение касается, кроме того, фармацевтических композиций, содержащих соединение согласно изобретению формулы I в эффективном количестве в сочетании с фармакологически приемлемым носителем. Фармацевтическая композиция может иметь вид твердого тела, например, порошка, гранул, таблеток, капсул или суппозиториев. Соответствующими твердыми носителями могут быть, например, фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, амидон, желатин, целлюлоза, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидин и воск. Фармацевтические композиции, содержащие соединения согласно изобретению, могут также быть жидкими, например растворами, эмульсиями, суспензиями и сиропами. Соответствующими жидкими носителями могут быть, например, вода, органические растворители, такие как глицерин или гликоли, а также их смеси с водой в разной пропорции, добавляемые в фармацевтически приемлемые масла и жиры. Фармацевтические композиции согласно изобретению могут назначаться, в частности, орально или посредством внутримышечной, внутрибрюшинной, внутривенной или подкожной инъекции. Объектом изобретения является также применение продуктов приведенной выше формулы I для получения медикаментов для лечения сердечно-сосудистых и церебрососудистых нарушений, разных форм воспаления и расстройств иммунной системы. Следующие примеры приведены для иллюстрации упомянутых выше процедур и ни в коем случае не ограничивают объема изобретения. Экспериментальная часть: ПРИМЕР 1: Салицилат аминогуанидина 420 мг (2,5 ммоля) аминогуанидина бикарбоната растворяли в 25 мл воды с подогревом до 70oC, добавляли при встряхивании водный раствор 400 мг салицилата натрия. Смесь нагревали в течение 20 минут и затем производили лиофилизацию (порошок белого цвета, точка плавления: 148oC). ПРИМЕР 2: Ибупрофенат аминогуанидина 420 мг (2,5 ммоля) аминогуанидина бикарбоната растворяли в 25 мл воды с подогревом до 70oC. Добавляли при встряхивании водный раствор 570 мг натриевой соли ибупрофена. Продолжали нагрев в течение 20 минут и затем производили лиофилизацию (порошок белого цвета, точка плавления: 134oC). ПРИМЕР 3: Индометацинат аминогуанидина Поступали, как описано в примере 1, но применяли индометацин вместо салицилата натрия (порошок белого цвета, точка плавления: 196oC). ПРИМЕР 4: Ацетилсалицилат метилгуанидина 450 мг (2,5 ммоля) ацетилсалициловой кислоты растворяли в 20 мл воды с содержанием 2,5 мл 1N NaOH. Затем добавляли 237,8 мг хлоргидрата метилгуанидина в 10 мл воды. Продолжали перемешивать в течение 15 минут. Получали прозрачный раствор. После лиофилизации образовывался порошок белого цвета (точка плавления: 153oC). 1H-ЯМР (100 МГц, 020): 7.3-6.6 (m, 4H, ароматический); 2.3 (s, 3H, NCH3); 1.8 (s, 3H, COCH3). ПРИМЕР 5: Салицилат метилгуанадина 345 мг (2,5 ммоля) салициловой кислоты в горячем виде растворяли в 20 мл воды с содержанием 2,5 мл 1N NaOH. Затем добавляли раствор хлоргидрата метилгуанидина (2,5 ммоля) в 10 мл воды. Продолжали перемешивать при 40oC в течение 10 минут. После лиофилизации получали порошок белого цвета (точка плавления: 140oC). 1H-ЯМР (100 МГц, D2O): 7-6.8 (m,4H, ароматический); 2.4 (s, 3H, NCH3). ПРИМЕР 6: Ибупрофен метилгуанидина 2,5 ммоля ибупрофена в горячем виде растворяли в 20 мл воды с содержанием 2,5 мл 1N NaOH. Добавляли раствор хлоргидрата метилгуанидина (2,5 ммоля) в 10 мл воды. Подогревали при перемешивании до 60oC в течение 15 минут. После лиофилизации получали порошок белого цвета (точка плавления: 174oC). 1H-ЯМР (100 МГц, D2O): 7.2 (s, 4H, ароматический); 3.4 (q, 1H, 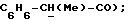 2.6 (s, 3H, NCH3); 2.25 (d, 2H, 2.6 (s, 3H, NCH3); 2.25 (d, 2H, 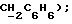 1.6 (m, 1H, 1.6 (m, 1H, 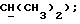 1.2 (d, 3H, -CH(CH3)-CO2H); 0.8 (d, 6H, 2CH3).
ПРИМЕР 7: Мефенамат метилгуанидина 1.2 (d, 3H, -CH(CH3)-CO2H); 0.8 (d, 6H, 2CH3).
ПРИМЕР 7: Мефенамат метилгуанидинаПоступали, как описано в примере 6, но применяли мефенаминовую кислоту вместо ибупрофена. При охлаждении соединение выпадало в осадок. Продукт фильтровали и сушили (точка плавления: 124oC). 1H-ЯМР (100 МГц, D2O): 8.1 (m, 1H, H в OdeCO3H); 7.2-6.8 (m, 6H, 2C6H6); 2.9 (s, 3H, NCH3); 2.4 и 2.3 (d, 2CH3C6H6). Применяя указанный выше способ, можно также получать следующие продукты, которые относятся к изобретению и являются предпочтительными (см. табл.1). Фармакологическое исследование продуктов согласно изобретению. Соединения согласно изобретению подвергали биологическим тестам in vitro с целью получения доказательства их активности при блокировании индуцируемой NO-синтазы и циклооксигеназы. Их сопоставляли с эталонными веществами, такими как аминогуанидин, L-нитроаргинин, ибупрофен, индометацин, ацетилсалициловая кислота. 1) Воздействие in vitro на индуцируемую NO-синтазу мышиных макрофагов J774A1: Тест состоял в измерении степени превращения под действием NO-синтазы L-аргинина в L-цитруллин методом Бредта и Снайдера (Bredt, Snyder) (Proceedings of the National Academy of Sciences USA (Труды Национальной академии наук США), 87, с. 682-685, 1990 г.). Мышиные макрофаги J774AI вырабатывают в большом количестве окись азота после активирования посредством липополисахаридов (LPS) и  – интерферона (IFN- – интерферона (IFN-  ). После активации под действием LPS и IFN- ). После активации под действием LPS и IFN-  клетки культивировали в среде DMEM (Модифицированная Дульбекко среда Игла), обогащенной 10% эмбриональной телячьей сывороткой при 37oC в атмосфере с содержанием 5% CO2. Посев производили из расчета 5000 клеток на см2 в склянки площадью 150 см2. Инкубация протекала в присутствии LPS (1 мкг/мл) и мышиного IFN- клетки культивировали в среде DMEM (Модифицированная Дульбекко среда Игла), обогащенной 10% эмбриональной телячьей сывороткой при 37oC в атмосфере с содержанием 5% CO2. Посев производили из расчета 5000 клеток на см2 в склянки площадью 150 см2. Инкубация протекала в присутствии LPS (1 мкг/мл) и мышиного IFN-  (50 ед./мл) в среде DMEM, обогащенной 10% эмбриональной телячьей сывороткой. NO-синтазу выделяли в экстракционном буферном растворе (HEPES 50 ммолей, pH 7,4, дитиотреитол 0,5 ммоля, пепстатин A 1 мг/мл, лейпептин 1 мг/мл, соевый ингибитор трипсина 1 мг/мл, антипаин 1 мг/мл и PMSF 10 мг/мл). После ультразвуковой обработки в экстракционном буферном растворе при 4oC гомогенаты подвергали ультрацентрифугированию (100000 g при 4oC в течение 1 часа).
Дозы помещали в стеклянные пробирки, в которые вводили 100 мкл инкубационного буфера с содержанием 100 ммолей HEPES, pH 7,4, 1 ммоль дитиотреитола, 2,5 ммоля CaCl2, 10 мкмолей тетрагидробиоптерина, 10 мкмолей FAD, 1 мг/мл BSA, 2 ммоля восстановленного NADPH, 2 ммоля EDTA и 2,5 ммоля CaCl2. Добавляли 26 мкл раствора с содержанием 100 нмолей меченого тритием аргинина (с удельной активностью 56,4 Ки/ммоль, Amersham) и 40 мкмолей нерадиоактивного аргинина. Реакцию инициировали добавкой 50 мкл гомогената, при этом окончательный объем составил 200 мкл (недостающие 25 мкл приходятся либо на воду, либо на испытуемый продукт). Через 15 мин реакцию останавливали введением 2 мл блокирующего раствора (20 ммолей HEPES, pH 5,5, 2 ммоля EDTA). После прохождения проб через колонку с 1 мл смолы DOWEX радиоактивность в жидком сцинтилляционном растворе измеряли спектрометром.
Результаты выразили величиной CI50 и свели в таблицу раздела 2 (первая графа результатов озаглавлена “Индуцируемая NO-синтаза, образование цитруллина”).
2) Воздействие in vitro на производство нитритов мышиными макрофагами J774Al: (50 ед./мл) в среде DMEM, обогащенной 10% эмбриональной телячьей сывороткой. NO-синтазу выделяли в экстракционном буферном растворе (HEPES 50 ммолей, pH 7,4, дитиотреитол 0,5 ммоля, пепстатин A 1 мг/мл, лейпептин 1 мг/мл, соевый ингибитор трипсина 1 мг/мл, антипаин 1 мг/мл и PMSF 10 мг/мл). После ультразвуковой обработки в экстракционном буферном растворе при 4oC гомогенаты подвергали ультрацентрифугированию (100000 g при 4oC в течение 1 часа).
Дозы помещали в стеклянные пробирки, в которые вводили 100 мкл инкубационного буфера с содержанием 100 ммолей HEPES, pH 7,4, 1 ммоль дитиотреитола, 2,5 ммоля CaCl2, 10 мкмолей тетрагидробиоптерина, 10 мкмолей FAD, 1 мг/мл BSA, 2 ммоля восстановленного NADPH, 2 ммоля EDTA и 2,5 ммоля CaCl2. Добавляли 26 мкл раствора с содержанием 100 нмолей меченого тритием аргинина (с удельной активностью 56,4 Ки/ммоль, Amersham) и 40 мкмолей нерадиоактивного аргинина. Реакцию инициировали добавкой 50 мкл гомогената, при этом окончательный объем составил 200 мкл (недостающие 25 мкл приходятся либо на воду, либо на испытуемый продукт). Через 15 мин реакцию останавливали введением 2 мл блокирующего раствора (20 ммолей HEPES, pH 5,5, 2 ммоля EDTA). После прохождения проб через колонку с 1 мл смолы DOWEX радиоактивность в жидком сцинтилляционном растворе измеряли спектрометром.
Результаты выразили величиной CI50 и свели в таблицу раздела 2 (первая графа результатов озаглавлена “Индуцируемая NO-синтаза, образование цитруллина”).
2) Воздействие in vitro на производство нитритов мышиными макрофагами J774Al:Данный тест использовали для измерения ингибирующей активности продуктов на NO-синтазу, индуцируемую клетками в культуре. Клетку культивировали в среде DMEM (Dulbecco’s Modfied Eagle’s Medium), обогащенной 10% эмбриональной телячьей сывороткой при 37oC в атмосфере с содержанием 5% CO2. Для проведения опытов их располагали на планшетах с 96 лунками (50000 клеток на 1 лунку) и инкубировали в среде DMEM без фенольного красного в присутствии 10% эмбриональной телячьей сыворотки, LPS (1 мкг/мл) и мышиного IFN-  (50 ед. /мл) в присутствии или в отсутствие испытуемых продуктов. Через 48 часов в культуральных средах замеряли концентрацию нитритов, образовавшихся в результате разложения NO, с помощью колориметрического метода по Green и др. Analytical Biochemistry 126, стр. 131-138, 1982 г.). Результаты были выражены величиной CI50 и представлены в таблице 2 раздела 2 (вторая графа результатов озаглавлена “Индуцируемая NO-синтаза, образование нитритов”) (см. табл. 2).
3) Воздействие in vitro на производство нитритов и PGE2 микроглиальными клетками крысы (50 ед. /мл) в присутствии или в отсутствие испытуемых продуктов. Через 48 часов в культуральных средах замеряли концентрацию нитритов, образовавшихся в результате разложения NO, с помощью колориметрического метода по Green и др. Analytical Biochemistry 126, стр. 131-138, 1982 г.). Результаты были выражены величиной CI50 и представлены в таблице 2 раздела 2 (вторая графа результатов озаглавлена “Индуцируемая NO-синтаза, образование нитритов”) (см. табл. 2).
3) Воздействие in vitro на производство нитритов и PGE2 микроглиальными клетками крысыМикроглиальные клетки выделяли из культур глиальных клеток, полученных из коры головного мозга новорожденной крысы Wistar по протоколу Thery и сотр. (1991). Микроглиальные клетки высевали на планшетах с 24 лунками из расчета по 5  105 клеток на 1 мл и 0,5 мл на лунку. Микроглиальные клетки инкубировали в присутствии LPS (10 мкг/мл) и ингибиторов в течение 24 часов при 37oC в атмосфере с содержанием 5% CO2. Через 24 часа отбирали надосадочную жидкость с целью измерения концентрации нитритов и PGE2. PGE2 дозировали с помощью коммерческого радиоиммунологического дозатора NEN по инструкции изготовителя. Для каждого образца ставили по две параллельные пробы. Результаты выражены в виде CI50 и рассчитаны с помощью линейной регрессии на линейном участке кривой ингибирования (программное обеспечение FigP6C). Дозирование нитритов проводилось по методу Green и др. (Analytical Biochemistry 126, стр. 131-138, 1982 г.).
Результаты были выражены в виде Cl50 и представлены в таблице 3 примера 2.
4) Воздействие in vitro на индуцируемую циклооксигеназу: 105 клеток на 1 мл и 0,5 мл на лунку. Микроглиальные клетки инкубировали в присутствии LPS (10 мкг/мл) и ингибиторов в течение 24 часов при 37oC в атмосфере с содержанием 5% CO2. Через 24 часа отбирали надосадочную жидкость с целью измерения концентрации нитритов и PGE2. PGE2 дозировали с помощью коммерческого радиоиммунологического дозатора NEN по инструкции изготовителя. Для каждого образца ставили по две параллельные пробы. Результаты выражены в виде CI50 и рассчитаны с помощью линейной регрессии на линейном участке кривой ингибирования (программное обеспечение FigP6C). Дозирование нитритов проводилось по методу Green и др. (Analytical Biochemistry 126, стр. 131-138, 1982 г.).
Результаты были выражены в виде Cl50 и представлены в таблице 3 примера 2.
4) Воздействие in vitro на индуцируемую циклооксигеназу:Циклооксигеназа существует в двух изоформах: COX-1 (конститутивной) и COX-2, индуцируемой митогенными, цитокинными и эндотоксинными воспалительными агентами. Соединения тестировали на ферментативную активность обеих полуочищенных изоформ. Принцип теста заключался в количественном определении степени превращения арахидоновой кислоты (AA) в PGE2 посредством COX-1 и COX-2. Метод был предложен Futaki и др. (Prostagiandins, 47, стр. 55-59, 1994 г.). COX-1 (синтаза-1 простагландина H, EC 1.14.9.1) хранилась при -80oC и была получена из семенного пузырька барана. COX-2 (синтаза-2 простагландина H) также хранилась при -80oC и получена из плаценты овцы. Пробирки заполняли 500 мкл буферного раствора (100 ммолей Tris-HCl, pH 8, 1 мкмоль гематина, 1 ммоль фенола) и соединениями согласно изобретению или эталонными веществами при концентрациях от 1 нмоля до 1 ммоля. Контрольными пробами служил буферный раствор без содержания ингибиторов. Через 2 минуты инкубации с использованием 5 ед. (COX-2) и 10 ед. (COX-1) фермента добавляли 5 мкл арахидоновой кислоты при 10 мкмолях и выдерживали в течение 2 минут. Реакцию останавливали добавлением 30 мкл 1N соляной кислоты. Экстракцию проводили на колонках Seppack C18 (Waters). После выпаривания до сухого остатка PGE2 измеряли радиоиммунным методом. Результаты выражены величиной Cl50 и сведены в нижеследующую таблицу 4. Формула изобретения
A  B, B,в которой А – ингибитор циклооксигеназы с карбоксильной функцией; В – соединение общей формулы Iв 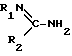 , ,в которой R1 – атом водорода, нитро- или фенильный радикал, при этом фенильный радикал может быть замещен одним или несколькими заместителями, выбранными из радикалов галоген, циано, нитро, трифторметил, низший алкил или низший алкокси; R2 – низший алкил, низший алкил-тиоалкил, фенил, который может быть замещен одним или несколькими атомами галогена, цикл, содержащий гетероатом, выбранный из атомов серы и кислорода; или амино, который может быть замещен радикалом, выбранным из радикалов амино или низшего алкила при условии, что если А означает ацетилсалициловую кислоту, а R1 – атом водорода, то R2 не является ни фенилом, замещенным или незамещенным, ни циклом, содержащим гетероатом. 2. Соли общей формулы I по п.1, отличающиеся тем, что соединение А выбрано из салицилатов, индометацина, сулиндака, фенаматов и производных пропионовой кислоты. 3. Соли общей формулы I по пп.1 и 2, отличающиеся тем, что А означает салициловую кислоту, салицилат метила, ацетилсалициловую кислоту, индометацин, сулиндак, мефенаминовую кислоту, меклофенаминовую кислоту или ибупрофен; В означает соединение приведенной выше общей формулы Iв, в которой R1 – атом водорода, нитро- или фенильный радикал, при этом фенильный радикал может быть замещен одним или несколькими заместителями, выбранными из хлора, фтора, циано, нитро, трифторметила, метила, этила, метокси, этокси и изопропилокси; R2 – радикал амино, гидразино, метиламино, этиламино, метил, этил, метил-тиометил, фенил, который может быть замещен одним или несколькими атомами галогена. 4. Соли общей формулы I по пп.1 – 3, представляющие собой следующие соединения: салицилат аминогуанидина; ибупрофенат аминогуанидина; индометацинат аминогуанидина; ацетилсалицилат метилгуанидина; салицилат метилгуанидина; ибупрофенат метилгуанидина; мефенамат метилгуанидина. 5. Соединение общей формулы I по п.1, обладающие свойством ингибитора NO-синтазы и циклооксигеназы. 6. Соединения общей формулы I по одному из пп.2 – 4, обладающие свойством ингибитора NO-синтазы и циклооксигеназы. 7. Способ получения солей производных амидина и ингибитора циклооксигеназы общей формулы I по п.1, отличающийся тем, что соединение формулы А подвергают взаимодействию с соединением формулы В в воде при температуре от комнатной до 70oC. 8. Фармацевтическая композиция, обладающая свойством ингибитора NO-синтазы и циклооксигеназы, содержащая активное начало и фармакологически приемлемый носитель, отличающаяся тем, что в качестве активного начала она содержит соединение по п.1 в эффективном количестве. РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 16.07.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||
