|
|
(21), (22) Заявка: 2007109330/04, 23.08.2005
(24) Дата начала отсчета срока действия патента:
23.08.2005
(30) Конвенционный приоритет:
23.08.2004 US 60/603,606
(43) Дата публикации заявки: 27.09.2008
(46) Опубликовано: 10.05.2010
(56) Список документов, цитированных в отчете о
поиске:
RU 2099331 C1, 20.12.1997. EP 0144748 A2, 03.11.1984.
(85) Дата перевода заявки PCT на национальную фазу:
23.03.2007
(86) Заявка PCT:
US 2005/029879 20050823
(87) Публикация PCT:
WO 2006/023889 20060302
Адрес для переписки:
119034, Москва, Пречистенский пер., 14, стр. 1, 4-й этаж, “Гоулингз Интернэшнл Инк.”, пат.пов. Ю.В.Дементьевой, рег. 560 560
|
(72) Автор(ы):
МИРАНДА Идгар И. (US),
ВЛАР Корнелис (US),
ЖУ Джингианг (US)
(73) Патентообладатель(и):
БРИСТОЛ-МАЕРС СКВИББ КОМПАНИ (US)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО ПРОДУКТА, УЧАСТВУЮЩЕГО В СИНТЕЗЕ ИРБЕСАРТАНА
(57) Реферат:
Настоящее изобретение относится к способу получения соединения формулы II, включающего реакцию смеси соединения формулы IVa и соединения формулы IVb с соединением формулы V или его фармацевтически приемлемой солью в присутствии в качестве основания КОН, NaOH и LiOH, восстановителя диалкилфосфита, катализатора переноса фаз тетраалкиламмонийхлорида; и, возможно, промывку соединения формулы II растворителем, затем, возможно, превращение соединения формулы II в фармацевтически приемлемую соль. Также изобретение относится к способу получения соединения формулы I. Технический результат: разработан новый способ получения соединения, используемого в качестве промежуточного продукта в синтезе ирбесартана. 3 н. и 11 з.п. ф-лы.
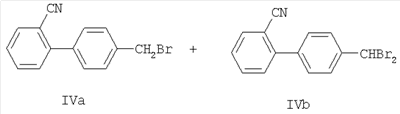



Область, к которой относится изобретение
Данное изобретение относится к способам получения ирбесартана и промежуточных продуктов для него. Ирбесартан представляет собой антагонист рецептора ангиотензина II и пригоден для лечения расстройств, ассоциируемых с ангиотензинном II.
Предпосылки создания изобретения
Ирбесартан является активным антагонистом рецептора ангиотензина II длительного действия, который особенно пригоден для лечения сердечно-сосудистых заболеваний, таких как повышенное давление и сердечная недостаточность. Ирбесартан имеет следующее строение:

и описан Bernhart et al., в патенте США  5,270,317. 5,270,317.
Сущность изобретения
Данное изобретение относится к различным способам получения ирбесартана и промежуточных продуктов для него. Один аспект настоящего изобретения предусматривает способ получения соединения, пригодного для синтеза ирбесартана, имеющего формулу II, или его фармацевтически приемлемой соли

включающий реакцию смеси соединения формулы IVa и соединения формулы IVb и возможно соединения формулы IVc
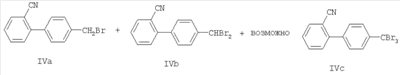
с соединением формулы V или его фармацевтически приемлемой солью

в присутствии основания и восстанавливающего агента и, возможно, в присутствии катализатора переноса фаз и необязательное превращение соединения формулы II в его фармацевтически приемлемую соль.
Другой аспект данного изобретения предусматривает способ получения соединения формулы I (ирбесартана) или его фармацевтически приемлемой соли из соединений формулы II

Дальнейший аспект данного изобретения предусматривает способ получения соединения II в практически чистой форме

включающий:
(а) кристаллизацию сырого соединения формулы II с применением по меньшей мере одного растворителя, выбранного из метилтрет.бутилового эфира и изопропанола, с образованием соединения II в кристаллической форме,
(б) промывку соединения формулы II в кристаллической форме, полученного на стадии (а), по меньшей мере одним растворителем, выбранным из метилтрет.бутилового эфира и изопропанола с получением соединения формулы II в чистом виде и
(в) возвращение в цикл растворителя, собранного со стадии (б), для кристаллизации сырого соединения формулы II при получении следующей партии, как описано на стадии (а).
Подробное описание изобретения
Сокращения
| HPLC |
– жидкостная хроматография высокого давления |
| МТВАС |
– метил-н-трибутиламмония хлорид |
| МТВЕ |
– метилтрет.бутиловый эфир |
| ГРА |
– изопропиловый спирт |
| NBS |
– N – бромсукцинимид |
Определения
Термин «алкил» или «алк» относится к линейному или разветвленному алкановому (углеводородному) радикалу, содержащему от 1 до 12 атомов углерода, предпочтительно 1-6 атомов углерода. Примеры «алкильных» групп включают метил, этил, пропил, изопропил, н – бутил, трет.бутил, изобутил, пентил, гексил, изогексил, гептил, 4,4-диметилпентил, октил, 2,2,4-триметилпентил, нонил, децил, ундецил, додецил и т.п. Термин «C1-С6 алкил» относится к линейному или разветвленному алкановому (углеводородному) радикалу, содержащему от 1 до 4 атомов углерода, такому как метил, этил, пропил, изопропил, н-бутил, трет.бутил, изобутил, пентил, изопентил, гексил и изогексил.
Термин «катализатор переноса фаз» относится к небольшому количеству химического агента, который приводит к увеличению скорости реакции между химическими группами, расположенными в разных фазах (несмешивающихся жидкостях или твердой и жидкой фазах) за счет экстракции одного из реагентов, наиболее часто аниона, через поверхность раздела фаз в другую фазу, чтобы могла протекать реакция. Эти катализаторы включают соли четвертичного аммония или фосфония (например, соли тетраалкиламмония, где алкилы могут быть одинаковыми или разными), или агенты, которые образуют комплексы с неорганическими катионами (например, краун-эфиры или другие криптанды). Катион катализатора не расходуется во время реакции, хотя анионный обмен имеет место.
Соединения по изобретению могут образовывать соли, которые также входят в объем данного изобретения. Ссылка на соединения формул I-V в данном описании подразумевает ссылку и на соли этих соединений, если не указано иное.
Термин «соль(-и)», используемый здесь, обозначает кислотные и/или основные соли, образованные с неорганическими и/или органическими кислотами и основаниями. Кроме того, когда соединение содержит как основную группу, например, без ограничения, пиридиновую или имидазольную, так и кислотную группу, например, без ограничения, карбоксильную, могут образовываться цвиттер-ионы («внутренние соли»), которые также охватываются термином «соли», используемым в данной заявке.
Предпочтительными являются фармацевтически приемлемые (то есть нетоксичные, физиологически приемлемые) соли, хотя другие соли также применяются, например, на стадиях выделения или очистки, которые могут применяться в процессе синтеза. Соли соединений могут получаться, например, при взаимодействии этих соединений с кислотой или основанием, например, с их эквивалентным количеством в такой среде, в которой соль осаждается, или в водной среде с последующей лиофилизацией.
Соединения по изобретению могут образовать соли с различными органическими и неорганическими кислотами. Примеры солей с кислотами включают ацетаты (например, те, которые образуются с уксусной кислотой или тригалоидуксусной кислотой, например, трифторуксусной кислотой), адипинаты, альгинаты, соли аскорбиновой кислоты, аспартаты, бензоаты, бензосульфонаты, бисульфаты, бораты, бутираты, цитраты, камфораты, камфосульфонаты, циклопентанпропионаты, диглюконаты, додецилсульфаты, этансульфонаты, фумараты, гликогептаноаты, глицерофосфаты, гемисульфаты, гептаноаты, гексаноаты, гидрохлориды, гидробромиды, гидроиодиды, гидроксиэтансульфонаты (например, 2-гидроксиэтансульфонаты), лактаты, малеаты, метансульфонаты, нафталинсульфонаты (например, 2-нафталинсульфонаты), никотинаты, нитраты, оксалаты, пектинаты, персульфаты, фенилпропионаты (например, 3-фенилпропионаты), фосфаты, пикраты, пивалаты, пропионаты, салицилаты, сукпинаты, сульфаты (такие, как соли, образованные с серной кислотой), сульфонаты, тартраты, тиоцианаты, толуолсульфонаты, такие как тозилаты, ундеканоаты и т.п.
Соединения по изобретению могут также образовать соли с различными органическими и неорганическими основаниями. Примеры солей с основаниями включают аммонийные соли, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли органических оснований (например, органических аминов), таких как бензатины, дициклогексиламины, гидрабамины (образовавшиеся с N,N-бис(дегидроабиетил)этилендиамином), N-метил – D-глюкамины, N-метил – D-гликамиды, трет.бутиламины и соли с аминокислотами, такими как аргинин, лизин и т.п. Основные азотсодержащие группы могут быть кватернизованы при помощи таких агентов, как низшие алкилгалогениды (например, метил-, этил-, пропил- и бутилхлориды, – бромиды и -йодиды), диалкилсульфаты (например, диметил-, диэтил-, дибутил- и диамилсульфаты), длинноцепные галоидные соединения (например, децил-, лаурил-, миристил- и стеарилхлориды, -бромиды и -йодиды), аралалкилгалоидные соединения (например, бензил- и фенетилбромиды) и др.
Пролекарства и сольваты соединений по изобретению также входят в объем изобретения. Используемый здесь термин «пролекарство» обозначает соединение, которое при введении субъекту претерпевает химическое превращение метаболическим или химическим способами с получением соединений формул I-V или их солей и/или их сольватов. Сольваты соединений формул I-V включают, например, гидраты.
Соединения формул I-V и их соли могут существовать в их таутомерной форме (например, как амиды или иминоэфиры). Все такие таутомерные формы также образуют часть данного изобретения.
Все стереомеры по изобретению (например, такие, которые могут существовать благодаря асимметричным атомам углерода в различных заместителях), включая энантиомерные формы и диастереомерные формы, также охвачены данным изобретением.
Отдельные стереоизомеры соединений по изобретению могут, например, не содержать других изомеров (например, чистый или практически чистый оптический изомер, имеющий специфическую активность), или могут представлять собой смеси, например, в виде рацематов, или со всеми другими, или другими выбранными стереоизомерами. Хиральные центры соединений по изобретению могут иметь S- или R – конфигурацию, как это определено IUРАС 1974 Recommendations.
Рацемические формы могут быть разрешены физическими методами, такими как, например, фракционная кристаллизация, разделение или кристаллизация диастереомерных производных или разделение методом хиральной хроматографии на колонках. Индивидуальные оптические изомеры могут быть получены из рацематов любым подходящим методом, включая, без ограничения, обычные методы, такие как, например, образование соли с оптически активной кислотой с последующей кристаллизацией.
Все конфигурационные изомеры соединений по изобретению заявлены или в виде смеси, или в чистой, или в практически чистой форме. Определение соединений согласно данному изобретению охватывает как цис- (Z) и транс- (Е) алкеновые изомеры, так и цис- и транс – изомеры циклических углеводородных или гетероциклических колец.
Согласно изобретению группы и их заместители выбирают так, чтобы обеспечить получение стабильных групп и соединений.
Способы получения
Способы получения соединений формул III показаны на следующих схемах. Растворители, температуры, величина давления и другие условия реакции могут быть легко выбраны специалистом. Исходные материалы коммерчески доступны или могут быть легко получены специалистом.
Соединение формулы I (ирбесартан) может быть получено по Схеме 1. Соединение 1 бромируют с получением смеси монобромированного продукта IVa и дибромированного продукта IVb с помощью бромирующего реагента, такого как Br2 или NBS, в среде органического растворителя, такого как CCl4, CHCl3 или CH2Cl2, и необязательно при наличии УФ-света или каталитического количества перекиси бензоила. Трибромированный продукт IVc может быть также получен, если применяют большой избыток брома. Br2 может быть получен in situ по реакции NaBrO3 или H2O2 с HBr в воде. Смесь соединений IVa и IVb и, возможно, IVc может быть моноалкилирована путем обработки соединения V или его фармацевтически приемлемой соли в присутствии основания, такого как NaH, и в присутствии восстановителя, такого как диалкилфосфит (то есть диэтилфосфит), с получением соединения формулы II. Когда применяют водное основание, такое как водная КОН или водная NaOH, используют также катализатор переноса фаз, такой как тетраалкиламмонийхлорид, в добавление к восстановителю, такому как диалкилфосфит (диэтилфосфит). Восстановитель селективно восстанавливает дибромсодержащее соединение IVb (или трибромсодержащее соединение IVc) до монобромированного соединения IVa, в то время как соединение IVa алкилируется с получением желаемого продукта моноалкилирования. Этот метод может быть применен для смеси соединений IVa, IVb в любом соотношении, то есть соотношение между IVa и IVb может меняться от 1%:99% до 99%:1%, Кроме того, этот метод работает также в присутствии любого количества соединения IVc. Наконец, соединение II реагирует с азидом, таким как NaN3 с получением соединения формулы I.
Схема I

Признаки и преимущества данного изобретения более полно видны из следующих примеров, которые приведены для целей иллюстрации и не ограничивают никоим образом объем данного изобретения.
Условия HPLC:
Колонка: Alltima C18 (Alltech 88050), 15,0 см длина ×4,6 мм внутренний диаметр, частицы размером 5 мк;
Температура в колонке: 40°С;
Растворитель А: буферный раствор А – 1,1 г гептансульфокислоты в 1 л воды, pH доводят до 2,5;
Растворитель В: метанол, скорость истечения: 1,2 мл/мин;
Градиент элюирования;
| Время, % |
А% |
%В |
| 0 мин |
50 |
50 |
| 35 мин |
15 |
85 |
Детектор: 240 нм
Объем инжекции: 10 мкл
Эти условия HPLC используют в нижеследующих примерах, если иное не оговорено,
Пример 1
Получение соединений формул IVa и IVb:

В круглодонную колбу объемом 1000 мл с рубашкой загружали 4′-метилдифенил – 2-карбонитрил (соединение I, 100 г) и CH2Cl2 (500 мл) в атмосфере азота. В колбе Эрленмейера объемом 500 мл, снабженной магнитной мешалкой, растворяли в воде (170 мл) бромат натрия (NaBrO3, 31,2 г). Раствор NaBrO3 перемещали в колбу объемом 1000 мл и охлаждали реакционную смесь до примерно температуры 5°С или менее. В колбу объемом 1000 мл добавляли водный раствор HBr (48%, 105,0 г) и полученную реакционную смесь возвращали в цикл в реактор с УФ – светом. Реакционную смесь выдерживали при температуре, равной 0-20°С, и продолжали цикл, пока реакция не казалась законченной по данным HPLC. Можно добавить дополнительно бромат натрия и бромистый водород. Количества соединения 2 и соединения 3 составляли примерно 80-90% и примерно 10-20%, соответственно. В реакционную смесь добавляли водный раствор метабисульфита натрия (2,0 г в 10 мл воды). Давали фазам осесть и метиленхлоридную фазу промывали водой и использовали на следующей стадии без дополнительной очистки.
Пример 2
Получение соединения II
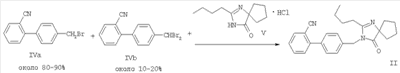
В трехгорлую колбу объемом 1 л загружали соединение V (134,0 г), МТБАС (5,0 г) и CH2Cl2 (170 мл) и охлаждали до температуры от -5 до 5°С. В эту колбу объемом 1 л добавляли медленно водный раствор КОН (182,6 г в 212 мл воды) и поддерживали температуру реакции при <5°С. В реакционную смесь медленно добавляли раствор соединения IVа и соединения IVb в метиленхлориде из Примера 1, поддерживая температуру равной 0-10°С. При температуре 0-10°С по каплям добавляли диэтилфосфит (39,66 г). Проверяли окончание реакции восстановления и затем можно добавить дополнительно диэтилфосфит.
Реакционной смеси давали нагреться до комнатной температуры (20-30°С) и перемешивали, пока реакция не завершилась по данным HPLC. Добавляли воду (150 мл) и разделяли фазы. Органический слой экстрагировали водой (230 мл) и отфильтровывали. Метиленхлорид (который содержал сырое соединение II) отгоняли и замещали примерно 400 мл МТВЕ (можно МТВЕ, полученный после промывки, описанной ниже). После охлаждения происходила кристаллизация (можно добавить затравочные кристаллы) и после дальнейшего охлаждения до температуры ниже 25°С выделяли кристаллы соединения II, промывали МТВЕ и сушили под вакуумом при температуре менее 60°С. Время удерживания при HPLC: 18,126 мин. Обычно выход составляет около 85-88%. Можно также использовать в качестве растворителя для кристаллизации и промывки IPA. Растворитель (а именно МТВЕ или IPA), использованный для промывки кристаллов соединения II, можно вернуть в цикл и применить для кристаллизации сырого соединения II при получении следующей партии. Так как растворитель для промывки содержит соединение II, а также примеси, было неожиданным, что этот растворитель может быть регенерирован и снова использован для кристаллизации сырого соединения формулы II при получении следующей партии без учета степени его чистоты, но приводя к увеличению его выхода.
Пример 3
Получение соединения формулы I

В реактор загружали соединение формулы II (1 кг), хлоргидрат триэтиламина (0,713 кг), азид натрия (0,337 кг) и N-метилпирролидинон (2,07 кг) и нагревают реакционную смесь до примерно 122°С при перемешивании. После завершения реакции по данным HPLC реакционную смесь охлаждали до примерно 45°С и добавляли водный раствор гидроокиси натрия (35%, 5,99 кг) и воду (3,0 кг), полученную смесь перемешивали при температуре между примерно 20 и примерно 40°С в течение примерно 0,5 ч. Водную фазу выгружали и обрабатывали органическую фазу толуолом (1,73 кг) и водой (5,0 кг) и перемешивали в течение примерно 0,5 ч при температуре примерно 20-30°С. Толуольную фазу выгружали и обрабатывали водную фазу, промывали этилацетатом (1,8 мг) и обрабатывали водным раствором НС1 до достижения величины pH до примерно 4,8-5,2. Происходило осаждение, и полученную суспензию перемешивали в течение примерно 1 ч при температуре примерно 20-25°С. Собирали осадок и промывали 3 раза водой (1,0 кг ×3). Технический влажный продукт перекристаллизовывали, используя смесь изопропанола (0,393 кг) и воды (4,5 кг). Время удерживания при HPLC: 11,725 мин. Выход соединения I составил примерно 87%.
Формула изобретения
1. Способ получения соединения формулы II или его фармацевтически приемлемой соли

включающий реакцию смеси соединения формулы IVa и соединения формулы IVb
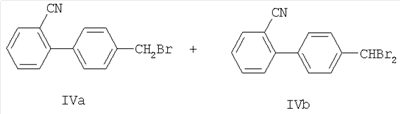
с соединением формулы V или его фармацевтически приемлемой солью

в присутствии в качестве основания КОН, NaOH и LiOH, восстановителя диалкилфосфита, катализатора переноса фаз тетраалкиламмонийхлорида; и, возможно, промывку соединения формулы II растворителем, затем, возможно, превращение соединения формулы II в фармацевтически приемлемую соль.
2. Способ по п.1, отличающийся тем, что восстановителем является диэтилфосфит.
3. Способ по п.1, отличающийся тем, что фармацевтически приемлемой солью соединения формулы V является гидрохлорид.
4. Способ по п.4, отличающийся тем, что основанием является водная КОН, катализатор переноса фаз представляет собой метил-н-трибутиламмония хлорид, восстановитель представляет собой диэтилфосфит и фармацевтически приемлемой солью соединения формулы V является гидрохлорид.
5. Способ по п.1, отличающийся тем, что соединение формулы II кристаллизуется из по меньшей мере одного растворителя, выбранного из метил-трет.бутилового эфира и изопропанола.
6. Способ по п.4, отличающийся тем, что соединение формулы II кристаллизуется из по меньшей мере одного растворителя, выбранного из метил-трет.бутилового эфира и изопропанола.
7. Способ по п.5, отличающийся тем, что включает промывку соединения формулы II по меньшей мере одним растворителем, выбранным из метил-трет.бутилового эфира и изопропанола, и возвращение растворителя для промывки в цикл для кристаллизации соединения формулы II.
8. Способ по п.6, отличающийся тем, что он дополнительно включает промывку соединения формулы II по меньшей мере одним растворителем, выбранным из метил-трет.бутилового эфира и изопропанола, и возвращение растворителя для промывки в цикл для кристаллизации соединения формулы II.
9. Способ получения соединения формулы I или его фармацевтически приемлемой соли

получение соединения формулы II или его фармацевтически приемлемой соли

при взаимодействии смеси соединения формулы IVa и соединения (формулы IVb)
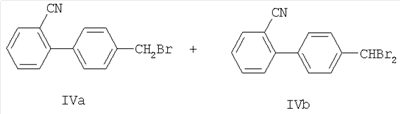
с соединением формулы V или его фармацевтически приемлемой солью

в присутствии основания КОН, NaOH и LiOH в качестве основания, диалкилфосфита в качестве восстановителя, катализатора переноса фаз тетраалкиламмонийхлорида, и, возможно, промывку соединения формулы II растворителем, затем, возможно, превращение соединения формулы II в фармацевтически приемлемую соль, с последующим взаимодействием соединения формулы II с азидом натрия в присутствии триэтиламина хлоргидрата и N-метилпиролидона с получением соединения формулы I.
10. Способ по п.9, отличающийся тем, что фармацевтически приемлемая соль соединения формулы V представляет собой гидрохлорид.
11. Способ по п.10, отличающийся тем, что тетраалкиламмонийхлорид представляет собой метилтри-н.бутиламмоний хлорид и диалкилфосфит представляет собой диэтилфосфит.
12. Способ получения соединения формулы II в практически чистой форме

включающий:
(а) кристаллизацию сырого соединения формулы II с применением по меньшей мере одного растворителя, выбранного из метил трет.бутилового эфира и изопропанола с получением соединения формулы II в кристаллической форме;
(б) промывку соединения формулы II в кристаллической форме, полученного на стадии (а) по меньшей мере одним растворителем, выбранным из метил трет.-бутилового эфира и изопропанола с получением соединения формулы II в практически чистой форме; и
(в) возвращение в цикл растворителя, использованного для промывки, со стадии (б) для кристаллизации сырого соединения формулы II при получении следующей партии, как описано на стадии (а).
13. Способ по п.12, отличающийся тем, что растворителем на стадиях (а), (б) и (в) является метил трет.бутиловый эфир.
14. Способ по п.12, отличающийся тем, что растворителем на стадиях (а), (б) и (в) является изопропанол.
|
|