Патент на изобретение №2387658
|
||||||||||||||||||||||||||
(54) БРОМГИДРАТ 4-МЕТОКСИ-7,7-ДИМЕТИЛ-9(5′-КАРБОКСИАМИЛ)АМИНО-6Н-7,8-ДИГИДРОПИРИМИДО(4,5-b)-1,4-БЕНЗТИАЗИН И СПОСОБ ЕГО ПОЛУЧЕНИЯ
(57) Реферат:
Описывается бромгидрат 4-метокси-7,7-диметил-9-(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо-(4,5-в)-1,4-бензтиазин (далее метиазин) и способ его получения. Метиазин обладает противоопухолевой и антиредуктазной активностью, имеющий цитостатическое и цитотоксическое действие, ингибирующее синтез нуклеиновых кислот, и может быть использован в медицине. Бромгидрат 4-метокси-7,7-диметил-9-(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо-(4,5-в)-1,4-бензтиазин формулы 1
получают при взаимодействии димедона с
Изобретение относится к области органической химии и касается нового, не описанного в литературе соединения, а именно бромгидрата 4-метокси-7,7-диметил-9(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо(4,5-в)-1,4-бензтиазина (далее метиазина), и способа его получения. Метиазин обладает противоопухолевой и антиредуктазной активностью, имеющий цитостатическое и цитотоксическое действие, ингибирующее синтез нуклеиновых кислот, и может быть использован в медицине. Заявленное соединение относится к группе гидрированных 1,3-диазафентиазинов, первые сведения о которых появились только в 1980 году. К настоящему времени в этой группе обнаружены вещества, обладающие разносторонней биологической активностью (анальгетической, противовоспалительной, антигипоксической), а также имеются данные, что соединения, относящиеся к этому классу, проявляют слабую противоопухолевую и антиредуктазную активность (Хим. Фарм. Ж. Задача изобретения – получение соединений группы гидрированных 1,3-фенотиазинов, обладающих улучшенными биологическими свойствами, в частности более широким спектром биологического действия, в том числе более широким спектром противоопухолевой активности и более глубокосторонней выраженностью. Поставленная задача достигается получением бромгидрата 4-метокси-7,7-диметил-9(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо(4,5-в)-бенз1,4-тиазин (метиазина), обладающего противоопухолевой и антиредуктазной активностью, имеющего цитостатическое и цитотоксическое действие, ингибирующего синтез нуклеиновых кислот. Способ заключается во взаимодействии димедона с Благодаря этому способу целевое соединение (метиазин) выделяют в виде бромгидрата, а не основания, то есть реакционную массу 2-бромкенаминокетона и 4-метокси-5-амино-6-меркаптопиримидина не обрабатывают водным раствором NaOH, так как основание метиазина растворимо в воде и еще лучше растворимо в растворах едких щелочей (присутствие в молекуле СООН группы).
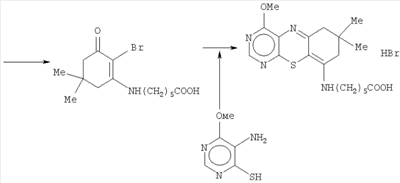
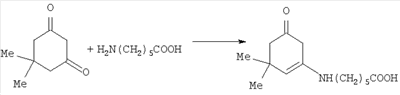
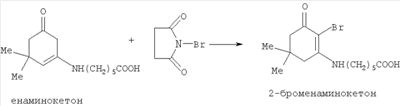
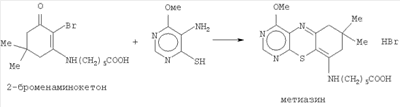
Известно, что доступная Схема синтеза Нижеследующий пример иллюстрирует получение заявленного соединения. 1. Получение енаминокетона В колбу объемом 1 л загружают 500 мл изопропилового спирта и при работающей мешалке прибавляют смесь, состоящую из 35 г димедона и 32.8 г 2. Получение 2-броменаминокетона В колбу объемом 1 л загружают смесь из 380 мл метанола и 65 мл воды, в колбу присыпают 28 г тонко измельченного бромсукцинимида. Содержимое колбы охлаждают до 0°С и при работающей мешалке загружают 40 г тонко измельченного енаминокетона, следя за тем, чтобы температура реакции не поднималась выше +2°С. После окончания загрузки реакционную массу выдерживают при 0°С в течение 2 часов и затем оставляют в ледяной бане на 12 часов. После такой выдержки отгоняют 250 мл растворителя и к оставшемуся остатку в колбе прибавляют 400 мл воды. Смесь перемешивают 30-40 мин и отфильтровывают выпавший осадок. Его промывают водой и сушат на воздухе, перекристаллизовывают из 600-700 мл этилацетата, получают 28-29 г бледно-бежевого кристаллического продукта (62-64%). Т пл. 114-116°С 3. Получение метиазина В колбу объемом 500 мл загружают смесь, состоящую из 350 мл изопропанола, 4 г меркаптопиримидина и 8 г броменаминокетона. К реакционной массе прибавляют 5 капель соляной кислоты и нагревают до кипения. В процессе реакции все твердые компоненты растворяются, и образуется раствор красного цвета. Кипячение продолжают 3-3,5 часа при перемешивании. Ход процесса контролируют хроматографически. К концу кипения на хроматограмме видно оранжевое пятно целевого продукта и следы исходных веществ (силуфол, элюэнт метанол:хлороформ 1/10). Колбу снабжают прямым холодильником и отгоняют 300-350 мл растворителя при работающей мешалке. К остатку, охлажденному до 30-40°С, прибавляют 250 мл ацетона и перемешивают 30-40 мин. Осадок метиазина отфильтровывают, промывают 50 мл чистого ацетона и сушат на воздухе. Получают около 9 г метиазина (75% выход) в виде оранжевого порошка с Т пл. 176-178°С. Хранится на воздухе без разложения. Легко растворим в воде и метаноле, плохо растворим в изопропаноле и нерастворим в бензоле, толуоле, петролейном и серном эфирах. Характеристика биологической активности метиазина Метиазин – оригинальное химическое соединение, по своей структуре не имеет аналогов в России и за рубежом. Углубленное биологическое исследование метиазина проведено в лаборатории экспериментальной химиотерапии опухолей ЦХЛС-ВНИХФИ под руководством доктора медицинских наук, профессора В.А.Чернова. Исследование осуществлялось по трем направлениям. – Выяснялась способность метиазина ингибировать фермент фолиевого обмена дигидрофолатредуктазу (ДФР) (проведено мнс, канд. биол. наук Н.А.Рябоконь по методике, описанной в работе [А.С.Соколова, Н.А.Рябоконь, Ю.А.Ершова. «Вопросы онкологии», 1975, 21(11), стр.45-50). – Изучалось цитостатическое и цитотоксическое действие в культурах опухолевых и нормальных клеток (проведено мнс Ю.А.Ершовой по вышеназванной методике). – Исследовалась способность метиазина тормозить рост перевиваемых опухолей экспериментальных животных (проведено снс, кмн А.С.Соколовой по методике в работе [В.А.Чернов, в книге «Методы экспериментальной химиотерапии, практическое руководство» под ред. Т.Н.Першина, М.: Медицина, 1971, стр.357-382). Обнаружено, что метиазин ингибирует ферментный препарат ДФР, выделенный из из печени крыс в концентрации 1·10-4 М на 95%, в концентрации 1·10-5 М – на 50%. Активность в отношении ДФР отмечалась также в концентрации 1·10-6 М на 30% и сохранялась в концентрации 1·10-7 М на 19%. Установлено, что метиазин ингибирует синтез нуклеиновых кислот, адаптированных к росту in vitro клеток лимфолейкоза NK/Ly: доза, вызывающая 50% ингибирование синтеза нуклеиновых кислот (ED50), составляет 250 Метиазин обладает цитостатическим действием в культурах опухолевых клеток (саркомы 45) и нормальных клеток (сердце куриного эмбриона). Так, для метиозина индекс торможения роста культуры клеток саркомы 45 (J) в концентрации 1·10-3 достигал 100%, в концентрации 1·10-4 М – 30%. В отношении культуры клеток сердца куриного эмбриона индекс торможения (J) в концентрации 1·10-3М составлял 90%, а в концентрации 1·10-4М ингибирование нормальных клеток не наблюдалось. Эти данные свидетельствуют о наличии у метиазина некоторой избирательности цитостатического действия в отношении опухолевой ткани по сравнению с нормальной. Высокая противоопухолевая активность обнаружена у метиазина в опытах in vivo: ингибирует рост ряда штаммов перевиваемых опухолей крыс. Так, метиазин тормозит рост саркомы Йенсена на 90-95%, саркомы М-1 на 70%, саркомы 45 на 30%. При этом метиазин проявляет умеренную цитотоксичность: при повторном внутрибрюшинном введении крысы хорошо переносят препарат в дозах до 100 мг/кг. Мыши более чувствительны к действию метиазина и хорошо переносят препарат в дозах 25 мг/кг. При ежедневных введениях в течение 7 дней метиазин тормозит рост асцитной формы рака Эрлиха до 85-90%, NK/Ly – 80-90%, карциномы 755 – 70-75%, саркомы АК и саркомы 37 на 70%. Таким образом, метиазин по химической структуре и своим биологическим свойствам может рассматриваться как новый тип ингибитора фермента фолиевого обмена дигидрофолатредуктазы, проявляющий высокую противоопухолевую активность в опытах in vitro и in vivo. Он отличается от известных ингибиторов ферментов фолиевого обмена – противоопухолевых препаратов аминоптерина и метотрексата иным спектром противоопухолевого действия и значительно меньшей токсичностью. Так, МПД (моментально переносимая доза) у мышей при однократном введении метотрексата 4 мг/кг, а для метиазина 100 мг/кг.
Формула изобретения
1. Бромгидрат 4-метокси-7,7-диметил-9(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо(4,5-b)-1,4-бензтиазин формулы 1 2. Способ получения бромгидрат 4-метокси-7,7-диметил-9-(5′-карбоксиамил)амино-6Н-7,8-дигидропиримидо-(4,5-b)-1,4-бензтиазина по п.1, заключающийся во взаимодействии димедона с
|
||||||||||||||||||||||||||

 443312-67-2, 25.01.2008. SU 562982, 07.07.1982. JP 6172365 A, 21.06.1994. US 5418231, 23.05.1995.
443312-67-2, 25.01.2008. SU 562982, 07.07.1982. JP 6172365 A, 21.06.1994. US 5418231, 23.05.1995.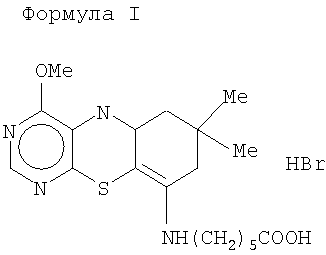
 -аминокапроновой кислотой в среде кипящего изопропанола с получением енаминокетона, который подвергают бромированию бромсукцинимидом с дальнейшей обработкой 4-метокси-5-амино-6-меркаптопиримидином в среде кипящего изопропанола. 2 н.п. ф-лы.
-аминокапроновой кислотой в среде кипящего изопропанола с получением енаминокетона, который подвергают бромированию бромсукцинимидом с дальнейшей обработкой 4-метокси-5-амино-6-меркаптопиримидином в среде кипящего изопропанола. 2 н.п. ф-лы.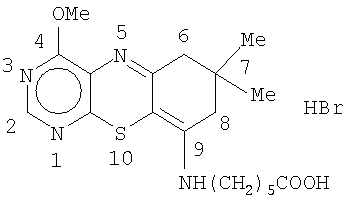
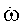 -аминокапроновая кислота является антиферментным препаратом и обладает регенерирующими свойствами. Поэтому сама кислота и ее производные применяются как кровоостанавливающие средства, средства для заживления ран, а также для ускорения срастания костей при переломах. Эти соединения также используются для рассасывания косметических рубцов при косметических операциях. Известно также, что производные аминокислот, к которым можно отнести и метиазин, в 4-5 раз быстрее проникают через мембраны опухолевых клеток по сравнению с нормальными клетками и приводят к повышенной концентрации препарата в опухолевых клетках. Можно было надеяться, что введение такого заместителя в молекулу заявленного соединения могло положительно сказаться на его биологических свойствах. Синтез заявленного соединения осуществляется по следующей схеме: димедон вводится во взаимодействие с омегоаминокароновой кислотой и получают енаминокетон. Последний подвергается бромированию бромсукцинимидом, и полученный 2-броменаминокетон вводится в реакцию с 4-метокси-5-амино-6-меркаптопиримидином, что и приводит к получению заявленного соединения.
-аминокапроновая кислота является антиферментным препаратом и обладает регенерирующими свойствами. Поэтому сама кислота и ее производные применяются как кровоостанавливающие средства, средства для заживления ран, а также для ускорения срастания костей при переломах. Эти соединения также используются для рассасывания косметических рубцов при косметических операциях. Известно также, что производные аминокислот, к которым можно отнести и метиазин, в 4-5 раз быстрее проникают через мембраны опухолевых клеток по сравнению с нормальными клетками и приводят к повышенной концентрации препарата в опухолевых клетках. Можно было надеяться, что введение такого заместителя в молекулу заявленного соединения могло положительно сказаться на его биологических свойствах. Синтез заявленного соединения осуществляется по следующей схеме: димедон вводится во взаимодействие с омегоаминокароновой кислотой и получают енаминокетон. Последний подвергается бромированию бромсукцинимидом, и полученный 2-броменаминокетон вводится в реакцию с 4-метокси-5-амино-6-меркаптопиримидином, что и приводит к получению заявленного соединения.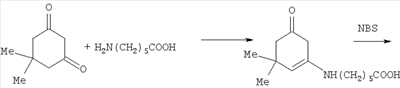
 .
.