Патент на изобретение №2387648
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ 3-ОКСО-1,3-ДИГИДРОБЕНЗО[С]ОКСЕПИН-4-КАРБОНОВОЙ КИСЛОТЫ
(57) Реферат:
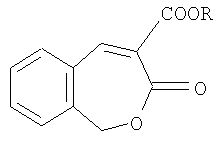
Изобретение относится к способу получения новых алкиловых эфиров 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты общей формулы
где R – метил, этил, пропил, изопропил, бутил, изопентил, заключающемся в том, что диалкиловые эфиры 2-(2-бромметилбензилиден)малоновой кислоты, полученные бромированием диалкиловых эфиров 2-(2-метилбензилиден)малоновой кислоты N-бромсукцинимидом, нагревают при температуре 190-220°С с одновременной отгонкой алкилбромида в течение 1-5 часов. Соединения могут найти применение в качестве промежуточных продуктов для синтеза различных органических соединений, в частности биологически активных.
Изобретение относится к органической химии, а именно к способу получения не описанных в литературе алкиловых эфиров 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты общей формулы
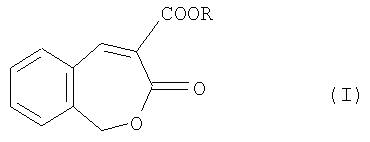
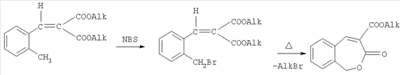
где R – метил, этил, пропил, изопропил, бутил, изопентил, которые могут найти применение в различных органических синтезах. Известно, что замещенный этиловый эфир 2-оксо-2,5-дигидробензо[b]оксепин-3-карбоновой кислоты получен наряду с другими продуктами при взаимодействии диметилацеталя диазоацетальдегида с этиловым эфиром кумарин-3-карбоновой кислоты [1]. Из патентной литературы известны производные 1,3-дигидробензо[b]оксепин-2- или -3-карбоновой кислот, обладающие гиполипидической и гипоглимической активностью [2]. Недостатком способа – прототипа является невозможность получения соединений формулы (I). Задачей создания изобретения является разработка способа получения не описанных в литературе алкиловых эфиров 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты, которые бы найдут широкое применение в качестве промежуточных продуктов в различных органических синтезах. Поставленная задача достигается тем, что диалкиловые эфиры 2-(2-бромметилбензилиден)малоновой кислоты, полученные бромированием диалкиловых эфиров 2-(2-метилбензилиден)малоновой кислоты N-бромсукцинимидом, нагревают при температуре 190-220°С с одновременной отгонкой алкилбромида в течение 1-5 часов. Температуру реакционной смеси и время нагревания контролировали по выделению соответствующего алкилбромида. Целевые продукты выделяются известными методами с выходами 45-77%. Процесс протекает по схеме Пример 1. Метиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты В круглодонную колбу помещали 0,1 моль диметилового эфира 2-(2-метилбензилиден)малоновой кислоты, 0,1 моль N-бромсукцинимида, 60 мл безводного четыреххлористого углерода и 0,1 г динитрила азо-бис-изомасляной кислоты. Реакционную смесь кипятили с обратным холодильником при освещении до исчезновения N-бромсукцинимида. После охлаждения сукцинимид отфильтровывали, промывали 20 мл четыреххлористого углерода, органический слой промывали холодной водой и сушили безводным сульфатом натрия. После отгонки растворителя диметиловый эфир 2-(2-бромметилбензилиден)малоновой кислоты нагревали на металлической бане при температуре 190°С с одновременной отгонкой метилбромида в течение 1 часа. Затем продукт отгоняли в вакууме при 1 мм рт.ст. и перекристаллизовывали из смеси бензола и гексана (1:1). Выход 16.4 г (77%), т.пл. 81-82°С. ИК спектр, Пример 2. Этиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты. Методика получения аналогична примеру 1. Нагревание 1.5 ч при температуре 200°С. Выход 17.4 г (75%), т.пл. 105-106°С. ИК спектр, Пример 3. Пропиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты. Методика получения аналогична примеру 1. Нагревание 2 ч при температуре 205°С. Выход 17.7 г (72%), т.пл. 101-102°С. ИК спектр, Пример 4. Изопропиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты. Методика получения аналогична примеру 1. Нагревание 2.5 ч при температуре 210°С. Выход 13.3 г (54%), т.пл. 91-92°С. ИК спектр, Пример 5. Бутиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты. Методика получения аналогична примеру 1. Нагревание 4 ч при температуре 215°С. Выход 18.0 г (69%), т.пл. 59-60°С. ИК спектр, Пример 6. Изопентиловый эфир 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты. Методика получения аналогична примеру 1. Нагревание 5 ч при температуре 220°С. Выход 12.3 г (45%), т.пл. 57-58°С. ИК спектр, Предлагаемый способ прост в осуществлении, позволяет получать с хорошим выходом не описанные в литературе алкиловые эфиры 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты, которые найдут применение в качестве промежуточных продуктов для синтеза новых гетероциклических соединений. Источники информации 1. Abdallah Н., Gree R., Carrie R. Bull. Soc. Chim. France, 1984, PT2, 338. 2. Патент РФ
Формула изобретения
Способ получения алкиловых эфиров 3-оксо-1,3-дигидробензо[с]оксепин-4-карбоновой кислоты общей формулы
|
||||||||||||||||||||||||||

 126
126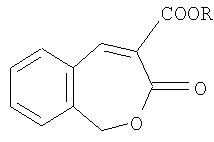
 , см-1: 1680 (ОС), 1715, 1735 (C=О). Спектр ЯМР 1Н,
, см-1: 1680 (ОС), 1715, 1735 (C=О). Спектр ЯМР 1Н,  , м.д.: 8.04 с (1Н, СН=), 7.30-7.46 м (4Н, Аr), 5.00 с (2Н, СН2Аr), 3.86 с (3Н, МеО). Найдено, %: С 65.91; Н 4.73. С12Н10О4. Вычислено, %: С 66.05; Н 4.62.
, м.д.: 8.04 с (1Н, СН=), 7.30-7.46 м (4Н, Аr), 5.00 с (2Н, СН2Аr), 3.86 с (3Н, МеО). Найдено, %: С 65.91; Н 4.73. С12Н10О4. Вычислено, %: С 66.05; Н 4.62.