Патент на изобретение №2387640
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 1-(АМИНОАЛКИЛ)ИНДОЛИНОВ
(57) Реферат:
Изобретение относится к усовершенствованному способу получения 1-(аминоалкил)индолинов, который заключается в том, что индолин взаимодействует с бромгидратом аминоалкилбромида в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением целевого продукта подщелачиванием водным NaOH, экстракцией органическими растворителями и перегонкой в вакууме. Способ позволяет повысить выход и чистоту целевого продукта, сократить время его получения.
Изобретение относится к области органической химии, а именно к способу получения индолинов с аминоалкильными заместителями у атома азота. Изобретение может быть использовано в различных органических синтезах для получения болеутоляющих, противовоспалительных лекарств и средств лечения заболеваний центральной нервной системы (Международный патент WO 03/053945, 2003; H.Rami et al. Bioorganic and Medicinal Chemistry Letters, 2006, 16, 3287-3291; S. Shapiro et al., J.Am.Chem.Soc., 1959, 81, 3083-3088). 1-(Аминоалкил)индолины могут также представлять интерес как радиопротекторы в связи с тем, что близкие по структуре индолилалкиламины при сравнительно низкой токсичности часто проявляют высокую радиозащитную активность (П.Г.Жеребченко. «Противолучевые свойства индолилалкиламинов». М., Атомиздат, 1971 г., стр.6-31; Н.Н.Суворов, B.C.Шашков. «Химия и фармакология средств профилактики радиационных поражений». М., Атомиздат, 1975 г., стр.122-139). Известен способ получения 1-(2-аминоэтил)индолина (выход ~65%) восстановлением 1-(2-аминоэтил)индола под действием бис(трифторацетокси)борана в среде тетрагидрофурана при 0-5°С (В.Maryanoff et al., J.Org.Chem., 1981, 46, 355-360). Недостатком способа является образование побочного продукта – 3-трифторацетил-1-(2-аминоэтил)индола, который загрязняет целевое соединение, а также труднодоступность исходного соединения. Последний получается с низким выходом (от 4 до 20%) 2-аминоэтилированием индола под действием тетрафторбората азиридиния из-за конкурирующего образования триптамина (Е.Pfiel et al., Angew.Chem.Int.Ed., 1967, 6, 178). Известен способ получения 1-(2-аминоэтил)индолина нагреванием индолина с Недостатками способа являются многостадийность и необходимость использования двойного избытка индолина (для связывания образующегося НВr). Известно получение 1-(2-аминоэтил)индолина кипячением смеси индолина, хлорацетонитрила и карбоната натрия в толуоле, содержащем 0,1% воды в течение 11 часов, с последующим восстановлением полученного (1-индолинил)ацетонитрила (выход 27%) литийалюминийгидридом в эфире, выход целевого соединения 51% (R.Mull, F.Park, Пат. США 3093632; 1963). Недостатками способа являются многостадийность, длительность процесса и низкий выход 1-(2-аминоэтил)индолина: в расчете на индолин он составляет всего 14%. Известен способ получения 1-(3-аминопропил)индолина цианэтилированием индолина под действием акрилонитрила в среде уксусной кислоты при 145°С в течение 12 часов с последующим восстановлением полученного N-( Недостатками способа являются многостадийность, длительность процесса и использование токсичного акрилонитрила. Известен способ получения 1-(2-аминоэтил)индолина кипячением индолина с бромгидратом Этот способ выбран нами в качестве прототипа как наиболее близкий по технической сущности. Недостатками способа являются низкий выход (26,7%), необходимость использования двойного избытка индолина (для связывания образующегося НВr), длительность процесса, а также необходимость отгонки толуола и проведения трудоемкой колоночной хроматографии для выделения продукта, что усложняет процесс. Задачей настоящего изобретения является разработка технологичного и эффективного способа получения 1-(аминоалкил)индолинов с хорошими выходами и высокой степенью чистоты. Поставленная задача решается путем взаимодействия индолина с бромгидратами аминоалкилбромидов в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением конечного продукта путем подщелачивания водным NaOH, экстракции органическими растворителями и перегонки в вакууме. Схема синтеза 1-(аминоалкил)индолинов(I-II) В качестве исходных соединений в синтезе целевых соединений (I-II) использованы индолин (99%-ный) фирмы «Acros», а также отечественные реактивы: бромгидрат Растворителем реакции является вода; бикарбонат натрия прибавляют к смеси индолина, бромгидрата и воды или в сухом виде (примеры 1 и 3), или в водном растворе (пример 2). Указанное соотношение реагентов является оптимальным для завершения алкилирования (длительность нагревания устанавливают ТСХ-методом). После обработки реакции и перегонки в вакууме получают целевые продукты (I-II) с выходами 65-70%, которые по данным ПМР- и масс-спектров имеют чистоту не менее 97%. При эквимолярном соотношении реагентов (1:1:1) не удается достичь полной конверсии индолина, примесь которого загрязняет целевые продукты (I-II), и их выходы снижаются. Использование большого избытка бромгидрата амина и NаНСО3 (более 1,4 моля на 1 моль индолина) нецелесообразно, так как это не приводит к увеличению выходов соединений (I-II). Алкилирование индолина бромгидратом 3-бромпропиламина идет труднее, чем с бромгидратом Изобретение иллюстрируется следующими примерами. Пример 1. В трехгорлую колбу объемом 1 л, снабженную мешалкой и обратным холодильником, помещают 49,41 г (0,415 моля) индолина, 102,14 г (0,498 моля) бромгидрата Найдено: С 74,04%; Н 8,81%; N 17,33%; М+ 162. С10Н14N2. Вычислено: С 74,07%; Н 8,64%; N 17,28%; М 162. Спектр ЯМР 1Н (CDCl3, Пример 2. Смесь 11,9 г (0,1 моля) индолина, 24,6 г (0,12 моля) бромгидрата Пример 3. Смесь 9,52 г (0,08 моля) индолина, 24,51 г (0,112 моля) бромгидрата 3-бромпропиламина и 20 мл воды нагревают при перемешивании до 95°С (в бане), затем прибавляют в течение 30 мин 9,4 г (0,112 моля) NаНСО3. Через 15 минут (при 95°С) реакционную смесь кипятят на колбонагревателе при перемешивании до окончания реакции (5-6 часов; ТСХ-анализ в системе ацетон – ССl4=1:3). После обработки реакции (аналогично примеру 1) перегонкой выделено 9,15 г (65%) 1-(3-аминопропил)индолина (II) в виде светло-желтого масла с т.кип. 105-109°/1 мм и nD Найдено: С 74,75%; Н 9,04%; N 15,72%; М+ 176. C11H16N2. Вычислено: С 75,00%; Н 9,09%; N 15,91%; М 176. Спектр ЯМР 1Н (CDCl3, Таким образом, предлагаемый способ является одностадийным, в отличие от способов-аналогов. Благодаря введению в реакцию третьего компонента – бикарбоната натрия и замене растворителя (вода вместо толуола) предлагаемый способ имеет следующие существенные преимущества перед прототипом: – повышение выходов (~ в 2,6 раза); – сокращение времени реакции в 9 раз (с 18 до 2 часов при синтезе I); – экономия индолина: на 1 моль бромгидрата требуется не 2, а 0,7-0,8 моля индолина; – технологичность: не нужно удалять растворитель реакции и осуществлять трудоемкую колоночную хроматографию для выделения продуктов. Высокая технологичность предлагаемого способа позволяет успешно применять его в промышленном масштабе. Кроме того, метод является экологически и пожаробезопасным, так как процесс проводят не в толуоле, а в воде.
Формула изобретения
Способ получения 1-(аминоалкил)индолинов путем взаимодействия индолина с бромгидратами аминоалкилбромидов в среде растворителя при нагревании, отличающийся тем, что реакцию проводят в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением конечного продукта путем подщелачивания водным NaOH, экстракции органическими растворителями и перегонки в вакууме.
|
||||||||||||||||||||||||||

 -бромэтилфталимидом при 100°С в течение 3,5 часов при соотношении реагентов 2:1 и последующим кипячением N-
-бромэтилфталимидом при 100°С в течение 3,5 часов при соотношении реагентов 2:1 и последующим кипячением N-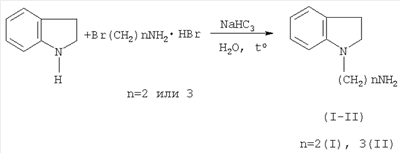
 299-06), 3-бромпропиламин гидробромид (ч., Реахим, ТУ 6-09-37-112-83) и натрий углекислый кислый (хч, Реахим, ГОСТ 4201-79).
299-06), 3-бромпропиламин гидробромид (ч., Реахим, ТУ 6-09-37-112-83) и натрий углекислый кислый (хч, Реахим, ГОСТ 4201-79). 20 1,5830 [лит.данные: т.кип. 154-160°/17 мм (R.Mull, F.Park, Пат. США 3093632; 1963)], чистого по ТСХ-анализу и ПМР- и масс-спектрам.
20 1,5830 [лит.данные: т.кип. 154-160°/17 мм (R.Mull, F.Park, Пат. США 3093632; 1963)], чистого по ТСХ-анализу и ПМР- и масс-спектрам. , м.д.): 1,35 (с, 2Н, NH2); 3,01 (м, 4Н, 2-СН2+3-СН2); 3,18 (т, 2Н, CH2NH2, J=7,2 Гц); 3,42 (т, 2Н, >NCH2, J=7,2 Гц); 6,59 (д, 1Н, Аr, J=7,8 Гц); 6,74 (т, 1Н, Аr, J=7,4 Гц); 7,14 (т, 2Н, Аr, J=7,8 Гц).
, м.д.): 1,35 (с, 2Н, NH2); 3,01 (м, 4Н, 2-СН2+3-СН2); 3,18 (т, 2Н, CH2NH2, J=7,2 Гц); 3,42 (т, 2Н, >NCH2, J=7,2 Гц); 6,59 (д, 1Н, Аr, J=7,8 Гц); 6,74 (т, 1Н, Аr, J=7,4 Гц); 7,14 (т, 2Н, Аr, J=7,8 Гц).