Патент на изобретение №2384566
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДА 3-ГИДРОКСИРЕМАНТАДИНА
(57) Реферат:
Изобретение относится к улучшенному способу получения 3-гидроксиремантадина, который обладает широким спектром биологической активности, применяется для профилактики и раннего лечения гриппа. Наличие гидроксильной группы в адамантановом ядре снижает токсичность и расширяет антивирусный спектр действия. Способ получения заключается в окислении (гидроксилировании) гидрохлорида ремантадина с помощью бромноватистой кислоты-НОВr, который в условиях реакции генерируется in situ из бромтрихлорметана-СВrСl3 и Н2О под действием Мо(СО)6. Процесс проводят при температуре 140-160°С в течение 6-10 часов, при мольном соотношении [ремантадин гидрохлорид]:[СВrСl3]: [Мо(СО)6]: [Н2O]=100:100:5:2000÷4000. Способ позволяет получить продукт с высоким выходом и высокого качества. В оптимальных условиях при конверсии ремантадина 90-99% единственным продуктом реакции является гидрохлорид 3-гидроксиремантадин. 1 табл.
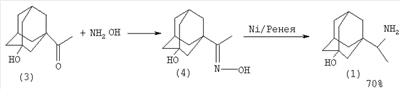
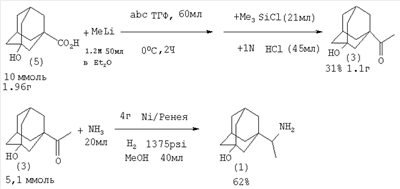
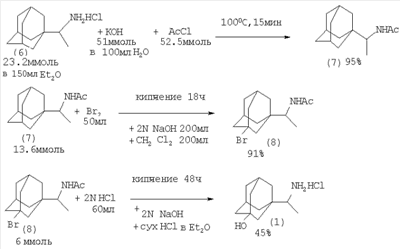
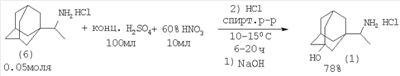
Изобретение относится к области органической химии, в частности к способу получения 3-гидроксиремантадина (гидрохлорида 1-(1-аминоэтил)-3-адамантанола). Производные адамантана обладают широким спектром биологической активности, такие лекарственные препараты на основе адамантана, как ремантадин, адапромин нашли применение для профилактики и раннего лечения гриппа. Наличие гидроксильной группы в адамантановом ядре снижает токсичность и расширяет антивирусный спектр действия (Е.И.Багрий. Адамантаны. М.: Наука, 1989, 264 с.[1]; В.И.Вотьяков, Е.И.Бореко, Г.В.Владыко и др. Перспективы развития химии каркасных соединений и их применение в отраслях промышленности. – Киев, 1986. С.12-16 [2]). 3-Гидроксиремантадин (1) (гидрохлорид 1-(1-аминоэтил)-3-адамантанол) можно получить из 3-бромадамантилкарбоновой кислоты (2). Вначале обработкой 3-бромадамантил-1-карбоновой кислоты (2) SOCl2, затем EtOMgCH(CO2Et)2 и кислотным гидролизом получают 1-ацетил-3-адамантанол (3) (выход 31%). 1-Ацетил-3-адамантанол вовлекается в реакцию с гидроксиламином, давая оксим (4). На последней стадии оксим (4) восстанавливают с помощью водорода никелем Ренея с получением целевого продукта – 3-гидроксиремантадина (выход 70%) (Г.И.Козушко, О.Миздох, В.И.Вотьяков, В.А.Русаев, В.Ф.Даниленко, Г.У.Степанова, К.И.Даниленко. Фарм.журн. (Киев), Недостатки метода: 1. Труднодоступность исходных реагентов 3-бромадамантанкарбоновой и этоксиброммалоновой кислот. 2. Многостадийность процесса. 3. Использование агрессивного SOCl2. 4. Токсичность гидроксиламина. 5. Низкий общий выход целевого продукта. Исходным соединением для получения 3-гидроксиремантадина (1) может служить 3-гидроксиадамантанкарбоновая кислота (5). На первой стадии оксикислоту (5) обрабатывают большим избытком метиллития с получением 1-ацетил-3-адамантанола (3), который при восстановительном аминировании с помощью жидкого аммиака и водорода под давлением в присутствии никеля Ренея при 100°С превращается в целевой 3-гидроксиремантадин с выходом 62% (H.Stetter, J.Meyer. Ber. Vol.95. Р.667 (1962) [4]; М.Л.Багал, В.И.Лантвоев. ЖОрХ Т.9, с.291 (1973) [5]). Метод имеет ряд существенных недостатков: 1. Необходимость использования большого избытка пожароопасного метиллития. 2. Использование абсолютированных растворителей. 3. Труднодоступность исходной гидроксикислоты. 4. Высокое давление водорода (~100 атм). Более коротким путем (3 стадии) 3-гидроксиремантадин (1) был получен из ремантадина (P.S.Manchand, R.L.Cerrut, J.A.Martin, C.H.Hill, J.H.Merett, E.Keech, R.B.Belshe, E.V.Connell, J.S.Sim. J.Med.Chem. V.33, Ацетилирование ремантадина (6) ацетилхлоридом привело к образованию ацетамида (7) с 95% выходом, обработка которого избытком брома дает 3-бром-1-ацетамидадамантан (8) (91%). Гидролиз (8) соляной кислотой приводит к целевому продукту с 45% выходом. Недостатки метода: 1. Использование большого избытка ядовитого брома. 2. Для проведения реакции гидролиза 3-бром-N-ацетил-1-(1-аминоэтил)адамантана, снятия ацетильной защиты и получения гидрохлорида 3-гидроксиремантадина требуется 10-20-кратный избыток NaOH и НСl, что приводит к образованию значительного количества сточных вод, содержащих NaOH и НСl, NaCl и СН3СООNа. 3. Низкий выход целевого продукта (суммарный выход (1), считая на 3 стадии, составляет 39%). Кратчайший путь синтеза 3-гидроксиремантадина заключается в окислении ремантадина смесью азотной и серной кислот (Л.Н.Лаврова, М.К.Индулен, Г.М.Рязанцева, В.С.Корытный, В.Г.Яшунский. Хим.-фарм.журн. Т.24, Реакцию проводят по следующей методике. К 100 мл концентрированной H2SO4 прибавляют 10 мл 60% НNО3 и при 10-15°С порциями добавляют 0.05 моля ремантадина. Смесь перемешивают в течение 6-20 ч, выливают на лед, подщелачивают и экстрагируют с помощью СНСl3 1-(1-аминоэтил)-3-адамантанол в виде основания. Экстракт сушат, растворитель отгоняют, остаток растворяют в спирте, обрабатывают спиртовым раствором HCl. 3-Гидроксиремантадин выделяют либо упариванием спиртового раствора, либо высаживанием эфиром. На основании сходства по двум признакам (исходный реагент – ремантадин, образование в результате реакции 3-гидроксиремантадина) за прототип взят метод окисления ремантадина с помощью серной и азотной кислот [7]. Прототип имеет следующие недостатки: 1. Использование большого избытка агрессивных концентрированных неорганических кислот (H2SO4 и НNО3). 2. Образование неорганических отходов (Na2SO4, NaNO3) в результате нейтрализации и сточных вод, которые необходимо утилизировать. 3. Усложнение процедуры выделения и очистки целевого продукта из-за неполной конверсии ремантадина и большого разбавления при смешении 0.05 молей ремантадина (9.55 г) и 100 мл H2SO4 (конц.). 4. Значительная продолжительность реакции (до 20 ч). Задачей настоящего изобретения является увеличение выхода 3-гидроксиремантадина (гидрохлорида 1-(1-аминоэтил)-3-адамантанола) и упрощение технологии его получения. Авторами предлагается способ получения 3-гидроксиремантадина, не имеющий указанных недостатков. Сущность способа заключается в окислении (гидроксилировании) ремантадина с помощью НОВr, который в условиях реакции генерируется in situ из бромтрихлорметана СВrСl3 и Н2О под действием Мо(СО)6 при 140-160°С в течение 6-10 часов, при мольном соотношении [ремантадин]: [СВrСl3]:[Мо(СО)6]:[H2O]=100:100:1÷5:2000÷4000. В оптимальных условиях при конверсии гидрохлорида 1-(1-аминоэтил)-3-адамантана 90-99% единственным продуктом реакции является 3-гидроксиремантадин гидрохлорид (1) Существенные отличия предлагаемого способа от прототипа. 1. Для получения 3-гидроксиремантадина гидроксилированием ремантадина используется система ВrССl3-Н2O-Мо(СО)6, генерирующая in situ сильный окислитель бромноватистую кислоту. Преимущества предлагаемого метода. 1. Доступность окислительной системы Н2О-СВrСl3. 2. Отсутствие агрессивных окислителей. 3. Селективность процесса и высокий выход целевого продукта. 4. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат. Предлагаемый способ поясняется примерами. Общая методика окисления (гидроксилирования) ремантадина В микроавтоклав из нержавеющей стали (V=17 мл) или стеклянную ампулу (V=20 мл) (результаты параллельных опытов практически не отличаются) под аргоном помещали 0.1-0.5 ммоль Мо(СО)6, 10 ммоль ремантадина (гидрохлорида 1-(1-аминоэтил)-3-адамантана), 10 моль ВrССl3 и 200-400 ммоль Н2О (которая играет роль реагента и растворителя одновременно), автоклав герметично закрывали (ампулу запаивали) и нагревали при 140-160°С в течение 6-10 часов. После окончания реакции микроавтоклав (ампулу) охлаждали до ~20°С, вскрывали, реакционную массу экстрагировали хлористым метиленом (5 мл × 3р), растворитель отгоняли, остаток кристаллизовали из этанола. Выход 31-99%. ПРИМЕР 1. В микроавтоклав помещали под аргоном 0.3 ммоль Мо(СО)6, 10 ммоль ремантадина (гидрохлорида 1-(1-аминоэтил)-3-адамантана), 10 ммоль ВrССl3 и 400 ммоль Н2О, автоклав закрывали и нагревали при 140°С в течение 10 часов. После окончания реакции автоклав охлаждали до комнатной температуры, вскрывали, после обработки реакционной массы, как указано выше, был выделен 3-гидроксиремантадин (гидрохлорида 1-(1-аминоэтил)-3-адамантанол) с выходом 90% (конверсия ремантадина 95%). Выделенный 3-гидроксиремантадин гидрохлорид имел т.пл. 323-324°С. ИК-спектр, 43.74 (C-1), 55.66 (СНNН3 Найдено (%): С 61.98; Н 9.37; Cl 15.32; N 6.09. C12H22ClNO. Вычислено (%): С 62.18; Н 9.57; Cl 15.30; N 6.04; О 6.91. Другие примеры, подтверждающие способ, приведены в таблице 1.
Формула изобретения
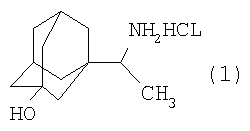
Способ получения гидрохлорида 3-гидроксиремантадина формулы (I):
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||

 1, с.29-31. МУХАМЕТШИНА Л.Ф. и др. «Новый метод гидроксилирования адамантана и его производных». XVIII Менделеевский съезд по общей и прикладной химии. Тезисы докладов.Т1. Пленарные доклады. Достижения и перспективы химической науки. – М.: Граница. 2007, с.352.
1, с.29-31. МУХАМЕТШИНА Л.Ф. и др. «Новый метод гидроксилирования адамантана и его производных». XVIII Менделеевский съезд по общей и прикладной химии. Тезисы докладов.Т1. Пленарные доклады. Достижения и перспективы химической науки. – М.: Граница. 2007, с.352.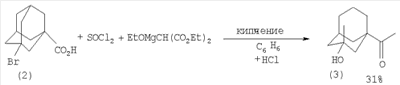
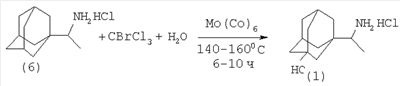
 , 2500-3500 мин-1 (NH и ОН). Спектр ЯМР 1H (СDСl3,
, 2500-3500 мин-1 (NH и ОН). Спектр ЯМР 1H (СDСl3,  , м.д., TMS): 1.57 m (2H, H2), 1.51 м (6H, H4, Н6, Н10), 2.27 м (2Н, Н5, Н7), 1.61-1.76 м (4Н, Н8, Н9), 1.24 (2H, Н8, Н9), 1.24 д (3Н, СН3), 3.09 кв (1H, СН), 7.20 с (3Н, NH3
, м.д., TMS): 1.57 m (2H, H2), 1.51 м (6H, H4, Н6, Н10), 2.27 м (2Н, Н5, Н7), 1.61-1.76 м (4Н, Н8, Н9), 1.24 (2H, Н8, Н9), 1.24 д (3Н, СН3), 3.09 кв (1H, СН), 7.20 с (3Н, NH3 +Сl–). Спектр ЯМР 13С (CDCl3,
+Сl–). Спектр ЯМР 13С (CDCl3,