Патент на изобретение №2384560
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИ-1-ФЕНИЛЭТАНОВ
(57) Реферат:
Настоящее изобретение относится к способу получения 1-алкокси-1-фенилэтанов общей формулы С6Н5СН(СН3)ОR (R=СН3, С2Н5, n-С3Н7, n-С4H9, n-С5Н11, n-С6Н13, n-C7H15, n-C8H17), которые обладают высокой термической стабильностью и могут быть использованы в качестве пластифицирующих агентов в хлорсодержащих полимерах и, кроме того, могут применяться в качестве компонента катализатора в процессах полимеризации и соолигомеризации олефинов. Способ включает взаимодействие стирола со спиртами нормального строения ROH, где R такое же, как указано выше, в присутствии катализатора – цеолита типа Y с мольным соотношением SiO2/Аl2O3=6,0-7,0, в Н-форме, при мольном соотношении стирол:спирт=1:1-3, температуре 80÷120°С и количестве катализатора 5-10 маc.%. Способ позволяет получить целевые продукты с высоким выходом. 1 табл.
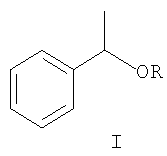
Изобретение относится к области органической химии, в частности к способу получения 1-алкокси-1-фенилэтанов общей формулы I:
где R=СН3, С2Н5, n-С3Н7, n-С4Н9, n-C5H11, n-С6Н13, n-C7H15, n-C8H17. Соединения АrСН(СН3)OR (где R, например, алкил-, алкенил-, арил-, алкарил- и циклоалифатические группа) обладают высокой термической стабильностью и могут быть использованы в качестве пластифицирующих агентов в хлорсодержащих полимерах [Пат. США солями (Hg(OAc)2, Hg(CF3COO)2, Hg(NO3)2 и др.) при 22°С. Последующее демеркурирование проводят in situ щелочным раствором NaBH4: Конверсия стирола максимальна в случае взаимодействия с метиловым спиртом (до 99%); с изопропиловым и трет-бутиловым спиртами конверсия стирола ниже и составляет 40-90%, кроме того, наряду с эфиром, образуется спирт АrСН(СН3)ОН. Недостатками этого способа является многостадийность, использование в качестве катализатора высокотоксичных солей ртути. Кроме того, процесс проводят с использованием больших количеств щелочи (NaOH), в результате чего образуются значительные объемы стоков. В патенте [Пат. США где R=СН3, С2Н5, i-С3Н7, n-С4Н9 Реакцию проводят при температуре от 50 до 150°С в автоклаве (в случае метанола и этанола) или в колбе. Концентрация катализатора составляет не более 5%, время реакции 6-10 часов. Сложность осуществления данной реакции состоит в том, что в присутствии кислотных катализаторов с высокой скоростью протекает олигомеризация стирола. Авторы отмечают, что параллельно с эфирами образуется значительное количество олигомеров стирола. Для уменьшения выхода олигомеров предложено использовать ингибитор полимеризации – пирогаллол. Конверсия стирола составляет 50-90%, выходы эфиров 60-80%. К недостаткам способа относится: невысокие выходы эфиров; необходимость стадий нейтрализации кислотного катализатора, отмывки и осушки реакционной массы; использование растворителя, который необходимо регенерировать по окончании реакции; большая длительность реакции.
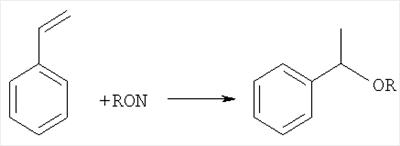
К недостаткам этого способа можно отнести недостаточно высокую активность катализатора в реакции получения эфиров стирола. Кроме того, известна низкая термическая стабильность катионообменных смол при повышенных температурах (120-150°С). Задачей настоящего изобретения является увеличение выхода 1-алкокси-1-фенилэтанов. Это достигается тем, что способ получения 1-алкокси-1-фенилэтанов формулы С6Н5СН(СН3)ОR (R=СН3, С2Н5, n-С3Н7, n-С4H9, n-С5Н11, n-С6Н13, n-C7H15, n-C8H17) взаимодействием стирола со спиртами нормального строения ROH (R=СН3, С2Н5, n-С3Н7, n-С4Н9, n-С3Н7, п-С6Н13, n-C7H15, n-C8H17) в присутствии кислотных катализаторов осуществляют, согласно изобретению, в присутствии цеолита HY с мольным соотношением SiO2/Аl2O3=6,0-7,0. Реакцию проводят при мольном соотношении стирол: спирт =1:1-3, температуре 80-120°С и количестве катализатора 5-10 мас.% (в расчете на реакционную смесь). После окончания реакции катализатор отделяют фильтрованием. Его можно использовать многократно без потери активности. Полученные 1-алкокси-1-фенилэтаны выделяют из реакционной массы вакуумной перегонкой. Образцы цеолита Y синтезировали согласно способу, описанному в патенте [Пат. 2090502 РФ, 1997]. Этот метод позволяет прямым синтезом получать цеолит NaY с мольным отношением SiO2/Аl2O3=6,0÷7,0. Указанный цеолит Y характеризуется высокой химической и термической стабильностью: не разрушается с образованием аморфной фазы при ионном обмене, выдерживает высокотемпературные обработки до 750-800°С в среде воздуха и водяного пара. Синтезированный цеолит NaY двух(трех)-кратным декатионированием переводили в NН4-форму, а затем последующим прокаливанием при 540°С в Н-форму. Степень обмена Na+ на Н+ составляла 80-97%. Сравнительный анализ заявляемого решения с прототипом показывает, что заявляемый способ отличается от прототипа тем, что взаимодействие стирола с н-спиртами проводят в присутствии цеолита HY с мольным соотношением SiO2/Al2O3=6,0÷7,0. Процесс этерификации осуществляют при мольном соотношении стирол: спирт =1:1÷3, температуре 80÷120°С и количестве катализатора 5÷10 мас.% (в расчете на реакционную смесь). Конверсия стирола составляет 78,0÷90,2 мол.%, селективность образования 1-алкокси-1-фенилэтанов – 90,5÷99,5 мол.%, димеров стирола – 0,5÷9,5 мол.%. В указанных условиях олигомерй стирола или вообще не образуются, или” присутствуют в небольших количествах (не более 9,5 мол.%). Максимальная степень олигомеризации стирола (п) составляет 2. Тримеры и более высокомолекулярные соединения отсутствуют. Предлагаемый способ осуществляют следующим образом. Катализатор – цеолит Y в Н-форме (мольное отношение SiО2/Al2O3 составляет 6,0÷7,0) перед опытами прокаливают в атмосфере воздуха при 540°С в течение 4 ч. Взаимодействие стирола со спиртами проводят в термостатированных металлических автоклавах или стеклянных реакторах. В автоклав (колбу) загружают стирол и спирт в мольном соотношении 1:1÷3, катализатор – цеолит HY в количестве 5-10 мас.% (на реакционную массу). Реакцию проводят при постоянном перемешивании при температуре 80-120°С в течение 5 ч. После окончания реакции фильтрованием отделяют катализатор. Реакционную массу разгоняют в вакууме. Анализ реакционной массы и продуктов осуществляют методом ГЖХ на хроматографе марки HRGS 5300 Mega Series “Carlo Erba” с пламенно-ионизационным детектором (капиллярная колонка 25 м, фаза SE-30, программирование температуры от 50 до 280°С со скоростью подъема 8°С/мин, температура детектора 250°С, температура испарителя 300°С, газ-носитель – гелий, 30 мл/мин). Предлагаемый способ иллюстрируется следующими примерами (табл.1). ПРИМЕР 1. В автоклав загружают 5,7 мл (0,05 моль) стирола и 4,0 мл (0,10 моль) метилового спирта, 0,84 г цеолита HY (SiO2/Аl2O3=6,0). Автоклав помещают в термостат. Реакцию проводят при постоянном перемешивании при температуре 110°С в течение 5 ч. Реакционную массу отфильтровывают от катализатора и разделяют вакуумной разгонкой. Получают 5,2 г продукта I (R=СН3). Конверсия стирола составляет 78,3 мол.%, селективность по 1-метокси-1-фенилэтану – 99,5% (т.кип. 78,6°С/50 мм рт.ст.; спектр ЯМР 1Н ( ПРИМЕР 2. В термостатируемую колбу загружают 4,6 мл (0,04 моль) стирола и 11,0 мл (0,12 моль) бутилового спирта, 1,3 г цеолита HY (SiO2/Аl2O3=6,0). Реакцию проводят при постоянном перемешивании при температуре 80°С в течение 5 ч. Реакционную массу отфильтровывают от катализатора и разделяют вакуумной разгонкой. Получают 6,3 г продукта I (R=n-С4Н9). Конверсия стирола составляет 90,2 мол.%, селективность по 1-бутокси-1-фенилэтану – 95,9% (т.кип. 95,1°С/10 мм рт.ст.; спектр ЯМР 1Н ( ПРИМЕРЫ 3-5. Аналогично примеру 1. Условия и результаты примеров представлены в таблице 1. ПРИМЕРЫ 6-10. Аналогично примеру 2. Условия и результаты примеров представлены в таблице 1.
Формула изобретения
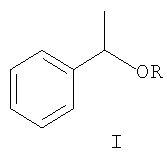
Способ получения 1-алкокси-1-фенилэтанов формулы I
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 2575444]. Эфиры I (где R=СН3, C2H5) предложено применять в качестве компонента катализаторов в процессах полимеризации и соолигомеризации олефинов [Пат. США
2575444]. Эфиры I (где R=СН3, C2H5) предложено применять в качестве компонента катализаторов в процессах полимеризации и соолигомеризации олефинов [Пат. США 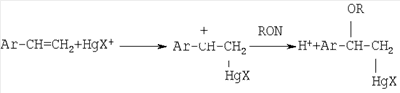
 , м.д.): 1.36 (d, 3, СН3), 3.18 (s, 3, ОСН3), 4.17 (q, 1, CH), 7.3 (m, 5, ArH); спектр ЯМР 13С (
, м.д.): 1.36 (d, 3, СН3), 3.18 (s, 3, ОСН3), 4.17 (q, 1, CH), 7.3 (m, 5, ArH); спектр ЯМР 13С ( =5 ч)
=5 ч)