Патент на изобретение №2384334
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) МНОГОКОМПОНЕНТНЫЙ КОМБИНИРОВАННЫЙ СОСТАВ, ОБЛАДАЮЩИЙ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ
(57) Реферат:
Изобретение относится к медицине, а именно к фармацевтической промышленности, и касается композиции, обладающей высокой туберкулостатической активностью, позволяет понизить токсичность, а следовательно, и побочные эффекты входящих в него ингредиентов: изониазида, рифампицина и пиразинамида. 4 табл.
Изобретение относится к области медицины и касается многокомпонентного фармацевтического состава, обладающего противотуберкулезной активностью и пригодного для лечения туберкулеза, вызванного изониазид-резистентными штаммами М.tuberculosis. Изменение социально-экономических условий и экологической обстановки в России привело в последние 10-15 лет к росту заболеваемости туберкулезом, которая в отдельных районах начинает принимать характер эпидемии. Фтизиатры отмечают не только рост заболеваемости, но и полирезистентность (устойчивость) возбудителя к однокомпонентным туберкулостатическим лекарственным средствам. Из уровня техники известны основные химиотерапевтические средства для лечения различных форм туберкулеза – производные изоникотиновой кислоты, прежде всего изониазид, а также антибиотики широкого спектра действия: стрептомицин, канамицин, рифампицин, обладающие высокой бактериостатической активностью в отношении микобактерий туберкулеза (Справочник Видаль Лекарственные препараты в России. Изд. 12-е переработанное, исправленное и дополненное. Астра Фарм Сервис, 2006 г., стр.1497, 1551, 1554). Благодаря высокой бактериостатической активности основным препаратом для лечения туберкулеза является изониазид. Особенностью терапии туберкулеза в настоящее время является одновременное назначение нескольких туберкулостатических лекарственных средств различных химических групп и механизмов действия. Достижение стойкого лечебного эффекта обеспечивается длительным курсом химиотерапии, который составляет от 6 до 12 месяцев; профилактические курсы проводят 2 раза в год продолжительностью 2-3 месяца (Фтизиатрия. Национальное руководство под ред. М.И.Прельмана, М.: ГЭОТАР-Медиа, 2007, стр.414-426). В связи с этим для обеспечения комфортности лечения больных целесообразно создание комплексных многокомпонентных лекарственных средств. Известны аналоги изобретения капсулы рифампицина, таблетки изониазида, таблетки пиразинамида (Справочник Видаль Лекарственные препараты в России. Изд. 12-е переработанное, исправленное и дополненное. Астра Фарм Сервис, 2006 г., стр.1497, 1551, 1554). Прототипом изобретения являются таблетки изониазида. Недостатками прототипа являются высокая токсичность, быстрая элиминация из организма, а также неудобство для применения больными, которое заключается в многократном ежедневном приеме нескольких таблеток в течение нескольких месяцев. В патенте РФ изониазида – 75,0 крахмальный клейстер 10% – 11,5 крахмал картофельный – 5,8 кислота стеариновая – 0,4 Субстанции изониазида, пиразинамида и рифампицина не обладают способностью к прямому таблетированию (Патент РФ Технической задачей предлагаемого изобретения является создание отечественного многокомпонентного состава для лечения туберкулеза, обладающего длительным сроком годности, высокой туберкулостатической активностью по отношению к микобактерии туберкулеза, устойчивых к изониазиду, а так же пониженной токсичностью. Данная техническая задача достигается за счет синергизма действующих веществ, введенных в композицию ингредиентов в гранулах на 100 г:
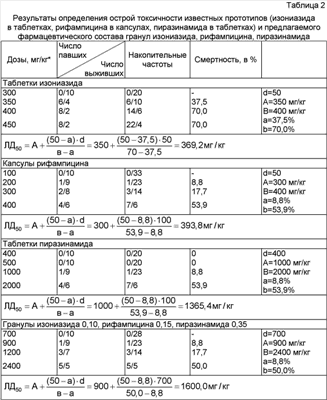
А также путем введения в качестве вспомогательных веществ пектина и поливинилпирролидона, которые обеспечат пролонгирование действия лекарственных веществ и понизят гепатотоксичность изониазида (Л.А.Саджая. Биохимическое обоснование путей снижения гепатотоксичности изониазида на основе сочетания с полисахаридами. Дис. канд. фармац. наук. – Пятигорск, 1999. – 120 с.). В заявляемый состав входят изониазид, пиразинамид, рифампицин и вспомогательные вещества, взятые в количестве от 10 до 40% от общей массы. В качестве вспомогательных веществ используют пектин в количестве от 10 до 30% от массы действующих веществ. Поливинилпирролидон вводится в количестве от 10 до 35% от массы действующего вещества, сахар молочный вводится в количестве от 10 до 30%. Фармацевтический состав выполнен в виде гранул. Состав соответствует требованиям, предъявляемым к фармацевтическим средствам, и обладает повышенной стабильностью при хранении. Пример 1 Приготовление гранул осуществляется методом влажного гранулирования продавливанием с использованием технологического приема раздельного влажного гранулирования изониазида, пиразинамида и рифампицина. Изониазид в количестве 0,500 кг предварительно измельчали в барабане шаровой мельницы вместе с шарами при оптимальной скорости в течение 5-8 минут. Измельченный продукт просеивали через сито-капрон Для приготовления увлажнителя на весах отвешивали 0,327 кг спирта этилового 95% и 0,173 кг воды и помещали их в емкость для приготовления увлажнителя. 0,500 кг пектина просеивали через сито Однородность и увлажненность массы контролировали органолептической пробой. Масса с оптимальной влажностью представляет собой влажную, компактную смесь, не прилипающую к пальцам руки, но рассыпающуюся на отдельные комочки при сдавливании. Далее осуществляли влажное гранулирование в грануляторе методом продавливания через сетку с диаметром отверстия 4 мм. Гранулят выгружали в лотки из нержавеющей стали тонким слоем 1-2 см. Сушку гранул производили в вакуум-сушильном шкафу при периодическом перемешивании при температуре 30-40°С и вакууме 0,7-0,8 кгс/см2. Продолжительность сушки 30-40 минут до остаточной влажности 2,5-3,0%. Рифампицин в количестве 0,750 кг измельчали в барабане шаровой мельницы вместе с шарами при оптимальной скорости в течение 5-8 минут. Измельченный продукт просеивали через сито-капрон Пиразинамид в количестве 1,750 кг измельчали в барабане шаровой мельницы вместе с шарами при оптимальной скорости в течение 5-8 минут. Измельченный продукт просеивали через сито-капрон Полученные гранулы пиразинамида по основному технологическому параметру – насыпной плотности – соответствовали гранулам рифампицина и изониазида, что послужило основанием для дальнейшего совместного сухого гранулирования. Совместное сухое гранулирование осуществляли на универсальном грануляторе через сетку с диаметром отверстий 2 мм. Гранулы представляли собой смесь красно-коричневых и белых частичек неправильной формы, обладающие необходимой механической прочностью, масса полученных гранул составляла 4,75 кг, выход – 95%. Установление сроков годности гранул проводили методом «ускоренного старения» в двух температурных режимах при 40 и 60°С, а также в естественных условиях («Инструкция по проведению работ с целью определения сроков годности лекарственных средств на основе метода «ускоренного старения» при повышенной температуре И 42-2-82»). В качестве опытных образцов использовали 3 серии гранул, а также таблетки пиразинамида, капсулы рифампицина, таблетки изониазида. О стабильности ингредиентов заявляемого фармацевтического состава и прототипов судили по содержанию посторонних примесей и количественному содержанию лекарственных веществ в испытуемых образцах. Контроль качества проводили через равные промежутки времени, эквивалентные 6 месяцам хранения. Для гранул срок хранения составил 3 года, для таблеток изониазида – 4 года, для таблеток пиразинамида – 3 года, для капсул рифампицина – 2 года. Для изучения специфической антимикробной активности патентуемого состава по отношению к изониазид-резистентным штаммам M.tuberculosis использовали метод абсолютных концентраций на среде Левенштейна-Йенсена (приказ МЗ РФ Результаты представлены в таблице 1, где «-» показывает отсутствие роста, которое свидетельствует о чувствительности к лекарственному препарату; «+» – рост микрофлоры на среде свидетельствует об устойчивости к лекарственному препарату. Анализ данных, представленных в таблице 1, свидетельствует о том, что патентуемый многокомпонентный фармацевтический состав в виде гранул обладает туберкулостатической активностью по отношению к 9 штаммам M.tuberculosis, устойчивых к действию изониазида, рифампицина и пиразинамида, применяемых индивидуально, следовательно, проявляемая туберкулостатическая активность обусловлена совместным воздействием на микобактерии туберкулеза трех лекарственных веществ. Определение острой токсичности гранул изониазида, рифампицина и пиразинамида, а также прототипов (таблеток изониазида, таблеток пиразинамида, капсул рифампицина) проводили на белых беспородных мышах обоего пола массой 18±2 г. Первой группе животных перорально вводили суспензию таблеток изониазида, диспергированных в 0,9% растворе натрия хлорида; второй группе – суспензию рифампицина в 0,9% растворе натрия хлорида; третьей – суспензию таблеток пиразинамида в 0,9% растворе натрия хлорида; четвертой – суспензию патентуемого многокомпонентного фармацевтического состава гранул изониазида, рифампицина и пиразинамида. Наблюдение за поведением и состоянием животных проводили в течение 10 дней. Далее рассчитывали величину ЛД50 по методике Беренса (М.Л.Беленький. Элементы количественного учета фармакологического эффекта. СПб.: Мед. лит., 1963. – 250 с). Результаты эксперимента представлены в таблице 2. В таблице приведены дозы лекарственных препаратов в пересчете на действующие вещества. Анализ полученных данных свидетельствует о том, что токсичность лекарственных веществ, введенных в виде гранул патентуемого фармацевтического состава, в 4,3 раза, 4,1 раза и в 1,2 раза ниже таковой для прототипов, а именно изониазида в таблетках, рифампицина в капсулах, пиразинамида в таблетках. Хроническую токсичность заявляемого фармацевтического состава, а также прототипов определяли на беспородных белых крысах с массой тела 200-250 г. Хроническую токсичность определяли на 5 группах животных по 10 крыс в каждой. Испытуемые вещества вводили перорально ежедневно в течение 6 месяцев. Первая группа крыс получала заявляемый фармацевтический состав, содержащий 40 мг/кг изониазида, 60 мг/кг рифампицина, 140 мг/кг пиразинамида, в виде суспензии в 0,9% растворе натрия хлорида. Вторая группа получала суспензию таблеточной массы таблеток изониазида в 0,9% растворе натрия хлорида в дозе 40 мг/кг в пересчете на действующее вещество. Третья группа получала суспензию рифампицина в 0,9% растворе натрия хлорида в дозе 60 мг/кг в пересчете на действующее вещество. Четвертая группа получала суспензию таблеток пиразинамида в 0,9% растворе натрия хлорида в дозе 140 мг/кг в пересчете на действующее вещество. Пятая группа – контрольная. В процессе эксперимента наблюдали за поведением и состоянием животных. После завершения опыта проводили биохимический и клинический анализ крови животных, а также гистологическое исследование печени, сердца, почек. В таблицах 3 и 4 представлены полученные результаты (среднее значение из 10 определений). Достоверность результатов по отношению к контролю составляет р<0,05. Результаты гематологических исследований крови животных, получавших заявляемый фармацевтический состав в виде гранул, свидетельствуют об отсутствии грубых отклонений от нормы и от соответствующих показателей в контроле. Понижение содержания альбумина в сыворотке крови крыс, получавших изониазид и рифампицин, свидетельствует о развитии хронической печеночной недостаточности. Увеличение содержания в сыворотке крови животных, получавших изониазид и рифампицин, аспартатаминотрансферазы (ACT) и аланинаминотрансферазы (АЛТ) и щелочной фосфатазы свидетельствует о некрозе клеток печени и о развитии у крыс гепатита. Снижение уровня холестерина (норма 3,9-7,2 мМ/л) может свидетельствовать о развитии острого гепатита у крыс, получавших изониазид и рифампицин. Следовательно, введение изониазида и рифампицина вызывает токсическое поражение печени. В сыворотке крыс, получавших гранулы изониазида, рифампицина, пиразинамида, как биохимические, так и клинические показатели крови в норме, что свидетельствует об отсутствии токсического влияния гранул на организм животных. При макро- и микроскопическом исследовании внутренних органов подопытных животных, получавших изониазид и рифампицин, отмечены грубые деструктивные изменения в печени. Кроме того, наблюдаются деструктивные изменения в почках крыс, получавших рифампицин. Во внутренних органах крыс, получавших гранулы изониазида, рифампицина, пиразинамида, деструктивные изменения отсутствуют. Применение предлагаемого комбинированного состава, обладающего выраженной туберкулостатической активностью и пониженной токсичностью, позволяет повысить эффективность совместного применения изониазида, рифампицина и пиразинамида, а также уменьшить побочные эффекты лекарственных веществ, входящих в состав гранул.
Формула изобретения
Комбинированный состав, обладающий противотуберкулезной активностью, содержащий изониазид, отличающийся тем, что дополнительно содержит рифампицин, пиразинамид, пектин, поливинилпирролидон, сахар при следующем соотношении ингредиентов, г на 100 г:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 2146130, 2000 г. описана композиция для лечения туберкулеза, содержащая 0,1 г изониазида и 0,01 г вспомогательных веществ на одну таблетку. В качестве вспомогательных веществ в таблетки включены крахмал картофельный или кукурузный, вода. В описании изобретения приведен следующий пример композиции:
2146130, 2000 г. описана композиция для лечения туберкулеза, содержащая 0,1 г изониазида и 0,01 г вспомогательных веществ на одну таблетку. В качестве вспомогательных веществ в таблетки включены крахмал картофельный или кукурузный, вода. В описании изобретения приведен следующий пример композиции: