Патент на изобретение №2382738
|
||||||||||||||||||||||||||
(54) СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ФТОРА
(57) Реферат:
Изобретение относится к сорбционно-осадительным способам очистки сточных вод от фтора и может быть использовано в горнодобывающей, металлургической, химической и других отраслях промышленности. Для осуществления способа проводят взаимодействие воды с церийсодержащим реагентом в виде сульфата церия (III) или сульфата церия (IV) в режиме гидролиза при регулировании рН в пределах 4-7. Реагент берут в соотношении 2,5-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде. В указанном интервале рН происходит связывание фтора в твердую фазу, образующуюся при гидролизе соединений церия, которую отделяют от жидкой фазы. Фторсодержащую твердую фазу обрабатывают 80-95% серной кислотой при 175-190°С с получением фтористого водорода и регенерированного сульфата церия (IV). Регенерированный сульфат церия (IV) может быть растворен в воде и обработан пероксидом водорода до обесцвечивания с получением регенерированного сульфата церия (III). Способ обеспечивает глубокую очистку сточных вод от фтор-иона и фторсодержащих комплексных соединений при обеспечении возможности очистки больших объемов сточных вод. Достигаемая глубина очистки сточных вод от фтора составляет 1,25-1,5 мг/л, а остаточное содержание сульфат-иона равно 165-340 мг/л, что не превышает ПДК для водоемов питьевого назначения. Фтор выделяют в виде товарных соединений – фторидов натрия или калия. Способ по изобретению несложен и может быть реализован в прудах-отстойниках с использованием стандартного оборудования. 4 з.п. ф-лы.
Изобретение относится к сорбционно-осадительным способам очистки сточных вод от фтора и может быть использовано в горнодобывающей, металлургической, химической и других отраслях промышленности. Известен способ очистки сточных вод от фтора (см. пат. 2228911 РФ, МПК7 C02F 1/28, 1/58, 1/52, 2004), согласно которому сточные воды, содержащие фтор-ион, обрабатывают водорастворимым сульфатным соединением титана, взятым в соотношении не менее 5 моль титана на 1 г-атом фтора, содержащегося в очищаемой сточной воде, при этом рН пульпы поддерживают в пределах 3,0-5,5, а отделенную твердую фазу обрабатывают серной кислотой при нагревании с получением фтористого водорода и спека, содержащего регенерированное сульфатное соединение титана. В зависимости от содержания фтора в сточной воде твердую фазу обрабатывают 55,0-93,5% серной кислотой при 120-130°С или 75,0-93,5% серной кислотой при 170-180°С. Достигаемая глубина очистки сточных вод от фтор-иона составляет 0,5-1,4 мг/л, остаточное содержание сульфат-иона достигает 444 мг/л. Фтор выделяют в виде фторида натрия или фтористоводородной кислоты. Недостатком данного способа является то, что он не является универсальным, поскольку при обеспечении эффективной очистки сточных вод от фтора, находящегося в виде фтор-иона, способ не позволяет удалять фтор из стоков, содержащих фтор в виде химически прочных комплексов, в частности с алюминием, титаном и железом. Недостатком данного способа является также то, что регенерация титансодержащего реагента затруднительна в связи с трудностью его смешения с серной кислотой и необходимостью последующего брикетирования смеси. Известен также способ очистки сточных вод от фтора (см. пат. 4717554 США, МПК4 C01F 17/00, C02F 1/58, 1988), присутствующего в виде фтор-иона или соединений фтора с кремнием, титаном, алюминием и др., путем взаимодействия содержащего фтор водного раствора с реагентом, в качестве которого используют водонерастворимые адсорбенты – гидратированные оксиды РЗЭ или нерастворимые гидратированные фториды, или фосфаты РЗЭ. По известному способу взаимодействие водного раствора и адсорбирующего реагента проводят в адсорбционной колонне при рН 2-7, отделяют очищенный раствор от насыщенного фтором реагента, проводят регенерацию реагента путем его обработки в адсорбционной колонне щелочным раствором с рН 10-14, содержащим, по крайней мере, одну щелочь, выбранную из группы: гидроксиды натрия, калия, аммония и органические амины. Затем щелочной раствор регенерируют осаждением из него растворенного фтора или его соединения путем добавления реагента в виде солей, оксидов и гидроксидов кальция, магния и алюминия, осаждающих фтор или соединения фтора. Для обеспечения контакта загрязненного фтором водного раствора с сорбентами их наносят на пористый органический полимерный материал, выбранный из группы, содержащей полиамид, целлюлозную смолу, полисульфон, полиакрилонитрил и сополимер этиленвиниловый спирт. Глубина очистки сточных вод от фтора, присутствующего в виде соединений фтора с кремнием, титаном и алюминием, составляет согласно примерам 15-17, соответственно, 6,46, 3,42 и 5,7 мг/л. Известный способ характеризуется недостаточной глубиной очистки стоков от фтора, присутствующего в виде его соединений с кремнием, титаном и алюминием, остаточное содержание которых выше допустимого содержания фтора в стоках, сбрасываемых в водоемы хозяйственно-питьевого и культурно-бытового водопользования, которое составляет 1,5 мг/л (см. ГН 2.1.5.1315-03 Предельно допустимые концентрации (ПДК) химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования). Известный способ может быть использован только для очистки стоков посредством сорбционных колонн, что снижает его универсальность и ограничивает применение, поскольку гетерогенная реакция сорбции обусловливает низкую производительность процесса, требуя для очистки больших объемов стоков, использования большого числа сорбционных колонн. Настоящее изобретение направлено на достижение технического результата, заключающегося в разработке универсального способа глубокой очистки сточных вод от фтор-иона и фторсодержащих комплексных соединений при обеспечении очистки больших объемов сточных вод и регенерации реагентов, используемых для осаждения фтор-иона и фторсодержащих соединений, а также при ограничении вторичного загрязнения очищенных стоков. Технический результат достигается тем, что в способе очистки сточных вод от фтора, включающем взаимодействие воды с церийсодержащим реагентом при регулировании рН, связывание фтора в твердую фазу, отделение ее от жидкой фазы и обработку фторсодержащей твердой фазы с регенерацией церийсодержащего реагента, согласно изобретению в качестве церийсодержащего реагента используют сульфат церия (III) или сульфат церия (IV), реагент берут в соотношении 2,5-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде, а рН поддерживают в пределах 4-7, при этом взаимодействие воды с церийсодержащим реагентом ведут в режиме гидролиза. Достижению технического результата способствует то, что сульфат церия (III) берут в соотношении 2,5-3,75 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде. Достижению технического результата способствует также то, что сульфат церия (IV) берут в соотношении 3,75-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде. Достижению технического результата способствует также и то, что обработку фторсодержащей твердой фазы осуществляют 80-95% серной кислотой при 175-190°C с получением фтористого водорода и регенерированного сульфата церия (IV). Достижению технического результата способствует и то, что регенерированный сульфат церия (IV) растворяют в воде и обрабатывают пероксидом водорода до обесцвечивания с получением регенерированного сульфата церия (III). Сущность изобретения заключается в том, что в результате проведенных исследований выявлено, что при взаимодействии воды, содержащей фтор в виде фтор-иона или комплексных анионов с кремнием, титаном, алюминием, железом, с водорастворимым церийсодержащим реагентом в виде сульфата церия (III) или сульфата церия (IV) при рН в диапазоне 4-7 происходит связывание фтора в образующуюся при гидролизе соединений церия твердую фазу. В указанном интервале величин рН гидролизуются и достаточно устойчивые к гидролизу комплексные анионы AlF6 Полученную твердую фазу обрабатывают концентрированной (80-95%) серной кислотой при температуре 175-190°C с регенерацией сульфата церия (IV) согласно реакции: Для регенерации сульфата церия (III) полученный сульфат церия (IV) растворяют в воде и обрабатывают пероксидом водорода до обесцвечивания согласно реакции: Существенные признаки заявленного изобретения, определяющие объем правовой охраны и достаточные для получения вышеуказанного технического результата, выполняют функции и соотносятся с результатом следующим образом. Использование в качестве церийсодержащего реагента сульфата церия (III) или сульфата церия (IV) обусловлено тем, что в диапазоне заданных концентраций церия они гидролизуются в интервале величин рН 4-7, образуя при взаимодействии с фтор-ионом малорастворимые гидроксофторидные в случае церия (III) или гидроксосульфатофторидные в случае церия (IV) комплексы, и могут быть успешно регенерированы. Кроме того, при использовании сульфата церия (III) снижается удельный расход реагента и уменьшается вторичное загрязнение воды ионами SO4 Соотношение церийсодержащего реагента и фтора в очищаемой сточной воде в количестве 2,5-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде, обусловлено тем, что при введении реагентов в очищаемую сточную воду в меньших количествах не обеспечивается очистка воды до ПДК. Поддержание рН в пределах 4-7 обусловлено тем, что в этом интервале величин рН достигается эффективное связывание фтора в практически нерастворимые соединения Се(ОН)3-xFx·nH2O или Ce(OH)2-xFxSO4·nH2O. При этом в интервале рН в пределах 5,5-7 образуются достаточно крупные легко осаждающиеся частицы фторсодержащей твердой фазы. При рН более 7 глубина очистки сточных вод от фтора резко снижается из-за протекающего гидролиза выпадающих фторсодержащих осадков Се(ОН)3-xFx·nH2O или Ce(OH)2-xFxSO4·nH2O, при этом возрастает остаточное содержание церия в очищенной воде. При рН менее 4 снижается эффективность очистки стоков от фтора. Взаимодействие воды с церийсодержащим реагентом в режиме гидролиза позволяет обеспечить взаимодействие образующихся при гидролизе сульфатов церия оснований Се(ОН)3·nH2O или Ce(OH)2SO4·nH2O с фтор-ионами во всем объеме поступающих на очистку стоков, исключить диффузионные ограничения протекания этой реакции, обеспечивая высокую скорость связывания фтор-ионов и, как следствие, возможность применения предлагаемого технического решения для очистки больших объемов стоков. Совокупность вышеуказанных признаков необходима и достаточна для достижения технического результата изобретения, заключающегося в повышении глубины очистки сточных вод от фтор-иона и фторсодержащих комплексных соединений при обеспечении очистки больших объемов сточных вод, регенерации церийсодержащих реагентов и ограничении вторичного загрязнения очищенных стоков. В частных случаях осуществления изобретения предпочтительны следующие конкретные операции и режимные параметры. Соотношение сульфата церия (III) и сульфата церия (IV) соответственно 2,5-3,75 и 3,75-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде, необходимо и достаточно для достижения ПДК по фтору и сульфат-иону в очищенных стоках. Обработка фторсодержащей твердой фазы 80-95% серной кислотой при 175-190°С позволяет синтезировать не загрязненный фтором сульфат церия (IV), обеспечив при этом высокую степень отгонки фтористого водорода. Использование при регенерации сульфата церия (IV) серной кислоты с концентрацией менее 80% не позволяет обеспечить проведение реакции (1) при температуре 175-190°С из-за более низких температур кипения этих составов. Концентрация серной кислоты более 95% нежелательна по технологическим причинам. Осуществление регенерации при температуре менее 175°С не обеспечивает высокую степень разрушения фторсульфоновой кислоты согласно реакции HSO3F+Н2О=H2SO4+ Обработка растворенного в воде сульфата церия (IV) пероксидом водорода до обесцвечивания раствора позволяет получить сульфат церия (III) по реакции (2). Вышеуказанные частные признаки изобретения позволяют осуществить глубокую очистку сточных вод от фтор-иона и фторсодержащих комплексных соединений в оптимальном режиме. Очистку фторсодержащих сточных вод согласно изобретению осуществляют следующим образом. Определяют содержание фтор-иона в воде. Берут необходимое количество водорастворимого сульфата церия (III) или сульфата церия (IV) исходя из соотношения: 2,5-3,75 г-атом церия (III) на 1 г-атом фтора, содержащегося в сточной воде, в случае использования сульфата церия (III), и 3,75-7,0 г-атом церия (IV) на 1 г-атом фтора, содержащегося в сточной воде, в случае использования сульфата церия (IV). Реагент вводят при перемешивании в загрязненную неорганическими соединениями фтора воду. Значение рН пульпы поддерживают в пределах 4-7 путем добавления соды или другой аналогичной щелочи. Образовавшиеся при гидролизе в этом интервале величин рН гидроксид церия (III) или гидроксосульфат церия (IV) взаимодействуют с фтор-ионом, образуя малорастворимые гидроксофторидные в случае церия (III) или гидроксосульфатофторидные в случае церия (IV) комплексы. Полученную фторсодержащую твердую фазу отделяют отстаиванием или фильтрацией от жидкой фазы – очищенной воды. Определяют остаточные содержания фтор-иона в очищенной сточной воде потенциометрическим методом с использованием фтор-селективного электрода, сульфат-иона – стандартным методом и церия – атомно-эмиссионной спектрометрией с индукционно-связанной плазмой. Проводят регенерацию использованного для осаждения фтора соединения церия. Для регенерации сульфата церия (IV) обрабатывают твердую фазу 80-95% серной кислотой при 175-190°C с отгонкой фтористого водорода и получением регенерированного сульфата церия (IV). Фтористый водород улавливают содой или поташом с получением фторидов натрия или калия. Регенерированный сульфат церия (III) получают в результате растворения регенерированного сульфата церия (IV) в воде с последующей обработкой раствора пероксидом водорода до обесцвечивания. Сущность заявляемого изобретения и его преимущества могут быть пояснены следующими примерами конкретного выполнения. Пример 1 Производят очистку 1 л сточной воды, содержащей 18,4 мг Na3AlF6 (10 мг/л фтора) при исходной величине рН воды 5,65. В сточную воду вводят 1200 мг Ce(SO4)2·4H2O (5,5 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 6 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют фильтрованием с получением 1600 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,3 мг/л, а сульфат-иона – 280 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 397 мг 80% H2SO4 и выдерживают при 175°С в течение 1 часа. Получают 1016 мг спека Ce(SO4)2, содержащего 3% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором соды с получением 19,23 мг фторида натрия NaF, пригодного для последующего использования. Степень извлечения фтора – 87% от исходного содержания в воде. Пример 2 Производят очистку 1 л сточной воды, содержащей 18,4 мг Na3AlF6 (10 мг/л фтора) при исходной величине рН воды 5,65. В сточную воду вводят 705 мг Се2(SO4)3·8H2O (3,75 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 7 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют отстаиванием в течение 3 часов с получением 650 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,42 мг/л, а сульфат-иона – 284 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 230 мг 95% H2SO4 и выдерживают при 190°С в течение 1 часа. Получают 702 мг спека Ce(SO4)2, содержащего 4% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором соды с получением 18,96 мг фторида натрия NaF, пригодного для последующего использования. Степень извлечения фтора – 85,8% от исходного содержания в воде. Спек Ce(SO4)2 в количестве 702 мг растворяют в 10 мл воды и добавляют 110 мг H2O2 с концентрацией 30 мас.%. Получают обесцвеченный раствор, содержащий 570 мг Ce2(SO4)3. Пример 3 Производят очистку 1 л сточной воды, содержащей 19,5 мг (NH4)3FeF6 (10 мг/л фтора) при исходной величине рН воды 3,95. В сточную воду вводят 1463 мг Ce(SO4)2·4H2O (7 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 5,8 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют отстаиванием в течение 1 часа с получением 1943 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,25 мг/л, а сульфат-иона – 340 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 418 мг 93,5% H2SO4 и выдерживают при 180°С в течение 1 часа. Получают 1243 мг спека Ce(SO4)2, содержащего 3,4% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором поташа с получением 26,76 мг фторида калия KF, пригодного для последующего использования. Степень извлечения фтора – 87,5% от исходного содержания в воде. Пример 4 Производят очистку 1 л сточной воды, содержащей 21,05 мг K2TiF6 (10 мг/л фтора) при исходной величине рН воды 3,61. В сточную воду вводят 705 мг Ce(SO4)2·4H2O (3,75 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 6 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют фильтрованием с получением 940 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,3 мг/л, а сульфат-иона – 165 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 200 мг 93,5% H2SO4 и выдерживают при 180°С в течение 1 часа. Получают 597 мг спека Ce(SO4)2, содержащего 3% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором соды с получением 19,23 мг фторида натрия NaF, пригодного для последующего использования. Степень извлечения фтора – 87% от исходного содержания в воде. Пример 5 Производят очистку 1 л сточной воды, содержащей 16,5 мг Na2SiF6 (10 мг/л фтора) при исходной величине рН воды 3,40. В сточную воду вводят 880 мг Ce(SO4)2·4H2O (4,32 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 5,5 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют фильтрованием с получением 1175 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,5 мг/л, а сульфат-иона – 206 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 250 мг 93,5% H2SO4 и выдерживают при 185°С в течение 1 часа. Получают 745 мг спека Ce(SO4)2, содержащего 3,1% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором соды с получением 18,8 мг фторида натрия NaF, пригодного для последующего использования. Степень извлечения фтора – 85% от исходного содержания в воде. Пример 6 Производят очистку 1 л сточной воды, содержащей 22,1 мг NaF (10 мг/л фтора) при исходной величине рН воды 5,65. В сточную воду вводят 470 мг Се2(SO4)3·8H2O (2,5 г-атом церия на 1 г-атом фтора), выдерживают при перемешивании в течение 15 минут, поддерживая рН пульпы равным 4 путем добавления раствора Na2CO3. Образовавшуюся при взаимодействии продуктов гидролиза фторсодержащую твердую фазу отделяют отстаиванием в течение 3 часов с получением 435 мг влажного осадка. Концентрация фтор-иона в очищенной воде равна 1,45 мг/л, а сульфат-иона – 190 мг/л, что не превышает ПДК для водоемов питьевого водопользования. Остаточное содержание церия в очищенной воде – менее 0,1 мг/л. Фторсодержащий влажный осадок обрабатывают 260 мг 85% H2SO4 и выдерживают при 190°С в течение 1 часа. Получают 469 мг спека Ce(SO4)2, содержащего 3,8% свободной H2SO4 (степень извлечения в пересчете на Се – более 99,97%) и газообразный фтористый водород, который поглощают раствором соды с получением 18,9 мг фторида натрия NaF, пригодного для последующего использования. Степень извлечения фтора – 85,5% от исходного содержания в воде. Спек Ce(SO4)2 в количестве 469 мг растворяют в 7 мл воды и добавляют 75 мг H2O2 с концентрацией 30 мас.%. Получают обесцвеченный раствор, содержащий 380 мг Се2(SO4)3. Из приведенных выше примеров видно, что способ очистки сточных вод от фтора согласно изобретению позволяет обеспечить глубокую очистку сточных вод от фтор-иона и фторсодержащих комплексных соединений при обеспечении возможности очистки больших объемов сточных вод. Достигаемая глубина очистки сточных вод от фтора составляет 1,25-1,5 мг/л, а остаточное содержание сульфат-иона равно 165-340 мг/л, что не превышает ПДК для водоемов питьевого назначения. Способ позволяет регенерировать реагенты для их повторного использования, а также практически исключить вторичное загрязнение очищенных стоков соединениями церия. Фтор выделяют в виде товарных соединений – фторидов натрия или калия. Способ согласно изобретению несложен и может быть реализован в прудах-отстойниках с использованием стандартного оборудования.
Формула изобретения
1. Способ очистки сточных вод от фтора, включающий взаимодействие воды с церийсодержащим реагентом при регулировании рН, связывание фтора в твердую фазу, отделение ее от жидкой фазы и обработку фторсодержащей твердой фазы с регенерацией церийсодержащего реагента, отличающийся тем, что в качестве церийсодержащего реагента используют сульфат церия (III) или сульфат церия (IV), реагент берут в соотношении 2,5-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде, а рН поддерживают в пределах 4-7, при этом взаимодействие воды с церийсодержащим реагентом ведут в режиме гидролиза. 2. Способ по п.1, отличающийся тем, что сульфат церия (III) берут в соотношении 2,5-3,75 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде. 3. Способ по п.1, отличающийся тем, что сульфат церия (IV) берут в соотношении 3,75-7,0 г-атом церия на 1 г-атом фтора, содержащегося в очищаемой сточной воде. 4. Способ по п.1, отличающийся тем, что обработку фторсодержащей твердой фазы осуществляют 80-95% серной кислотой при 175-190°C с получением фтористого водорода и регенерированного сульфата церия (IV). 5. Способ по п.1 или 4, отличающийся тем, что регенерированный сульфат церия (IV) растворяют в воде и обрабатывают пероксидом водорода до обесцвечивания с получением регенерированного сульфата церия (III).
|
||||||||||||||||||||||||||

 3-, TiF6
3-, TiF6
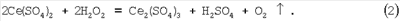
 HF, что не позволяет достичь требуемой полноты отгонки фтора в виде фтористого водорода. Температура более 190°С нецелесообразна, так как начинается разложение образующегося сульфата церия (IV) на CeO2 и SO3.
HF, что не позволяет достичь требуемой полноты отгонки фтора в виде фтористого водорода. Температура более 190°С нецелесообразна, так как начинается разложение образующегося сульфата церия (IV) на CeO2 и SO3.