Патент на изобретение №2382596
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ОБНАРУЖЕНИЯ СОСУДОВ, ПИТАЮЩИХ ОПУХОЛЬ, В ЭКСПЕРИМЕНТЕ
(57) Реферат:
Изобретение относится к экспериментальной медицине и магнитно-резонансной томографии, может быть использовано в онкологии для диагностики и терапии злокачественных опухолей. Вводят животным с привитыми опухолями внутривенно 10% золь аскорбатферрита или цитратферрита от 0,02 мл до 0,2 мл в полиглюкине. Затем вводят магневист. Магнитно-резонансную томографию проводят с получением T1-, Т2– и Т2*-взвешенных 3D изображений. Способ позволяет увеличить контрастность, яркость и продолжительность МРТ-изображений сосудов, питающих опухоль. 1 ил., 3 табл.
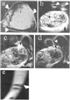
Изобретение относится к экспериментальной медицине и магнитно-резонансной томографии (МРТ), может быть использовано в онкологии для диагностики и терапии злокачественных опухолей и метастазов различной локализации. Образование сосудов, питающих опухоль, не является генетически обусловленным и происходит в зоне развивающейся опухоли в процессе неоангиогенеза из существующих в тканях капилляров. Для успешной доставки препаратов в процессе внутрисосудистой регионарной химиотерапии необходимо знать расположение сосудов, питающих опухоль. Известны способы рентгенологического и компьютерного томографического обнаружения сосудов путем внутривенного введения иодсодержащих рентгеноконтрастных препаратов с последующими рентгенографическим и компьютерным рентгенографическим исследованиями [1-3]. Недостатком данных способов является: – изображение опухоли обычно представлено на рентгенограммах в виде темных пятен, сливающихся с изображениями сосудов, что не создает истинной картины расположения сосудов, снижая достоверность результатов и диагностическую ценность данного способа. Известен способ контрастирования сосудов путем введения магневиста (МРТ-позитивного контрастного препарата), полупериод нахождения которого в плазме составляет менее 15 минут, с последующим T1 взвешенным изображением на магнитно-резонансных томограммах (прототип) [4]. Данный способ позволяет получить через 4 минуты и поддерживать до 30 минут яркость магнитно-резонансных изображений органов и тканей. Недостатками прототипа являются: – на МР-томограммах изображения опухоли и сосудов сливаются с фоном, что значительно снижает достоверность результатов исследования и их диагностическую ценность; – короткий полупериод нахождения магневиста в плазме крови. Задачей изобретения является создание более информативного способа обнаружения сосудов, питающих опухоль. Указанная задача решается следующим образом: – животному внутривенно вводят ферриты (аскорбатферрит или цитратферрит) в полиглюкине (МРТ-негативные контрастные препараты, подавляющие сигналы протонов нормальных тканей). Через 6 минут после введения визуализируются структуры опухолевых тканей и опухолевой капсулы с питающими опухоль сосудами в виде светлых изображений на темном фоне, контраст которых сохраняется в течение 40 часов (чертеж а, Табл.1). Для увеличения яркости МРТ-изображений внутривенно вводят до 50% традиционной дозы магневиста (0,1 ммол/кг-1), который усиливает сигналы тканей, не содержащих ферриты, и в течение 30 минут создает высокую яркость магнитно-резонансных изображений органов и тканей животного. Заявленный способ осуществляется на самках мышей C57B1/6j с привитыми опухолями аденокарциномы молочной железы Ca 755, через 6-10 дней опухоли пальпируют. В период от 3 часов до 30 часов до проведения МРТ-сканирования (Табл. 2, 3) внутривенно вводят от 0,02 мл до 0,2 мл 10% золя аскорбатферрита в полиглюкине (Таблица 1). При этом повышается контраст изображений органов и тканей, структуры капсулы и сосудов, питающих опухоль (чертеж, a-d). Дополнительное внутривенное введение 0,01-0,05 ммол/кг-1 магневиста за 6 минут до МРТ усиливает контраст и яркость изображений опухоли, капсулы и сосудов, питающих опухоли на томограммах (чертеж, b-е). Полученные данные обрабатывают статистически по стандартизованным критериям, за достоверные принимают различия при Прививку опухоли мышам и оценку полученных результатов проводят согласно рекомендациям по химиотерапии злокачественных опухолей [5]. 80 мышам С57В1/6j весом 18-21 г, в возрасте 6-10 недель, разводки вивария ГУ РОПЦ им Н.Н. Блохина РАМН имплантируют под кожу правого второго соска 1×106 клеток/мышь аденокарциному молочной железы Ca 755 в стерильном 0,9% растворе хлорида натрия, pH 7,4, в объеме 0,2 мл. Через 6-10 дней после прививки из общего количества отбирают 70 мышей, размеры опухолей которых достигают 10-17 мм. Объем каждой опухоли вычисляют как V=0,5·(l·n2), где V – объем, l – длина, n – площадь опухоли. Мышей с привитыми опухолями делят на 6 групп: 1, 2, 3, 4, 5 и 6. Первая – контрольная группа 20 мышей, 2, 3, 4, 5 и 6 – опытные группы по 10 мышей в каждой. Подготовка к магнитно-резонансному томографическому обнаружению сосудов, питающих опухоли, аденокарциномы молочной железы Ca 755 на мышах C57B1/6j. Мышам контрольной группы за период от 6 минут до 30 часов перед магнитно-резонансной томографией внутривенно вводят по 1 мл полиглюкина. Мышам опытных групп за такой же период времени внутривенно вводят от 0,01 до 0,1 мл 10% золя аскорбатферрита или от 0,01 до 0,1 мл 10% золя цитратферрита в полиглюкине и проводят сканирование на магнитном-резонансном биоспектротомографе BIOSPEC ВС 70/30 USR. (Bruker) в режимах T1-взвешенных; Т2*-взвешенных {500/15 [время повторения, мсек/время эхо, мсек] и Т2-взвешенных (1900/80) спин-эхо и Т2-взвешенных градиент-эхо (500/15)} изображений. Мониторинг жизнеобеспечения осуществляют с помощью Model 1025 smol Animal Monitoring and Gating System. (Operation Mammal) SA Instruments, Inc. Предварительные опыты проводят на 2 мышах каждой группы: измеряют интенсивность сигнала и проводят визуальный анализ изображений на томограммах, определяя локализацию и структуру опухоли и сосудов, питающих опухоль. 1 (контрольная группа): при внутривенном введении 0,1 мл полиглюкина за 6 минут до магнитно-резонансной томографии отмечено незначительное увеличение яркости изображений без усиления контраста на томограммах, которое не обеспечивает обнаружение сосудов, питающих опухоли. 2 группа: внутривенное введение 0,01 мл 1% золя цитратферрита в полиглюкине (диаметр наночастиц 6-14 нм) за 6 минут до магнитно-резонансной томографии вызывает незначительное усиление контраста изображений на томограммах, которое не обеспечивает обнаружение сосудов, питающих опухоли. 3 группа: внутривенное введение 0,1 мл 1% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6-14 нм) за 1 час до магнитно-резонансной томографии вызывает усиление контраста изображений на томограммах, которое обеспечивает обнаружение сосудов, питающих опухоли. 4 группа: внутривенное введение 0,1 мл 10% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6-600 нм) за 24 часа до магнитно-резонансной томографии вызывает усиление контраста изображений на томограммах, которые обеспечивают обнаружение сосудов, питающих опухоли. 5 группа: внутривенное введение 0,1 мл 10% золя цитратферрита (диаметр наночастиц 6-24 нм) в полиглюкине за 13 часов до магнитно-резонансной томографии вызывает усиление контраста изображений на томограммах, которое обеспечивает обнаружение сосудов, питающих опухоли. 6 группа: внутривенное введение 0,4 мл 1% золя аскорбатферрита (диаметр наночастиц 6-260 нм) за 30 часов до магнитно-резонансной томографии и последующее внутривенное введение 0,004 мл магневиста за 4 минуты до магнитно-резонансной томографии вызывает усиление контраста и яркости изображений на томограммах, которое обеспечивает обнаружение сосудов, питающих опухоли. Заявленный способ иллюстрируется примерами 1-6, чертеж (а-е) и таблицами 1-3. Пример 1 За 6 минут до проведения магнитно-резонансной томографии в хвостовую вену мышей 1 группы вводят 0,1 мл полиглюкина, с последующим поочередным проведением T1-, Т2– и Т2*-взвешенных 3D сканирований в течение 30 часов. На томограммах отмечаются увеличение контраста и незначительное повышение яркости МРТ-изображений. Сосуды, питающие опухоль, не определяются. Пример 2 В хвостовую вену мышей 2 группы за 20 часов до томографии вводят 0,1 мл 10% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6-600 нм). Проводят T1-, T2– и Т2*-взвешенные 3D сканирования. При визуальном анализе структуры опухолей на томограммах обнаруживаются сосуды, питающие опухоль, яркость изображений низкая (чертеж, a, b). Пример 3 В хвостовую вену мышей 3 группы за 20 часов до томографии вводят 0,2 мл 1% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6-30 нм) и за 4 минуты до сканирования внутривенно вводят 0,05 ммол/кг-1 магневиста. Затем получают T1-, T2– и Т2*-взвешенные 3D изображения. На томограммах сохраняются контраст и яркость изображений, обнаруживаются сосуды, питающие опухоли (чертеж, b, с). Пример 4 За 26 часов до томографии в хвостовую вену мышей 4 группы вводят 0,04 мл 10% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6 – 600 нм) и за 6 минут до сканирования внутривенно вводят 0,003 мл магневиста. Получают Т2– и Т2*-взвешенные 3D изображения. На томограммах выявлено усиление контраста и яркости изображений, обнаруживаются сосуды, питающие опухоли (чертеж, b, с). Пример 5 За 30 часов до магнитно-резонансной томографии в хвостовую вену мышей 5 группы вводят 0,1 мл 10% золя цитратферрита в полиглюкине (диаметр наночастиц 6-24 нм) и за 8 минут до сканирования внутривенно вводят 0,003 мл магневиста с последующим получением и Т2-, T2*-взвешенных 3D изображений. На томограммах отмечают стабилизацию яркости изображений, обнаруживаются сосуды, питающие опухоли (чертеж, b-d). Пример 6 За 40 часов до магнитно-резонансной томографии в хвостовую вену мышей 6 группы вводят 0,04 мл 10% золя аскорбатферрита в полиглюкине (диаметр наночастиц 6-600 нм) и за 10 минут до сканирования внутривенно вводят 0,05 ммол/кг-1 магневиста с последующим получением Т2-, Т2*-взвешенных 3D изображений. Отмечено повышение интенсивности сигнала, повышение контраста и яркости МРТ-изображений опухолей на томограммах (чертеж, a-d), обнаруживаются поверхностные и глубинные сосуды, питающие опухоли: чертеж, (а) – два сосуда, питающие опухоль, (стрелки); чертеж, (b) – капсула (короткая черная стрелка), с которой соединены два деформированных сосуда, питающие опухоль (белые стрелки), которые заканчиваются в стенках капсулы, в опухолевой ткани встречаются функционирующие сосуды (длинная черная стрелка); (с) – яркая кровь, обогащенная магневистом, поступает из сосуда (черная стрелка), питающего опухоль, в капсулу (белые маленькие стрелки); (d) – обогащенная магневистом кровь поступает из сосудов, питающих опухоль (белые стрелки), в сосуды капсулы (черная стрелка); (e) – деформированная часть сосуда, питающего опухоль, поражена опухолевыми клетками (стрелка). Усиление четкости изображений при магнитно-резонансной томографии за счет повышения контраста и яркости при внутривенном введении аскорбатферрита или цитратферрига и магневиста достижимо при условии подбора соответствующих количественных соотношений вводимых контрастных препаратов, очередности и временных интервалов их введения, поскольку возможно взаимное гашение яркости и размывание контраста, что приводит к нечетким малоинформативным МРТ-изображениям. Для получения высокоинформативных МРТ-изображений последовательность введения и количественные соотношения аскорбатферрита, цитратферрита и магневиста определяют по таблицам 1-3. Таблицы (1-3): – (1) зависимость контраста и яркости изображений на томограммах от введенных препаратов; – (2) зависимость контраста и яркости изображений на томограммах от временного интервала, прошедшего после введения контрастных препаратов: цитратферрит 0,2 мл, 10%; аскорбатферрит 0,2 мл, 10%; магневист 0,05 ммол/кг-1; – (3) зависимость контраста и яркости изображений на томограммах от времени, прошедшего после введения контрастных препаратов: цитратферрит 10% 0,2 мл; аскорбатферрит 10% 0,2 мл; магневист 0,05 ммол/кг-1. При внутривенном введении золей аскорбатферрита и цитратферрита проникновение наночастиц в опухоль и в метастазы затруднено. Из-за повышенного внутриопухолевого давления и атипичного строения сосудов, питающих опухоли. Наночастицы концентрируются в капсуле, окружающей опухоль. Концентрация ферритов в опухоли и метастазах повышается значительно медленнее, чем в нормальных тканях. В связи с чем увеличивается магнитная гетерогенность и разность между величинами сигналов опухолевых и нормальных тканей, усиливающих контраст изображений на томограммах. Усиление контраста изображений на томограммах биологических тканей наночастицами заявленных ферритов позволяет наблюдать изменения морфологии капсулы и сосудов, питающих опухоль, в реальном времени (чертеж, а-е), которые подтверждаются результатами патоморфологических и гистопатологических исследований. Для подтверждения обнаруженных опухолей и сосудов, питающих опухоль, проводят сравнительное изучение данных патоморфологических и гистопатологических исследований с результатами магнитно-резонансной томографии. Кусочки тканей, взятые из мест расположения опухолей и сосудов, питающих опухоли, имплантированные под кожу мышам, вызывают рост аденокарциномы молочной железы Ca 755 у сингенных животных. При усилении контраста и яркости изображений на томограммах биологических тканей наночастицами аскорбатферрита в комбинации с магневистом обнаруживаются опухоли, капсулы, сосуды, питающие опухоли (чертеж, a-d), и инвазия опухолевых клеток в стенки сосуда, питающего опухоль (чертеж, е). Подтвержденные патоморфологическими и гистопатологическими методами данные магнитно-резонансной томографии используют для коррекции планов терапии опухолей. Для одновременного достижения требуемых контраста и яркости изображений за 6 минут-40 часов до магнитно-резонансной томографии вводят 10% золи аскорбатферрита 0,2 мл; цитратферрита 0,2 мл в полиглюкине и дополнительно за 4-12 минут перед магнитно-резонансной томографией вводят магневист 0,05 ммол/кг-1. Чертеж (а, b, с, d, e). (а, b, с, d) МРТ-изображения опухолей аденокарциномы молочной железы Ca 755 у мышей С57В1/6j: (а) – капсула, содержащая опухоль, видны 2 сосуда, питающие опухоль, (стрелки); (b) – два деформированных сосуда, питающие опухоль (белые стрелки), которые заканчиваются в стенках капсулы (короткая черная стрелка), в опухолевых тканях встречаются функционирующие сосуды (длинная черная стрелка); (с) – поверхностный сосуд (черная стрелка), питающий опухоль, соединен с сосудами капсулы (белые маленькие стрелки), функционирующие глубинные опухолевые сосуды (тонкие черные стрелки); (d) – обогащенная магневистом яркая кровь поступает из сосудов, питающих опухоль (белые стрелки), в капсулу (черная стрелка) и в функционирующие глубинные опухолевые сосуды (тонкие черные стрелки); (е) – деформированная часть сосуда, питающего опухоль, поражена опухолевыми клетками (стрелка). Технический результат заявленного способа состоит в увеличении: – контраста и яркости МРТ-изображений сосудов, питающих опухоль; – продолжительности и эффективности получения МРТ-изображений сосудов, питающих опухоль. Это позволяет изучить структуру и функциональное состояние сосудов, питающих опухоль, для направленной доставки препаратов в процессе регионарной химиотерапии и оценить ее эффективность. По результатам МРТ планируют объем оперативных вмешательств, лучевых и химиотерапевтических воздействий, что приводит к снижению диагностических и терапевтических ошибок. Источники информации 1. Долгушин Б.И. Методы лучевой диагностики в онкологии. Энциклопедия клинической онкологии. Главный ред. Давыдов М.И. Москва, РЛС-2004, 30-33. 2. Ширяев С.В. Ядерная медицина в онкологии. Энциклопедия клинической онкологии. Главный ред. Давыдов М.И. Москва, РЛС-2004, 117-125. 3. Летягин В.П. Злокачественные образования молочной железы у женщин и мужчин. Энциклопедия клинической онкологии. Главный ред. Давыдов М.И. Москва, РЛС-2004, 374-389. 4. Тютин Л.А., Шимановский Н.Л., Трофимова Т.Н. 15 лет клинического применения магневиста – первого магнитно-резонансного средства. Медицинская визуализация 2004, 5. Ларионов Л.Ф. Химиотерапия злокачественных опухолей. Мед. Лит. М., 1962. 6. Реброва О.Ю. Статистический анализ медицинских данных, Медиа Сфера, Москва (2002).
Формула изобретения
Способ обнаружения сосудов, питающих опухоль, путем внутривенного введения магневиста с последующей магнитно-резонансной томографией, отличающийся тем, что предварительно внутривенно вводят 10% золь аскорбатферрита или цитратферрита от 0,02 до 0,2 мл в полиглюкине, а магнитно-резонансную томографию проводят с получением T1-, Т2– и Т2*-взвешенных 3D-изображений.
РИСУНКИ
TH4A – Переиздание описания изобретения к патенту Российской Федерации
Причина переиздания: Коррекция в тексте реферата, формулы и описания изобретения
Извещение опубликовано: 10.06.2010 БИ: 16/2010
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 7 (11), 3132-3138.
7 (11), 3132-3138. <0,05 [6].
<0,05 [6].