|
|
(21), (22) Заявка: 2006131591/04, 04.02.2005
(24) Дата начала отсчета срока действия патента:
04.02.2005
(30) Конвенционный приоритет:
06.02.2004 US 60/542,490
04.11.2004 US 60/624,937
(43) Дата публикации заявки: 20.03.2008
(46) Опубликовано: 20.02.2010
(56) Список документов, цитированных в отчете о
поиске:
Shah et al. «Overriding Imatinib Resistance with a Novel ABL Kinase Inhibitor» SCIENCE, 2004, Vol.305,  5682, 399-401. RU 2199538 C2, 27.02.2003. US 6596746 B1, 22.07.2003. 5682, 399-401. RU 2199538 C2, 27.02.2003. US 6596746 B1, 22.07.2003.
(85) Дата перевода заявки PCT на национальную фазу:
06.09.2006
(86) Заявка PCT:
US 2005/003728 20050204
(87) Публикация PCT:
WO 2005/077945 20050825
Адрес для переписки:
119034, Москва, Пречистенский пер., 14, стр.1, 4 этаж, “Гоулингз Интернэшнл Инк.”, В.Н.Дементьеву
|
(72) Автор(ы):
ЧЕН Банг-Чи (US),
ДРОГИНИ Роберто (CA),
ЛАЖЁНЕСС Жан (CA),
ДИМАРКО Джон Д. (US),
ГАЛЕЛЛА Майкл (US),
ЧИДАМБАРАМ Рамакришнан (US)
(73) Патентообладатель(и):
БРИСТОЛ-МАЕРС СКВИББ КОМПАНИ (US)
|
(54) СПОСОБ ПОЛУЧЕНИЯ 2-АМИНОТИАЗОЛ-5-АРОМАТИЧЕСКИХ КАРБОКСАМИДОВ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ
(57) Реферат:
Изобретение относится к кристаллическому моногидрату соединения формулы (IV)
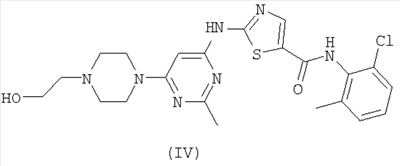 , ,
Кристаллический моногидрат имеет порошковую рентгенограмму включающую четыре или более значений 2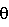 , выбранных из группы, состоящей из: 18.0±0.2, 18.4±0.2, 19.2±0.2, 19.6±0.2, 21.2±0.2, 24.5±0.2, 25.9±0.2 и 28.0±0.2. Изобретение также относится к способу получения кристаллического моногидрата, к фармацевтической композиции для лечения нарушений, обусловленных протеинтирозинкиназой, содержащей кристаллический моногидрат, к кристаллическому бутанольному сольвату соединения формулы (IV) и к кристаллическому этанольному сольвату соединения формулы (IV). 5 н. и 3 з. п. ф-лы, 1 табл., 6 ил. , выбранных из группы, состоящей из: 18.0±0.2, 18.4±0.2, 19.2±0.2, 19.6±0.2, 21.2±0.2, 24.5±0.2, 25.9±0.2 и 28.0±0.2. Изобретение также относится к способу получения кристаллического моногидрата, к фармацевтической композиции для лечения нарушений, обусловленных протеинтирозинкиназой, содержащей кристаллический моногидрат, к кристаллическому бутанольному сольвату соединения формулы (IV) и к кристаллическому этанольному сольвату соединения формулы (IV). 5 н. и 3 з. п. ф-лы, 1 табл., 6 ил.
Текст описания приведен в факсимильном виде.                                                             
Формула изобретения
1. Кристаллический моногидрат соединения формулы (IV)
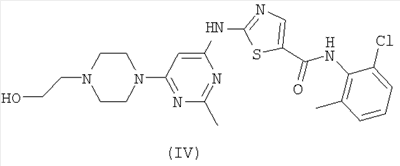 , ,
характеризующийся порошковой рентгенограммой (CuK  =1.5418Å при температуре около 23°С), включающей четыре или более значений 2 =1.5418Å при температуре около 23°С), включающей четыре или более значений 2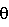 , выбранных из группы, состоящей из: 18.0±0.2, 18.4±0.2, 19.2±0.2, 19.6±0.2, 21.2±0.2, 24.5±0.2, 25.9±0.2 и 28.0±0.2 и следующими параметрами элементарной ячейки: , выбранных из группы, состоящей из: 18.0±0.2, 18.4±0.2, 19.2±0.2, 19.6±0.2, 21.2±0.2, 24.5±0.2, 25.9±0.2 и 28.0±0.2 и следующими параметрами элементарной ячейки:
Размеры элементарной ячейки: а(Å)=13.8632(7);
b(Å)=9.3307(3);
с(Å)=38.390(2);
Объем=4965.9(4)Å3
Пространственная группа Pbca
Молекулы/элементарная ячейка 8
Плотность (вычисленная) (г/см3) 1.354.
2. Соединение по п.1, отличающееся тем, что оно характеризуется порошковой рентгенограммой, показанной на Фигуре 1.
3. Соединение по п.1, отличающееся тем, что оно характеризуется термограммой, полученной методом дифференциальной сканирующей калориметрии, и показателями термогравиметрического анализа, соответствующими результатам, изображенным на Фигуре 2.
4. Соединение по п.1, отличающееся тем, что на одну молекулу соединения формулы (IV) приходится одна молекула воды.
5. Способ получения кристаллического моногидрата соединения формулы (IV) по п.1, заключающийся в нагревании и растворении соединения формулы (IV) в смеси этанол/вода и кристаллизации моногидрата из смеси этанол/вода при ее охлаждении.
6. Фармацевтическая композиция для лечения нарушений, обусловленных протеинтирозинкиназой, содержащая терапевтически эффективное количество соединения по любому из пп.1-4 и фармацевтически приемлемый носитель.
7. Кристаллический бутанольный сольват соединения формулы (IV)
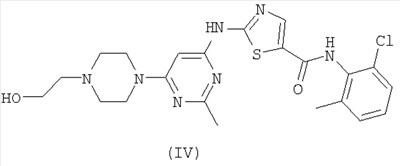 , ,
характеризующийся следующими параметрами элементарной ячейки:
Размеры элементарной ячейки: а(Å)=22.8102(6);
b(Å)=8.4691(3);
с(Å)=15.1436(5);
Объем=2910.5(2) Å3
Пространственная группа P21/a
Молекулы/элементарная ячейка 4
Плотность (вычисленная) (г/см3) 1.283.
8. Кристаллический этанольный сольват соединения формулы (IV)
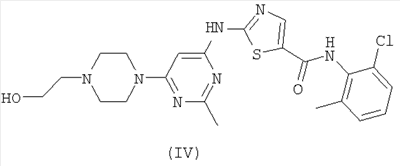 , ,
характеризующийся порошковой рентгенограммой (СuК  =1.5418Å при температуре около 23°С), включающей четыре или более значений 2 =1.5418Å при температуре около 23°С), включающей четыре или более значений 2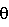 , выбранных из группы, состоящей из: 5.8±0.2, 11.3±0.2, 15.8±0.2, 17.2±0.2, 19.5±0.2, 24.1±0.2, 25.3±0.2 и 26.2±0.2. , выбранных из группы, состоящей из: 5.8±0.2, 11.3±0.2, 15.8±0.2, 17.2±0.2, 19.5±0.2, 24.1±0.2, 25.3±0.2 и 26.2±0.2.
РИСУНКИ
|
|