Патент на изобретение №2381748
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНОГО ИСХОДА У БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ ВИРУСНОЙ И АЛКОГОЛЬНОЙ ЭТИОЛОГИИ
(57) Реферат:
Изобретение относится к медицине, а именно к гастроэнтерологии, и предназначено для прогнозирования неблагоприятного исхода у больных циррозом печени вирусной и алкогольной этиологии. Определяют пиковую скорость кровотока в печеночной артерии УпикПА (см/с) и объемную скорость кровотока в верхней брыжеечной вене УобВБВ (мл/мин) методом ультразвуковой допплерографии. При УпикПА
Изобретение относится к области медицины, в частности к гастроэнтерологии, конкретно к способам прогнозирования неблагоприятного исхода у больных циррозом печени (ЦП) вирусной и алкогольной этиологии. Портальная гипертензия является одним из основных проявлений ЦП. Степень выраженности данного синдрома коррелирует с риском развития осложнений и смерти [1]. Наиболее информативной и прогностически ценной методикой исследования портальной гипертензии является инвазивная методика измерения давления в воротной вене [2, 3, 4]. Получаемый показатель HVPG (печеночный венозный градиент давления) является надежным прогностическим маркером развития кровотечения из варикозных вен и летального исхода [4, 5, 6,]. При HVPG от 10 до 12 мм рт.ст. появляется варикозное расширение вен пищевода [7]. Значения HVPG >12 мм рт.ст. большинство исследователей характеризуют как неблагоприятный прогностический признак в плане развития осложнений и смерти [4, 8, 9]. Отмечено, что уменьшение HVPG на 20% от исходного на фоне лечения Появились исследования, показывающие наличие корреляции HVPG с допплеровскими показателями печеночного кровотока у больных ЦП [7, 10, 11]. Многочисленные группы исследователей изучали прогностические возможности допплеровских показателей печеночного кровотока. Zoli М. и соавт [12] в 1993 году привели данные о прогностической роли скорости кровотока в воротной вене. При значениях, меньших 10 см/с, у больных компенсированным ЦП продолжительность жизни была меньше. De Vries P.J. [13] и соавт. выявили, что неблагоприятный прогноз у больных ЦП (кровотечение из варикозных вен и смерть) ассоциирован с показателями ранней постпрандиарной максимальной скорости воротного кровотока и спленомегалией. Ohta М. и соавт [14], исследуя 120 больных ЦП (17 из которых умерли) в течение 23-х месяцев, определили, что плоская форма волны в правой печеночной вене при допплеровском УЗИ является независимым прогностическим фактором у больных ЦП. Kayacetin E. и соавт. выяснили, что у больных ЦП с кровотечением из варикозных вен пищевода увеличена объемная скорость кровотока в селезеночной вене и индекс переполнения селезеночной вены (исследовано 45 больных ЦП) [15]. Li F.H. и соавт [16] обнаружили, что прогностическим фактором развития кровотечения из варикозных вен является скорость гепатофугального кровотока (т.е. в направлении от печени) в левой желудочной вене (>15 см/с), однако, данных о статистических различиях между группами с и без кровотечения не представлено. Линейный кровоток в воротной вене не показал себя в качестве прогностического фактора развития кровотечения. Kogo М. и соавт. предложили прогностическую модель с учетом состояния портальной гемодинамики [17]. В исследование были включены 160 больных ЦП. Срок наблюдения – 5 лет. Вычислен прогностический индекс PI (ПИ) на основании регрессионной модели Кокса. ПИ=0,042×возраст+0,913×HCC+0,989×PVTT+1,079×PUV shunt (HCC – наличие гепатоцеллюлярной карциномы, PVTT – опухолевый тромбоз воротной вены, PUV shunt – наличие шунтирования по околопупочной вене). Больные с более высоким ПИ имели более высокую вероятность наступления летального исхода. Macias-Rodriguez М.А. и соавт. наблюдали за 75 больными ЦП класса А по Чайлд-Пью в течение 39 месяцев. Выявлено, что независимыми прогностическими факторами летального исхода являются мужской пол (риск в 4,6 раза выше), диаметр воротной вены >13 мм, спленомегалия >145 мм. Если у мужчин наблюдаются описанные параметры воротной вены и спленомегалия, то риск смерти увеличивается в 6 раз [18]. В другой работе De Vries P.J. и соавт., изучая портальную гемодинамику у 59 больных ЦП (19 умерли и у 14 развилось кровотечение из варикозных вен) на протяжении 47 месяцев, не выявили корреляции между объемной скоростью портального кровотока, с одной стороны, и выживаемостью и развитием кровотечения из варикозных вен, с другой стороны [19]. У 23 больных портальный кровоток исследовался в динамике. Уменьшение объемной скорости воротного кровотока было выявлено у 5 больных с летальным исходом. Авторы статьи делают заключение, что объемный портальный кровоток может быть стабилен (отсутствовать динамика) вплоть до терминальной стадии ЦП, в которой и наблюдается его снижение. Baik S.K. и соавт. определили независимые факторы неблагоприятного прогноза у больных ЦП:HVPG Резюмируя вышесказанное, следует отметить некоторую противоречивость полученных прогностических допплеровских параметров, которые подтверждаются одними авторами и не выявляются другими. Возможно, это обусловлено этиологической и расовой разнородностью групп больных ЦП. Определенный вклад могли также внести различия в используемой диагностической аппаратуре и нюансы подготовки больных к исследованию (необходимо воздержание от приема пищи в течение 6-8 часов). Очень многое зависит и от квалификации специалиста, непосредственно проводящего исследование. Поэтому очень важно проводить данные исследования в своей стране и своем регионе, чтобы представлять реальные прогностические возможности данного способа диагностики. Прогностические параметры (по конечным твердым точкам) допплеровского исследования печеночного кровотока у больных ЦП, полученные отечественными исследователями, в литературе не встретились. Работы отечественных исследователей, посвященные допплеровскому исследованию печеночного кровотока, затрагивают, в основном, вопросы диагностики и разграничения гепатитов и ЦП [20, 21, 22]. Отсутствие прогностических работ по допплеровскому исследованию печеночного кровотока при ЦП в России определяют актуальность данных исследований. Полученные прогностические параметры позволят изучать влияние на них вазоактивных лекарственных препаратов с целью определения наиболее перспективных средств для улучшения прогноза у больных ЦП. Наиболее близким к предлагаемому способу по точности является инвазивная методика измерения давления в воротной вене путем ее пунктирования [6]. Однако использование данной методики связано с большим риском для жизни пациента. Новая техническая задача – расширение ассортимента наиболее информативных способов прогнозирования, дающих возможность прогнозировать неблагоприятный исход у более широкой группы пациентов, обладающих наименьшим количеством или отсутствием осложнений. Для решения поставленной задачи в способе прогнозирования неблагоприятного исхода у больных циррозом печени вирусной и алкогольной этиологии путем определения параметров портального кровотока определяют пиковую скорость кровотока в печеночной артерии VпикПА (см/с) и объемную скорость кровотока в верхней брыжеечной вене VобВБВ (мл/мин) методом ультразвуковой допплерографии и при VпикПА Способ осуществляют следующим образом. У больных циррозом печени вирусной и алкогольной этиологии путем определения параметров портального кровотока, определяют пиковую скорость кровотока в печеночной артерии VпикПА (см/с) и объемную скорость кровотока в верхней брыжеечной вене VобВБВ (мл/мин) методом ультразвуковой допплерографии и при VпикПА Предлагаемые критерии подобраны на основании анализа результатов клинических наблюдений за пациентами, страдающими ЦП. Проведено обсервационное одномоментное перспективное исследование 88 больных ЦП вирусной (В, С, В+С), алкогольной и смешанной (алкогольно-вирусной) этиологии с оценкой конечной твердой точки – наступления летального исхода от ЦП или его осложнений. Возраст больных от 30 лет до 71 года (Ме=49,5 лет), 33 мужчины и 55 женщин. Момент включения в исследование – верификация в стационаре ОКБ г.Томска ЦП или поступление в стационар в связи с декомпенсацией ЦП. Диагноз ЦП подтвержден морфологически (лапароскопия с биопсией) у 3 больных, у остальных выставлен на основании наличия признаков диффузного повреждения печени, наличия синдрома печеночно-клеточной недостаточности, синдрома портальной гипертензии (варикозное расширение вен желудка и пищевода, асцит). Этиология ЦП определена указанием в анамнезе на многолетнее злоупотребление алкоголем и данными вирусологического исследования сыворотки крови на маркеры вирусов гепатита В (HBsAg, а/т классов М и G к HBcorAg, ДНК HBV), С (а/т классов М и G к HCV, РНК HCV) и D (а/т к HDV). Из исследования исключены больные с тяжелой сопутствующей патологией: правожелудочковой хронической сердечной недостаточностью, сахарным диабетом тяжелого течения, онкопатологией, туберкулезом, болезнями почек с почечной недостаточностью, болезнями легких с дыхательной недостаточностью. Период наблюдения от 1 месяца до 24 месяцев. За все время наблюдения умерли 37 пациентов. Все больные ЦП были разделены на 2 группы (умершие – 1 гр. и выжившие – 2 гр.) по периодам – 6 месяцев (умерли 16, выжили 72), 12 месяцев (умерли 29, выжили 56), 18 месяцев (умерли 35, выжили 28) и 24 месяца (умерли 37, выжили 12). Группы умерших и выживших больных ЦП по указанным периодам были сопоставимы по полу и возрасту. Всем больным проводилось ультразвуковое исследование сосудов системы воротной вены и печеночной артерии в режимах серошкальной визуализации и импульсноволновой допплерографии на аппарате Logiq-7 (General Electric, USA) с помощью датчика частотой 3,5 МГц. Исследование проводилось не ранее, чем через 8 часов после приема пищи. Оценивались следующие показатели портального кровотока: диаметр верхней брыжеечной вены (dВБВ), объемная (VобВБВ) и линейная скорости кровотока в верхней брыжеечной вене (VлинВБВ), диаметр воротной вены (dBB), объемная (VобBB) и линейная скорости кровотока в воротной вене (VлинВВ), диаметр селезеночной вены (dCB), объемная (VобСВ) и линейная скорости кровотока в селезеночной вене (VлинСВ), диаметр печеночной артерии (dПА), объемная (VобПА) и пиковая скорость кровотока в печеночной артерии (VпикПА), сплено-портальный индекс (СПИ)=VoбCB/VoбBB×100%. Статистическая обработка данных проводилась с помощью программы Statistica v6.0 (StatSoft, США). Проверка групп на нормальность распределения признаков проведена с помощью критерия Лиллиефорса. Сопоставимость групп по полу и возрасту проверялась при помощи непараметрического критерия Манна-Уитни. Статистически значимыми считались отличия при р<0,05. Группы 1 и 2 сравнивались по полученным допплерографическим параметрам. Распределение признаков в сравниваемых группах не подчинялось законам нормального распределения, поэтому сравнение показателей между группами проводилось при помощи 95% доверительного интервала (ДИ) для медианы распределения. Статистически значимыми считались отличия (Р=95%), когда медианы признака сравниваемых групп не содержались в 95% ДИ противоположной группы. В результате получены статистически значимые отличия по следующим параметрам: для 6 месяцев – VпикПА, для 18 и 24 месяцев – VпикПА и VобВБВ. Данные представлены в таблице, где приведены показатели VпикПА и VобВБВ у умерших и выживших пациентов за периоды 6, 18 и 24 месяца. Проведен анализ доверительных интервалов сравниваемых показателей для определения пороговых прогностических значений. Исключая области пересечения доверительных интервалов сравниваемых величин, получаются пороговые прогностические значения показателей: VпикПА – 103 см/с для прогноза 6-месячной летальности; VобВБВ – 395 мл/мин и VпикПА – 103 см/с для прогноза 18-месячной летальности; VобВБВ – 340 мл/мин и VпикПА – 95 см/с. Установлены прогностическая ценность превышения порога (ПЦПП), свидетельствующая о вероятности наступления летального исхода при превышении порога и прогностическая ценность уменьшения порога (ПЦУП), определяющая вероятность отсутствия летального исхода для подпороговых значений. ПЦПП=количество успешных прогнозов летальности при превышении порога / (количество ложных летальных прогнозов при превышении порога+количество успешных прогнозов летальности при превышении порога). ПЦУП=количество успешных прогнозов отсутствия летальности для подпороговых значении / количество ложных прогнозов отсутствия летальности для подпороговых значений+количество успешных прогнозов отсутствия летальности для подпороговых значений). С учетом прогностической ценности сформулированы прогностические правила. 1. Прогноз на 6 месяцев: при VпикПА 2. Прогноз на 18 месяцев: при VпикПА 3. Прогноз на 24 месяца: при VпикПА>95 см/с, вероятность летальности 92%, а при VпикПА При определении вероятности летального исхода по двум показателям (VпикПА и VобВБВ) для 18 и 24-месяцев выбирается прогноз с большей вероятностью летального исхода. Пример 1. В отделение гастроэнтерологии ОКБ г.Томска поступил больной Л., 42 года, с диагнозом ЦП алкогольной этиологии (диагноз установлен 2 года назад). При поступлении больной предъявлял жалобы на увеличение живота, слабость. При объективном исследовании выявлены: субиктеричность склер, асцит, гепато- и спленомегалия. Печеночная энцефалопатия 2 ст. В общем анализе крови – гемоглобин 115 г/л, лейкоциты 7,5×109/л, СОЭ 22 мм/ч. В биохимическом анализе крови – альбумины 29 г/л, общий билирубин 56,3 мкмоль/л. Протромбиновый индекс 70%. По данным ЭГДС – варикозное расширение вен пищевода и желудка 3 степени. По данным ультразвуковой допплерографии печеночного кровотока VпикПА=100 см/с. По шкале Чайлда-Пью – класс С (10 баллов). У родственников возник вопрос о прогнозе на 6 месяцев. Основываясь на выработанных критериях прогноза по показателю VпикПА для 6 месяцев (пороговое значение – 103 см/с), вероятность летального исхода равна 7,7%. С учетом определенного прогноза больному проведена коррекция лечения и определен план долговременной терапии. Прогноз подтвердился – больной прожил 12 месяцев. Это позволило родственникам планировать и решить все юридические проблемы при жизни больного. Пример 2. В отделение гастроэнтерологии ОКБ г.Томска поступила больная З., 47 лет, с диагнозом ЦП вирусной (HBV+HCV) этиологии в связи с ухудшением состояния. Диагноз установлен 1 год назад. При поступлении больная предъявляла жалобы на отсутствие аппетита, горечь во рту, слабость, боли в коленных и тазобедренных суставах. При объективном исследовании выявлены спленомегалия и дефицит массы тела (индекс массы тела 21,4 кг/м2). Печеночной энцефалопатии нет. В общем анализе крови -гемоглобин 110 г/л, лейкоциты 5,7×109/л, СОЭ 17 мм/ч. В биохимическом анализе крови альбумины 33 г/л, общий билирубин 24,9 мкмоль/л. Протромбиновый индекс 90%. По данным ЭГДС – варикозное расширение вен пищевода и желудка 2-3 степени. По данным УЗИ – небольшое количество жидкости в брюшной полости. По данным ультразвуковой допплерографии печеночного кровотока VпикПА=125 см/сек, VобВБВ=403 мл/мин. По шкале Чайлда-Пью – класс В (7 баллов). Возник вопрос о прогнозе на период 1,5 года, в течение которого больная планировала отправиться на консультацию и возможную трансплантацию печени в Германию. Согласно предлагаемому способу определяют VпикПА и VобВБВ, оказалось, что для 18-месячного прогноза показатели больной превышают пороговые значения (соответственно 103 см/сек и 395 мл/мин), из чего следует, что вероятность летального исхода в этот период составляет 73,3% (по показателю, отражающему худший прогноз). К сожалению, наш прогноз подтвердился и больная умерла через 14 месяцев, не дождавшись операции пересадки печени, хотя при классе В по Чайлду-Пью можно было надеяться на лучший прогноз. Пример 3. В отделение гастроэнтерологии ОКБ г.Томска в плановом порядке поступил больной К., 54 года, с диагнозом ЦП вирусной (HBV) этиологии по направлению поликлиники с места жительства. Цель госпитализации – обследование и коррекция лечения. Диагноз ЦП установлен 0,5 года назад. Больной предъявлял жалобы на быструю утомляемость. При объективном исследовании выявлена гепато- и спленомегалия. Печеночной энцефалопатии нет. В общем анализе крови – гемоглобин 135 г/л, лейкоциты 6,8×109/л, СОЭ 12 мм/ч. В биохимическом анализе крови – альбумины 35 г/л, общий билирубин 19,9 мкмоль/л. Протромбиновый индекс 78%. По данным ЭГДС – варикозное расширение вен пищевода и желудка 2 степени. По данным УЗИ – асцит. По данным ультразвуковой допплерографии печеночного кровотока УпикПА-98 см/с, VобВБВ – 320 мл/мин. По шкале Чайлда-Пью – класс В (7 баллов). Мы проследили судьбу пациента в течение 2 лет после данной госпитализации. Прогноз на 24 месяца по критериям VпикПА (пороговое значение 95 см/с) и VобВБВ (пороговое значение 340 мл/мин) определен по показателю УпикПА, как отражающему более выраженные нарушения печеночной гемодинамики у данного больного, и соответственно вероятность наступления летального исхода в течение 24 месяцев равнялась 92%. С учетом определенного прогноза проведена коррекция патогенетической терапии для улучшения качества жизни больного. Больной умер через 19 месяцев после настоящей госпитализации, что подтвердило наш прогноз. Прогрессирование ЦП связано с усугублением портальной гипертензии, которое проявляется увеличением шунтирования крови по анастомозам воротной вены. ВБВ является самым крупным сосудом, образующим портальную вену, и содержит наибольший объем крови среди всех притоков, поэтому VобВБВ будет увеличиваться при прогрессировании синдрома портальной гипертензии. Что касается увеличения VпикПА, то этот процесс называется артериализацией печеночного кровотока в ответ на уменьшение воротного кровотока и является закономерным патогенетическим механизмом прогрессирования портальной гипертензии [23]. Таким образом, полученные нами показатели как патогенетически, так и количественно отражают выраженность портальной гипертензии и являются независимыми прогностическими признаками ЦП. Преимущество изобретения заключается в возможности определения прогноза у больных ЦП доступной, неинвазивной методикой для периодов 6,18 и 24 месяца.
Источники информации 1. Bosch J., Garcia-Pagan J.C. Pathophysiology of portal hypertension and its complications. In: Bircher J., Benhamou J.P., Mclntyre N. et al. Oxford Textbook of Clinical Hepatology, Volume 1- 2nd ed. New York: Oxford University Press; 1999. p.653-60. 2. Perello A., Escorsell A., Bru C. et al. Wedged hepatic venous pressure adequately reflects portal pressure in hepatitis С virus-related cirrhosis. Hepatology 1999; 30: 1393-7. 3. Groszmann R.J., Wongcharatrawee S. The hepatic venous pressure gradient: anything worth doing should be done right. Hepatology 2004; 39: 280-2. 4. Lalema W., Van Landeghem L., Wilmer A., Fevery J., Nevens F. Portal Hypertension: From Pathophysiology to Clinical Practice. Liver Int 2005; 25(6): 1079-90. 5. Baik S.K., Jee M.G., Jeong P.H., Kim J.W., Ji S.W., Kim H.S. et al. Relationship of hemodynamic indices and prognosis in patients with liver cirrhosis. Korean J Intern Med 2004; 19(3): 165-70. 6. Vorobioff J., Groszmann R.J., Picabea E. et al. Prognostic value of hepatic venous pressure gradient measurements in alcoholic cirrhosis: a 10-year prospective study. Gastroenterology. 1996; 111(3): 701-9. 7. Vizzutti F., Arena U., Rega L. et al. Performance of Doppler Ultrasound in the Prediction of Severe Portal Hypertension in Hepatitis С Virus-Related Chronic Liver Disease. Liver Int 2007; 27(10): 1379-88. 8. Garcia-Tsao G., Groszmann R.H., Fischer R.L., et al. Portal pressure, presence of gastrointestinal varices and variceal bleeding. Hepatology 1985; 31: 419-24. 9. Casado M., Bosch J., Garcia-Pagan J.C. et al. Clinical events after transjugular intrahepatic porto-systemic shunt: correlation with hemodynamic findings. Gastroenterology 1998; 114: 1296-303. 10. Taourel P., Blanc P., Dauzat M. et al. Doppler study of mesenteric, hepatic, and portal circulation in alcoholic cirrhosis: relationship between quantitative Doppler measurements and the severity of portal hypertension and hepatic failure. Hepatology 1998; 28(4): 932-6. 11. Kim M.Y., Baik S.K., Park D.H. et al. Damping Index of Doppler Hepatic Vein Waveform to Assess the Severity of Portal Hypertension and Response to Propranolol in Liver Cirrhosis: A Prospective Nonrandomized Study. Liver Int 2007; 27(8): 1103-10. 12. Zoli M., Iervese Т., Merkel C. et al. Prognostic significance of portal hemodynamics in patients with compensated cirrhosis. J Hepatol 1993; 17(1): 56-61. 13. De Vries P.J., De Hooge P., Hoekstra J.B., Van Hattum J. Blunted postprandial reaction of portal venous flow in chronic liver disease, assessed with duplex Doppler: significance for prognosis. J Hepatol 1994; 21(6): 966-73. 14. Ohta M., Hashizume M., Kawanaka H. et al. Prognostic significance of hepatic vein waveform by Doppler ultrasonography in cirrhotic patients with portal hypertension. Am J Gastroenterol 1995; 90(10):1853-7. 15. Kayacetin E., Efe D., Do 16. Li F.H., Hao J., Xia J.G., Li H.L., Fang H. Hemodynamic analysis of esophageal varices in patients with liver cirrhosis using color Doppler ultrasound. World J Gastroenterol 2005; 11(29): 4560-5. 17. Kogo M., Nebashi Y., Taniguchi H., Yoneyama K., Imawari M., Kiuchi Y. Evaluation of paraumbilical vein as a prognostic index of severe liver cirrhotic patients with portal-systemic shunts. Minerva Gastroenterol Dietol 2006; 52(4):371-8. 18. Macias-Rodriguez M.A., Rendon-Unceta P., Martinez-Sierra M.C., Teyssiere-Blas I., Diaz-Garcia F., Martin-Herrera L. Prognostic usefulness of ultrasonographic signs of portal hypertension in patients with Child-Pugh stage A liver cirrhosis. Am J Gastroenterol 1999; 94(12): 3595-600. 19. De Vries P.J., Hoekstra J.B., De Hooge P., Van Hattum J. Portal venous flow and follow-up in patients with liver disease and healthy subjects. Assessment with duplex Doppler. Scand J Gastroenterol 1994; 29(2): 172-7. 20. Федотов И.Г., Митьков В.В. Значение допплерографии сосудов чревного русла на фоне пищевой нагрузки в диагностике диффузных заболеваний печени. Ультразв. и функц. диагн. 2001; 2:19-24. 21. Митьков В.В., Садоков В.М., Хитрова А.Н., Черешнева Ю.Н., Краснова Т.В., Митькова М.Д. Неинвазивная допплерографическая диагностика цирроза печени на основе анализа времени поступления эхоконтрастного вещества в печеночные вены. Ультразв. и функц. диагн. 2001; 2: 14-8. 22. Митьков В.В., Митькова М.Д., Федотов И.Г., Серебренников В.А., Черешнева Ю.Н., Кравченко Н.А. Оценка портального кровотока при циррозе печени. Ультразв. диагн. 2000; 4: 10-7. 23. Zoli М., Magalotti D., Bianchi G. et al. Functional hepatic flow and Doppler-assessed total hepatic flow in control subjects and patients with cirrhosis. J Hepatol 1995; 23: 129-34.
Формула изобретения
Способ прогнозирования неблагоприятного исхода у больных циррозом печени вирусной и алкогольной этиологии путем определения параметров портального кровотока, отличающийся тем, что определяют пиковую скорость кровотока в печеночной артерии УпикПА (см/с) и объемную скорость кровотока в верхней брыжеечной вене УобВБВ (мл/мин) методом ультразвуковой допплерографии и при УпикПА
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||

 2, 2001, с.19-24. PUGLIESE D. et al. Portal hemodynamics after meal in normal subjects and in patients with chronic liver disease studied by echo-Doppler flowmeter, Am J Gastroenterol., 1987 Oct, 82(10), p.1052-1056.
2, 2001, с.19-24. PUGLIESE D. et al. Portal hemodynamics after meal in normal subjects and in patients with chronic liver disease studied by echo-Doppler flowmeter, Am J Gastroenterol., 1987 Oct, 82(10), p.1052-1056.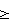 103 см/с, определяют вероятность наступления летального исхода в течение 6 месяцев; при УпикПА
103 см/с, определяют вероятность наступления летального исхода в течение 6 месяцев; при УпикПА -блокаторами уменьшает риск кровотечения из варикозных вен [4]. Неинвазивной методикой точно получить значение HVPG в настоящее время нельзя. Ограничения инвазивной методики связаны с повышенным риском кровотечения у больных ЦП, наличием асцита, проблемой динамического контроля (повторных исследований) и доступностью данного исследования только в крупных центрах.
-блокаторами уменьшает риск кровотечения из варикозных вен [4]. Неинвазивной методикой точно получить значение HVPG в настоящее время нельзя. Ограничения инвазивной методики связаны с повышенным риском кровотечения у больных ЦП, наличием асцита, проблемой динамического контроля (повторных исследований) и доступностью данного исследования только в крупных центрах. 103 см/с вероятность летальности – 28,9%, а при VпикПА<103 см/с вероятность летальности 7,7%.
103 см/с вероятность летальности – 28,9%, а при VпикПА<103 см/с вероятность летальности 7,7%.
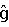 an C. Portal and splenic hemodynamics in cirrhotic patients: relationship between esophageal variceal bleeding and the severity of hepatic failure. J Gastroenterol 2004 Jul; 39(7): 661-7.
an C. Portal and splenic hemodynamics in cirrhotic patients: relationship between esophageal variceal bleeding and the severity of hepatic failure. J Gastroenterol 2004 Jul; 39(7): 661-7.