Патент на изобретение №2381227
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ЗАМЕЩЕННЫЕ БЕНЗОТИАЗОЛЫ
(57) Реферат:
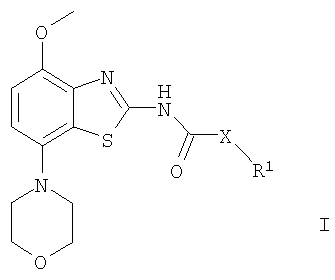
Изобретение относится к производным бензотиазола общей формулы (I) и их фармацевтически приемлемым кислотно-аддитивным солям, оптически чистым энантиомерам, рацематам и диастереомерным смесям в качестве лигандов рецептора аденозина и к фармацевтическому препарату на их основе. Соединения могут найти применение для лечения и профилактики заболеваний, опосредованных рецепторами аденозина А2А, например болезни Альцгеймера, некоторых депрессивных состояний, токсикомании, болезни Паркинсона. В общей формуле (I)
R1 представляет собой С3-7циклоалкил, замещенный группой OR, или 2-(7-окса-бицикло[2.2.1]гепт-1-ил)-этил; R представляет собой водород или С(O)-низший алкил; Х представляет собой -CHR’-; и R’ представляет собой водород или низший алкил. 2 н. и 6 з.п. ф-лы.
Изобретение относится к соединениям общей формулы
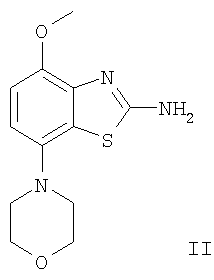
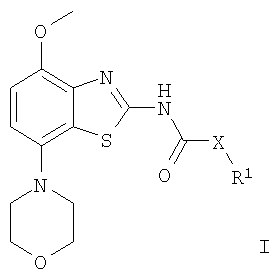
где R1 представляет собой циклоалкил, замещенный группой OR, или 2-(7-окса-бицикпо[2.2.1]гепт-1-ил)-этил; R представляет собой водород, низший алкил или С(O)-низший алкил; Х представляет собой -CHR’-; и R’ представляет собой водород или низший алкил; и к их фармацевтически приемлемым кислотно-аддитивным солям, оптически чистым энантиомерам, рацематам или диастереомерным смесям. Неожиданно было установлено, что соединения общей формулы I являются лигандами аденозинового рецептора. В особенности, соединения настоящего изобретения обладают хорошим сродством к A2A-рецептору и высокой селективностью к А1– и А3-рецепторам. Аденозин моделирует широкий диапазон физиологических функций, взаимодействуя со специфическими рецепторами клеточной поверхности. Первая обзорная работа, посвященная возможности использования аденозиновых рецепторов в качестве мишеней для лекарств была опубликована в 1982 году. Аденозин структурно и метаболически имеет отношение к биоактивным нуклеотидам аденозинтрифосфату (АТФ), аденозиндифосфату (АДФ), аденозинмонофосфату (АМФ) и циклическому аденозинмонофосфату (цАМФ), к биохимическому метилирующему агенту S-аденозил-L-метионину (SAM); и структурно к коферментам НАД, ФАД и коферменту А; и к РНК. Аденозин и эти родственные соединения вместе важны в регулировании многих видов клеточного метаболизма и в модуляции различных активностей центральной нервной системы. Рецепторы аденозина классифицированы как A1, A2A, A2B и А3 рецепторы, относящиеся к семейству G-белок сопряженных рецепторов. Активация аденозиновых рецепторов под действием аденозина инициирует механизм передачи сигналов. Эти механизмы зависят от G-белка, ассоциированного с рецептором. Каждый подтип аденозиновых рецепторов традиционно отличается по влиянию на эффекторную систему аденилатциклазы, которая использует цАМФ в качестве вторичного мессенджера. A1 и А3 рецепторы, сопряженные с Gi-белками, ингибируют аденилатциклазу, приводя к уменьшению уровней клеточного цАМФ, тогда как A2A и A2B рецепторы, сопряженные с Gs-белками, активируют аденилатциклазу, приводя к увеличению уровней клеточного цАМФ. Известно, что система A1 рецептора включает активацию фосфолипазы С и модуляцию ионных калиевых и кальциевых каналов. Также подтип А3, кроме его ассоциации с аденилатциклазой, стимулирует фосфолипазу С и активирует ионные кальциевые каналы. A1 рецептор (326-328 аминокислот) был клонирован из различных биологических видов (семейство псовых, человек, крыса, собака, цыпленок, семейство бычьих, морская свинка) с идентичностью последовательности 90-95% среди видов млекопитающих. A2A рецептор (409-412 аминокислот) был клонирован из семейства псовых, крысы, человека, морской свинки и мыши. A2B рецептор (332 аминокислоты) был клонирован из человека и мыши с 45% гомологией A2B рецептора человека с A1 и A2A рецепторами человека. А3 рецептор (317-320 аминокислот) был клонирован из человека, крысы, собаки, кролика и овцы. Предполагают, что подтипы A1 и A2A рецепторов играют комплементарные роли в аденозиновом регулировании энергоснабжения. Аденозин, который представляет собой метаболический продукт АТФ, диффундирует из клетки и действует локально, активируя аденозиновые рецепторы для уменьшения потребности в кислороде (A1) или увеличения снабжения кислородом (A2A), и восстановления, таким образом, баланса энергоснабжения: потребность внутри ткани. Действия обоих подтипов должны увеличивать количество доступного кислорода в ткани и предохранять клетки от повреждения, вызванного краткосрочным дисбалансом кислорода. Одной из важнейших функций эндогенного аденозина является предупреждение повреждений при травмах, таких как гипоксия, ишемия, гипотензия и судорожная активность. Кроме того, известно, что связывание агониста аденозинового рецептора с мастоцитами, экспрессирующими крысиный А3 рецептор, приводит к повышенным концентрациям трифосфат инозитола и внутриклеточного кальция, которые потенцируют антиген-индуцированную секрецию воспалительных медиаторов. Таким образом, А3 рецептор играет роль в опосредованных астматических приступах и других аллергических откликах. Аденозин является нейромодулятором, способным модулировать многие виды физиологической функции мозга. Эндогенный аденозин, центральное звено между энергетическим обменом и неврональной активностью, изменяется согласно поведенческому состоянию и (пато)физиологическим состояниям. При состояниях увеличенной потребности и уменьшенной доступности энергии (таких как гипоксия, гипогликемия и/или чрезмерная неврональная активность) аденозин обеспечивает значительный защитный механизм обратной связи. Взаимодействие с аденозиновыми рецепторами представляет многообещающую цель для терапевтического вмешательства в ряд неврологических и психиатрических расстройств, таких как эпилепсия, онемение, двигательные расстройства (болезнь Паркинсона или Хантингтона), болезнь Альцгеймера, депрессия, шизофрения или пагубное привыкание. Увеличение высвобождения нейротрансмиттеров происходит в результате повреждений, таких как гипоксия, ишемия и судороги. В итоге эти нейротрансмиттеры являются ответственными за дегенерацию нейронов и смерть нейронов, которая вызывает повреждение мозга или смерть человека. Поэтому аденозиновые A1-агонисты, которые имитируют центральные ингибиторные эффекты аденозина, могут быть полезны как нейрозащитные агенты. Аденозин был предложен в качестве эндогенного противосудорожного агента, ингибирующего высвобождение глутамата из возбудительных нейронов и ингибирующий неврональный разряд. Следовательно, аденозиновые агонисты можно использовать как противоэпилептические агенты. Аденозиновые антагонисты стимулируют активность ЦНС и, как установлено, эффективны в качестве агентов, усиливающих когнитивную способность. Селективные A2a антагонисты обладают терапевтическим потенциалом при лечении различных форм слабоумия, например болезни Альцгеймера, и нейродегенеративных расстройств, например инсульта. Антагонисты аденозинового А2а рецептора модулируют активность стриарных ГАМК-ергических нейронов и регулируют плавные и хорошо согласованные движения, предлагая, таким образом, возможное лечение симптомов Паркинсона. Также аденозин вовлечен в ряд физиологических процессов, приводящих к седации, гипнозу, шизофрении, беспокойству, боли, нарушению дыхания, депрессии и привыканию к наркотическим средствам (амфетамину, кокаину, опиоидам, этанолу, никотину, каннабиноидам). Следовательно, лекарства, действующие через аденозиновые рецепторы, обладают терапевтическим потенциалом как седативные средства, мышечные релаксанты, нейролептические препараты, анксиолитики, болеутоляющие средства, стимуляторы дыхания, антидепрессанты и применимы для лечения наркотической зависимости. Также их можно использовать при лечении СДВГ (синдрома дефицита внимания с гиперактивностью). Аденозин в сердечно-сосудистой системе играет важную роль как кардиозащитный агент. Уровни эндогенного аденозина увеличиваются в ответ на ишемию и гипоксию и предохраняют сердечную ткань во время и после травмы (предобработка). Действуя в A1 рецепторе, аденозиновые A1 агонисты могут предохранить от повреждения, вызванного ишемией миокарда и реперфузией. Модулирующее влияние A2a рецепторов на адренергическую функцию может иметь значение для ряда расстройств, таких как болезнь коронарных артерий и сердечная недостаточность. А2а антагонисты могут быть терапевтически полезны в случаях, при которых требуется усиленный антиадренергический отклик, например во время острой ишемии миокарда. Также селективные антагонисты A2a рецепторов могут усиливать эффективность аденозина при прекращении супражелудочковых аритмий. Аденозин модулирует многие виды почечной функции, включая высвобождение ренина, скорость клубочковой фильтрации и почечный кровоток. Соединения, которые противодействуют нежелательному действию аденозина на почечную функцию, обладают потенциалом почечных защитных агентов. Кроме того, аденозиновые А3 и/или A2B антагонисты могут быть полезны при лечении астмы и других аллергических откликов или при лечении сахарного диабета и ожирения. Многочисленные документы описывают современные данные относительно аденозиновых рецепторов, например следующие публикации: Bioorganic & Medicinal Chemistry, 6, (1998), 619-641, Bioorganic & Medicinal Chemistry, 6, (1998), 707-719, J. Med. Chem., (1998), 41, 2835-2845, J. Med. Chem., (1998), 41, 3186-3201, J. Med. Chem., (1998), 41, 2126-2133, J. Med. Chem., (1999), 42, 706-721, J. Med. Chem., (1996), 39, 1164-1171, Arch. Pharm. Med. Chem., 332, 39-41, (1999), Am.J.Physiol., 276, H1113-1116, (1999) или Naunyn Schmied, Arch. Pharmacol. 362, 375-381, (2000). Предметом настоящего изобретения являются соединения формулы 1 как таковые, применение соединений формулы 1 и их фармацевтически приемлемых солей для изготовления лекарств для лечения расстройств, связанных с аденозиновым А2 рецептором, их изготовление, лекарства, основанные на соединении в соответствии с данным изобретением и их производство, а также применение соединений формулы 1 при контроле или предотвращении заболеваний, основанных на модуляции аденозиновой системы, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, нейропротективное действие, шизофрения, беспокойство, боль, нарушения дыхания, депрессия, привыкание к наркотическим средствам, таким как амфетамин, кокаин, опиоиды, этанол, никотин, каннабиноиды, или для лечения астмы, аллергических откликов, гипоксии, ишемии, судорог и наркотической зависимости. Кроме того, соединения настоящего изобретения могут быть полезны в качестве седативных средств, мышечных релаксантов, нейролептических препаратов, противоэпилептических средств, противосудорожных препаратов и кардиозащитных агентов для расстройств, таких как ишемическая болезнь сердца (болезнь коронарных артерий) и сердечная недостаточность. Наиболее предпочтительными показаниями согласно настоящему изобретению являются те, которые основываются на антагонистической активности к A2A рецептору и которые включают расстройства центральной нервной системы, например лечение или предотвращение болезни Альцгеймера, некоторых депрессивных расстройств, привыкания к наркотическим средствам, нейропротективного действия, болезни Паркинсона, а также СДВГ. Используемый здесь термин «низший алкил» обозначает насыщенную неразветвленную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода, например метил, этил, пропил, изо-пропил, н-бутил, изо-бутил, 2-бутил, трет-бутил и т.п. Предпочтительными низшими алкильными группами являются группы с 1 -4 атомами углерода. Термин «циклоалкил» обозначает насыщенную карбоциклическую группу, содержащую 3-7 атомов углерода. Термин «фармацевтически приемлемые кислотно-аддитивные соли» включает в себя соли с неорганическими и органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п. Предпочтительными соединениями настоящей заявки являются соединения формулы I, где R1 представляет собой замещенный циклопентил и Х представляет собой -СН2-, например, (цис)-2-(3-ацетокси-цикпопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид, (цис)-2-(3-ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид, (-)-(цис)-2-(3-гидрокси-циклопентил)-N-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид или (+)-(цис)-2-(3-гидрокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид. Также предпочтительными являются соединения, где R1 представляет собой замещенный циклогексил и Х представляет собой -CH2-, например, (цис)-2-(4-гидрокси-циклогексил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид или (транс)-2-(4-гидрокси-цикпогексил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид. Другим предпочтительным воплощением данного изобретения являются те соединения, где R1 представляет собой 2-(7-окса-бицикло[2.2.1]гепт-1-ил)-этил, например, (рац)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-2-(7-окса-бицикло[2.2.1]гепт-1-ил)-пропионамид. Данные соединения формулы I и их фармацевтически приемлемые соли можно получить известными из предшествующего уровня техники способами, например, описанными ниже, при которых подвергают взаимодействию соединение формулы
с соединением формулы
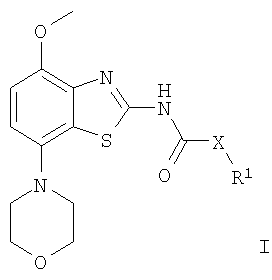
с получением соединения формулы
где R1 и Х имеют приведенные выше значения, и при желании переводят полученные соединения в фармацевтически приемлемые кислотно-аддитивные соли. В примерах 1-7 получение соединений формулы I описано более подробно. Исходные реагенты являются известными соединениями либо их можно получить известными из предшествующего уровня техники способами. Получение соединений формулы I Промежуточное соединение 7-(морфолин-4-ил)-4-метокси-бензотиазол-2-иламин можно получить способами, описанными в WO 01/97786. Также в WO 01/97786 описано получение соединений формулы (I) с использованием промежуточного соединения формулы (II). Например, соединение формулы I можно получить следующим образом: К раствору замещенной циклоалкануксусной кислоты и N,N-диметилформамида в дихлорметане добавляют оксалилхлорид и полученный в результате раствор перемешивают в течение приблизительно 18 часов при температуре окружающей среды. После выпаривания летучих компонентов в вакууме остаток переносят в толуол и опять выпаривают досуха. Затем полученный хлорангидрид кислоты формулы (III) растворяют в дихлорметане и последовательно добавляют N-этил-диизопропиламин и 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин (II). После перемешивания в течение приблизительно 2 часов при температуре окружающей среды смесь охлаждают до комнатной температуры и добавляют насыщенный водный гидрокарбонат натрия, экстрагируют и высушивают. Разделением с помощью препаративной хиральной ВЭЖХ получают требуемое соединение формулы I. Выделение и очистка соединений Выделение и очистку описанных здесь соединений и промежуточных соединений можно осуществить, если требуется, с помощью любой подходящей процедуры разделения или очистки, такой как, например, фильтрование, экстракция, кристаллизация, колоночная хроматография, тонкослойная хроматография, хроматография в толстом слое, препаративная жидкостная хроматография низкого или высокого давления или комбинацией этих процедур. Конкретные иллюстрации подходящих процедур разделения и выделения могут быть сделаны путем ссылки на получения и примеры, приведенные ниже. Однако другие эквивалентные процедуры разделения или выделения, конечно, также могут быть использованы. Соли соединений формулы I Соединения формулы I могут быть основными, например, в тех случаях, когда остаток R содержит основную группу, такую как группировка алифатического или ароматического амина. В таких случаях соединения формулы 1 можно превратить в соответствующую кислотно-аддитивную соль. Превращение осуществляют, добавляя по меньшей мере стехиометрическое количество соответствующей кислоты, такой как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п. Обычно свободное основание растворяют в инертном органическом растворителе, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол и т.п., и добавляют кислоту в аналогичном растворителе. Температуру поддерживают в диапазоне от 0°С до 50°С. Полученная в результате соль выпадает в осадок спонтанно или может быть выделена из раствора с менее полярным растворителем. Кислотно-аддитивные соли основных соединений формулы I можно превратить в соответствующие свободные основания, добавляя по меньшей мере стехиометрический эквивалент подходящего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и т.п. Соединения формулы I и их фармацевтически приемлемые соли присоединения обладают ценными фармакологическими свойствами. В частности, было установлено, что соединения настоящего изобретения являются лигандами аденозинового рецептора и обладают высоким сродством к аденозиновому A2A рецептору. Соединения исследовали в соответствии с нижеприведенным тестом. Аденозиновый A2A рецептор человека Аденозиновый A2a рецептор человека рекомбинантным путем экспрессировали в клетках яичника китайского хомячка (СНО), используя систему экспрессии вируса Semiliki forest. Клетки собирали, дважды промывали, центрифугируя, гомогенизировали и опять промывали, центрифугируя. Конечный промытый мембранный осадок суспендировали в Tris буфере (50 мМ), содержащем 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 and 10 мМ MgCl2 (pH 7,4) (буфер А). Анализ связывания [3H]-SCH-58261 (Dionisotti et al., 1997, Br. J. Pharmacol. 121, 353; 1 нМ) проводили на 96-луночном планшете в присутствии 2,5 мкг мембранного белка, 0,5 мг микрошариков с иммобилизованным Ysi-поли-L-лизином для SPA-анализа и 0,1 Ед. аденозиндезаминазы в конечном объеме 200 мкл буфера А. Неспецифическое связывание определяли, используя родственный ксантину амин (ХАС; 2 мкМ). Соединения тестировали при 10 концентрациях от 10 мкМ до 0,3 нМ. Все анализы проводили в двух экземплярах и повторяли, по меньшей мере, два раза. Аналитические планшеты инкубировали в течение 1 часа при комнатной температуре перед центрифугированием и затем связанные лиганды определяли, используя сцинтилляционный счетчик Packard Topcount. Значения ИК50 вычисляли, используя программу вычерчивания нелинейных кривых, и Ki значения рассчитывали по уравнению Ченга-Пруссова. pKi значения соединений настоящей заявки находятся в пределах от 7,7 до 8,5. Предпочтительные соединения показывают pKi>8,0.
Соединения формулы I и фармацевтически приемлемые соли соединений формулы I можно применять в качестве лекарств, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить перорально, например, в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным также может быть ректальное введение, например, в форме суппозиториев, парентеральное, например, в форме растворов для инъекций. Соединения формулы 1 можно переработать с фармацевтически инертными неорганическими или органическими носителями для получения фармацевтических препаратов. Лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и т.п. можно использовать, например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Однако в зависимости от природы активного вещества в случае мягких желатиновых капсул носители обычно не требуются. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, глицерин, растительные масла и т.п. Подходящими носителями для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и т.п. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, ароматизаторы, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Также они еще могут содержать другие терапевтически ценные вещества. Лекарства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный носитель, также являются предметом настоящего изобретения, как и способ их изготовления, при котором одно или более соединений формулы 1 и/или фармацевтически приемлемых кислотно-аддитивных солей и, если требуется, одно или более других терапевтически ценных веществ превращают в галеновою лекарственную форму вместе с одним или более терапевтически инертным носителем. Согласно данному изобретению соединения формулы I, а также их фармацевтически приемлемые соли являются полезными при контроле или предотвращении расстройств, основанных на антагонистической активности к аденозиновому рецептору, таких как болезнь Альцгеймера, болезнь Паркинсона, нейропротективное действие, шизофрения, беспокойство, боль, нарушения дыхания, депрессия, астма, аллергические отклики, гипоксия, ишемия, судороги и наркотическая зависимость. Кроме того, соединения настоящего изобретения могут быть полезны в качестве седативных средств, мышечных релаксантов, нейролептических препаратов, противоэпилептических средств, противосудорожных препаратов и кардиозащитных агентов и для изготовления соответствующих лекарств. Наиболее предпочтительными показаниями согласно настоящему изобретению являются те, которые включают расстройства центральной нервной системы, например лечение или предотвращение болезни Паркинсона, нейропротективное действие или некоторые депрессивные расстройства. Дозировка может варьировать в широких пределах и, конечно, должна быть подобрана по индивидуальным потребностям в каждом конкретном случае. В случае перорального введения дозировка для взрослого человека может варьировать от приблизительно 0,01 мг до приблизительно 1000 мг в день соединения общей формулы I или соответствующего количества его фармацевтически приемлемой соли. Суточную дозировку можно вводить в виде однократной дозы и разделенными дозами и, кроме того, верхний предел можно превысить, когда установлено, что это необходимо. Приготовление таблеток (влажная грануляция) Процедура изготовления 1. Смешивают 1, 2, 3 и 4 и гранулируют с очищенной водой. 2. Высушивают гранулы при 50°С. 3. Пропускают гранулы через подходящее помольное оборудование. 4. Добавляют 5 и перемешивают в течение трех минут; сжимают под соответствующим прессом. Приготовление капсул
Процедура изготовления 1. Смешивают 1, 2 и 3 в подходящей мешалке в течение 30 минут. 2. Добавляют 4 и 5 и перемешивают в течение 3 минут. 3. Заполняют подходящую капсулу. Следующие получение и примеры иллюстрируют изобретение, но подразумевается, что они не ограничивают его объем. Пример 1 (цис)-2-(3-Ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид К раствору (рац)-(цис)-3-(ацетилокси)-циклопентануксусной кислоты (770 мг, 4,1 ммоль) и N,N-диметилформамида (0,01 мл, 0,13 ммоль) в дихлорметане (10 мл) добавляли оксалилхлорид (1,4 мл, 17 ммоль) и полученный в результате раствор перемешивали в течение 18 часов при температуре окружающей среды. После выпаривания летучих компонентов в вакууме остаток переносили в толуол (10 мл) и опять выпаривали досуха. Затем полученный хлорангидрид кислоты растворяли в дихлорметане (20 мл) и последовательно добавляли N-этил-диизопропиламин (2,5 мл, 15 ммоль) и 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин (960 мг, 3,6 ммоль). После перемешивания в течение 2 часов при температуре окружающей среды и еще в течение часа при 50°С смесь охлаждали до комнатной температуры, добавляли насыщенный водный гидрокарбонат натрия (15 мл) и дважды экстрагировали дихлорметаном (каждый раз по 20 мл). После высушивания над сульфатом магния и выпаривания растворителей, с помощью флэш-хроматографии (силикагель, элюент: дихлорметан/этилацетат в соотношении 85:15) получали (рац)-(цис)-2-(3-ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид в виде грязно-белого твердого вещества. В ходе разделения с помощью препаративной хиральной ВЭЖХ (Chiralpack AD, элюент: гептан/изопропанол в соотношении 85:15) получали указанное в заголовке соединение как первый элюируемый изомер. Светло-желтое твердое вещество (выход 4%). MS: m/e=434 (M+H+), т.пл. 171-172°C. Согласно общему способу примера 1 получали соединения примеров 2-7. Пример 2 (цис)-2-(3-Ацетокси-цикпопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид Используя 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин и (рац)-(цис)-3-хлоркарбонилметил-циклопентиловый эфир уксусной кислоты, получали (рац)-(цис)-2-(3-ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид. В ходе разделения с помощью препаративной хиральной ВЭЖХ (Chiralpack AD, элюент: гептан/изопропанол в соотношении 85:15) получали указанное в заголовке соединение как последний элюируемый изомер. Светло-желтые кристаллы (выход 4%). MS: m/e=434 (M+H+), т.пл. 172-173°С. Пример 3 (-)-(цис)-2-(3-Гидрокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид (цис)-2-(3-Ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид (первый элюируемый изомер, 64 мг, 0,15 ммоль), карбонат калия (82 мг, 0,59 ммоль) и метоксид натрия (5,4 М в метаноле, 1,37 мкл, 0,0074 ммоль) перемешивали вместе в метаноле (6 мл) в течение 4 часов при температуре окружающей среды. Выпаривание растворителя, растворение в метиленхлориде и экстракция с насыщенным карбонатом натрия давали, после высушивания и выпаривания метиленхлорида, неочищенный продукт. После кристаллизации из диэтилового эфира получали указанное в заголовке соединение в виде светло-желтых кристаллов (выход 91%). MS: m/e=392 (М+Н+), т.пл. 168-171°С, Пример 4 (+)-(цис)-2-(3-Гидрокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид (цис)-2-(3-Ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид (последний элюируемый изомер, 64 мг, 0,15 ммоль), карбонат калия (82 мг, 0,59 ммоль) и метоксид натрия (5,4 М в метаноле, 1,37 мкл, 0,0074 ммоль) перемешивали вместе в метаноле (6 мл) в течение 4 часов при температуре окружающей среды. Выпаривание растворителя, растворение в метиленхлориде и экстракция с насыщенным карбонатом натрия давали, после высушивания и выпаривания метиленхлорида, неочищенный продукт. После кристаллизации из диэтилового эфира получали указанное в заголовке соединение в виде светло-желтых кристаллов (выход 90%). MS: m/e=392 (M+H+), т.пл. 167-170°С, Пример 5 (цис)-2-(4-Гидрокси-циклогексил)-N-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид Используя 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин и (цис)-4-хлоркарбонилметил-циклогексиловый эфир уксусной кислоты, синтезировали указанное в заголовке соединение точно таким же способом, как (цис)-2-(3-ацетокси-циклопентил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид, и получали его в виде светло-желтых кристаллов (выход 33%). MS: m/e=406 (M+H+), т.пл. 212-216°С. Пример 6 (транс)-2-(4-Гидрокси-циклогексил)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамид Используя 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин и (транс)-4-хлоркарбонилметил-циклогексиловый эфир уксусной кислоты, синтезировали указанное в заголовке соединение точно таким же способом, как описано для (цис)-2-(4-гидрокси-циклогексил)-N-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-ацетамида, и получали его в виде светло-желтых кристаллов (выход 51%). MS: m/e=406 (M+H+), т.пл. 190-192°С. Пример 7 (рац)-N-(4-Метокси-7-морфолин-4-ил-бензотиазол-2-ил)-2-(7-окса-бицикло[2.2.1]гепт-1 -ил)-пропионамид Используя 4-метокси-7-морфолин-4-ил-бензотиазол-2-иламин и 2-(7-окса-бицикло[2.2.1]гепт-1-ил)-пропионил хлорид, получали указанное в заголовке соединение в виде белого твердого вещества (выход 67%). MS: m/e=418 (M+H+), т.пл. 195-197°С. Пример 8 (промежуточное соединение) (рац)-2-(7-0кса-бицикло[2.2.1]гепт-1-ил)-пропионовая кислота Указанное в заголовке соединение получали в ходе стандартной реакции Виттига-Хорнера из 4-гидроксициклогексанона, этилового эфира 2-(диэтокси-фосфорил)-пропионовой кислоты и гидрида натрия (J. Boutagy, R. Thomas, Chem. Rev. 1974, 74, 87-99) и последующего омыления с гидроксидом калия в этаноле. После рекристаллизации из н-гептана получали указанное в заголовке соединение в виде белого твердого вещества. EI-MS: m/e=170(M+), 1H-ЯМР (90 МГц, CDCl3, TMC):
Формула изобретения
1. Соединения общей формулы 2. Соединения формулы I по п.1, где R1 представляет собой замещенный циклопентил и Х представляет собой -СН2-. 3. Соединения формулы I по п.2, где соединения представляют собой 4. Соединения формулы I по п.1, где R1 представляет собой замещенный циклогексил и Х представляет собой -СН2-. 5. Соединения формулы I по п.4, где соединения представляют собой 6. Соединения формулы I по п.1, где R1 представляет собой 2-(7-окса-бицикло[2.2.1]гепт-1-ил)-этил. 7. Соединения формулы I по п.6, где соединение представляет собой 8. Фармацевтический препарат, обладающий свойствами лиганда аденозинового рецептора А2А, содержащий одно или более соединений по любому из пп.1-7 и фармацевтически приемлемые эксципиенты.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

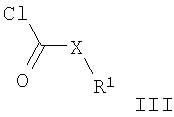



 589=-4,87 (CH2Cl2, с=1,1%).
589=-4,87 (CH2Cl2, с=1,1%). 1,3 (d, J=8 Гц, 3Н, Me), 1,7 (m, 8H, CH2), 3,0 (q, J=8 Гц, 1H, СН-Ме), 4,6 (t, J=4,5 Гц, 1Н, СН-O), 7,2 (s, 1H, СООН), т.пл. 61-62°С, т.кип. 120°С (0,008 мбар).
1,3 (d, J=8 Гц, 3Н, Me), 1,7 (m, 8H, CH2), 3,0 (q, J=8 Гц, 1H, СН-Ме), 4,6 (t, J=4,5 Гц, 1Н, СН-O), 7,2 (s, 1H, СООН), т.пл. 61-62°С, т.кип. 120°С (0,008 мбар).