|
|
(21), (22) Заявка: 2006146877/04, 20.06.2005
(24) Дата начала отсчета срока действия патента:
20.06.2005
(30) Конвенционный приоритет:
24.06.2004 SE 0401657-2
(43) Дата публикации заявки: 27.07.2008
(46) Опубликовано: 10.02.2010
(56) Список документов, цитированных в отчете о
поиске:
WO 01/14333 A1, 01.03.2001. WO 99/25686 A1, 27.05.1999. EP 1013276 A1, 28.06.2000. WO 03/042177 A1, 22.05.2003. WO 03/042205 A1, 22.05.2003. RU 2001128769 A, 10.05.2004.
(85) Дата перевода заявки PCT на национальную фазу:
24.01.2007
(86) Заявка PCT:
SE 2005/000952 20050620
(87) Публикация PCT:
WO 2006/001751 20060105
Адрес для переписки:
191036, Санкт-Петербург, а/я 24, “НЕВИНПАТ”, пат.пов. А.В.Поликарпову
|
(72) Автор(ы):
ТАКЕР Хауард (GB)
(73) Патентообладатель(и):
АстраЗенека АБ (SE)
|
(54) ХИМИЧЕСКИЕ СОЕДИНЕНИЯ I
(57) Реферат:
Изобретение относится к новому соединению N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамиду или к его фармацевтически приемлемым солям. Изобретение также относится к способу получения соединения по п.1, а также к фармацевтической композиции. Технический результат – получение нового биологически активного соединения, обладающего активностью в отношении CCR5 (хемокинового рецептора 5). 3 н. и 3 з.п. ф-лы, 2 табл.
Изобретение относится к гетероциклическим производным, обладающим фармацевтической активностью, к способам получения таких производных, к фармацевтическим композициям, содержащим такие производные, и к применению таких производных в качестве активных терапевтических агентов.
Фармацевтически активные производные пиперидина раскрыты в WO 03/042205. Необходимо, чтобы фармацевтические препараты были биодоступны, и соединения по настоящему изобретению демонстрируют лучшие уровни биодоступности и большую избирательность (например пониженную мускариновую активность) по сравнению с соединениями из WO 03/042205.
Хемокины являются хемотаксическими цитокинами, которые высвобождаются самыми разнообразными клетками для привлечения макрофагов, Т-клеток, эозинофилов, базофилов и нейтрофилов в сайты воспаления и играют также определенную роль в созревании клеток иммунной системы. Хемокины играют важную роль в иммунном и воспалительном ответах при различных заболеваниях и расстройствах, включая астму и аллергические заболевания, а также аутоиммунные патологии, такие как ревматоидный артрит и атеросклероз. Эти небольшие секретируемые молекулы относятся к растущему суперсемейству белков массой 8-14 кДа, характеризующихся консервативным мотивом из четырех цистеинов. Хемокиновое суперсемейство может быть разделено на две основные группы, имеющие характерные структурные мотивы: семейства Cys-X-Cys (C-X-C, или  ) и Cys-Cys (C-C, или ) и Cys-Cys (C-C, или  ). Их различают по вставке одной аминокислоты между ближайшей к NH парой цистеиновых остатков и сходству последовательностей. ). Их различают по вставке одной аминокислоты между ближайшей к NH парой цистеиновых остатков и сходству последовательностей.
Хемокины C-X-C включают несколько мощных хемоаттрактантов и активаторов нейтрофилов, таких как интерлейкин-8 (IL-8) и нейтрофил-активирующий пептид 2 (NAP-2).
Хемокины С-С включают мощные хемоаттрактанты моноцитов и лимфоцитов, но не нейтрофилов, такие как хемотаксические белки моноцитов 1-3 человека (МСР-1, МСР-2 и МСР-3), RANTES (регулируемый при активации, экспрессируемый и секретируемый нормальными Т-клетками), эотаксин и воспалительные белки макрофагов 1 и 1 и 1 (MIP-1 (MIP-1 и MIP-1 и MIP-1 ). ).
Исследования продемонстрировали, что действия хемокинов опосредованы подсемействами сопряженных с G-белком рецепторов, среди которых находятся рецепторы, обозначенные CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3 и CXCR4. Эти рецепторы представляют собой хорошие мишени для разработки лекарственных средств, поскольку агенты, модулирующие эти рецепторы, будут полезны в лечении расстройств и заболеваний, таких как расстройства и заболевания, упомянутые выше.
Рецептор CCR5 экспрессируется на Т-лимфоцитах, моноцитах, макрофагах, дендритных клетках, микроглии и других типах клеток. Они обнаруживают и реагируют на несколько хемокинов, в основном на “регулируемый при активации, экспрессируемый и секретируемый нормальными Т-клетками” (RANTES), воспалительные белки макрофагов (MIP) MIP-1 и MIP-1 и MIP-1 и белок-хемоаттрактант моноцитов 2 (МСР-2). и белок-хемоаттрактант моноцитов 2 (МСР-2).
В результате происходит рекрутинг клеток иммунной системы в сайты заболевания. При многих заболеваниях этими клетками являются клетки, экспрессирующие CCR5, которые прямо или опосредованно вносят вклад в повреждение тканей. Следовательно, ингибирование рекрутинга этих клеток полезно при широком диапазоне заболеваний.
CCR5 также представляет собой корецептор для ВИЧ-1 (вирус иммунодефицита человека 1) и других вирусов, давая этим вирусам возможность проникать в клетки. Блокирование рецептора антагонистом CCR5 или индуцирование интернализации рецептора агонистом CCR5 защищает клетки от вирусной инфекции.
Согласно настоящему изобретению предложено соединение формулы (I):
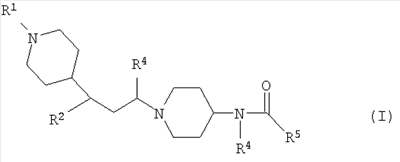
где
R1 представляет собой S(O)2R6, S(O)2NR10R11, C(O)R7 или C(O)NHR7;
R2 представляет собой 3,5-дифторфенил, 3-трифторметилфенил или 3-фтор-5-хлорфенил;
R3 представляет собой водород или С1-4алкил;
R4 представляет собой водород, метил, этил, аллил или циклопропил;
R5 представляет собой фенил(С1-2)алкил или фенил(С1-2алкил)NH, где фенильные кольца возможно замещены галогено, циано, нитро, гидрокси, С1-4алкилом, С1-4алкокси, группой S(O)k(С1-4алкил), S(O)2NR8R9, группой NHS(O)2(С1-4алкил), NH2, группой NH(С1-4алкил), группой N(С1-4алкил)2, NHC(O)NH2, C(O)NH2, группой С(O)NH(С1-4алкил), группой С(O)N(С1-4алкил)2, группой NHC(O)(С1-4алкил), СО2Н, группой CO2(С1-4алкил), группой C(O)(С1-4алкил), CF3, CHF2, CH2F, CH2CF3 или OCF3;
k означает 0, 1 или 2;
R6 представляет собой C1-6алкил [возможно замещенный С1-4алкокси, фенилом {который сам возможно замещен галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, OCF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)} или гетероарилом {который сам возможно замещен галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(C1-4алкил) или группой S(O)2(С1-4алкил)}], С3-7циклоалкил, тетрагидропиранил, фенил {возможно замещенный галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, OCF3, группой (С1-4алкил)C(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)} или гетероарил {возможно замещенный галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)};
R7 представляет собой водород, C1-6алкил [возможно замещенный галогено (например фторо), С1-4алкокси, фенилом {который сам возможно замещен галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, OCF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)} или гетероарилом {который сам возможно замещен галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)}], С3-7циклоалкил, тетрагидропиранил, фенил {возможно замещенный галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, OCF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)} или гетероарил {возможно замещенный галогено, С1-4алкилом, С1-4алкокси, циано, нитро, CF3, группой (С1-4алкил)С(O)NH, S(O)2NH2, С1-4алкилтио, группой S(O)(С1-4алкил) или группой S(O)2(С1-4алкил)};
R8 и R9 независимо представляют собой водород или С1-4алкил, или вместе с атомом азота или кислорода могут быть связаны с образованием 5- или 6-членного кольца, которое возможно замещено С1-4алкилом, С(O)Н или группой С(O)(С1-4алкил);
R10 и R11 независимо представляют собой водород или С1-4алкил, или могут быть связаны с образованием 5- или 6-членного кольца, которое возможно замещено С1-4алкилом или фенилом (где фенильное кольцо возможно замещено галогено, циано, нитро, гидрокси, С1-4алкилом, С1-4алкокси, группой S(O)mC1-4алкил, S(O)2NH2, группой S(O)2NH(С1-4алкил), группой S(O)2N(С1-4алкил)2, группой NHS(O)2(С1-4алкил), NH2, группой NH(С1-4алкил), группой N(С1-4алкил)2, NHC(O)NH2, C(O)NH2, группой С(O)NH(С1-4алкил), группой NHC(O)(С1-4алкил), CO2H, группой CO2(С1-4алкил), группой C(O)(С1-4алкил), CF3, CHF2, CH2F, CH2CF3 или OCF3);
или его фармацевтически приемлемая соль.
Некоторые соединения по настоящему изобретению могут существовать в различных изомерных формах (таких как энантиомеры, диастереоизомеры, геометрические изомеры или таутомеры). Настоящее изобретение охватывает все такие изомеры и их смеси во всех соотношениях.
Подходящие соли включают соли присоединения кислоты, такие как гидрохлорид, гидробромид, фосфат, ацетат, фумарат, малеат, сукцинат, тартрат, цитрат, оксалат, метансульфонат или пара-толуолсульфонат.
Соединения по изобретению могут существовать в виде сольватов (например гидратов), и настоящее изобретение охватывает все такие сольваты.
Алкильные группы и группировки являются прямоцепочечными или разветвленными и представляют собой, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил или трет-бутил. Метил здесь иногда сокращен до Me.
Фторалкил включает, например, от одного до шести, например от одного до трех атомов фтора и включает, например, группу CF3. Фторалкил представляет собой, например, CHF2, CH2F, CF3 или CH2CF3.
Циклоалкил представляет собой, например, циклопропил, циклопентил или циклогексил.
Фенил(С1-2алкил)алкил представляет собой, например, бензил, 1-(фенил)эт-1-ил или 1-(фенил)эт-2-ил.
Фенил(С1-2алкил)NH представляет собой, например, бензиламино.
Гетероарил представляет собой ароматическое 5- или 6-членное кольцо, возможно конденсированное с одним или более чем одним другим кольцом, содержащее по меньшей мере один гетероатом, выбранный из группы, включающей в себя азот, кислород и серу; или его N-оксид, или его S-оксид, или S-диоксид. Гетероарил представляет собой, например, фурил, тиенил (также известный как тиофенил), пирролил, тиазолил, изотиазолил, пиразолил, оксазолил, изоксазолил, имидазолил, [1,2,4]-триазолил, пиридинил, пиримидинил, индолил, бензо[b]фурил (также известный как бензофурил), бензо[b]тиенил (также известный как бензотиенил или бензотиофенил), индазолил, бензимидазолил, бензотриазолил, бензоксазолил, бензотиазолил, 1,2,3-бензотиадиазолил, имидазопиридинил (такой как имидазо[1,2а]пиридинил), тиено[3,2-b]пиридин-6-ил, 1,2,3-бензоксадиазолил (также известный как бензо[1,2,3]тиадиазолил), 2,1,3-бензотиадиазолил, бензофуразан (также известный как 2,1,3-бензоксадиазолил), хиноксалинил, пиразолопиридин (например, 1H-пиразоло[3,4-b]пиридинил), хинолинил, изохинолинил, нафтиридинил (например, [1,6]нафтиридинил или [1,8]нафтиридинил), бензотиазинил или дибензотиофенил (также известный как дибензотиенил); или его N-оксид, или его S-оксид, или S-диоксид. Гетероарил также может представлять собой пиразинил. Гетероарил представляет собой, например, пиридинил, пиримидинил, индолил или бензимидазолил.
Когда R8 и R9 вместе с атомом азота или кислорода связаны с образованием 5- или 6-членного кольца, тогда указанное кольцо представляет собой, например, пиперазинильное или морфолинильное кольцо.
Когда R10 и R11 связаны с образованием 5- или 6-членного кольца, тогда это образованное кольцо представляет собой, например, пиперинильное кольцо.
В одном из конкретных аспектов настоящего изобретения предложено соединение по изобретению, где R6 представляет собой C1-6алкил (например, С1-4алкил, такой как метил) или С3-7циклоалкил (такой как циклогексил).
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R1 представляет собой S(O)2R6, где R6 такой, как определено выше (например, R6 представляет собой С1-4алкил). Например, R1 представляет собой S(O)2СН3.
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R2 представляет собой 3,5-дифторфенил.
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R3 представляет собой водород.
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R4 представляет собой этил или циклопропил. В еще одном аспекте настоящего изобретения предложено соединение формулы (I), где R4 представляет собой этил.
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R5 представляет собой фенил(С1-2)алкил (например, бензил) или фенил(С1-2алкил)NH (например, бензиламино), где фенильные кольца замещены (например, в пара-положении) группой S(O)2(С1-4алкил) (например, группой S(O)2СН3).
В еще одном аспекте настоящего изобретения предложено соединение по изобретению, где R5 представляет собой бензил, где фенильное кольцо замещено в пара-положении группой S(O)2(С1-4алкил) (например, группой S(O)2СН3).
В еще одном аспекте настоящего изобретения предложена фармацевтически приемлемая соль соединения по изобретению, например соль гидрохлорид, гидробромид, фосфат, ацетат, фумарат, малеат, сукцинат, тартрат, цитрат, оксалат, метансульфонат или пара-толуолсульфонат соединения по изобретению (например, соль фумарат или сукцинат).
Атом углерода, помеченный знаком ^ в представленной ниже формуле (I)
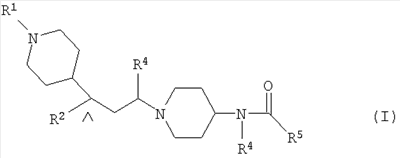
всегда является хиральным и имеет, например, абсолютную R-конфигурацию. Таким образом, в еще одном аспекте настоящего изобретения предложено соединение по изобретению, имеющее абсолютную R-конфигурацию по атому углерода ^, идентифицированному выше. В еще одном аспекте настоящего изобретения предложена фармацевтически приемлемая соль соединения по изобретению, имеющая абсолютную R-конфигурацию по атому углерода ^, идентифицированному выше.
В еще одном аспекте настоящего изобретения предложено соединение формулы (Ia)
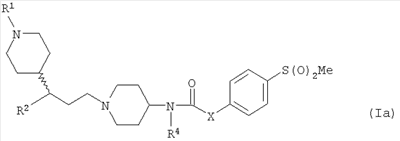
где R1, R2 и R4 такие, как определено выше, и Х представляет собой CH2 или NHCH2. В еще одном аспекте настоящего изобретения предложена фармацевтически приемлемая соль соединения формулы (Ia), где R1, R2 и R4 такие, как определено выше, и Х представляет собой CH2 или NHCH2.
В еще одном аспекте настоящего изобретения предложено соединение формулы (I), имеющее абсолютную R-конфигурацию по атому углерода ^, идентифицированному выше, где:
R1 представляет собой S(O)2R6 [где R6 такой, как определено выше (например, R6 представляет собой С1-4алкил, такой как метил)];
R2 представляет собой 3,5-дифторфенил;
R3 представляет собой водород;
R4 представляет собой этил или циклопропил [например, R4 представляет собой этил];
R5 представляет собой фенил(С1-2)алкил или фенил(С1-2алкил)NH, где фенильные кольца замещены (например, в пара-положении) группой S(O)2(С1-4алкил) (например, группой S(O)2СН3) [например, R5 представляет собой бензил, где фенильное кольцо замещено в пара-положении группой S(O)2(С1-4алкил) (например, группой S(O)2СН3)];
или фармацевтически приемлемая соль соединения формулы (I) [например, соль гидрохлорид, гидробромид, фосфат, ацетат, фумарат, малеат, сукцинат, тартрат, цитрат, оксалат, метансульфонат или пара-толуолсульфонат (например, соль фумарат или сукцинат)].
В еще одном аспекте настоящего изобретения предложено соединение формулы (Ia), имеющее абсолютную R-конфигурацию на идентифицированном выше атоме углерода ^, где:
R1 представляет собой S(O)2R6 [где R6 является таким, как определено выше (например, R6 представляет собой С1-4алкил, такой как метил)];
R2 представляет собой 3,5-дифторфенил;
R4 представляет собой этил или циклопропил [например, R4 представляет собой этил];
Х представляет собой СН2 или NHCH2 [например, Х представляет собой СН2];
или фармацевтически приемлемая соль соединения формулы (Ia) [например, соль гидрохлорид, гидробромид, фосфат, ацетат, фумарат, малеат, сукцинат, тартрат, цитрат, оксалат, метансульфонат или пара-толуолсульфонат (такая как соль фумарат или сукцинат)].
В еще одном аспекте настоящего изобретения предложено соединение:
N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамид;
соль сукцинат N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида;
соль фумарат N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида; или
N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[3-(метилсульфонил)фенил]ацетамид.
Соединения, перечисленные в Таблице I, иллюстрируют изобретение.
| ТАБЛИЦА I |
| Таблица I включает соединения формулы (Ia) |
 |
Соединение  |
Стереохимия |
R1 |
R2 |
R4 |
х |
| 1 |
R |
метансульфонил |
3,5-дифторфенил |
Этил |
СН2 |
| 2 |
R |
метансульфонил |
3,5-дифторфенил |
Этил |
NHCH2 |
| 3 |
R |
метансульфонил |
3-CF3-фенил |
Этил |
СН2 |
| 4 |
R |
метансульфонил |
3,5-дифторфенил |
циклопропил |
СН2 |
| 5 |
R |
метансульфонил |
3-фтор-5-хлорфенил |
Этил |
СН2 |
| 6 |
R |
метансульфонил |
3-фторфенил |
Этил |
СН2 |
В еще одном аспекте изобретения предложено каждое индивидуальное соединение, перечисленное в Таблице I.
Соединения по изобретению могут быть получены с использованием или модифицированием методик, способов, схем или примеров из WO 03/042205.
Таким образом, соединение по изобретению может быть получено путем взаимодействия соединения формулы (II):
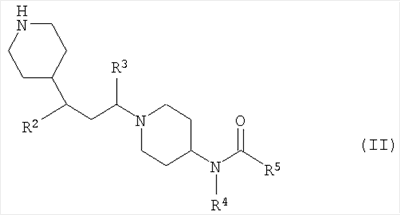
где R2, R3, R4 и R5 такие, как определено выше,
в зависимости от соединения по изобретению, которое желательно получить, в реакцию с:
а) кислотой формулы R1CO2H в присутствии подходящего агента сочетания (например, PyBrOP [бром-трис-пирролидинфосфония гексафторфосфат] или HATU [O-(7-азабензотриазол-1-ил)-N,N,N’,N’-тетраметилурония гексафторфосфат]) в присутствии подходящего основания (такого как три(С1-6алкил)амин, например, диизопропилэтиламин) в подходящем растворителе (например, N-метилпирролидиноне или хлорированном растворителе, таком как дихлорметан) при комнатной температуре (например, 10-30°С); или
б) хлорангидридом формулы R1C(O)Cl или сульфонилхлоридом формулы R1S(O)2Cl в присутствии подходящего основания (такого как а три(С1-6алкил)амин, например триэтиламин или диизопропилэтиламин) в подходящем растворителе (например, хлорированном растворителе, таком как дихлорметан) при комнатной температуре (например, 10-30°С).
Альтернативно соединение по изобретению может быть получено путем сочетания соединения формулы (III):
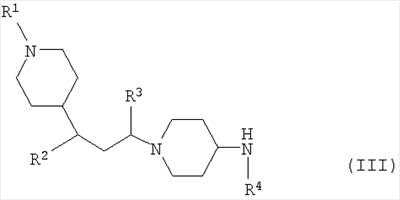
где R1, R2, R3 и R4 такие, как определено выше, с:
а) кислотой формулы R5CO2H в присутствии подходящего агента сочетания (например, PyBrOP или HATU) в присутствии подходящего основания (такого как три(С1-6алкил)амин, например, диизопропилэтиламин) в подходящем растворителе (например, N-метилпирролидиноне или хлорированном растворителе, таком как дихлорметан) при комнатной температуре (например, 10-30°С); или
б) хлорангидридом формулы R5C(O)Cl в присутствии подходящего основания (такого как три(С1-6алкил)амин, например, триэтиламин или диизопропилэтиламин), в подходящем растворителе (например, хлорированном растворителе, таком как дихлорметан) при комнатной температуре (например, 10-30°С).
Соединение по изобретению может быть получено путем восстановительного аминирования соединения формулы (IV):
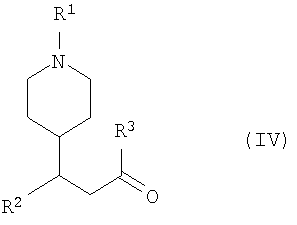
соединением формулы (V):
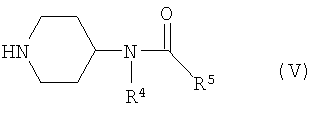
в присутствии NaBH(OAc)3 (где Ас представляет собой С(О)СН3) и уксусной кислоты в подходящем растворителе (таком как C1-6алифатический спирт, например, этанол) при комнатной температуре (например, 10-30°С).
Соединение формулы (V) может быть получено путем удаления защитной группы (PG) из соединения формулы (VI). Например, когда PG представляет собой бензилоксилкарбонил или бензил, удаление может быть осуществлено путем гидрирования (например, водородом в присутствии катализатора палладий на углероде); когда PG представляет собой трет-бутилоксикарбонил, удаление может быть осуществлено путем обработки кислотой (такой как соляная кислота или трифторуксусная кислота)
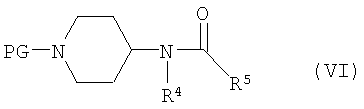
Соединение по изобретению также может быть получено путем алкилирования соединения формулы (V) соединением формулы (VII):
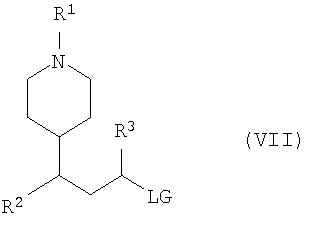
где R1, R2 и R3 такие, как определено выше, и IG представляет собой уходящую группу (такую как галогенид, мезилат, тозилат или трифлат), в присутствии подходящего основания (такого как карбонат калия или третичный амин (например, основание Хюнига или триэтиламин)) в подходящем растворителе (таком как ацетонитрил или тетрагидрофуран (ТГФ)) при комнатной температуре (например, 10-30°С). Соединения формулы (VII) могут быть получены способами, описанными в патентной или научной литературе, либо рутинным адаптированием этих способов.
В описанных способах подходящие защитные группы и подробности способов добавления и удаления таких групп можно найти в “Protective Groups in Organic Synthesis”, 3rd Edition (1999) by Greene and Wuts.
Исходные вещества для этих способов имеются в продаже или могут быть получены известными из литературы способами, адаптированием известных из литературы способов или в соответствии с описанием WO 03/042205.
В еще одном аспекте изобретения предложены способы получения соединений формулы (I) или (Ia). Многие промежуточные соединения в этих способах являются новыми и предложены в качестве дополнительных аспектов изобретения.
Соединение по изобретению, или его фармацевтически приемлемая соль, может быть использовано в лечении следующих заболеваний:
1) дыхательные пути: обструктивные заболевания дыхательных путей, включая астму, в том числе бронхиальную, аллергическую, эндогенную, экзогенную, вызванную физической нагрузкой, вызванную лекарствами (включая аспирин и нестероидные противовоспалительные средства (NSAID)) и вызванную пылью астму, как перемежающуюся, так и постоянную и всех степеней тяжести, и другие причины гипереактивности дыхательных путей; хроническое обструктивное заболевание легких (ХОЗЛ); бронхит, включая инфекционный и эозинофильный бронхит; эмфизема; бронхоэктаз; кистозный фиброз; саркоидоз; легкого “фермера” и родственные заболевания; гиперчувствительный пневмонит; фиброз легкого, включая эндогенный фиброзный альвеолит, идиопатические интерстициальные пневмонии, фиброз, осложняющий противоопухолевую терапию и хроническую инфекцию, в том числе туберкулез и аспергиллез и другие грибковые инфекции; осложнения после трансплантации легкого; васкулитные и тромботические расстройства сосудистой сети легкого и легочная гипертензия; противокашлевая активность, включая лечение хронического кашля, ассоциированного с воспалительными и секреторными состояниями дыхательных путей, и ятрогенного кашля; острый и хронический ринит, включая медикаментозный ринит и вазомоторный ринит; круглогодичный и сезонный аллергический ринит, включая нервный ринит (сенная лихорадка); назальный полипоз; острая вирусная инфекция, включая простуду, и инфекция, вызванная респираторно-синцитиальным вирусом, вирусом гриппа, коронавирусом (в том числе SARS (вирус атипичной пневмонии)) и аденовирусом;
2) кости и суставы: кожные высыпания, ревматического или подагрического происхождения, связанные с остеоартритом/остеоартрозом или включающие остеоартрит/остеоартроз, как первичные, так и вторичные по отношению к, например, врожденной дисплазии бедра; шейный и поясничный спондилит, и боль в спине, и боль в шее; ревматоидный артрит и болезнь Стилла; серонегативные спондилоартропатии, включая анкилозирующий спондилоартрит, псориатический артрит, реактивный артрит и недифференцированную спондилоартропатию; септический артрит и другие инфекционные артропатии и костные расстройства, такие как туберкулез, включая болезнь Потта и синдром Понке; острый и хронический синовит, вызванный кристаллами, включая уратную подагру, болезнь, связанную с отложениями пирофосфата кальция, и воспаление сухожилия, сумки и синовиального воспаления, связанное с отложениями кальциевого апатита; болезнь Бехчета; первичный и вторичный синдром Шегрена; системный склероз и ограниченная склеродерма; системная красная волчанка, смешанное заболевание соединительной ткани, и недифференцированное заболевание соединительной ткани; воспалительные миопатии, включая дерматомиозит и полимиозит; ревматическая полимиалгия; ювенильный артрит, включая идиопатические кожные высыпания ревматического или подагрического происхождения любой зоны иннервации сустава и ассоциированные синдромы, и ревматизм и его системные осложнения; васкулитиды, включая гигантоклеточный артериит, синдром Такаясу, гранулематозный аллергический ангиит, нодозный полиартериит, микроскопический полиартериит, и васкулитиды, ассоциированные с вирусной инфекцией, реакциями гиперчувствительности, криоглобулинами и парапротеинами; поясничная боль; семейная средиземноморская лихорадка, синдром Макла-Уэльса и семейная ирландская лихорадка, болезнь Кикучи; вызванные лекарствами артралгии, тендониты и миопатии;
3) боль и ремоделирование соединительной ткани при скелетно-мышечных расстройствах вследствие травмы [например, спортивной травмы] или заболевания: кожные высыпания ревматического или подагрического происхождения (например, ревматоидный артрит, остеоартрит, подагра или кристаллическая артропатия), другие заболевания суставов (такие как дегенерация межпозвоночного диска или дегенерация височно-нижнечелюстного сустава), ремоделирование кости (например, остеопороз, болезнь Педжета или остеонекроз), полихондрит, склеродерма, смешанное расстройство соединительной ткани, спондилоартропатии или периодонтальное заболевание (например, периодонтит);
4) кожа: псориаз, атопический дерматит, контактный дерматит или другие экзематозные дерматозы, и реакции гиперчувствительности отложенного типа; фито- и фотодерматит; себоррейный дерматит, герпетиформный дерматит, плоский лишай, склерозирующий и атрофический лишай, гангренозная пиодерма, кожный саркоид, дискоидная красная волчанка, пемфигус, пемфигоид, врожденный буллезный эпидермолиз, крапивница, отек Квинке, васкулитиды, токсические эритемы, кожная эозинофилия, гнездная алопеция, мужская алопеция, синдром Свита, синдром Вебера-Кристиана, полиморфная эритема; инфекционный и неинфекционный целлюлит; панникулит; кожные лимфомы, немеланомный рак кожи и другие диспластические поражения; вызванных лекарствами расстройства, включая локальные лекарственные сыпи;
5) глаза: блефарит; конъюнктивит, включая хронический и весенний аллергический конъюнктивит; ирит; ранний и поздний увеит; хориоидит; аутоиммунное заболевание; дегенеративные или воспалительные расстройства, поражающие сетчатку; офтальмит, включая симпатический офтальмит; саркоидоз; инфекции, в том числе вирусные, грибковые и бактериальные инфекции;
6) желудочно-кишечный тракт: глоссит, гингивит, периодонтит; эзофагит, включая рефлюкс; эозинофильный гастроэнтерит, мастоцитоз, болезнь Крона, колит, в том числе неспецифический язвенный колит, проктит, анальный зуд; заболевание брюшной полости, синдром раздраженной толстой кишки и пищевые аллергии, которые могут оказывать воздействие далеко от кишки (например, мигрень, ринит или экзема);
7) абдоминальные: гепатит, включая аутоиммунный, алкогольный и вирусный гепатит; фиброз и цирроз печени; холецистит; острый и хронический панкреатит;
8) мочеполовые: нефрит, включая интерстициальный и гломерулонефрит; нефротический синдром; цистит, включая острый и хронический (интерстициальный) цистит и язву Ханнера; острый и хронический уретрит, простатит, эпидидимита, оофорит и сальпингит; вульвовагинит; болезнь Пейрони; эректильная дисфункция (как у мужчин, так и у женщин);
9) отторжение трансплантата: острое и хроническое после трансплантации, например почки, сердца, печени, легкого, костного мозга, кожи или роговицы либо после переливания крови; или хроническое заболевание “трансплантат против хозяина”;
10) ЦНС: болезнь Альцгеймера и другие, приводящие к слабоумию расстройства, включая болезнь Кройцфельдта Якоба (CJD) и новый вариант болезни Кройцфельдта Якоба (nvCJD); амилоидоз; рассеянный склероз и другие демиелинизирующие синдромы; церебральный атеросклероз и васкулит; височный артериит; астенический бульбарный паралич; острая и хроническая боль (острая, перемежающаяся или постоянная, центрального или периферического происхождения), в том числе висцеральная боль, головная боль, мигрень, тригеминальная невралгия, атипичная лицевая боль, боль в суставах и костях, боль, возникающая из-за рака и инвазии опухоли, невропатические болевые синдромы, в том числе диабетические, постгерпетические и ВИЧ-ассоциированные невропатии; нейросаркоидоз; осложнений злокачественных, инфекционных или аутоиммунных процессов на центральную и периферическую нервную систему;
11) другие аутоиммунные и аллергические расстройства, включая тиреоидит Хашимото, диффузный токсический зоб, болезнь Аддисона, сахарный диабет, идиопатическая тромбоцитопеническая пурпура, эозинофильный фасциит, гипер-IgE синдром, антифосфолипидный синдром;
12) другие расстройства с воспалительным или иммунологическим компонентом, в том числе синдром приобретенного иммунодефицита (СПИД), лепра, синдром Сезари и паранеопластические синдромы;
13) сердечно-сосудистая система: атеросклероз, поражающий коронарное и периферическое кровообращение; перикардит; миокардит, воспалительные и аутоиммунные кардиомиопатии, в том числе миокардиальный саркоидоз; ишемические реперфузионные повреждения; эндокардит, вальвулит и аортит, в том числе инфекционный (например, сифилитический) аортит; васкулитиды; расстройства проксимальных и периферических вен, включая флебит и тромбоз, в том числе тромбоз глубоких вен и осложнения варикозного расширения вен;
14) онкология: лечение распространенных видов рака, в том числе опухолей предстательной железы, молочной железы, легкого, яичника, поджелудочной железы, кишечника и ободочной кишки, желудка, кожи и головного мозга и злокачественностей, поражающих костный мозг (включая лейкемии) и лимфопролиферативные системы, такие как ходжкинская и неходжкинская лимфомы, включающее предупреждение и лечение метастазирования и рецидивов опухолей, и паранеопластических синдромов; или
15) желудочно-кишечный тракт: заболевание брюшной полости, проктит, эозинофильный гастроэнтерит, мастоцитоз, болезнь Крона, неспецифический язвенный колит, микроскопический колит, перемежающийся колит, расстройство раздраженной кишки, синдрома раздраженной кишки, невоспалительная диарея, пищевые аллергии, которые оказывают воздействие далеко от кишки, например мигрень, ринит и экзема;
у теплокровного животного, такого как человек.
Соединения по изобретению обладают активностью как фармацевтические препараты, в частности как модуляторы (такие как агонисты, частичные агонисты, обратные агонисты или антагонисты) активности хемокиновых рецепторов (например CCR5), и могут быть использованы в лечении аутоиммунных, воспалительных, пролиферативных или гиперпролиферативных заболеваний, или заболеваний, опосредованных иммунной системой (включая отторжение трансплантированных органов или тканей и синдром приобретенного иммунодефицита (СПИД)).
Соединения по настоящему изобретению также полезны в ингибировании проникания вирусов (таких как вирус иммунодефицита человека (ВИЧ)) в клетки-мишени и, таким образом, полезны для профилактики инфицирования вирусами (такими как ВИЧ), лечении вирусной инфекции (такой как ВИЧ) и профилактик и/или лечения синдрома приобретенного иммунодефицита (СПИД).
Согласно изобретению предложены соединение формулы (I) или (Ia) или его фармацевтически приемлемая соль для применения в способе лечения теплокровного животного (например, человека) терапией (включая профилактику).
Согласно настоящему изобретению предложен способ модулирования активности хемокинового рецептора (например, активности рецептора CCR5) у теплокровного животного, например человека, нуждающегося в таком лечении, включающий введение указанному животному эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли.
Согласно настоящему изобретению также предложено применение соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли в качестве лекарственного средства, например лекарственного средства для лечения отторжения трансплантата, респираторного заболевания, псориаза или ревматоидного артрита (например, ревматоидного артрита). [Респираторное заболевание представляет собой, например, ХОЗЛ, астму {такую как бронхиальная, аллергическая, эндогенная, экзогенная или пылевая астма, в частности хроническая или застарелая астма (например поздняя астма или гиперреактивность дыхательных путей)} или ринит {острый, аллергический, атрофический ринит или хронический ринит, включая казеозный хронический ринит, хронический гипертрофический ринит, гнойный ринит, сухой ринит или медикаментозный ринит; пленчатый ринит, в том числе крупозный, фибринозный или псевдопленчатый ринит или скрофулезный ринит; сезонный ринит, в том числе нервный ринит (сенная лихорадка) или вазомоторный ринит}; и в частности астму или ринит].
В еще одном аспекте настоящего изобретения предложено применение соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли в изготовлении лекарственного средства для использования в терапии (например, модулировании активности хемокиновых рецепторов (например, активности рецептора CCR5 (например, ревматоидного артрита)) у теплокровного животного, например человека).
Согласно изобретению также предложены соединение формулы (I) или (Ia) или его фармацевтически приемлемая соль для применения в качестве лекарственного средства, например лекарственного средства для лечения ревматоидного артрита.
В еще одном аспекте настоящего изобретения предложены применение соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли в изготовлении лекарственного средства для использования в терапии (например, модулировании активности хемокиновых рецепторов (например, активности рецептора CCR5 (например ревматоидного артрита)) у теплокровного животного, например человека).
Согласно изобретению также предложено применение соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли в изготовлении лекарственного средства для применения в лечении следующий заболеваний:
1) дыхательные пути: обструктивные заболевания дыхательных путей, включая астму, в том числе бронхиальную, аллергическую, эндогенную, экзогенную, вызванную физической нагрузкой, вызванную лекарствами (включая аспирин и нестероидные противовоспалительные лекарства (NSAID)) и вызванную пылью астму как перемежающуюся, так и постоянную и всех степеней тяжести, и другие причины гипереактивности дыхательных путей; хроническое обструктивное заболевание легких (ХОЗЛ); бронхит, включая инфекционный и эозинофильный бронхит; эмфизема; бронхоэктаз; кистозный фиброз; саркоидоз; легкого “фермера” и родственные заболевания; гиперчувствительный пневмонит; фиброз легкого, включая эндогенный фиброзный альвеолит, идиопатические интерстициальные пневмонии, фиброз, осложняющий противоопухолевую терапию и хроническую инфекцию, в том числе туберкулез и аспергиллез и другие грибковые инфекции; осложнения после трансплантации легкого; васкулитные и тромботические расстройства сосудистой сети легкого и легочная гипертензия; противокашлевая активность, включая лечение хронического кашля, ассоциированного с воспалительными и секреторными состояниями дыхательных путей, и ятрогенного кашля; острый и хронический ринит, включая медикаментозный ринит и вазомоторный ринит; круглогодичный и сезонный аллергический ринит, включая нервный ринит (сенная лихорадка); назальный полипоз; острая вирусная инфекция, включая простуду, и инфекция, вызванная респираторно-синцитиальным вирусом, вирусом гриппа, коронавирусом (в том числе SARS (вирус атипичной пневмонии)) и аденовирусом;
2) кости и суставы: кожные высыпания ревматического или подагрического происхождения, связанные с остеоартритом/остеоартрозом или включающие остеоартрит/остеоартроз как первичные, так и вторичные по отношению к, например, врожденной дисплазии бедра; шейный и поясничный спондилит, боль в спине и боль в шее; ревматоидный артрит и болезнь Стилла; серонегативные спондилоартропатии, включая анкилозирующий спондилоартрит, псориатический артрит, реактивный артрит и недифференцированную спондилоартропатию; септический артрит и другие инфекционные артропатии и костные расстройства, такие как туберкулез, включая болезнь Потта и синдром Понке; острый и хронический синовит, вызванный кристаллами, включая уратную подагру, болезнь, связанную с отложениями пирофосфата кальция, и воспаление сухожилия, сумки и синовиального воспаления, связанное с отложениями кальциевого апатита; болезнь Бехчета; первичный и вторичный синдром Шегрена; системный склероз и ограниченная склеродерма; системная красная волчанка, смешанное заболевание соединительной ткани, и недифференцированное заболевание соединительной ткани; воспалительные миопатии, включая дерматомиозит и полимиозит; ревматическая полимиалгия; ювенильный артрит, включая идиопатические кожные высыпания ревматического или подагрического происхождения любой зоны иннервации сустава и ассоциированные синдромы, и ревматизм и его системные осложнения; васкулитиды, включая гигантоклеточный артериит, синдром Такаясу, гранулематозный аллергический ангиит, нодозный полиартериит, микроскопический полиартериит, и васкулитиды, ассоциированные с вирусной инфекцией, реакциями гиперчувствительности, криоглобулинами и парапротеинами; поясничная боль; семейная средиземноморская лихорадка, синдром Макла-Уэльса и семейная ирландская лихорадка, болезнь Кикучи; вызванные лекарствами артралгии, тендониты и миопатии;
3) боль и ремоделирование соединительной ткани при скелетно-мышечных расстройствах вследствие травмы [например, спортивной травмы] или заболевания: кожные высыпания ревматического или подагрического происхождения (например, ревматоидный артрит, остеоартрит, подагра или кристаллическая артропатия), другие заболевания суставов (такие как дегенерация межпозвоночного диска или дегенерация височно-нижнечелюстного сустава), ремоделирование кости (например, остеопороз, болезнь Педжета или остеонекроз), полихондрит, склеродерма, смешанное расстройство соединительной ткани, спондилоартропатии или периодонтальное заболевание (например, периодонтит);
4) кожа: псориаз, атопический дерматит, контактный дерматит или другие экзематозные дерматозы, и реакции гиперчувствительности отложенного типа; фито- и фотодерматит; себоррейный дерматит, герпетиформный дерматит, плоский лишай, склерозирующий и атрофический лишай, гангренозная пиодерма, кожный саркоид, дискоидная красная волчанка, пемфигус, пемфигоид, врожденный буллезный эпидермолиз, крапивница, отек Квинке, васкулитиды, токсические эритемы, кожная эозинофилия, гнездная алопеция, мужская алопеция, синдром Свита, синдром Вебера-Кристиана, полиморфная эритема; инфекционный и неинфекционный целлюлит; панникулит; кожные лимфомы, немеланомный рак кожи и другие диспластические поражения; вызванных лекарствами расстройства, включая локальные лекарственные сыпи;
5) глаза: блефарит; конъюнктивит, включая хронический и весенний аллергический конъюнктивит; ирит; ранний и поздний увеит; хориоидит; аутоиммунное заболевание; дегенеративные или воспалительные расстройства, поражающие сетчатку; офтальмит, включая симпатический офтальмит; саркоидоз; инфекции, в том числе вирусные, грибковые и бактериальные инфекции;
6) желудочно-кишечный тракт: глоссит, гингивит, периодонтит; эзофагит, включая рефлюкс; эозинофильный гастроэнтерит, мастоцитоз, болезнь Крона, колит, в том числе неспецифический язвенный колит, проктит, анальный зуд; заболевание брюшной полости, синдром раздраженной толстой кишки и пищевые аллергии, которые могут оказывать воздействие далеко от кишки (например, мигрень, ринит или экзема);
7) абдоминальные: гепатит, включая аутоиммунный, алкогольный и вирусный гепатит; фиброз и цирроз печени; холецистит; острый и хронический панкреатит;
8) мочеполовые: нефрит, включая интерстициальный и гломерулонефрит; нефротический синдром; цистит, включая острый и хронический (интерстициальный) цистит и язву Ханнера; острый и хронический уретрит, простатит, эпидидимита, оофорит и сальпингит; вульво-вагинит; болезнь Пейрони; эректильная дисфункция (как у мужчин, так и у женщин);
9) отторжение трансплантата: острое и хроническое после трансплантации, например почки, сердца, печени, легкого, костного мозга, кожи или роговицы либо после переливания крови; или хроническое заболевание “трансплантат против хозяина”;
10) ЦНС: болезнь Альцгеймера и другие приводящие к слабоумию расстройства, включая болезнь Кройцфельдта Якоба (CJD) и новый вариант болезни Кройцфельдта Якоба (nvCJD); амилоидоз; рассеянный склероз и другие демиелинизирующие синдромы; церебральный атеросклероз и васкулит; височный артериит; астенический бульбарный паралич; острая и хроническая боль (острая, перемежающаяся или постоянная, центрального или периферического происхождения), в том числе висцеральная боль, головная боль, мигрень, тригеминальная невралгия, атипичная лицевая боль, боль в суставах и костях, боль, возникающая из-за рака и инвазии опухоли, невропатические болевые синдромы, в том числе диабетические, постгерпетические и ВИЧ-ассоциированные невропатии; нейросаркоидоз; осложнения злокачественных, инфекционных или аутоиммунных процессов на центральную и периферическую нервную систему;
11) другие аутоиммунные и аллергические расстройства, включая тиреоидит Хашимото, диффузный токсический зоб, болезнь Аддисона, сахарный диабет, идиопатическая тромбоцитопеническая пурпура, эозинофильный фасциит, гипер-IgE синдром, антифосфолипидный синдром;
12) другие расстройства с воспалительным или иммунологическим компонентом, в том числе синдром приобретенного иммунодефицита (СПИД), лепра, синдром Сезари и паранеопластические синдромы;
13) сердечно-сосудистая система: атеросклероз, поражающий коронарное и периферическое кровообращение; перикардит; миокардит, воспалительные и аутоиммунные кардиомиопатии, в том числе миокардиальный саркоидоз; ишемические реперфузионные повреждения; эндокардит, вальвулит и аортит, в том числе инфекционный (например, сифилитический) аортит; васкулитиды; расстройства проксимальных и периферических вен, включая флебит и тромбоз, в том числе тромбоз глубоких вен и осложнения варикозного расширения вен;
14) онкология: лечение распространенных видов рака, в том числе опухолей предстательной железы, молочной железы, легкого, яичника, поджелудочной железы, кишечника и ободочной кишки, желудка, кожи и головного мозга и злокачественностей, поражающих костный мозг (включая лейкемии) и лимфопролиферативные системы, такие как ходжкинская и неходжкинская лимфомы, включающее предупреждение и лечение метастазирования и рецидивов опухолей, и паранеопластических синдромов; или
15) желудочно-кишечный тракт: заболевание брюшной полости, проктит, эозинофильный гастроэнтерит, мастоцитоз, болезнь Крона, неспецифический язвенный колит, микроскопический колит, перемежающийся колит, расстройство раздраженной кишки, синдрома раздраженной кишки, невоспалительная диарея, пищевые аллергии, которые оказывают воздействие далеко от кишки, например мигрень, ринит и экзема; у теплокровного животного, такого как человек.
В еще одном аспекте изобретения также предложено применение соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли в изготовлении лекарственного средства для применения в лечении:
1) (респираторный тракт) обструктивных заболеваний дыхательных путей, включая хроническое обструктивное заболевание легких (ХОЗЛ) (такое как необратимое ХОЗЛ); астмы {такой как бронхиальная, аллергическая, эндогенная, экзогенная или пылевая астма, в частности хроническая или застарелая астма (например, поздняя астма или гиперреактивность дыхательных путей)}; бронхита {такого как эозинофильный бронхит}; острого, аллергического, атрофического ринита или хронического ринита, включая казеозный ринит, гипертрофический ринит, гнойный ринит, сухой ринит или медикаментозный ринит; пленчатый ринит, включая крупозный, фибринозный или псевдопленчатый ринит или скрофулезный ринит; сезонный ринит, включая нервный ринит (сенная лихорадка) или вазомоторный ринит}; саркоидоза; заболевания легкого “фермера” и родственных заболеваний; назального полипоза; пневмосклероза или идиопатической интерстициальной пневмонии;
2) (кости и суставы) артритов, включая ревматические, инфекционные, аутоиммунные, серонегативных спондилоартропатий (таких, как анкилозирующий спондилоартрит, псориатический артрит или болезнь Рейтера), болезни Бехчета, синдрома Шегрена или системного склероза;
3) (кожа и глаза) псориаза, атопического дерматита, контактного дерматита или других экзематозных дерматитов, себоррейного дерматита, плоского лишая, пузырчатки, буллезного пемфигоида, врожденного буллезного эпидермолиза, крапивницы, ангиобластов, эритемных васкулитидов, кожных эозинофилий, увеита, гнездной алопеции или весеннего конъюнктивита;
4) (желудочно-кишечный тракт) заболеваний брюшной полости, проктита, эозинофильного гастроэнтерита, мастоцитоза, болезни Крона, неспецифического язвенного колита, воспалительного заболевания кишечника или пищевых аллергий, которые оказывают далеко от кишечника (например, мигрени, ринита и экземы);
5) (отторжение трансплантата) острого и хронического, например после трансплантации почки, сердца, печени, легкого, костного мозга, кожи или роговицы; или хронического заболевания “трансплантат против хозяина”; и/или
6) (другие ткани или заболевания) болезни Альцгеймера, рассеянного склероза, атеросклероза, синдрома приобретенного иммунодефицита (СПИД), волчанки (такой, как системная красная волчанка или системная волчанка), эритематоза, тиреоидита Хашимото, тяжелой миастении, сахарного диабета типа I, нефротического синдрома, эозинофильного фасцита, гипер-IgE синдрома, лепры (такой как лепроматозная лепра), периодонтального заболевания, синдрома Сезари, идиопатической тромбоцитопенической пурпуры или расстройств менструального цикла;
у теплокровного животного, такого как человек.
Согласно настоящему изобретению предложен также способ лечения болезненного состояния, опосредованного хемокинами (например, болезненного состояния, опосредованного CCR5) у теплокровного животного, например человека, включающему введение млекопитающему, нуждающемуся в таком лечении, эффективного количества соединения формулы (I) или (Ia) или его фармацевтически приемлемой соли.
Для применения соединения по изобретению или его фармацевтически приемлемой соли для терапевтического лечения теплокровного животного, например человека, в частности для модулирования активности хемокиновых рецепторов (например, рецептора CCR5), в соответствии со стандартной фармацевтической практикой обычно готовят препарат указанного ингредиента в виде фармацевтической композиции.
Таким образом, в еще одном аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая соединение формулы (I) или (Ia) или его фармацевтически приемлемую соль (активный ингредиент) и фармацевтически приемлемый адъювант, разбавитель или носитель. В еще одном аспекте настоящего изобретения предложен способ приготовления указанной композиции, включающий смешивание активного ингредиента с фармацевтически приемлемым адъювантом, разбавителем или носителем. В зависимости от способа введения фармацевтическая композиция должна содержать от 0,05 до 99 масс.% (массовых процентов), например от 0,05 до 80 масс.%, например от 0,10 до 70 масс.% (например от 0,10 до 50 масс.%) активного ингредиента, причем все массовые проценты даны в расчете на общую массу композиции.
Фармацевтические композиции по изобретению можно вводить стандартным для болезненного состояния, которое лечат, способом, например путем местного (такого как в легкое и/или дыхательные пути или на кожу), перорального, ректального или парентерального введения. Для этих целей могут быть приготовлены препараты соединений по изобретению способами, известными в данной области, в форме, например, аэрозолей, сухих порошковых препаратов, таблеток, капсул, сиропов, порошков, гранул, водных или масляных растворов или суспензий, (жидких) эмульсий, диспергируемых порошков, суппозиториев, мазей, кремов, капель и стерильных инъекционных водных или масляных растворов или суспензий.
Подходящая фармацевтическая композиция по изобретению представляет собой композицию, которая подходит для перорального введения в стандартной лекарственной форме, например в форме таблетки или капсулы, которая содержит от 0,1 мг до 1 г активного ингредиента.
В еще одном аспекте фармацевтическая композиция по изобретению представляет собой композицию, подходящую для внутривенной, подкожной или внутримышечной инъекции.
Каждый пациент может получать, например, внутривенную, подкожную или внутримышечную дозу от 0,01 до 100 мг/кг соединения, например в пределах от 0,1 до 20 мг/кг, причем композицию вводят от 1 до 4 раз в сутки. Внутривенная, подкожная и внутримышечная доза может быть введена инъекцией болюса. Альтернативно внутривенная доза может быть введена непрерывной инфузией в течение определенного периода времени. Альтернативно каждый пациент должен получать суточную дозу для перорального введения, которая приблизительно эквивалентна суточной парентеральной дозе, причем композицию вводят от 1 до 4 раз в сутки.
Ниже приведены примеры фармацевтических лекарственных форм, содержащих соединение формулы (I) или (Ia) или его фармацевтически приемлемую соль (далее соединение X) для терапевтического или профилактического применения у людей:
(а)
| Таблетка I |
мг/таблетку |
| Соединение Х |
100 |
| Лактоза, Европейская Фармакопея |
179 |
| Натриевая кроскармелоза |
12,0 |
| Поливинилпирролидон |
6 |
| Стеарат магния |
3,0 |
(б)
| Таблетка II |
мг/таблетку |
| Соединение Х |
50 |
| Лактоза, Европейская Фармакопея |
229 |
| Натриевая кроскармелоза |
12,0 |
| Поливинилпирролидон |
6 |
| Стеарат магния |
3,0 |
(в)
| Таблетка III |
мг/таблетку |
| Соединение X |
1,0 |
| Лактоза, Европейская Фармакопея |
92 |
| Натриевая кроскармелоза |
4,0 |
| Поливинилпирролидон |
2,0 |
| Стеарат магния |
1,0 |
(г)
| Капсула |
мг/капсулу |
| Соединение X |
10 |
| Лактоза, Европейская Фармакопея |
389 |
| Натриевая кроскармелоза |
100 |
| Стеарат магния |
1,0 |
(д)
| Инъекция I |
(50 мг/мл) |
| Соединение Х |
5,0 масс./об.% |
| Изотонический водный раствор |
До 100% |
В качестве вспомогательных веществ для приготовления препаратов могут быть использованы буферы, фармацевтически приемлемые сорастворители, такие как полиэтиленгликоль, полипропиленгликоль, глицерин или этанол, или комплексообразующие агенты, такие как гидроксипропил- -циклодекстрин. -циклодекстрин.
Вышеуказанные препараты могут быть получены по стандартным методикам, общеизвестным в фармацевтической области. Таблетки (а)-(в) могут быть покрыты энтеросолюбильной оболочкой традиционными способами, например способами, обеспечивающими покрытие оболочкой из фталата ацетата целлюлозы.
Изобретение также относится к комбинированной терапии, при которой для лечения одного либо более чем одного или более перечисленных состояний соединение по изобретению или его фармацевтически приемлемую соль, или фармацевтическую композицию, или препарат, содержащий соединение по изобретению, вводят одновременно или последовательно или в виде комбинированного препарата с другим терапевтическим агентом или агентами.
В частности, для лечения воспалительных заболеваний, таких как (без ограничения) ревматоидный артрит, остеоартрит, астма, аллергический ринит, хроническое обструктивное заболевание легких (ХОЗЛ), псориаз и воспалительное заболевание кишечника, соединения по изобретению можно комбинировать с агентами, перечисленными ниже.
Нестероидные противовоспалительные средства (далее NSAID), включающие неизбирательные ингибиторы циклооксигеназы СОХ-1/СОХ-2, применяемые местно или системно (такие как пироксикам, диклофенак, пропионовые кислоты, такие как напроксен, флурбипрофен, фенопрофен, кетопрофен и ибупрофен, фенаматы, такие как мефенамовая кислота, индометацин, сулиндак, азапропазон, пиразолоны, такие как фенилбутазон, салицилаты, такие как аспирин); избирательные ингибиторы СОХ-2 (такие как мелоксикам, целекоксиб, рофекоксиб, вальдекоксиб, лумарококсиб, парекоксиб и эторикоксиб); ингибирующие циклооксигеназу доноры оксида азота (CINOD); глюкокортикостероиды (вводимые местным, пероральным, внутримышечным, внутривенным или внутрисуставным путем); метотрексат; лефлуномид; гидроксихлорохин; d-пеницилламин; аранофин или другие парентеральные или пероральные препараты на основе золота; анальгетики; диацереин; внутрисуставные препараты, такие как производные гиалуроновой кислоты; и пищевые добавки, такие как глюкозамин.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли вместе с цитокином, или агонистом, или антагонистом цитокиновой функции (включая агенты, действующие на цитокиновые сигнальные пути, такие как модуляторы системы SOCS (белки-супрессоры цитокиновой сигнализации), включая альфа-, бета- и гамма-интерфероны; инсулиноподобным фактором роста типа I (IGF-1); интерлейкинами (IL), включая IL 1-17, и антагонистами или ингибиторами интерлейкинов, такими как анакинра; ингибиторами фактора некроза опухоли альфа (TNF-a), такими как анти-TNF моноклональные антитела (например, инфликсимаб; адалимумаб и CDP-870) и антагонистами рецепторов TNF, включая молекулы иммуноглобулина (например, этанерцепт) и низкомолекулярные агенты, такие как пентоксифиллин.
Кроме того, изобретение относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с моноклональным антителом против В-лимфоцитов (таким как CD20 (ритуксимаб), MRA-alL16R и Т-лимфоцитов, CTLA4-Ig, HuMax II-15).
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с модулятором функции хемокинового рецептора, таким как антагонист CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10 и CCR11 (для семейства С-С); CXCR1, CXCR2, CXCR3, CXCR4 и CXCR5 (для семейства С-Х-С) и СХ3СР1 для семейства С-Х3-С.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с ингибитором матриксной металлопротеазы (ММР), т.е. стромелизинами, коллагеназами и желатиназами, а также агреканазой, например коллагеназой-1 (ММР-1), коллагеназой-2 (ММР-8), коллагеназой-3 (ММР-13), стромелизином-1 (ММР-3), тромелизином-2 (ММР-10) и стромелизином-3 (ММР-11) и ММР-9 и ММР-12, включая такие агенты, как доксициклин.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и ингибитора биосинтеза лейкотриенов, ингибитора 5-липоксигеназы (5-LO) или антагониста белка, активирующего 5-липоксигеназу (FLAP), такого как зилейтон; АВТ-761; фенлейтон; тепоксалин; Abbott-79175; Abbott-85761; N-(5-замещенный)-тиофен-2-алкилсульфонамид; 2,6-ди-трет-бутилфенолгидразоны; метокситетрагидропираны, такие как Zeneca ZD-2138; соединение SB-210661; пиридинилзамещенное 2-цианонафталиновое соединение, такое как L-739010; 2-цианохинолиновое соединение, такое как L-746,530; или индольное, или хинолиновое соединение, такое как МК-591, МК-886 и BAYx1005.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и антагониста рецепторов лейкотриенов (LT) B4, LTC4, LTD4 и LTE4, выбранного из группы, состоящей из фенотиазинов-3-1, например L-651392; амидиносоединений, например CGS-25019c; бензоксаламинов, таких как онтазоласт; бензолкарбоксимидамидов, таких как BIIL 284/260; и таких соединений, как зафирлукаст, аблукаст, монтелукаст, пранлукаст, верлукаст (МК-679), RG-12525, Ro-245913, иралукаст (CGP 45715А) и BAYx7195.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и ингибитора фосфодиэстеразы (PDE), такого как метилксантанин, включая теофиллин и аминофиллин; избирательного ингибитора изофермента PDE, включая ингибитор PDE4, ингибитор изоформы PDE4D или ингибитор PDE5.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и антагониста гистаминового рецептора типа 1, такого как цетиризин, лоратадин, деслоратадин, фексофенадин, акривастин, ферфенадин, астемизол, азеластин, левокабастин, хлорфенирамин, прометазин, циклизин или мизоластин, применяемой перорально, местно или парентерально.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и ингибитора протонного насоса (такого как омепразол) или гастропротективного антагониста гистаминового рецептора типа 2.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и антагониста гистаминового рецептора типа 4.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и агониста альфа-1/альфа-2 адренорецептора, являющегося вазоконстрикторным симпатомиметиком, такого как пропилгекседрин, фенилэфрин, фенилпропаноламин, эфедрин, псевдоэфедрин, нафазолина гидрохлорид, оксиметазолина гидрохлорид, тетрагидрозолина гидрохлорид, ксилометазолина гидрохлорид, трамазолина гидрохлорид или этилнорэпинефрина гидрохлорид.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и антихолинергических агентов, включая антагонист мускаринового рецептора (М1, М2 и М3), такой как атропин, гиосцин, гликопирролят, ипратропия бромид, тиотропия бромид, окситропия бромид, пирензепин или телензепин.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и агониста бета-адренорецептора (включая подтипы 1-4 бета-рецепторов), такого как изопреналин, сальбутамол, формотерол, сальметерол, тербуталин, орципреналин, битолтерола мезилат или пирбутерол или его хиральный энантиомер.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и хромона, такого как хромогликат натрия или недокромил натрия.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с глюкокортикоидом, таким как флунизолид, триамцинолона ацетонид, беклометазона дипропионат, будезонид, флутиказона пропионат, циклезонид или мометазона фуроат.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с агентом, который модулирует ядерный рецептор гормонов, такой как рецептор, активируемый пероксисомальным пролифератором (PPAR).
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с иммуноглобулином (Ig), или препаратом Ig, или антагонистом, или антителом, модулирующим функцию Ig, таким как анти-IgE антитело (например, омализумаб).
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и другого противовоспалительного агента, применяемого системно или местно, такого как талидомид или его производное, ретиноид, дитранол или кальципотриол.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и комбинаций аминосалицилатов и сульфапиридина, таких как сульфасалазин, месалазин, балсалазид, и олсалазин, и иммуномодулирующих агентов, таких как тиопурины и кортикостероиды, такие как будезонид.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли с антибактериальным агентом, таким как производное пенициллина, тетрациклин, макролид, бета-лактам, фторхинолон, метронидазол, ингалируемый аминогликозид; противовирусным агентом, включая ацикловир, фамцикловир, валацикловир, ганцикловир, цидофовир, амантадин, римантадин, рибавирин, занамавир и оселтамавир; ингибитором протеазы, таким как индинавир, нельфинавир, ритонавир и саксинавир; нуклеозидным ингибитором обратной транскриптазы, таким как диданозин, ламивудин, ставудин, зальцитабин или зидовудин; или ненуклеозидным ингибитором обратной транскриптазы, таким как невирапин или эфавиренз.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и сердечно-сосудистого агента, такого как блокатор кальциевых каналов, блокатор бета-адренорецептора, ингибитор ангиотензин-конвертирующего фермента (АСЕ), антагонист рецептора ангиотензина-2; агента, снижающего уровень липидов, такого как статин или фибрат; модулятора морфологии клеток крови, такого как пентоксифиллин; тромболитического агента или антикоагулянта, такого как ингибитор агрегации тромбоцитов.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и агента, действующего на центральную нервную систему (ЦНС), такого как антидепрессант (такой как сертралин), антипаркинсоническое лекарственное средство (такое как депренил, L-дофа, ропинирол, прамипексол, ингибитор МАОВ (моноаминоксидаза В), такой как селегин и расагилин, ингибитор comP (олигомерный матриксный белок хряща), такой как тасмар, ингибитор А-2, ингибитор обратного захвата дофамина, антагонист NMDA (N-метил-D-аспарагиновая кислота), агонист никотина, агонист дофамина или ингибитор нейрональной синтазы оксида азота, или лекарственное средство против болезни Альцгеймера, такое как донепезил, ривастигмин, такрин, ингибитор СОХ-2, пропентофиллин или метрифонат.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли и агента для лечения острой или хронической боли, такого как аналгетик центрального или периферического действия (например опиоид или его производное), карбамазепин, фенитоин, вальпроат натрия, амитриптилин или другие антидепрессанты, парацетамол или нестероидное противовоспалительное средство.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли вместе с применяемым парентарально или местно (включая ингаляцию) местным анестезирующим агентом, таким как лигнокаин или его производное.
Соединение по настоящему изобретению или его фармацевтически приемлемая соль также могут быть применены в комбинации со средством против остеопороза, включая гормональное средство, такое как ралоксифен, или бифосфонат, такой как алендронат.
Настоящее изобретение также относится к комбинации соединения по изобретению или его фармацевтически приемлемой соли вместе с: (1) ингибитором триптазы; (2) антагонистом фактора активации тромбоцитов (PAF); (3) ингибитором интерлейкин-конвертирующего фермента (ICE); (4) ингибитором инозинмонофосфатдегидрогеназы (IMPDH); (5) ингибиторами молекул адгезии, включая антагонист VLA-4; (6) катепсином; (7) ингибитором киназы, таким как ингибитор тирозинкиназы (такой как Btk, Itk, Jak3 или MAP, например гефитиниб или иматиниба мезилат), серин/треониновой киназы (таким как ингибитор MAP киназы, такой как р38, JNK, протеинкиназа А, В или С, или IKK), или киназы, вовлеченной в регуляцию клеточного цикла (такой как циклинзависимая киназа); (8) ингибитором глюкозо-6-фосфатдегидрогеназы; (9) антагонистом кинин-B.sub1.- или В.sub2-рецептора; (10) противоподагрическим агентом, например колхицином; (11) ингибитором ксантиноксидазы, например аллопуринолом; (12) агентом, способствующим выведению мочевой кислоты, например пробенецидом, сульфинпиразоном или бензбромароном; (13) секретагогом гормона роста; (14) трансформирующим фактором роста (TGF ); (15) тромбоцитарным фактором роста (PDGF); (16) фактором роста фибробластов, например основным фактором роста фибробластов (bFGF); (17) гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF); (18) капсаициновым кремом; (19) антагонистом тахикининового NK.sub1. или NK.sub3. рецептора, таким как NKP-608C, SB-233412 (тальнетант) или D-4418; (20) ингибитором эластазы, таким как UT-77 или ZD-0892; (21) ингибитором TNF-альфа-конвертирующего фермента (ТАСЕ); (22) ингибитором индуцибельной синтазы оксида азота (iNOS); (23) молекулой-гомологом рецептора хемоаттрактантов, экспрессируемой на клетках ТН2 (такой как антагонист CRTH2); (24) ингибитором Р38; (25) агентом, модулирующим функцию Toll-подобных рецепторов (TLR); (26) агентом, модулирующим активность пуринергических рецепторов, таких как Р2Х7; или (27) ингибитором активации фактора транскрипции, такого как NF ); (15) тромбоцитарным фактором роста (PDGF); (16) фактором роста фибробластов, например основным фактором роста фибробластов (bFGF); (17) гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF); (18) капсаициновым кремом; (19) антагонистом тахикининового NK.sub1. или NK.sub3. рецептора, таким как NKP-608C, SB-233412 (тальнетант) или D-4418; (20) ингибитором эластазы, таким как UT-77 или ZD-0892; (21) ингибитором TNF-альфа-конвертирующего фермента (ТАСЕ); (22) ингибитором индуцибельной синтазы оксида азота (iNOS); (23) молекулой-гомологом рецептора хемоаттрактантов, экспрессируемой на клетках ТН2 (такой как антагонист CRTH2); (24) ингибитором Р38; (25) агентом, модулирующим функцию Toll-подобных рецепторов (TLR); (26) агентом, модулирующим активность пуринергических рецепторов, таких как Р2Х7; или (27) ингибитором активации фактора транскрипции, такого как NF B, API или STATS. B, API или STATS.
Соединение по изобретению или его фармацевтически приемлемая соль также можно применять в комбинации с существующим терапевтическим агентом для лечения рака; подходящие агенты, например, включают:
(1) антипролиферативное/антинеопластическое лекарственное средство или их комбинация, которое применяется в лечебной онкологии, такое как алкилирующий агент (например, цисплатин, карбоплатин, циклофосфамид, азотистый аналог иприта, мелфалан, хлорамбуцил, бусульфан или нитрозомочевина); антиметаболит (например, антифолат, например, фторпиримидин, такой как 5-фторурацил или тегафур, ральтитрексед, метотрексат, цитозина арабинозид, гидроксимочевина, гемцитабин или паклитаксел); противоопухолевый антибиотик (например, антрациклин, такой как адриамицин, блеомицин, доксорубицин, даномицин, эпирубицин, идарубицин, митомицин-С, дактиномицин или митрамицин); антимитотический агент (например, алкалоид барвинка, такой как винкристин, винбластин, виндезин или винорелбин, или таксоид, такой как таксол или таксотер); или ингибитор топоизомеразы (например, эпиподофиллотоксин, такой как этопозид, тенипозид, амсакрин, топотекан или камптотецин);
(2) цитостатический агент, такой как антиэстроген (например, тамоксифен, торемифен, ралоксифен, дролоксифен или йодоксифен), отрицательный регулятор эстрогенового рецептора (например, фульвестрант), антиандроген (например, бикалутамид, флутамид, нилутамид или ципротерона ацетат), антагонист LHRH (рилизинг-фактор лютеинизирующего гормона) или агонист LHRH (например, гозерелин, лейпрорелин или бусерелин), прогестоген (например, мегестрола ацетат), ингибитор ароматазы (например, анастрозол, летрозол, воразол или эксеместан) или ингибитор 5 -редуктазы, такой как финастерид; -редуктазы, такой как финастерид;
(3) агент, ингибирующий инвазию раковыми клетками (например, ингибитор металлопротеиназы, такой как маримастат или ингибитор рецепторной функции урокиназного активатора плазминогена);
(4) ингибитор функции фактора роста, например антитело против фактора роста (например, анти-erbb2 антитело трастузумаб или анти-erbb1 антитело цетуксимаб [С225]), ингибитор фарнезилтрансферазы, ингибитор тирозинкиназы или ингибитор серин/треонинкиназы, ингибитор семейства эпидермальных факторов роста (например, ингибитор тирозинкиназы семейства EGFR, такой как N-(3-хлор-4-фторфенил)-7-метокси-6-(3-морфолинопропокси)хиназолин-4-амин (гефитиниб, AZD1839), N-(3-этинилфенил)-6,7-бис(2-метоксиэтокси)хиназолин-4-амин (эрлотиниб, OSI-774) или 6-акриламидо-N-(3-хлор-4-фторфенил)-7-(3-моролинопропокси)хиназолин-4-амин (CI 1033)), ингибитор семейства тромбоцитарных факторов роста или ингибитор семейства факторов роста гепатоцитов;
(5) антиангиогенный агент, такой как агент, ингибирующий эффекты сосудистого эндотелиального фактора роста (например, антитело против сосудистого эндотелиального фактора роста бевацизумаб, соединение, раскрытое в WO 97/22596, WO 97/30035, WO 97/32856 или WO 98/13354), или соединение, действующее по другому механизму (например, линомид, представляющий собой ингибитор функции интегрина  v v 3 или ангиостатин); 3 или ангиостатин);
(6) агент, разрушающий сосудистые клетки, такой как комбретастатин А4, или соединение, раскрытое в WO 99/02166, WO 00/40529, WO 00/41669, WO 01/92224, WO 02/04434 или WO 02/08213;
(7) агент, используемый в антисмысловой терапии, например агент, направленно действующий на одну из мишеней, перечисленных выше, такой как ISIS 2503, анти-ras антисмысловой агент;
(8) агент, применяемый в генной терапии, например для замены аберрантных генов, таких как аберрантный р53 или аберрантный BRCA1 или BRCA2, GDEPT (пролекарственная терапия ген-направленным ферментом), например с использованием цитозиндеаминазы, тимидинкиназы или бактериальной нитроредуктазы, и для повышения толерантности пациента к химиотерапии или радиотерапии, например генная терапия с использованием гена мультилекарственной резистентности;
(9) агент, применяемый в иммунотерапии, например для ex vivo и in vivo увеличения иммуногенности опухолевых клеток пациента, например для трансфекции цитокинами, такими как интерлейкин 2, интерлейкин 4 или гранулоцитарно-макрофагальный колониестимулирующий фактор, для уменьшения Т-клеточной анергии, с использованием трансфицированных иммунных клеток, таких как цитокин-трансфицированные дендритные клетки, с использованием цитокин-трансфицированных линий опухолевых клеток и с использованием антиидиотипических антител; или
(10) соединение, используемое в лечении СПИД и/или ВИЧ-инфекции, например агент, который предотвращает или ингибирует захват вирусного белка gр120 клеткой-хозяином CD4 {например, растворимый CD4 (рекомбинантный); анти-CD4 антитело (или модифицированное/рекомбинантное антитело), например PRO542; антитело против группы 120 (или модифицированное/рекомбинантное антитело); или другой агент, который мешает связыванию группы 120 с CD4, например, BMS806}; агент, который предотвращает связывание с хемокиновым рецептором, иным чем CCR5, используемым вирусом ВИЧ {такой как агонист или антагонист CXCR4 или анти-СХСР4 антитело}; соединение, которое мешает слиянию оболочки вируса ВИЧ с клеточной мембраной {такой как антитело против группы 41; энфувиртид (Т-20) или Т-1249}; ингибитор DC-SIGN (специфичный для дендритных клеток неинтегрин, захватывающий внутриклеточную молекулу адгезии-1, также известный как CD209) {такой как анти-DC-SIGN антитело или ингибитор связывания DC-SIGN}; ингибитор обратной транскриптазы, представляющий собой нуклеозидный/нуклеотидный аналог {например, зидовудин (АZТ), невирапин, диданозин (ddI), зальцитабин (ddC), ставудин (d4T), ламивудин (3ТС), абакавир, адефовир или тенофовир (например, в форме свободного основания или в форме фумарата дизопроксила)}; ненуклеозидный ингибитор обратной транскриптазы {например, невирапин, делавирдин или эфавиренз}; ингибитор протеазы {например, ритонавир, индинавир, саксинавир (например в форме свободного основания или в форме мезилатной соли), нельфинавир (например, в форме свободного основания или в форме мезилатной соли), ампренавир, лопинавир или атазанавир (например, в форме свободного основания или в форме сульфатной соли)}; ингибитор рибонуклеотидной редуктазы {например, гидроксимочевина}; или антиретровирусный агент {например, эмтрицитабин}.
Изобретение иллюстрируется приведенными ниже не ограничивающими Примерами, в которых, если не указано иное:
1) температуры даны в градусах Цельсия (°С); операции проводили при комнатной температуре или при температуре окружающей среды, то есть при температуре в пределах 18-25°С;
2) органические растворы сушили над безводным сульфатом магния; выпаривание растворителя осуществляли на роторном испарителе при пониженном давлении (600-4000 Па; 4,5-30 мм рт.ст.) с температурой бани до 60°С;
3) если не указано иное, хроматография представляет собой флэш-хроматографию на силикагеле; тонкослойную хроматографию (ТСХ) проводили на силикагелевых пластинах; если упоминается колонка “Bond Elut”, то имеется в виду колонка, содержащая 10 г или 20 г диоксида кремния с размером частиц 40 микрон, причем диоксид кремния находится в одноразовом шприце на 60 мл на подложке, представляющей собой пористый диск, от Varian, Harbor City, California, USA, под наименованием “Меgа Bond Elut SI”. Если упоминается “колонка Isolate SCX”, то имеется в виду колонка, содержащая бензолсульфоновую кислоту (с незаделанным концом), от International Sorbent Technology Ltd., 1st House, Duffryn Industial Estate, Ystrad Mynach, Hengoed, Mid 30 Glamorgan, UK. Если упоминается “PS-трис-аминная акцепторная смола Argonaut SCX”, то имеется в виду колонка, содержащая бензолсульфоновую кислоту (с незаделанным концом), от International Sorbent Technology Ltd., 1st House, Duffryn Industial Estate, Ystrad Mynach, Hengoed, Mid 30 Glamorgan, UK. Если упоминается “PS-трис-аминная акцепторная смола Argonaut “, то имеется в виду трис-(2-аминоэтил)аминополистирольная смола от Argonaut Technologies Inc., 887 Industrial Road, Suite G, San Carlos, California, USA. “, то имеется в виду трис-(2-аминоэтил)аминополистирольная смола от Argonaut Technologies Inc., 887 Industrial Road, Suite G, San Carlos, California, USA.
4) как правило, реакции контролировали ТСХ, и реакционное время приведено только для иллюстрации;
5) выходы, если они даны, служат только для иллюстрации и необязательно это будут выходы, которые могут быть получены в результате упорной разработки способа; если требовалось больше материала, процедуры получения повторяли;
6) данные 1H ЯМР, если они приведены, приведены в форме дельта-значений для основных диагностических протонов в миллионных долях (млн-1) относительно тетраметилсилана (ТМС) в качестве внутреннего стандарта, которые определены при 300 МГц с использованием, если не указано иное, пердейтерированного ДМСО (диметилсульфоксид) (CD3SOCD3) в качестве растворителя; константы связывания (J) даны в Гц;
7) химические символы имеют их обычные значения; использованы единицы и символы СИ;
8) соотношения растворителей указаны в процентах по объему;
9) масс-спектры (МС) регистрировали с энергией электрона 70 электрон-вольт в режиме химической ионизации при атмосферном давлении (ХИАД) с использованием прямой экспозиции образца; там, где это указано, ионизацию осуществляли электрораспылением (ЭР); если приведены значения m/z, то они приведены, как правило, только для ионов, которые показывают исходную массу, и, если не указано иное, приведенный масс-ион представляет собой положительный масс-ион – (М+Н)+;
10) определение характеристик ЖХ-МС (жидкостная хроматография/масс-спектрометрия) осуществляли с использованием пары насосов Gilson 306 с пробоотборником Gilson 233 XL и масс-спектрометра Waters ZMD4000. ЖХ выполняли на колонке Water Symmetry 4,6×50 С18 с размером частиц 5 микрон. Элюенты представляли собой: А, вода с 0,05% муравьиной кислоты и Б, ацетонитрил с 0,05% муравьиной кислоты. Градиент элюента проходил с 95% А до 95%
Б в течение 6 минут. Там, где это указано, ионизацию осуществляли электрораспылением (ЭР); если приведены значения m/z, то они приведены, как правило, только для ионов, которые показывают исходную массу, и, если не указано иное, приведенный масс-ион представляет собой положительный масс-ион – (М+Н)+; и
11) использованы следующие сокращения:
ДМФ N,N-диметилформамид;
Т.пл. температура плавления;
TMEDA N,N,N’,N’-тетраметилэтилендиамин;
ТГФ тетрагидрофуран.
ПРИМЕР 1
Этот Пример иллюстрирует получение N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида (Соединение 1 в Таблице I)
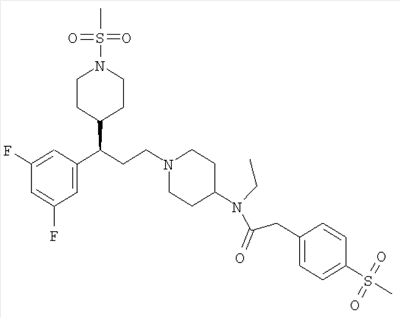
Триацетоксиборгидрид натрия (2,5 г) добавляли к раствору (3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропаналя (1,98 г) и N-этил-2-[4-(метилсульфонил)фенил]-N-пиперидин-4-илацетамида (1,94 г) в дихлорметане (100 мл), и эту смесь перемешивали в течение 2 часов, затем промывали 2М NaOH (2×100 мл) и сушили. Органические вещества наносили на 50 г картридж SCX2 и элюировали метанолом (6×50 мл) и 1М метанольным аммиаком (7×50 мл). Объединенные метанольно-аммиачные промывочные жидкости выпаривали досуха с получением указанного в заголовке соединения в виде белой пены, выход 2,6 г. ЯМР (CDCl3): 1.2-2.1 (m, 19H), 2.3-2.7 (m, 3H), 2.75 (s, 3H), 2.8-2.9 (m, 2H), 3.0 (s, 3H), 3.3 (q, 2H), 3.7-3.9 (m, 4H), 6.65 (m, 3H), 7.4 (m, 2H), 7.9 (d, 2H).
ПРИМЕР 2
Этот Пример иллюстрирует получение сукцинатной соли N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида.
Горячий раствор янтарной кислоты (59 мг) в этаноле (3 мл) добавляли к горячему раствору N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида (640 мг) в этаноле (16 мл) и этой смеси давали возможность охладиться. Через 24 часа смесь растирали шпателем и оставляли стоять в течение еще 24 часов. Твердое вещество отфильтровывали и сушили, т.пл. 175-175,5°С. Это твердое вещество перекристаллизовывали из этанола (14 мл) с получением указанного в заголовке соединения, т.пл. 177-177,5°С.
ПРИМЕР 3
Этот Пример иллюстрирует получение фумаратной соли N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида.
Горячий раствор фумаровой кислоты (55 мг) в метаноле (3 мл) добавляли к горячему раствору N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида (300 мг) в метаноле (4 мл) и этой смеси давали возможность охладиться. Смесь затем охлаждали в ледяной бане и оставляли стоять в холодильнике в течение 14 часов. Твердое вещество отфильтровывали и сушили при 60°С в вакууме в течение 2 часов, т.пл. 164-166,5°С.
ПРИМЕР 4
Этот Пример иллюстрирует получение N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[3-(метилсульфонил)фенил]ацетамида.
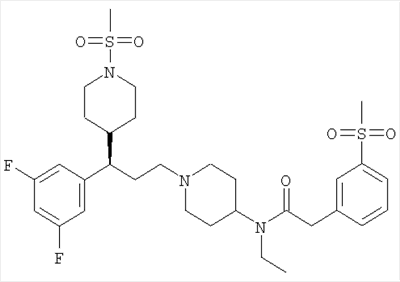
3-(Метилсульфонил)фенилуксусную кислоту (96 мг) растворяли в дихлорметане (5 мл) и добавляли карбонилдиимидазол (73 мг). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Добавляли N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этиламин (200 мг) в дихлорметане (5 мл) и эту реакционную смесь оставляли стоять при комнатной температуре в течение 72 часов. Добавляли PS-изоцианатную смолу (1 мм/г) (0,5 г) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов, затем фильтровали и упаривали. Остаток очищали колоночной хроматографией, элюируя смесью этилацетат-20% метанола/этилацетат с получением указанного в заголовке соединения в виде пены (105 мг).
ЯМР CDCl3: 1.0-2.1 (m, 21 Н), 2.3-2.6 (m, 3H), 2.65 (s, 3H), 2.9 (s, 3H), 3.3 (m, 2H), 3.65 (d, 1H), 3.7 (m, 2H), 3.75 (d, 1H), 6.6 (m, 3H), 7.5 (m, 2H), 7.75 (m, 2H).
Способ А
Получение (3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропаналя
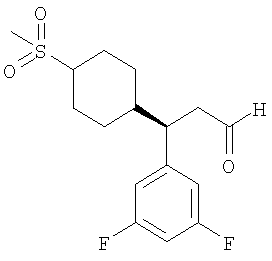
Стадия 1. Получение (2Е)-3-[1-(метилсульфонил)пиперидин-4-ил]акрилоилхлорида
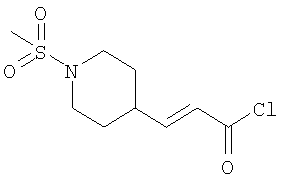
Оксалилхлорид (5,1 г) добавляли к раствору (2Е)-3-[1-(метилсульфонил)пиперидин-4-ил]акриловой кислоты (9,4 г) в дихлорметане, содержащем 2-3 капли ДМФ и эту смесь перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь выпаривали досуха и непосредственно полученный остаток использовали на следующей стадии.
Стадия 2. Получение (4R,5S)-1,5-Ibметил-3-{(2Е)-3-[1-(метилсульфонил)пиперидин-4-ил]проп-2-еноил}-4-фенилимидазолидин-2-она
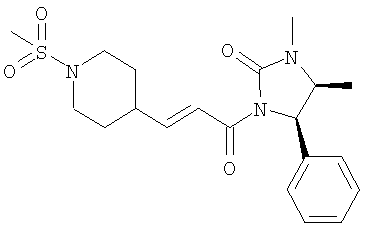
Бис(триметилсилил)амид лития (8 мл 1М раствора в ТГФ) по каплям добавляли к суспензии (4R,5S)-1,5-диметил-4-фенил-2-имидазолидинона (1,52 г) в ТГФ (20 мл) в атмосфере аргона при -10°С. Реакционную смесь перемешивали при -10°С в течение 10 минут, давали ей возможность нагреться до 0°С и выдерживали при этой температуре в течение 10 минут, затем вновь охлаждали до -10°С. По каплям добавляли раствор полученного на стадии 1 хлорангидрида (2 г, растворенного в 10 мл дихлорметана), реакционной смеси давали возможность нагреться до комнатной температуры и промывали водой (100 мл). Водный экстракт экстрагировали этилацетатом (3×50 мл), этилацетатные экстракты сушили и остаток пропускали через 90 г колонку Biotage, элюируя градиентом растворителей (50% этилацетата/изогексан – 70% этилацетата/изогексан). Выход 1,89 г. ЖХ-МС МН+ 406, ЯМР (CDCl3): 0.8 (d, 3Н), 1.5-1.6 (m, 3Н), 1.9 (m, 2H), 2.3 (m, 1H), 2.7 (m, 2H), 2.75 (s, 3Н), 2.8 (s, 3Н), 3.75 (m, 2H), 3.9 (m, 1H), 5.3 (d, 1H), 6.85 (d-d, 1H), 7.1 (d, 1H), 7.2-7.35 (m, 3Н), 7.45 (d,1H).
Стадия 3. Получение (4S,5R)-1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропаноил}-3,4-диметил-5-фенилимидазолидин-2-она
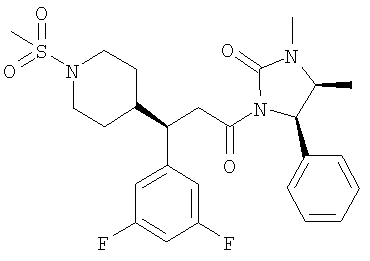
Стадия А
TMEDA (11,6 г) добавляли к суспензии йодида меди (19,4 г) в ТГФ (240 мл) в атмосфере аргона, и эту смесь перемешивали в течение 45 минут, затем охлаждали до -70°С. В течение 10 минут добавляли раствор 3,5-дифторфенилмагнийбромида в ТГФ (201,1 мл 0,5М раствора в ТГФ), и эту смесь перемешивали при -70°С в течение 30 минут.
Стадия Б
Трифлат ди-н-бутилбора (100,7 мл 1М раствора в дихлорметане) добавляли к суспензии (4R,5S)-1,5-диметил-3-{(2Е)-3-[1-(метилсульфонил)пиперидин-4-ил]проп-2-еноил}-4-фенилимидазолидин-2-она (20,41 г) [Стадия 2] в ТГФ, поддерживаемом при -40°С, и перемешивание продолжали в течение 10 минут, смесь охлаждали до -70°С и добавляли через канюлю в суспензию купрата, полученную на стадии А. Реакционную смесь перемешивали при -70°С в течение 1 часа и давали ей возможность нагреться до комнатной температуры, затем добавляли насыщенный раствор хлорида аммония (200 мл). ТГФ выпаривали и добавляли этилацетат (200 мл). Через эту смесь в течение 1 часа пропускали воздух. Этилацетатный слой собирали и водный слой экстрагировали этилацетатом (2×100 мл). Объединенные этилацетатные экстракты промывали насыщенным раствором хлорида аммония (2×100 мл), сушили и упаривали досуха. Остаток очищали хроматографией на диоксиде кремния, элюируя градиентом растворителей с этилацетата-изогексана (1:1) до чистого этилацетата с получением указанного в заголовке соединения в виде белого твердого вещества, выход 25 г. ЯМР (CDCl3) 0.78 (d, 3Н), 1.2-1.6 (m, 6H), 1.9 (m, 1H), 2.4-2.65 (m, 2H), 2.75 (s, 3H), 2.85 (s, 3Н), 3-3.2 (m, 2H), 3.7-3.9 (m, 4H), 5.2 (d, 1H), 6.6 (m, 3H), 6.85 (m, 2H), 7.2 (m, 3H).
Стадия 4. Получение (3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропан-1-ола
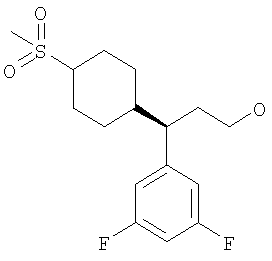
Боргидрид лития (48 мл 2М раствора в ТГФ) добавляли к раствору (4S,5R)-1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропаноил}-3,4-диметил-5-фенилимидазолидин-2-она (25 г) в ТГФ (200 мл), эту смесь нагревали при 70°С в течение 3 часов, затем давали ей возможность охладиться до комнатной температуры, перемешивание продолжали в течение 16 часов. Осторожно добавляли этанол (20 мл) и реакционную смесь подкисляли до рН 4 добавлением 2М HCl. ТГФ выпаривали, остаток растворяли в дихлорметане (100 мл), промывали водой (100 мл) и сушили. Растворитель удаляли и продукт очищали хроматографией на колонке Biotage 65, элюируемой смесью 1:1 этилацетат/изогексан. Выход 13 г. ЯМР (CDCl3): 1.2-1.8 (m, 5H), 1.95-2.2 (m, 2H), 2.5-2.7 (m, 3Н), 2.75 (s, 3Н), 3.3-3.6 (m, 2H), 3.7-3.9 (m, 2H), 6.65 (m, 3Н).
Стадия 5. Получение указанного в заголовке соединения
Перйодинан Десс-Мартина (5,09 г) добавляли к раствору (R) 3-(N-метансульфонилпиперидин-4-ил)-3-(3,5-дифторфенил)пропанола (4,0 г) в дихлорметане (100 мл) и эту смесь перемешивали в течение 1,5 часов. Реакционную смесь промывали 2М NaOH (2×100 мл) и сушили. Раствор указанного в заголовке соединения в дихлорметане использовали в последующих реакциях.
Способ Б
N-этил-2-[4-(метилсульфонил)фенил]-N-пиперидин-4-илацетамид
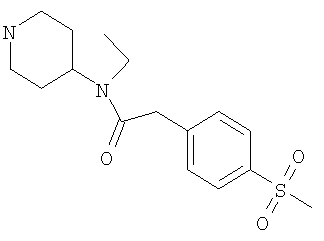
Стадия 1: Получение дигидрохлорида 1-фенилметил-4-этиламинопиперидина
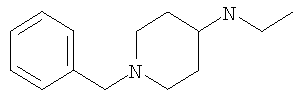
К раствору 1-фенилметил-4-пиперидона (25,0 г, 132 ммоль) в ТГФ (250 мл) добавляли гидрохлорид этиламина (12,0 г, 147 моль) и метанол (50 мл), полученную смесь перемешивали при комнатной температуре в течение 10 мин. Порциями добавляли триацетоксиборгидрид натрия (40 г, 189 ммоль), полученную смесь перемешивали при комнатной температуре в течение 1 ч. Добавляли 2М раствор гидроксида натрия (250 мл), полученную смесь экстрагировали диэтиловым эфиром. Органические экстракты сушили (K2CO3) и упаривали с получением 1-фенилметил-4-этиламинопиперидина в виде масла. Его растворяли в этаноле (500 мл), в него добавляли концентрированную соляную кислоту (20 мл). Образовавшиеся кристаллы собирали, промывали диэтиловым эфиром и сушили с выходом (38 г); ЯМР: (CDCl3): 1.10 (t, 3H), 1.40 (m, 2H), 1.83 (m, 2H), 2.02 (m, 2H), 2.65 (q, 2H), 2.85 (m, 2H), 3.50 (s, 2H), 3.75 (m, 1H), 7.2-7.4 (m, 5H); МС: 219 (МН+).
Стадия 2: Получение N-(1-бензилпиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида
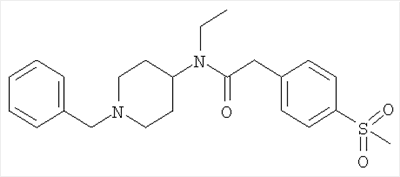
К раствору дигидрохлорида 1-фенилметил-4-этиламинопиперидина (32,0 г, 110 ммоль) в ДХМ (500 мл) при перемешивании для обеспечения полного растворения добавляли N,N-диизопропилэтиламин (60 мл). Добавляли 4-метансульфонилфенилуксусную кислоту (25,0 г, 117 ммоль), 4-диметиламинопиридин (2,0 г) и дициклогексилкарбодиимид (25,0 г, 121 ммоль), полученную смесь перемешивали при комнатной температуре в течение 20 ч. Осадок удаляли фильтрованием, полученный раствор последовательно промывали 2 н. водной HCl, водой и 1 н. водным NaOH, сушили (МgSO4) и упаривали. Остаток очищали хроматографией на силикагеле (элюент: 10% МеОН/этилацетат) с получением указанного в подзаголовке соединения (35 г, 76%); ЯМР: 1.00 и 1.14 (t, 3H), 1.45 и 1.70 (m, 2H), 1.95 (br m, 2H), 2.80 (br m, 2H), 3.18 (s, 3H), 3.20 и 3.33 (q, 2H), 3.45 (s, 2H), 3.80 и 3.87 (s, 2H), 3.70 и 4.10 (m, IH), 7.2-7.3 (m, 5H), 7.48 (m, 2H), 7.82 (m, 2H); MC: 415 (МН+).
Стадия 3: Получение указанного в заголовке соединения
К раствору N-(1-бензилпиперидин-4-ил)-N-этил-2-[4-(метилсульфонил)фенил]ацетамида (34 г, 82 ммоль) в этаноле (600 мл) добавляли формиат аммония (40 г). Смесь продували аргоном и добавляли 30% Pd на углероде (4,2 г). Полученную смесь перемешивали при кипячении с обратным холодильником в течение 4 ч, затем давали ей возможность охладиться и фильтровали через диатомитовую землю. Фильтрат упаривали до густого масла, которое затвердевало при стоянии, дав указанное в заголовке соединение (24,9 г, 94%). ЯМР: 1.02 и 1.15 (t, 3H), 1.4-1.6 (br m, 4H), 2.45 (m, 2H), 2.93 (br m, 2H), 3.18 (s, 3H), 3.20 и 3.32 (q, 2H), 3.72 и 4.18 (m, 1H), 3.80 и 3.87 (s, 2H), 7.50 (m, 2H), 7.85 (m, 2H); MC: 325 (МН+).
ПРИМЕР 5
Способность соединений ингибировать связывание RANTES оценивали анализом связывания радиолиганда in vitro. Мембраны получали из клеток яичника китайского хомячка, экспрессирующих рекомбинантный человеческий рецептор CCR5. Эти мембраны инкубировали с 0,1 нМ йодированным RANTES гранулами для сцинтилляционного проксимального анализа и различными концентрациями соединений по изобретению в 96-луночных планшетах. Количество йодированных RANTES, связавшихся с рецептором, определяли путем подсчета сцинтилляций. Строили конкурентные кривые для соединений и рассчитывали концентрацию соединения, вытеснившего 50% связанного йодированного RANTES (IC50). Соединения формулы (I), имеющие IC50 менее 50 мкМ, образуют еще один аспект изобретения.
ПРИМЕР 6
Способность соединений ингибировать связывание MIP-1 оценивали анализом связывания радиолиганда in vitro. Мембраны получали из клеток яичника китайского хомячка, экспрессирующих рекомбинантный человеческий рецептор CCR5. Эти мембраны инкубировали с 0,1 нМ йодированным MIP-1 оценивали анализом связывания радиолиганда in vitro. Мембраны получали из клеток яичника китайского хомячка, экспрессирующих рекомбинантный человеческий рецептор CCR5. Эти мембраны инкубировали с 0,1 нМ йодированным MIP-1 гранулами для сцинтилляционного проксимального анализа и различными концентрациями соединений по изобретению в 96-луночных планшетах. Количество йодированных MIP-1 гранулами для сцинтилляционного проксимального анализа и различными концентрациями соединений по изобретению в 96-луночных планшетах. Количество йодированных MIP-1 , связавшихся с рецептором, определяли путем подсчета сцинтилляций. Строили конкурентные кривые для соединений и рассчитывали концентрацию соединения, вытесняющего 50% связанного йодированного MIP-1 , связавшихся с рецептором, определяли путем подсчета сцинтилляций. Строили конкурентные кривые для соединений и рассчитывали концентрацию соединения, вытесняющего 50% связанного йодированного MIP-1 (IC50). Соединения формулы (I), имеющие IC50 менее 50 мкМ, образуют еще один аспект изобретения. (IC50). Соединения формулы (I), имеющие IC50 менее 50 мкМ, образуют еще один аспект изобретения.
Результаты этого испытания для некоторых соединений по изобретению представлены в Таблице II, где эти результаты представлены в виде значений Pic50. Значение Pic50 представляет собой отрицательный логарифм (по основанию 10) результата IC50, так что IC50 1 мкМ (то есть 1×10-6 М) дает Pic50, равный 6. Если соединение тестировали более одного раза, то приведенные ниже данные представляют собой среднее значение результатов подтверждающих тестов.
| Таблица II |
Соединение  |
Таблица  |
Pic50 |
| 1 |
I |
9,5 |
| 2 |
I |
9,3 |
| 3 |
I |
8,45 |
| 4 |
I |
8,8 |
| 5 |
I |
9,4 |
| 6 |
I |
9 |
Формула изобретения
1. Соединение N-(1-{(3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил) пиперидин-4-ил]пропил}пиперидин-4-ил)-N-этил-2-[4-(метилсульфонил) фенил]ацетамид или его фармацевтически приемлемая соль.
2. Соединение по п.1, представляющее собой его соль фумарат или сукцинат.
3. Способ получения соединения по п.1, включающий восстановительное аминирование (3R)-3-(3,5-дифторфенил)-3-[1-(метилсульфонил)пиперидин-4-ил]пропаналя N-этил-2-[4-(метилсульфонил)фенил]-N-пиперидин-4-илацетамидом в присутствии NaBH(ОАс)3 (где Ас представляет собой С(О)СН3) и уксусной кислоты в подходящем растворителе при комнатной температуре.
4. Фармацевтическая композиция, обладающая активностью в отношении CCR5 (хемокинового рецептора 5), содержащая соединение по п.1 или его фармацевтически приемлемую соль и фармацевтически приемлемый адъювант, разбавитель или носитель.
5. Соединение по п.1 или его фармацевтически приемлемая соль для применения в качестве лекарственного средства для терапии болезненных состояний, опосредованных CCR5.
6. Соединение по п.1 или его фармацевтически приемлемая соль в изготовлении лекарственного средства для применения в терапии болезненных состояний, опосредованных CCR5.
|
|