Патент на изобретение №2380347
|
||||||||||||||||||||||||||
(54) СУЛЬФИРОВАННЫЕ ФЕНОЛЫ С НИТРОФЕНОЛАМИ КАК ИНГИБИТОРЫ ПОЛИМЕРИЗАЦИИ
(57) Реферат:
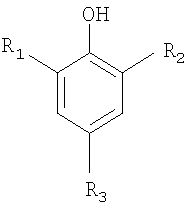
Изобретение относится к способу ингибирования преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров. Способ заключается в добавлении к указанным мономерам эффективного количества комбинации из, по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы (I): где (1) R2 выбирается из группы, состоящей из водорода и углеводорода; и (2) R1 и R3 независимо выбираются из группы, состоящей из водорода и SO3H, при условии, что, по меньшей мере, один из R1 и R3 выбран как SO3H, по меньшей мере, одного ингибитора, представляющего собой нитрофенол, и, при желании, одного ингибитора, выбранного из группы, состоящей из нитроксильных соединений и нитрозоанилинов, и амина. (I)
Техническим результатом является повышение эффективности процесса и его экономичности. 3 н. и 17 з.п. ф-лы.
Уровень техники изобретения 1. Область техники, к которой относится изобретение Настоящее изобретение относится к ингибированию полимеризации этиленненасыщенных мономеров путем добавления к ним комбинаций сульфированного фенола и нитрофенола. 2. Описание предшествующего уровня техники Многие этиленненасыщенные мономеры склонны к нежелательной полимеризации на разных стадиях их производства, обработки, обращения, хранения и использования. Полимеризация, как, например, термическая полимеризация, в процессе их очистки приводит к потере мономера, т.е. к более низким выходам, и увеличению вязкости любой смолы, которая может быть получена. Обработка и обращение более вязких смол впоследствии требует более высоких температур и большей работы (затрат энергии) для удаления остаточного мономера. Полимеризация может также приводить к засорению оборудования, особенно в случае производства акриловых мономеров. Такая полимеризация приводит к потерям в эффективности производства по причине отложения полимера в или на используемом оборудовании. Эти отложения должны время от времени удаляться, давая дополнительную потерю в производстве мономера. Было предложено и использовано большое число соединений для ингибирования неконтролируемой и нежелательной полимеризации этиленненасыщенных мономеров. Тем не менее, многие из них не удовлетворяли полностью. В патенте US Патент US В патенте US Патент US В патенте US Патент US В патенте US В патенте US В патенте US Патент US Патенты SU 1027150; 1139722; и 1558888 описывают пониженное образование полимера в нормальных технологических условиях (без ингибитора), но не защищают систему при ситуациях аварийного прекращения подачи рабочего материала, т.е. отсутствует какой-либо ретардантный эффект. Вышеперечисленные патенты приведены здесь в качестве ссылок. Сущность изобретения В соответствии с настоящим изобретением было найдено, что ингибирующие системы, содержащие сульфированные фенолы, проявляют себя как превосходные ингибиторы и ретарданты преждевременной полимеризации этиленненасыщенных мономеров, особенно винилароматических соединений, когда используются вместе с нитрофенолами, такими как, например, 2,4-динитро-о-втор-бутилфенол (DNBP). При желании эта ингибирующая система может быть использована в комбинации с соединениями нитроксильно-радикального типа или нитрозоанилинами и аминами. Преимуществом настоящего изобретения является то, что сульфированные фенолы могут быть получены в процессе производства DNBP. Так как DNBP является предпочтительным вторым компонентом заявленной ингибирующей смеси, оба компонента могут производиться в одном и том же процессе. Соответственно, производство может быть упрощено посредством приготовления обоих компонентов в одном и том же процессе в одном и том же месте. Это обеспечивает экономическое преимущество, заключающееся в том, что материал может быть получен в уже существующем процессе малыми средствами, без дополнительного вложения денег. С точки зрения покупателя, экономическая выгода реализуется по причине небольших затрат средств на производство (дешевизны) и по причине реализации оптимальной схемы производства заявленной смеси. Другими особенностями являются использование небольшого количества ингибитора и значительно подавленная полимеризация. Таким образом, цель настоящего изобретения состоит в разработке высокоэффективной и недорогой системы для ингибирования полимеризации с исключительно объективными ингибирующими и ретардантными способностями. Эта и другие цели достигаются посредством настоящего изобретения, которое относится к методу ингибирования преждевременной полимеризации и роста цепи полимера этиленненасыщенных мономеров и включает в себя добавление к указанным мономерам эффективного количества комбинации из (A) по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы:
где (1) R2 выбирается из группы, состоящей из водорода и углеводорода; и (2) R1 и R3 независимо выбираются из группы, состоящей из водорода и SO3H, при условии, что, по меньшей мере, один из R1 и R3 выбран как SO3H; и (B) по меньшей мере, одного ингибитора, представляющего собой нитрофенол. (C) по меньшей мере, одного ингибитора, выбранного из группы, состоящей из нитроксильных соединений и нитрозоанилинов; и (D) по меньшей мере, одного амина. С другой стороны, настоящее изобретение относится к композиции, включающей в себя комбинацию из (A) по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы:
где (1) R2 выбирается из группы, состоящей из водорода и углеводорода; и (2) R1 и R3 независимо выбираются из группы, состоящей из водорода и SO3H, при условии, что, по меньшей мере, один из R1 и R3 выбирается как SO3H; (B) по меньшей мере, одного ингибитора, представляющего собой нитрофенол; (C) по меньшей мере, одного ингибитора, выбранного из группы, состоящей из нитроксильных соединений и нитрозоанилинов; и (D) по меньшей мере, одного амина. Описание предпочтительного варианта осуществления Как было указано выше, настоящее изобретение относится к ингибирующей системе, включающей в себя композицию из (A) по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы:
где (1) R2 выбирается из группы, состоящей из водорода и углеводорода; и (2) R1 и R3 независимо выбираются из группы, состоящей из водорода и SO3H, при условии, что, по меньшей мере, один из R1 и R3 выбран как SO3H; (B) по меньшей мере, одного ингибитора, представляющего собой нитрофенол; В предпочтительном варианте осуществления ингибирующая система также включает в себя, по меньшей мере, один амин и, по меньшей мере, один дополнительный ингибитор, выбранный из группы, состоящей из нитроксильных соединений и нитрозоанилинов. Если R2 – углеводородный радикал, то это предпочтительно алкил или алкенил прямой или разветвленной цепи, содержащий от 1 до 50 атомов углерода, более предпочтительно от 1 до 18 углеводородных атомов, включая, но не ограничиваясь ими: метил, этил, пропил, бутил, пентил, гексил, гептил, октил, 2-этил-гексил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, олеил, нонадецил, эйкозил, генейкозил, докозил, трикозил, тетракозил, пентакозил, триаконтил, изомеры вышеназванных (такие как, например, изопропил, втор-бутил, неопентил и т.д.) и подобные; или циклические алкильные группы, такие как циклопентил, циклогексил, циклогептил, циклооктил и циклододецил. Нитрофенолы, которые могут быть использованы при осуществлении настоящего изобретения, включают, но не ограничиваются ими: 2,6-динитро-4-метилфенол, 2-нитро-4-метилфенол, 2,4-динитро-1-нафтол, 2,4,6-тринитрофенол (пикриновая кислота), 2,4-динитро-6-метилфенол, 2,4-динитрофенол, 2,4-динитро-6-втор-бутилфенол, 4-циано-2-нитрофенол, 3-иодо-4-циано-5-нитрофенол, м-нитро-п-крезол, 2,6-динитро-п-крезол и подобные. 2,4-Динитро-6-втор-бутилфенол является предпочтительным. Если ингибирующая система, соответствующая настоящему изобретению, содержит дополнительно ингибитор, представляющий собой нитроксильное соединение, то данное нитроксильное соединение, – предпочтительно, стабильный стерически-нагруженный нитроксильный компонент, имеющий структурную формулу:
где R4 и R7 независимо выбираются из группы, состоящей из водорода, алкила и гетерозамещенного алкила, и R5 и R6 независимо выбираются из группы, состоящей из алкила и гетерозамещенного алкила; и X1 и X2 (1) независимо выбираются из группы, состоящей из галогена, циано, COOR7, -S-COR7, -OCOR7, (где R7 алкил или арил), амидо, -S-C6H5, карбонил, алкенил или алкил, содержащие от 1 до 15 атомов углерода, или (2) оба формируют циклическую структуру, содержащую азот. В частном предпочтительном варианте осуществления стабильный стерически-нагруженный нитроксильный компонент имеет структурную формулу:
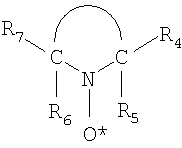
где R4 и R7 независимо выбираются из группы, состоящей из водорода, алкила и гетерозамещенного алкила, и R5 и R6 независимо выбираются из группы, состоящей из алкила и гетерозамещенного алкила, и
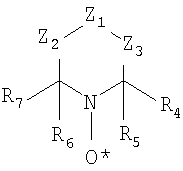
часть (изображенная выше) представляет собой атомы, соединенные в пяти-, шести- или семичленный гетероцикл. Соответственно, один из нескольких классов циклических нитроксидов, который может быть использован при осуществлении настоящего изобретения, может быть представлен следующей структурной формулой:
где Z1, Z2 и Z3 независимо выбираются из группы, состоящей из кислорода, серы, вторичных аминов, третичных аминов, фосфора в различных степенях окисления и замещенных или незамещенных углеродных атомов, таких как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHOH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CR8OR9, >CHNR8R9, >CCONR8R9, >C=NOH, >C=CH-C6H5, >CF2, >CCl2, >CBr2, >CI2, >CR8PR13R14R15 и подобных, где R8 и R9 независимо выбирают из группы, состоящей из водорода, алкила, арила и ацила, и R13, R14 и R15 независимо выбираются из группы, состоящей из неподеленной электронной пары, алкила, арила, =О, OR16 и NR17R18, где R16, R17 и R18 независимо выбираются из группы, состоящей из водорода, алкила и арила. Если R8 и/или R9 – алкилы, то предпочтительно, чтобы они были низшими алкилами (т.е. содержащими от одного до пяти атомов углерода, например метил, этил, пропил, бутил, пентил и их изомеры). Если R8 и/или R9 арилы, то предпочтительно, чтобы они были арилами, содержащими от 6 до 10 атомов углерода, например фенил или нафтил, которые к тому же могут быть замещены группами, обладающими низким стерическим эффектом, например низшими алкилами, галогенами и подобным. Если R8 и/или R9 – ацилы, то предпочтительно, чтобы они были ацилами следующей структуры:
где R19 алкил, арил, OR20 или NR20R21, и где R20 и R21 – алкилы, арилы, или
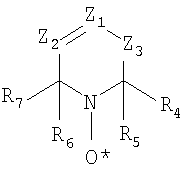
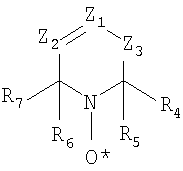
где R22 – алкил или арил. Если R19, R20, R21 или R22 алкилы, то предпочтительно алкилы, содержащие от 1 до 15 атомов углерода, более предпочтительно, низшие алкилы, содержащие от 1 до 5 атомов углерода, как описано выше. Если R19, R20, R21 или R22 арилы, то предпочтительно арилы, содержащие от 6 до 10 атомов углерода, как описано выше. Другой из остальных классов циклических нитроксидов, который может быть использован при осуществление настоящего изобретения, может быть представлен следующей структурной формулой:
где Z1 и Z2 – одинаковые или разные группы: азот или замещенные, или незамещенные атомы углерода, такие как =C(H)-, =C(CH3)-, =C(COOH)-, =C(COOCH3)-, =C(COOC2H5)-, =C(OH)-, =C(CN)-, =C(NR8R9)-, =C(CONR8R9)- и подобное, и где Z3, R8 и R9, – как описано выше. Циклические нитроксиды, использованные при осуществлении настоящего изобретения, могут также быть пятичленными циклическими производными. Эти соединения со структурной формулой:
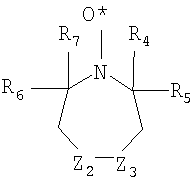
где Z2 и Z3 – одинаковые или разные группы: сера, кислород, вторичные амины, третичные амины, фосфор в разных степенях окисления или замещенные или незамещенные атомы углерода, такие как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHOH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CR8OR9, >CHNR8R9>, >CCONR8R9, >C=NOH, >C=CH-C6H5, CF2, CCl2, CBr2, CI2, >CR8PR13R14R15 и подобные, где разные R, как описано выше. Циклические нитроксиды, использованные при осуществлении настоящего изобретения, могут также иметь структуру:
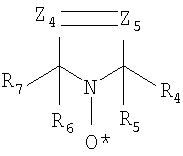
где Z4 и Z5 – одинаковые или различные группы, которые могут быть азотом или замещенным или незамещенным углеродным атомом, такие как =C(H)-, =C(CH3)-, =C(COOH)-, =C(COOCH3)>, =C(COOC2H5)-, =C(OH)-, =C(CN)-, =C(NR8R9)-, =C(CONR8R9)- и подобные, где R8 и R9, как описано выше. Другой класс циклических нитроксидов, которые могут быть использованы при осуществлении настоящего изобретения, представлен структурной формулой:
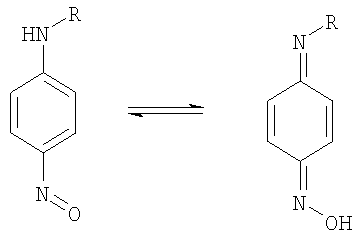
где Z2 и Z3 одинаковые или разные группы: сера, кислород, вторичные амины, третичные амины или замещенные или незамещенные атомы углерода, такие как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHOH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CHNR8R9, >CONR8R9, >R8OR9, >C=NOH, >C=CH-C6H5, CF2, CCl2, CBr2, CI2, >CR8PR13R14R15 и подобные, где разные R-группы, как описано выше. Также две или более нитроксильные группы могут быть представлены в одной и той же молекуле, например, путем связывания через одну или более Z частей посредством связующей группы E, как описано в патенте US Как было указано выше, для всех приведенных выше нитроксильных структур R4 и R7 независимо выбираются из группы, состоящей из водорода, алкила и гетерозамещенного алкила, и R5 и R6 независимо выбираются из группы, состоящей из алкила и гетерозамещенного алкила. Такие алкильные (или гетерозамещенный алкил) группы от R4 до R7 могут быть одинаковыми или разными и предпочтительно содержать от 1 до 15 углеродных атомов, например метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил и подобные, и их изомеры, например трет-бутил, 2-этилгексил и подобные. Более предпочтительно, если радикалы от R4 до R7 независимо выбираются из низших алкилов (или гетерозамещенных низших алкилов), содержащих от одного до 5 атомов углерода (например, метил, этил, пропил, бутил, пентил и их изомеры). Если гетерозаместители имеют место быть, то они могут, например, включать галоген, кислород, серу, азот и подобные. Наиболее предпочтительно, если все радикалы от R4 до R7 являются метилами. Примеры подходящих нитроксидных свободных радикалов, которые могут использоваться в комбинации с донорами водорода или электроноакцепторами при осуществлении настоящего изобретения, включают, но не ограничиваются ими: N,N-ди-трет-бутилнитроксид; N,N-ди-трет-амилнитроксид; N-трет-бутил-2-метил-1-фенил-пропилнитроксид; N-трет-бутил-1-диэтилфосфоно-2,2-диметилпропилнитроксид; 2,2,6,6-тетраметилпиперидинилокси; 4-амино-2,2,6,6-тетраметилпиперидинилокси; 4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-оксо-2,2,6,6-тетраметилпиперидинилокси; 4-диметиламино-2,2,6,6-тетраметилпиперидинилокси; 4-этаноилокси-2,2,6,6-тетраметилпиперидинилокси; 2,2,5,5-тетраметилпирролидинилокси; 3-амино-2,2,5,5-тетраметилпирролидинилокси; 2,2,4,4-тетраметил-1-окса-3-азациклопентенил-3-окси; 2,2,4,4-тетраметил-1-окса-3-пирролинил-1-окси-3-карбоновая кислота; 2,2,3,3,5,5,6,6-октаметил-1,4-диазациклогексил-1,4-диокси; 4-бро-2,2,6,6-тетраметилпиперидинилокси; 4-хлоро-2,2,6,6-тетраметилпиперидинилокси; 4-иодо-2,2,6,6-тетраметилпиперидинилокси; 4-фтор-2,2,6,6-тетраметилпиперидинилокси; 4-циано-2,2,6,6-тетраметилпиперидинилокси; 4-карбокси-2,2,6,6-тетраметилпиперидинилокси; 4-карбометокси-2,2,6,6-тетраметилпиперидинилокси; 4-карбоэтокси-2,2,6,6-тетраметилпиперидинилокси; 4-циано-4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-метил-2,2,6,6-тетраметилпиперидинилокси; 4-карбоэтокси-4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-гидрокси-4-(1-гидроксипропил)-2,2,6,6-тетраметилпиперидинилокси; 4-метил-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбометокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбоэтокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-амино-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-амидо-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 3,4-дикето-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4-оксиимино-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4-бензилиден-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4,4-дибромо-2,2,5,5-тетраметилпирролидинилокси; 2,2,3,3,5,5-гексаметилпирролидинилокси; 3-карбоксимидо-2,2,5,5-тетраметилпирролидинилокси; 3-оксиимино-2,2,5,5-тетраметилпирролидинилокси; 3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-циано-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-карбометокси-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-карбоэтокси-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 2,2,5,5-тетраметил-3-карбоксамидо-2,5-дигидроксипиррол-1-оксил; 2,2,5,5-тетраметил-3-амино-2,5-дигидропиррол-1-оксил; 2,2,5,5-тетраметил-3-карбоэтокси-2,5-дигидропиррол-1-оксил; 2,2,5,5-тетраметил-3-циано-2,5-дигидропиррол-1-оксил; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)сукцинат, бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)адипат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)себацинат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)н-бутилмалонат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)фталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)изофталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)терефталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)гексагидротерефталат; N,N’-бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)адипамид; N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)капролактам; N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)додецилсукцинамид; 2,4,6-трис-[N-бутил-N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)]с-триазин; 4,4′-этилен-бис(1-оксил-2,2,6,6-тетраметилпиперазин-3-он); и подобные. Использованная здесь аббревиатура TEMPO означает 2,2,6,6-тетраметил-1-пиперидинилокси. Таким образом, 4-амино-TEMPO означает 4-амино-2,2,6,6-тетраметил-1-пиперидинилокси; 4-гидрокси-TEMPO – это 4-гидрокси-2,2,6,6-тетраметил-1-пиперидинилокси (также известный в науке/технике как HTEMPO); 4-оксо-TEMPO означает 4-оксо-2,2,6,6-тетраметил-1-пиперидинилокси; и т.д. Предпочтительно, когда одним членом комбинации, используемой при осуществлении настоящего изобретения, является 4-амино-TEMPO, 4-оксо-TEMPO, 4-гидрокси-TEMPO или TEMPO. Комбинации из двух или более вышеназванных, например 4-амино-TEMPO и 4-оксо-TEMPO, также могут использоваться. Такие стабильные нитроксидные свободные радикалы могут быть получены по известным способам. (См., например, патенты US Когда ингибирующая система, соответствующая настоящему изобретению, дополнительно содержит ингибитор – нитрозоанилин, то это может быть N-нитрозоанилин или C-нитрозоанилин. Предпочтительно, нитрозоанилиновой компонентой является C-нитрозоанилин. C-нитрозоанилины могут быть приготовлены путем C-нитрозирования соответствующих анилинов в любом стандартном варианте, используемом для C-нитрозирования ароматических аминов. Например, реакция амина с холодной азотистоводородной кислотой приводит к N-нитрозосоединению, которое перегруппировывается в п-нитрозоанилин под действием избытка соляной кислоты. В некоторых случаях более эффективно проводить нитрозирование и перегруппировку в одну стадию, проводя реакцию в метаноле в присутствии избытка хлороводорода в безводных условиях. Этот способ описан в патенте US
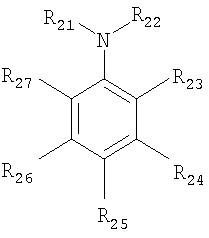
См., например, Sidgwick, N.V., The Organic Chemistry of Nitrogen, Third Edition, Clarendon Press, Oxford, 1966. Так могут присутствовать обе формы, в основном, в растворе при повышенных температурах, и можно ожидать наличие вклада в ингибирующую активность обеих этих форм. Нитрозоанилины, которые могут использоваться при осуществлении настоящего изобретения, предпочтительно, имеют структуру:
где R21 и R22 независимо выбираются из группы, состоящей из водорода, алкила, арила, ацила, гидроксила, алкокси, нитрозо и сульфонила, или R21 и R22 могут формировать цикл – арил, циклоалкил, полиарил или гетероцикл; радикалы от R23 до R27 независимо выбираются из группы, составленной из водорода, алкила, арила, ацила, гидроксила, алкокси, ацилокси, NR28(R29), нитро, нитрозо, галоген и сульфонил, или любые две соседние R’s могут формировать цикл – арил, циклоалкил, полиарил или гетероцикл, при условии, что, по меньшей мере, один из радикалов от R23 до R27 должен быть нитрозогруппой; и R28 и R29 независимо выбираются из группы, составленной из водорода, алкила, арила, ацила и нитрозо. Предпочтительно, R28 – водород и R29 – алкил. Если ингибирующая система, соответствующая настоящему изобретению, включает дополнительный ингибитор – амин, то амин может быть первичным, вторичным или третичным и может содержать алкильные группы, арильные группы или их комбинации. Такие амины включают, но не ограничиваются ими: Этиленненасыщенный мономер, преждевременная полимеризация и рост цепи полимера, который является объектом настоящего изобретения, может быть любым таким мономером, для которого случайная полимеризация и/или рост полимерной цепи в процессе его производства, хранения и/или распределения является проблемой. Среди мономеров, для которых будет полезно применение настоящего изобретения: стирол, Этиленненасыщенные мономеры необязательно должны быть постоянно стабилизированы наличием ингибитора(ов) специально, когда мономеры нагреваются, как, например, при перегонке, но возможность их стабилизации рассматривается тогда, когда при наличии ингибитора(ов) A) в статической системе заметно увеличивается время, в течение которого мономеры можно нагревать до начала полимеризации и/или роста цепи полимера, B) в динамической системе количество образовавшегося полимера при постоянной температуре остается постоянным во времени, и/или C) скорость роста полимерной цепи полимера значительно меньше, чем в отсутствие системы, ингибирующей полимеризацию. По опыту современной науки/техники понятно, что, по желанию, ловушки свободных радикалов могут быть включены в варианты осуществления настоящего изобретения. Например, могут добавляться: воздух или O2, как описано в патенте US Ингибиторы полимеризации могут вводиться в мономер для защиты посредством любых действенных процедур. Они могут, например, добавляться в виде концентрированного раствора в подходящем растворителе или другими возможными методами. Также индивидуальные ингибирующие компоненты могут вводиться по отдельности в перегонную систему вместе с подающимся материалом и/или через отдельные и разные точки поступления при условии, что реализуется эффективное распределение ингибирующей композиции. Так как ингибиторы постепенно расходуются в процессе перегонки, важно поддерживать соответствующие количества ингибиторов в перегонном аппарате, добавляя их в процессе перегонки. Добавление ингибиторов может осуществляться или непрерывно, или время от времени, для того, чтобы поддержать концентрацию ингибитора выше минимально допустимого уровня. Как правило, общая концентрация ингибиторов лежит в области от ~1 до ~2000 м.д. по отношению к ингибируемому мономеру; предпочтительно, от ~5 до ~1000 м.д., в зависимости от используемых условий. Отношения количества первого компонента (A) ко второму (B), взятые по отношению к сумме этих двух компонент, от ~1 до ~100 вес.% A: от ~99 до ~0 вес.% B; предпочтительно, около 25-75 вес.% A: около 75-25 вес.% B; более предпочтительно, около 50-75 вес.% A: около 50-25 вес.% B. Преимущества и важные особенности настоящего изобретения будут лучше видны из следующих примеров. ПРИМЕРЫ Пример 1 Концентрированная H2SO4 (280 г, 2,8 моль) была помещена в однолитровую колбу, снабженную механической мешалкой, термопарой, рубашкой нагрева, холодильником и пластиковой трубкой. Кислота предварительно нагревалась до 40°C и 300 г о-втор-бутилфенола (OSBP) (2 моль) быстро загружался через пластиковую трубку так, чтобы система нагрелась до 82°C. Через 40 мин после того, как начальная температура 40°C достигала 82°C, реакционная смесь подогревалась для поддержания температуры 82°C. Так дополнительно выдерживалось 1 ч 45 мин. Продукт, сульфированный OSBP (SOSBP), использовался вместе с DNBP для проведения тестовых экспериментов ингибитора. Пример 2 Ингибирующие и ретардантные свойства этого материала по отношению к стиролу были измерены при проведении Continuous Dynamic Reboiler Test, регистрируя образование полимера с помощью УФ-спектрометрии. В соответствии с этим экспериментом, ингибитор добавляется к стиролу (мономер), предварительно очищенному от трет-бутилкатехола (TBC) перегонкой. Стирол (180 г) помещается в колбу, погруженную в масляную баню. Температура стирола обычно равна 116°C. В процессе эксперимента свежий материал подается в колбу со скоростью 3 г/мин, и в то же время с той же скоростью материал забирается из колбы. Постоянный режим продолжается, пока не наступит равновесие. Для режима с прекращением подачи материала – подача и отвод прерываются. При постоянном режиме образцы берутся каждый час, при режиме с прекращением подачи материала – каждые 5-10 мин. Через 5 часов постоянного режима с концентрациями 50 м.д./100 м.д. SOSBP/DNBP регистрировалось 0,0007% полимера, в то время как при 1,5 ч режима с прекращением подачи материала – 0,024% полимера. Пример 3 В процессе Continuous Dynamic Reboiler Test SOSBP/NMP/DNBP при концентрациях соответственно 250 м.д./285 м.д./250 м.д. регистрируется 0,0039 полимера при постоянном режиме и 0,25% полимера через два часа после прекращения подачи материала. NMP (1-метил-2-пирролидинон) добавлялся для нейтрализации кислого SOSBP. Пример 4 В процессе Continuous Dynamic Reboiler Test SOSBP/DNBP при концентрациях соответственно 250 м.д./250 м.д. регистрируется 0,0004% полимера через 5 ч при постоянном режиме и 0,025% полимера – через два часа после прекращения подачи материала. Пример 5 В процессе Continuous Dynamic Reboiler Test N,N-диэтил-4-нитрозоанилин/SOSBP/NMP/DNBP при концентрациях соответственно 100 м.д./250 м.д./170 м.д./250 м.д. регистрируется 0,0038% полимера через 5 ч при постоянном режиме и 0,315% полимера – через два часа после прекращения подачи материала. Пример 6 В процессе Continuous Dynamic Reboiler Test 4-оксо-TEMPO/SOSBP/NMP/DNBP при концентрациях соответственно 100 м.д./250 м.д./187 м.д./250 м.д. регистрируется 0,0004% полимера через 5 ч при постоянном режиме и 0,016% полимера через два часа после прекращения подачи материала. Пример 7 В процессе Continuous Dynamic Reboiler Test одного DNBP при концентрации 500 м.д. регистрируется 0,11% полимера при постоянном режиме и 1,18% полимера – через два часа после прекращения подачи материала. Ввиду многих изменений и модификаций, которые могут быть осуществлены без отступления от принципов, лежащих в основе настоящего изобретения, для понимания области защиты, которая реализуется изобретением, акцент должен делаться на прикрепленные формулы изобретения.
Формула изобретения
1. Способ ингибирования преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества комбинации из (А) по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы 2. Способ по п.1, в котором R2 – алкил или алкенил прямой или разветвленной цепи, содержащий от 1 до 50 атомов углерода. 3. Способ по п.2, в котором R2 выбирается из группы, состоящей из: метил, этил, пропил, бутил, пентил, гексил, гептил, октил, 2-этил-гексил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, олеил, нонадецил, эйкозил, генейкозил, докозил, трикозил, тетракозил, пентакозил, триаконтил, изомеры вышеназванных: циклопентил, циклогексил, циклогептил, циклооктил и циклододецил. 4. Способ по п.2, в котором R2 – втор-бутил. 5. Способ по п.1, в котором нитрофенол выбирается из группы, состоящей из: 2,6-динитро-4-метилфенол, 2-нитро-4-метилфенол, 2,4-динитро-1-нафтол, 2,4,6-тринитрофенол (пикриновая кислота), 2,4-динитро-6-метилфенол, 2,4-динитрофенол, 2,4-динитро-6-втор-бутилфенол, 4-циано-2-нитрофенол, 3-иодо-4-циано-5-нитрофенол, м-нитро-п-крезол и 2,6-динитро-п-крезол. 6. Способ ингибирования преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества комбинации из (А) по меньшей мере, одного ингибитора, представляющего собой сульфированный фенол общей формулы 7. Способ по п.6, в котором R2 – алкил или алкенил прямой или разветвленной цепи, содержащий от 1 до 50 атомов углерода. 8. Способ по п.7, в котором R2 выбирается из группы, состоящей из: метил, этил, пропил, бутил, пентил, гексил, гептил, октил, 2-этил-гексил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, олеил, нонадецил, эйкозил, генейкозил, докозил, трикозил, тетракозил, пентакозил, триаконтил, изомеры вышеназванных: циклопентил, циклогексил, циклогептил, циклооктил и циклододецил. 9. Способ по п.7, в котором R2 – втор-бутил. 10. Способ по п.6, в котором нитрофенол выбирается из группы, состоящей из: 2,6-динитро-4-метилфенол, 2-нитро-4-метилфенол, 2,4-динитро-1-нафтол, 2,4,6-тринитрофенол (пикриновая кислота), 2,4-динитро-6-метилфенол, 2,4-динитрофенол, 2,4-динитро-6-втор-бутилфенол, 4-циано-2-нитрофенол, 3-иодо-4-циано-5-нитрофенол, м-нитро-п-крезол и 2,6-динитро-п-крезол. 11. Способ по п.6, в котором (С) – стабильный стерически-нагруженный нитроксильный компонент, имеющий структурную формулу 12. Способ по п.6, в котором (С) – нитрозоанилин с общей формулой 13. Способ по п.6, в котором (D) выбирается из группы, состоящей из: 14. Композиция для ингибирования преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающая в себя комбинацию из: 15. Композиция по п.14, в которой R2 – алкил или алкенил прямой или разветвленной цепи, содержащий от 1 до 50 атомов углерода. 16. Композиция по п.15, в которой R2 выбирается из группы, состоящей из: метил, этил, пропил, бутил, пентил, гексил, гептил, октил, 2-этил-гексил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, олеил, нонадецил, эйкозил, генейкозил, докозил, трикозил, тетракозил, пентакозил, триаконтил, изомеры вышеназванных, циклопентил, циклогексил, циклогептил, циклооктил и циклододецил. 17. Композиция по п.14, в которой нитрофенол выбирается из группы, состоящей из: 2,6-динитро-4-метилфенол, 2-нитро-4-метилфенол, 2,4-динитро-1-нафтол, 2,4,6-тринитрофенол (пикриновая кислота), 2,4-динитро-6-метилфенол, 2,4-динитрофенол, 2,4-динитро-6-втор-бутилфенол, 4-циано-2-нитрофенол, 3-иодо-4-циано-5-нитрофенол, м-нитро-п-крезол и 2,6-динитро-п-крезол. 18. Композиция по п.14, в которой (С) – стабильный стерически-нагруженный нитроксильный компонент, имеющий структурную формулу 19. Композиция по п.14, в которой (С) – нитрозоанилин с общей формулой 20. Композиция по п.14, в которой (D) выбирается из группы состоящей из:
|
||||||||||||||||||||||||||

 2867672 описывается, что полимеризация неингибированного стирола, конденсирующегося в виде жидкости на поверхностях, охватывающих газовую часть пространства выше уровня жидкости основной части стирола в реакторе, может быть минимизирована посредством распыления на поверхностях, окружающих газовую фазу, ингибитора полимеризации.
2867672 описывается, что полимеризация неингибированного стирола, конденсирующегося в виде жидкости на поверхностях, охватывающих газовую часть пространства выше уровня жидкости основной части стирола в реакторе, может быть минимизирована посредством распыления на поверхностях, окружающих газовую фазу, ингибитора полимеризации. -атомах углерода и (ii) от 99,95 до 95,5 вес.%, по отношению ко всей смеси (B), по меньшей мере, одного нитросоединения.
-атомах углерода и (ii) от 99,95 до 95,5 вес.%, по отношению ко всей смеси (B), по меньшей мере, одного нитросоединения.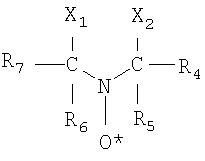

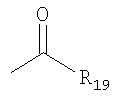
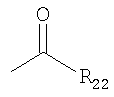
 -нафтиламин, изопропоксидифениламин, альдол-
-нафтиламин, изопропоксидифениламин, альдол-