|
|
(21), (22) Заявка: 2007101044/14, 18.07.2005
(24) Дата начала отсчета срока действия патента:
18.07.2005
(30) Конвенционный приоритет:
16.07.2004 GB 0416004.0
(43) Дата публикации заявки: 27.08.2008
(46) Опубликовано: 27.01.2010
(56) Список документов, цитированных в отчете о
поиске:
WO 91/06241, 16.05.1991. WO 00/04386, 27.01.2000. WO 2005/039405, 06.05.2005. SU 1096557, 07.06.1984. SU 1117519, 07.10.1984.
(85) Дата перевода заявки PCT на национальную фазу:
16.02.2007
(86) Заявка PCT:
GB 2005/002820 20050718
(87) Публикация PCT:
WO 2006/008505 20060126
Адрес для переписки:
191186, Санкт-Петербург, а/я 230, “АРС-ПАТЕНТ”, пат.пов. С.В.Новоселовой
|
(72) Автор(ы):
ОМТВЕЙТ Торе (NO),
МИРТАХЕРИ Пейман (NO)
(73) Патентообладатель(и):
АЛЕРТИС МЕДИКАЛ АС (NO)
|
(54) ЭЛЕКТРОХИМИЧЕСКИЙ ДАТЧИК ДЛЯ ИЗМЕРЕНИЙ IN VIVO ИЛИ EX VIVO ПАРЦИАЛЬНОГО ДАВЛЕНИЯ ДИОКСИДА УГЛЕРОДА В ЖИВЫХ ТКАНЯХ
(57) Реферат:
Изобретение относится к медицинской диагностике. Датчик для измерения pCO2 включает закрытую камеру, ограниченную по меньшей мере частично мембраной, проницаемой для диоксида углерода. Внутри камеры имеются два электрода. Камера содержит жидкость, по существу свободную от электролита, в контакте с электродами и мембраной. Жидкость содержит неионное вспомогательное вещество, чтобы предотвратить вытекание воды вследствие осмотического градиента через используемую мембрану. Технический результат заключается в повышении точности измерения за счет исключения явления различия осмотичности между органом и жидкостью в камере датчика. 3 з.п. ф-лы, 1 табл., 5 ил.
Область техники
Изобретение касается физиологического датчика, в частности датчика парциального давления диоксида углерода (углекислого газа) (pCO2), например, in vivo или ex vivo, например, на поверхностях тканей тела или органов или внутри них.
Предшествующий уровень техники
Ишемия представляет собой медицинский термин, характеризующий нехватку кровоснабжения органа. В серьезных случаях это может привести к гибели пораженной ткани (инфаркту). Для измерения в ткани pCO2, которое является параметром, значительно увеличивающимся в течение ранних и обратимых стадий ишемии, может быть создан датчик. Такой датчик предпочтительно обеспечивает способность идентифицировать начало ишемии посредством данных в реальном времени.
Ишемия является самой распространенной причиной смерти в западном мире. Таким образом, например, инфаркт миокарда, инфаркт мозга и другие состояния, характеризующиеся гипоперфузией одного или более органов, являются главными факторами смертности.
Реперфузия, или устранение ишемии, часто возможна, если ишемия обнаружена вовремя. Таким образом, раннее обнаружение ишемии с последующим соответствующим химическим лечением (например, такими препаратами, как стрептокиназа, урокиназа или t-PA, которые служат для лизиса тромбов или эмболов) или хирургическим вмешательством может спасти пораженный орган, а также жизнь пациента.
В то время как сердце можно контролировать непрерывно в отношении ишемии, используя электрокардиографию (ЭКГ), другие органы могут стать серьезно ишемизированными и подвергнуться необратимому повреждению прежде, чем будет обнаружены симптомы. Действительно многие органы “молчат”, когда наступает ишемия. Явление бессимптомного инфаркта миокарда теперь хорошо известно. Кроме того, печень и почка могут быть серьезно ишемизированы без серьезных симптомов прежде, чем повреждение органа станет необратимым.
Известно, что существует определенная связь между pCO2 в органе или на его поверхности и наличием ишемии в этом органе. В ходе метаболического ацидоза ткани, например, в ходе анаэробного метаболизма, который встречается при ишемии в любом органе или ткани, образуются большие количества диоксида углерода. CO2 в реальных условиях свободно проникает через мембрану клетки, и, поскольку в потоке крови, отходящей от пораженной ишемией ткани, CO2 отсутствует или его количество снижено, происходит увеличение содержания CO2 в ишемизированной ткани, и pCO2 в ишемизированной ткани или на ней увеличивается. Вообще, в здоровом органе максимум pCO2 в крови (венозная кровь) составляет 7-10 кПа, а максимум pCO2 в здоровой (аэробной) ткани составляет приблизительно на 1-6 кПа выше, хотя максимумы могут изменяться от органа к органу, например, 8-12 кПа для почки, 7-11 кПа для печени, 8-12 кПа для серозы кишечника, и 12-19 кПа для слизистой оболочки кишечника. Там, где снабжение кислородом падает ниже критического уровня, значения pCO2, измеренные в ткани, могут повыситься в 3-10 раз, и увеличенные уровни pCO2 ясно указывают на анаэробный метаболизм и, следовательно, на ишемию.
Простой датчик, в частности, пригодный для измерения рСО2, например, как одно из средств контроля ишемии, описан в WO 00/04386.
Этот датчик включает закрытую камеру, ограниченную по меньшей мере частично мембраной, по существу непроницаемой для воды, но проницаемой для диоксида углерода. Камера содержит по меньшей мере два электрода и пленку по существу свободной от электролита жидкости, например деионизированной воды. Жидкость контактирует с мембраной и обоими электродами таким образом, что углекислый газ, проникающий через мембрану, увеличивает концентрацию ионов бикарбоната в жидкости и, следовательно, ее проводимость.
Изобретатели установили, что при некоторых обстоятельствах даже по существу водонепроницаемая мембрана может сделать возможным проникновение жидкости через мембрану, если имеется достаточно большой осмотический градиент через мембрану. Например, если датчик используется in vivo, достаточно большое осмотическое давление через мембрану может быть вызвано различием в осмотичности между органом и жидкостью в камере, что заставляет воду проникать через мембрану. Это нежелательно, поскольку отражается на концентрации ионов бикарбоната в камере.
Раскрытие изобретения
Настоящее изобретение нацелено на решение этой недавно установленной проблемы.
В первом аспекте изобретение предлагает физиологическое измерительное устройство (датчик) для измерения pCO2, причем устройство включает:
закрытую камеру, ограниченную по меньшей мере частично мембраной, проницаемой для диоксида углерода; и
по меньшей мере два электрода внутри камеры,
причем камера содержит жидкость, по существу свободную от электролита, находящуюся в контакте с электродами и мембраной, и
жидкость содержит неионное вспомогательное вещество.
Таким образом, согласно изобретению, жидкость в камере содержит неионное вспомогательное вещество. Этим способом может быть увеличена осмотичность жидкости в камере для предотвращения перетекания жидкости через мембрану, без влияния на электрические характеристики жидкости.
Вспомогательное вещество должно иметь по меньшей мере изотоническую концентрацию, то есть должно быть изоосмотическим с водным раствором 0,9 % мас./об. NaCl. Таким образом, осмотичность вспомогательного вещества в камере может быть больше, чем осмотичность 0,9 % мас./об. водного NaCl, предпочтительно больше, чем осмотичность 1,8 % мас./об. водного NaCl (в два раза больше, чем изотоническая концентрация). Могут использоваться осмотичности больше, чем осмотичность 4,5 % мас./об. водного NaCl (в пять раз больше, чем изотоническая концентрация), или даже больше, чем осмотичность 9 % мас./об. водного NaCl (в десять раз больше, чем изотоническая концентрация).
Можно использовать любое подходящее вспомогательное вещество, которое является инертным для реакции бикарбоната в камере. Вспомогательное вещество также должно быть растворимым в жидкости, например воде. Желательно также, чтобы вспомогательное вещество представляло собой общепринятый фармацевтический эксципиент для внутривенного применения и с низкой вязкостью, чтобы заполнение камеры было простым. Вспомогательное вещество предпочтительно должно допускать стерилизацию и быть устойчивым при хранении. Желательно, чтобы вспомогательное вещество ингибировало рост микроорганизмов.
Подходящим вспомогательным веществом является полиэтиленгликоль (ПЭГ), и в настоящее время предпочтительным вспомогательным веществом является пропиленгликоль.
Термин “по существу свободная от электролита” означает, что жидкость имеет ионную осмотичность не больше, чем осмотичность при 37°С 5 мМ водного раствора хлористого натрия, предпочтительно не больше, чем осмотичность 500 мкМ раствора хлористого натрия, более предпочтительно не больше, чем осмотичность 10-5-10-6 М раствора HCl.
Предпочтительно жидкость в контакте с электродами является водной, и особенно предпочтительно жидкость представляет собой воду, по существу свободную от электролита, как определено выше. Аналогично могут использоваться другие растворители, которые реагируют с CO2 с увеличением или уменьшением их проводимости, например, путем генерирования или нейтрализации ионов. На практике, однако, было найдено, что особенно хорошо действуют деионизированная или дистиллированная вода с добавлением или без добавления сильной кислоты (например, HCl) в концентрации 0,1-100 мкМ, предпочтительно 0,5-50 мкМ, более предпочтительно приблизительно 1 мкМ. Функция этой небольшой добавки кислоты вообще заключается в поддержании pH жидкости в диапазоне 6 или ниже, чтобы избежать существенных вкладов в проводимость за счет гидроксильных ионов и поддержать линейность измерений pCO2.
Главными компонентами датчика рСО2 являются электродная камера, мембрана, проницаемая для CO2, образующая по меньшей мере часть стенки электродной камеры, причем первый и второй электроды имеют поверхности в пределах указанной камеры (или образуют внутренние поверхности указанной камеры), и жидкость (вообще, по существу свободная от электролита вода) в электродной камере в контакте с мембраной и первым и вторым электродами. Датчик включает источник питания переменного тока, устройство измерения проводимости (или сопротивления), генератор сигнала (который может быть частью устройства измерения) и, возможно, передатчик сигнала, или выполнен с возможностью присоединения к указанным устройствам.
Механизм, с помощью которого определяют pCO2 с использованием датчика по изобретению, является простым. В чистом протонном растворителе, например воде, электрическое сопротивление является высоким из-за малочисленности ионов. Добавление СО2 приводит к образованию (с водой) ионов H+ и HCO– 3 и, таким образом, к уменьшению электрического сопротивления. Поскольку единственным фактором, ответственным за уменьшение сопротивления в датчике, является CO2, проходящий через мембрану, то изменение сопротивления позволяет измерить pCO2. 3 и, таким образом, к уменьшению электрического сопротивления. Поскольку единственным фактором, ответственным за уменьшение сопротивления в датчике, является CO2, проходящий через мембрану, то изменение сопротивления позволяет измерить pCO2.
Из константы равновесия для уравнения Н2О+СО2 H++НСО3 H++НСО3 – концентрация СО2 равна – концентрация СО2 равна  рСО2 (где значение рСО2 (где значение  при 25°С равно 0,310). Электрическая проводимость для протонов равна при 25°С равно 0,310). Электрическая проводимость для протонов равна 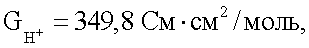 для гидроксилов для гидроксилов 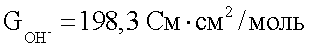 и для бикарбоната равна и для бикарбоната равна 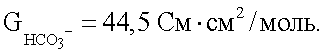 Концентрации H+ и ОН– изменяются обратно пропорционально, а концентрации H+ и НСО3 Концентрации H+ и ОН– изменяются обратно пропорционально, а концентрации H+ и НСО3 – – прямо пропорционально величине рСО2. Общая проводимость раствора таким образом фактически пропорциональна рСО2, так как вклад ОН– является минимальным. Проводимость раствора Gраствора таким образом представлена уравнением – – прямо пропорционально величине рСО2. Общая проводимость раствора таким образом фактически пропорциональна рСО2, так как вклад ОН– является минимальным. Проводимость раствора Gраствора таким образом представлена уравнением

где 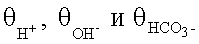 представляют собой коэффициенты активности для трех разновидностей ионов. представляют собой коэффициенты активности для трех разновидностей ионов.
Таблица 1 ниже показывает пример измеренных значений рСО2 и рН и соответствующие расчетные значения концентраций H+, ОН– и НСО3 –, демонстрируя увеличение H+ и НСО3 –, демонстрируя увеличение H+ и НСО3 – с увеличением pCO2. – с увеличением pCO2.
| Таблица |
| Номер образца |
рСО2 (кПа) |
pH |
[Н+] (ммоль/л) |
[ОН–] (ммоль/л) |
[НСО3 –] (ммоль/л) –] (ммоль/л) |
| 1 |
6,38 |
5,141 |
7,23Е-06 |
1,38Е-09 |
7,23Е-06 |
| 2 |
9,64 |
5,060 |
8,71Е-06 |
1,15Е-09 |
8,71Е-06 |
| 3 |
15,37 |
4,891 |
1,29Е-05 |
7,78Е-10 |
1,29Е-05 |
| 4 |
25,88 |
4,760 |
1,74Е-05 |
5,75Е-10 |
1,74Е-05 |
| 5 |
31,48 |
4,664 |
2,17Е-05 |
4,61Е-10 |
2,17Е-05 |
(pCO2 и pH измерены с помощью стандартного анализатора газа в крови AB L(R) System 625 при 37°С).
Электрическую проводимость измеряют в пленке растворителя в датчике по изобретению. Это может быть сделано путем подачи постоянного напряжения (или тока) на электроды и измерения изменений тока (или напряжения), которые соответствуют изменениям проводимости при поступлении CO2 в растворитель через мембрану. Предпочтительно, однако, подавать переменное синусоидальное напряжение с постоянным максимальным значением и измерять падение напряжения на электродах. Проводимость раствора тогда равна току, проходящему через электрод, деленному на падение напряжения на электродах.
Датчик pCO2 может функционировать при подаче переменного электрического напряжения на электроды, посредством чего возникает переменный ток в жидкости. Жидкость должна реагировать с углекислым газом с изменением его проводимости. Электрическое напряжение может иметь частоту 20-10000 Гц, предпочтительно 100-4000 Гц.
Датчики pCO2 по изобретению снабжены или выполнены с возможностью присоединения к электрическому источнику питания, выполненному с возможностью подачи на электроды переменного электрического напряжения с частотой 100-10000 Гц. Частота предпочтительно более 1 кГц. Частота предпочтительно меньше 5 кГц, более предпочтительно менее 2 кГц. При частотах ниже 100 Гц чувствительность определения рСО2 ниже из-за электрополяризации, и, кроме того, отклик прибора становится чрезмерно медленным, тогда как при частотах более 10 кГц чувствительность снова меньше из-за низкого сопротивления емкостей в датчике.
Источником питания может быть источник питания переменного тока или, как вариант, источник постоянного тока в соединении с генератором, то есть комбинация, которая вместе составляет источник питания переменного тока.
Источник электропитания предпочтительно представляет собой такой источник, чтобы максимальная плотность тока через жидкость у электродов была не более 50 А/м2, предпочтительно не более 30 А/м2, более предпочтительно не более 20 А/м2, в частности не более 10 А/м2, и наиболее предпочтительно приблизительно 1 А/м2 или ниже. Более высокие значения плотности тока 20 А/м2 или более должны использоваться только при более высоких частотах, например, 1-10 кГц. Наименьшая максимальная плотность тока определяется пределами обнаружения, но применяются значения до 10-8 А/м2. Однако наименьшая максимальная плотность тока вообще равна по меньшей мере 0,1 мкА/м2.
Работая при таких плотностях тока и частотах напряжения, и при соответствующей конструкции, датчик может определить проводимость/сопротивление жидкости, в которую мигрирует CO2, без какой-либо по значительной потери точности, возникающей в результате электрополяризации электродов.
Для очень высокой точности напряжение или ток на электродах (и, следовательно, сопротивление или проводимость жидкости между электродами) определяют, используя синхронный усилитель, установленный на ту же самую частоту, что и частота генератора напряжения или электрического источника питания.
Кроме того, предпочтительно включение в схему обнаружения высокочастотного фильтра, чтобы отсекать ток с частотой менее 100 Гц, предпочтительно менее 150 Гц. Фильтр предпочтительно представляет собой пассивный фильтр, например конденсатор и резистор.
Источник питания и электрическая схема детектора, если желательно, могут быть включены в датчик по изобретению. В этом случае, если желательно, чтобы датчик являлся беспроводным, он предпочтительно также снабжается средствами, позволяющими обнаружить сигнал на расстоянии, например, передатчиком, в частности, радиопередатчиком. В этом случае датчик может быть имплантирован, например пациентам с повышенным риском.
Может быть предусмотрен дополнительный электрод, электрически соединенный с пациентом, например с кожей пациента. Сигнал от этого дополнительного электрода может обрабатываться вместе с сигналом от датчика для компенсации электромагнитного шума от пациента.
Эффекты электрополяризации значительно уменьшаются при увеличении площади поверхности электродов, находящихся в контакте с жидкостью, например, при размещении электродов в ячейках, расположенных вдали от плоскости мембраны, или при использовании неплоских поверхностей электрода, например грубых или текстурированных поверхностей. Поэтому вообще желательно иметь как можно большее отношение площади поверхности электрода к площади жидкого контакта, насколько это возможно, и как можно меньшую толщину слоя жидкости над как можно большей площадью контакта с мембраной. При этом уменьшаются время отклика и электрополяризация, могут использоваться более низкие частоты, и влияние емкостей рассеяния также значительно уменьшаются.
Увеличение электрического сопротивления относительно сопротивления электродов может быть достигнуто путем сокращения площади поперечного сечения электрического потока через жидкость между электродами в зоне, в которой жидкость находится в контакте с мембраной, например, уменьшая толщину слоя жидкости для части электрического потока между электродами, и/или путем обеспечения относительно большой площади контакта между каждым электродом и жидкостью.
Сопротивление жидкости у мембраны и между электродами может быть увеличено при использовании структурных элементов, образующих границы жидкостных каналов через мембрану между электродами, например, располагая мембрану поперек или рядом с изолирующей частью стенки камеры, в которой такие каналы образованы, например, с помощью травления. Аналогично между мембраной и стенкой камеры может располагаться пористая прокладка, образующая границы толщины слоя жидкости.
Действительно, такие прокладки важно использовать там, где в условиях испытываемого давления мембрана является достаточно гибкой, и толщина слоя жидкости за мембраной слишком мала для того, чтобы измерить проводимость при изменении давления.
В предпочтительной конструкции датчик включает:
корпус датчика, имеющий продольную ось;
по меньшей мере два электрода, расположенные на расстоянии друг от друга в направлении, поперечном к продольной оси корпуса датчика;
множество опорных элементов, вытянутых наружу от оси корпуса датчика и образующих между смежными опорными элементами по меньшей мере один жидкостный канал, который обеспечивает прохождение жидкости между электродами; и
газопроницаемую мембрану, поддерживаемую опорными элементами и образующую внешнюю стенку жидкостного канала.
Эта конструкция обеспечивает компактную конфигурацию датчика с продольной геометрией, которая пригодна для введения в орган. Кроме того, опорные элементы способны обеспечить физическую поддержку мембраны, так же как образование границ жидкостных каналов с малой площадью поперечного сечения, которые позволяют провести точное измерение.
Для уменьшения эффекта электрополяризации, упомянутого выше, электроды могут располагаться в полости корпуса датчика, которая имеет бóльшую площадь поперечного сечения, чем жидкостные каналы. При этом плотность тока вокруг электродов уменьшается за счет большого объема жидкости.
Электроды датчика могут быть вытянуты в длину, например, параллельно продольной оси корпуса датчика.
Точно так же жидкостный канал или каналы могут быть поперечными, например, перпендикулярными продольной оси корпуса датчика. В предпочтительной конструкции датчик включает множество жидкостных каналов. Например, датчик может включать по меньшей мере три жидкостных канала.
Опорные элементы могут располагаться поперек продольной оси корпуса датчика. Например, опорные элементы могут быть перпендикулярны продольной оси корпуса датчика в периферическом направлении. В предпочтительной конструкции опорные элементы имеют форму колец, образованных вокруг продольной оси корпуса датчика. Поперечное сечение опорных элементов может быть любой подходящей формы. Было найдено, что, в частности, опорные элементы с по существу треугольным, в частности, пилообразным поперечным сечением, особенно легко формируются с помощью литья под давлением. С другой стороны, может использоваться по существу прямоугольное поперечное сечение. Опорные элементы могут быть сформированы как единое целое с корпусом датчика, например, с помощью литья под давлением. Датчик предпочтительно включает по меньшей мере четыре опорных элемента.
Корпус датчика и/или датчик могут вообще быть цилиндрическими. Мембрана может быть устроена таким образом, чтобы окружать тело датчика.
Описанная геометрия может быть применена к любому подходящему датчику. В предпочтительной конструкции датчик представляет собой датчик pCO2.
Если датчик сконструирован с использованием жидкостной пленки, электроды предпочтительно изготовлены из или покрыты таким инертным материалом, что удельное сопротивление жидкости не изменяется значительно при хранении. Подходящие материалы включают платину (особенно платиновую чернь), золото, серебро, алюминий и углерод. Золото особенно предпочтительно. В общем, предпочтительны инертные электроды, которые не выделяют сольватированные ионы.
Мембрана может быть изготовлена из любого материала, который является проницаемым для CO2, и по существу непроницаемым для растворителя жидкости, любого электролита и воды. Могут использоваться политетрафторэтиленовые, например, из Тефлона®, силиконового каучука, полисилоксановые, полиолефиновые или другие изолирующие полимерные пленки, например, толщиной от 0,5 до 250 мкм. Чем толще мембрана, тем вообще медленнее отклик датчика. Однако чем тоньше мембрана, тем больше опасность неоднородности или пробивки или другого повреждения. Удобно, однако, когда мембрана имеет толщину 1-100 мкм, предпочтительно 50-100 мкм.
Стенки камеры датчика по изобретению могут быть изготовлены из любого подходящего материала, например пластмассы. Предпочтительно материал должен быть способен выдерживать условия, обычно используемые при стерилизации, например при радиационной стерилизации (например, с использованием гамма-излучения) или тепловой стерилизации (например, при температуре около 121°С, которая используется при стерилизации в автоклаве). В случае тепловой стерилизации жидкость вообще является стерильной при заполнении датчика после стерилизации. Стенки камеры и мембраны могут быть изготовлены из того же самого материала, например Тефлона®, обработанного таким образом, чтобы иметь самоподдерживающиеся стенки и более тонкую газопроницаемую мембрану.
Датчики по изобретению вообще относительно недороги и поэтому, в отличие от известных датчиков, могут быть устройствами одноразового применения. Кроме того, электродная камера может быть сделана чрезвычайно маленькой без особых трудностей (в отличие от известного стеклянного электрода, содержащего датчики, для которых миниатюризация создает неразрешимые проблемы с сопротивлением).
Эта конструкция представляет собой датчик, в частности датчик рСО2, который может быть легко введен в ткань животного, включая человека, который может оставаться в ткани в ходе процесса контроля и который может быть легко удален после завершения контроля.
Устройство является достаточно маленьким, чтобы не причинять чрезмерного беспокойства контролируемой ткани. Соответственно устройство может иметь максимальный диаметр 2 мм, предпочтительно 1 мм.
В соответствии с настоящим изобретением легко изготовить датчики, имеющие размер и конфигурацию, особенно подходящие для измерений рСО2 на поверхности органа, протока или ткани или в органе, протоке или ткани, например в мозге, сердце, печени, почке, кишке или мускуле. Это представляет особенный интерес, поскольку дает возможность проверить работу органа, протока или ткани, например, в течение и после трансплантации, при интенсивной терапии, после травм, и т.д. и таким образом позволяет проводить раннее обнаружение ишемий.
Парциальное давление, определенное датчиком, может быть значением, определенным количественно, или это может быть просто указанием на то, что рСО2 является выше или ниже одного или более пороговых значений, указывающих на ишемию или ее отсутствие, значений, которые могут отличаться согласно положению места измерения рСО2.
Датчик может использоваться для однократного измерения рСО2 или более предпочтительно может использоваться для непрерывного или повторяющегося контроля, особенно у пациентов с повышенным риском, например пациента при интенсивной терапии, подвергающегося или выздоравливающего после операции по трансплантации ткани или органа, с установленной нестабильной стенокардией, выздоравливающего после операции коронарного шунтирования артерии, страдающего от травмы (например, скелетной мышцы), или страдающего от гиповолемии (например, удара).
Устройство может включать набор датчиков для измерения соответствующих физиологических параметров. Например, устройство может включать комплект датчиков. Такие датчики могут измерять одно или более значений парциального давления диоксида углерода, парциального давления кислорода, температуры, pH или, например, концентрации глюкозы. В настоящем предпочтительном воплощении устройство включает температурный датчик и датчик pCO2.
Краткое описание графических материалов
Теперь будет описан вариант осуществления настоящего изобретения, только с целью примера, со ссылкой на сопровождающие графические материалы, в которых:
Фиг.1 представляет собой блок-схему всей системы датчиков, включающей датчик по изобретению;
Фиг.2 представляет собой блок-схему, иллюстрирующую принцип измерения для датчика в системе на Фиг.1;
Фиг.3 представляет собой частичный разрез датчика по изобретению;
Фиг.4 представляет собой разрез по линии А-А на Фиг.3;
Фиг.4а представляет собой увеличенный вид детали, обозначенной кругом на Фиг.4; и
Фиг.5 представляет собой вид датчика на Фиг.3 с удаленной мембраной.
Осуществление изобретения
В соответствии с настоящим изобретением, система датчиков pCO2 включает одноразовый блок 1 датчиков, блок 2 электронной панели и блок 3 контроля, как показано на Фиг.1.
Одноразовый блок 1 датчиков поставляют упакованным и стерилизованным. Он состоит из защищенного мембраной кондуктометрического датчика 4 с диаметром менее 1 миллиметра, и температурного датчика 5, объединенного в блоке датчика. Провода 6 с помощью соединителя электрически соединяют датчик 4 и щуп 5 с блоком 2 электронной панели. Как вариант, между блоком 1 датчиков и блоком 2 панели может быть обеспечена беспроводная связь.
Блок 2 электронной панели посылает сигналы к блоку и получает сигналы от блока 1 датчиков. Он размещается на коже пациента, осуществляет обработку сигнала и передает подготовленный сигнал на контрольно-управляющий блок 3.
Контрольно-управляющий блок 3 построен на основе портативного персонального компьютера 7 с платой 8 ввода/вывода PCMCIA и программным обеспечением Labview (доступно от National Instruments Corporation of Austin, Texas).
Датчик 4 pCO2 используется для измерения уровня (парциального давления) CO2 (рСО2) в жидкости, в соответствии с принципом измерения, проиллюстрированным на Фиг.2. Измерительная камера состоит из двух небольших каналов 9 с одним электродом 10, помещенным в каждый канал. Эти два канала 9 связаны одним или более проходами 11, окруженными полупроницаемой мембраной 12, то есть мембраной, которая позволяет переносить только CO2 внутрь датчика 4 и из него. Весь объем датчика заполнен деионизированной водой и 5% пропиленгликоля. Проводимость в воде зависит от рСО2, и, измеряя проводимость между электродами 10 в объеме, можно получить информацию о рСО2.
Как показано на Фиг.3-5, блок 1 датчиков включает пластмассовый корпус 23, изготовленную с помощью литья под давлением, который является по существу цилиндрическим и окружен полупроницаемой мембраной 12. Корпус 23 имеет конический наконечник 24 на своем дистальном конце и часть 25 корпуса, которая вытянута от наконечника 24. На части 25 корпуса установлены путем приклеивания два золотых электрода 10. Электроды 10 вытянуты в длину вдоль противоположных сторон части 25 корпуса и расположены в соответствующих углублениях в части 25 корпуса.
Между наконечником 24 и частью 25 корпуса выполнен выступ 26 в форме усеченного конуса для фиксации мембраны 12. Соответствующий выступ 26 также выполнен на проксимальном конце части 25 корпуса. Мембрана 12 может быть приклеена к корпусу 23, но важно, чтобы клей, используемый для фиксации мембраны 12 и электродов 10, был подобран такой, чтобы он не выделял ионы в заполненную водой камеру, образованную между частью 25 корпуса 23 и мембраной 12. Кроме того, уплотняющие поверхности корпуса 23 могут быть сделаны по желанию гидрофобными, чтобы избежать образования водной пленки, в которую могут выделяться ионы.
Мембрана 12 может также быть прикреплена к корпусу 23 посредством обжимного соединения и мягкой прокладки, если необходимо. Мембрана 12 сама может действовать как прокладка, особенно если мембрана 12 выполнена из силиконового каучука. Для обжимного соединения может использоваться термоусадочная муфта. С другой стороны, в местах, соответствующих местоположениям фиксирующего выступа 26, могут использоваться металлические обжимные кольца.
Часть 25 корпуса 23 снабжена множеством ребер 27, которые сформированы в виде пилообразного профиля для легкости литья под давлением. Ребра 28 обеспечивают механическую опору мембраны 12, а также образуют границы жидкостных проходов 11, требуемых для эффективного функционирования датчика 4. Между каждым электродом 10 и жидкостными проходами, образованными между ребрами 27, предусмотрен резервуар 9, сформированный углублением, в котором расположен электрод 10. Резервуар 9 обеспечивает область относительно низкой плотности тока вокруг электродов 10 для уменьшения эффектов электрополяризации.
В процессе изготовления мембрану 12 закрепляют на корпусе 23, устройство погружают в деионизированную воду и раствор пропиленгликоля так, чтобы камера, ограниченная мембраной 12, электродами 10, и ребрами 27, была полностью заполнена жидкостью. Таким образом, эта камера формирует датчик рСО2, как показано схематично на Фиг.2.
Возможно, чтобы датчик включал больше чем одну измерительную камеру. Например, с каждой стороны корпуса 23 могут быть предусмотрены два параллельных электрода 10, разделенные стенкой. Таким образом образуется камера датчика между одним электродом 10 с одной стороны корпуса 23 через жидкостные проходы 11 между ребрами 27 сверху корпуса 23 к одному из электродов 10 с другой стороны опоры 23. Соответствующая камера датчика предусмотрена между другим электродом 10 и жидкостными проходами 11 в нижней части корпуса 23. Электрод 10 от каждой из этих камер может быть электрически связан с соответствующим электродом от другой камеры так, чтобы электрический сигнал от датчика отражал проводимость обеих камер.
В проксимальный конец корпуса 23 встроен температурный датчик 5 в виде термопары. Температурный датчик 5 используется и для корректировки вычислений рСО2 и для измерения температуры ткани, которые отображаются в блоке 3 и содержат информацию для медицинского диагноза. Температурный датчик 5 имеет наименьший диапазон измерения 33-42°С и наименьшую точность ±0,2°С.
Плоский кабель 6 электрически и механически связан с электродами 10 и температурным датчиком 5. Электроды 10 сформированы в виде продолжения проводов плоского кабеля 6. С другой стороны, электроды могут быть сформированы путем нанесения покрытия на корпус 23. Там, где кабель 6 и соединение с корпусом 23 достаточно крепкие, кабель 6 может применяться для вытягивания блока 1 датчиков из положения, в котором он использовался. С другой стороны, для обеспечения прочной внешней механической связи может быть предусмотрен шнур из кевлара, например, встроенный в плоский кабель 6.
Мембрана 12 может быть вытянута в проксимальном направлении от корпуса 23 с кабелем 6 с образованием катетера вокруг кабеля 6. С другой стороны, может быть предусмотрен отдельный катетер 28. В этом случае, катетер 28 связан с опорой 23 вблизи электродов 10 и мембраны 12.
Конец катетера, объединенный с датчиком 4, помещают на 0,5-4 см в ткань органа при хирургических процедурах, чтобы контролировать ишемию в течение периода вплоть до двух недель. Датчик может использоваться в ортопедической и восстановительной хирургии, и в таких органах, как печень, почки, сердечная мышца, мозг и кишечник. Может использоваться инструмент ввода (не показан) для того, чтобы ввести датчик 4, и могут использоваться вспомогательные средства для фиксации наконечника датчика в определенном положении.
Блок 1 датчиков имеет максимальный диаметр 1 мм, и максимальное расстояние от наконечника катетера до элемента датчика составляет 2 мм. Датчик 4 имеет наименьший диапазон измерения рСО2 2-25 кПа, с минимальной определяемой разностью рСО2 0,2 кПа. Максимальное время ответа датчика 4 составляет 20 секунд. Максимальный допустимый ток измерения в любой области жидкостной камеры является таким, что j<1 мА/см2, в то время как входное измерительное напряжение составляет не более 50 милливольт.
Электроды 10 покрыты золотом, и их общая площадь составляет приблизительно 0,3 мм2. Частота измерения fизмерения должна быть выше 100 Гц. При более низких частотах эффекты поляризации в измерительной камере оказывают сильное влияние на измерения. При частотах более 10 кГц существенной проблемой становится низкое сопротивление емкостей. Сопротивление измерения Rизмерения находится в диапазоне от 500 кОм до 7 МОм.
Датчик 4 электрически соединен с блоком 2 электронной панели, установленной на коже пациента, с помощью плоского кабеля 6, который имеет длину от 5 см до 1 метра. Максимальный диаметр кабеля/катетера составляет 1 мм, и предпочтительная длина кабеля/катетера составляет 25 см. Кабель/катетер является мягким и гибким, чтобы чрезмерно не беспокоить примыкающую ткань и органы. Кабель/катетер и его соединения являются также достаточно прочными, чтобы противостоять значительным силам натяжения, которые могут возникнуть при правильном и неправильном использовании.
При стерилизации, хранении и транспортировке блок 1 датчиков покрыт деионизированной, стерильной водой, не содержащей эндотоксинов, чтобы гарантировать, что там не существует никакой потери воды из резервуара датчика.
Как показано на Фиг.1 и 2, блок 2 электронной панели включает генератор 13 синусоидального напряжения, который обеспечивает напряжение по меньшей мере 5 вольт и электропитание 50 мВ и питается от батареи 14. Фильтр 15 предназначен для фильтрации или усреднения сигнала на входе в синхронный усилитель 16. Может использоваться пассивный фильтр, который уменьшает расход тока. Предусилитель 17 объединен с сервомеханизмом для удаления компоненты постоянного тока из сигнала с целью уменьшения эффектов электролиза. Согласно конструкции сервомеханизма, выходной сигнал предусилителя подается обратно на его вход через фильтр нижних частот. Таким образом, обратно подаются только компоненты постоянного тока с выхода и компенсируют любой постоянный ток, прошедший через датчик рСО2. Этим способом обеспечивается отсутствие прохождения через датчик рСО2 какого-либо постоянного тока, который повредил бы электроды. Операционный усилитель, используемый на этой стадии, потребляет минимальный ток и имеет большое значение CMMR (коэффициент подавления синфазного сигнала). В то же самое время ток смещения минимален. Синхронный усилитель 16 усиливает сигнал переменного тока от датчика 4. Это может быть достигнуто с помощью операционных усилителей или с использованием комплекта интегральных схем по меньшей мере с 1%-ой точностью для обнаружения сигнала при частотах ниже 1 кГц. Гальваническое разделение 19, например, оптопара или катушечное соединительное устройство предназначено для предотвращения передачи шума от контрольно-управляющего блока 3 и связанного с ним кабеля 18. Предпочтение обычно отдается оптопаре из-за соотношения шум-сигнал. Блок 20 усиления и подготовки температурного сигнала предназначен для усиления сигнала от температурного датчика 5. Электронный блок 2 питается от перезаряжаемой и заменяемой батареи 14 стандартного типа. Емкость батареи достаточна для 14 дней непрерывной работы. Блок 2 также снабжен светодиодным индикатором 21 вкл/выкл и индикатором состояния батареи (не показан). Связь между блоком 2 и контрольно-управляющим блоком 3 является аналоговой и осуществляется через экранированный кабель 18. Однако блок панели 2 может включать аналого-цифровой преобразователь, так что связь между блоком панели 2 и блоком контроля 3 может быть цифровой, например, осуществляться с помощью цифровой проводной или цифровой беспроводной передачи. Кабель 18 имеет длину по меньшей мере 4 м и является легким и гибким.
Как показано на Фиг. 1 и 2, переменный ток производится генератором 13 синусоидального напряжения и подается на один из электродов 10 датчика рСО2 и на синхронный усилитель 16. Высокочастотный сигнал от другого электрода 10 датчика рСО2 подается через фильтр 15 на малошумящий усилитель 17 и оттуда на синхронный усилитель 16, где он сравнивается с опорным сигналом, производимым генератором 13 синусоидального напряжения. Несовпадающие по фазе компоненты, то есть нежелательные компоненты сигнала, отбрасываются, а остальная часть сигнала усиливается. Усиленный сигнал пропорционален рСО2 (или проводимости) и передается для записи или дальнейшей обработки на контрольно-управляющий блок 3.
Блок 2 электронной панели может также быть электрически связан с электродом сравнения (не показан), который электрически связан с кожей пациента. Сигнал от электрода сравнения может использоваться, чтобы скомпенсировать сигналы от блока 1 датчиков для воздействия на электромагнитный шум, производимый пациентом.
Отдельный блок 2 может получать сигналы от нескольких блоков 1 датчиков и обеспечивать мультиплексный вывод данных на блок 3.
Блок 3 включает портативный персональный компьютер 7, включающий CD-RW и инфракрасный порт, а также плату 8 ввода/вывода PCMCIA и может обрабатывать сигналы по меньшей мере от 4 различных блоков 2 одновременно. Плата 8 PCMCIA может иметь встроенную негальваническую связь. Источник электропитания 22 для блока 3 одобрен с медицинской точки зрения и работает при напряжении как 110 В, так и 230 В.
Функции программного обеспечения блока контроля 3 могут быть осуществлены в пакете программ Labview, доступном от National Instruments of Austin, Texas, и могут обрабатывать данные от 4 различных блоков панели одновременно. Программное обеспечение предоставляет средство для калибровки датчика(ов) с тремя точками калибровки и калибровочной функцией второго порядка. Программное обеспечение может быть изменено, чтобы поддержать любое другое число точек калибровки и тип калибровочной функции. Программное обеспечение также имеет средство сглаживания сигнала от датчика 4 в определенные интервалы времени. Можно иметь по меньшей мере два сигнальных уровня измеряемых значений и два сигнальных уровня для их градиентов. Градиенты измеряемых значений рассчитываются для индивидуально определенных интервалов времени. Сигнал тревоги является видимым и слышимым. Можно остановить индикацию сигнала тревоги при сохранении других активных сигналов тревоги. Контрольно-управляющий блок 3 может регистрировать все измеренные значения, установки параметров и сигналы тревоги в течение всей сессии. При интервале регистрации данных, равном 30 секундам по меньшей мере для 10 двухнедельных сессий, должно иметься устройство хранения на жестком диске. Запись сессии может быть сохранена на перезаписываемый компакт-диск в формате, читаемом Microsoft Excel.
Резюмируя, физиологический датчик для измерения рСО2 включает закрытую камеру, ограниченную по меньшей мере частично мембраной, проницаемой для диоксида углерода. Внутри камеры находятся два электрода. Камера содержит жидкость, по существу свободную от электролита, находящуюся в контакте с электродами и мембраной. Жидкость содержит неионное вспомогательное вещество, чтобы предотвратить вытекание воды из-за осмотического градиента через используемую мембрану.
Формула изобретения
1. Датчик для измерения парциального давления диоксида углерода в живых тканях (pCO2), включающий:
закрытую камеру, ограниченную по меньшей мере частично мембраной, проницаемой для диоксида углерода; и
по меньшей мере два электрода внутри камеры,
причем камера содержит жидкость, по существу, свободную от электролита, т.е. имеющую ионную осмотичность не больше, чем осмотичность при 37°С 5 мМ водного раствора хлористого натрия, находящуюся в контакте с электродами и мембраной, и
жидкость содержит неионное вспомогательное вещество.
2. Датчик по п.1, отличающийся тем, что неионное вспомогательное вещество представляет собой пропиленгликоль.
3. Датчик по п.1, отличающийся тем, что жидкость, по существу, свободна от электролита, является деионизованной или дистиллированной водой.
4. Датчик по п.1, отличающийся тем, что неионное вспомогательное вещество присутствует в жидкости, по существу свободной от электролита, по меньшей мере в изотонической концентрации, то есть осмолярность жидкости в камере по меньшей мере эквивалентна концентрации 0,9%-ного раствора хлорида натрия.
РИСУНКИ
|
|