|
(21), (22) Заявка: 2007144412/15, 29.11.2007
(24) Дата начала отсчета срока действия патента:
29.11.2007
(43) Дата публикации заявки: 10.06.2009
(46) Опубликовано: 20.01.2010
(56) Список документов, цитированных в отчете о
поиске:
Адрес для переписки:
194156, Санкт-Петербург, пр. Пархоменко, 15, ФГУ “ФЦСКИЭ им. В.А. Алмазова Росмедтехнологии”, патентный отдел
|
(72) Автор(ы):
Иванов Владимир Игоревич (RU),
Дорофейков Владимир Владимирович (RU),
Вавилова Ангелина Викторовна (RU)
(73) Патентообладатель(и):
Федеральное государственное учреждение “Федеральный центр сердца, крови и эндокринологии имени В.А. Алмазова Федерального агентства по высокотехнологичной медицинской помощи” (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТРОМБОТИЧЕСКОГО ЭФФЕКТА АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ
(57) Реферат:
Изобретение относится к аналитической химии, а именно к контролю за эффективностью антиагрегантной терапии при лечении сердечно-сосудистых заболеваний. Основным антитромботическим препаратом в лечении обострений ишемиической болезни сердца до настоящего времени остается ацетилсалициловая кислота (АСК). Вместе с тем, от 4 до 45% пациентов оказываются биохимически резистентными к ее действию. Предлагаемый способ количественного определения антитромботического эффекта АСК in vitro основан на измерении параметров индуцированной агрегации тромбоцитов непосредственно в цельной крови импедансным методом до и после инкубации проб с АСК. Способ позволяет повысить чувствительность, точность, воспроизводимость, сократить временя анализа. 1 ил.
Изобретение относится к актуальной проблеме современной клинической и профилактической медицины – контролю за эффективностью антиагрегантной терапии при лечении сердечно-сосудистых заболеваний, в частности острого коронарного синдрома (ОКС) и инфаркта миокарда (ИМ).
Основным антитромботическим препаратом в лечении обострений ишемиической болезни сердца (ИБС) до настоящего времени остается ацетисалициловая кислота (АСК), имеющая чрезвычайно выгодное соотношение «пользы и стоимости» лечения [3]. Независимая от других вмешательств способность АСК снижать смертность больных ИМ была убедительно продемонстрирована в многочисленных международных исследованиях (ISIS-2, IST, CAST).
Вместе с тем, в последние годы установлено, что существует большая категория больных, у которых АСК неспособна в должной мере подавлять функциональную активность тромбоцитов и у которых, несмотря на прием препарата, возникают ишемические осложнения. По данным разных авторов от 4 до 45% пациентов оказываются биохимически резистентными к действию АСК [5, 7, 9].
Рутинное исследование антитромботического эффекта ацетилсалициловой кислоты в значительной мере тормозится отсутствием в клинике методов ее адекватной лабораторной диагностики. Известные способы оценки индивидуальной чувствительности больных к АСК (по времени капиллярного кровотечения, по уровню экскреции 11-дегидро-тромбоксана В2) малоспецифичны и имеют недостаточную воспроизводимость [5].
Наиболее близким аналогом (прототипом) данного изобретения является способ оценки эффективности приема АСК [1] по ее влиянию на параметры индуцированной различными агонистами агрегации кровяных пластинок в богатой тромбоцитами плазме (метод оптической агрегатометрии Борна [6]). Метод позволяет количественно оценивать скорость и амплитуду процесса агрегации in vitro. Для изучения антиагрегационных свойств в пробирку с обогащенной тромбоцитами плазмой предварительно вносили раствор АСК в конечной концентрации в кювете 25 мМ и инкубировали в течение 10 минут. Затем вносился индуктор (АДФ или адреналин) и регистрировалась агрегация в течение 10 минут. Результаты сравнивались с показателями агрегации, вызванной индукторами без предварительного воздействия АСК, с вычислением суммарного индекса агрегации тромбоцитов (СИАТ).
Основными недостатками указанного способа являются: 1) низкие чувствительность и точность метода, что обусловливает необходимость использования высоких концентраций АСК и объясняет отсутствие положительных результатов при использовании в качестве агониста АДФ; 2) длительность, трудоемкость и критичность [4, 8] процесса приготовления богатой тромбоцитами плазмы (БТП); 3) в ходе центрифугирования кровяные пластинки подвергаются значительным механическим воздействиям, которые существенно изменяют их функциональную состоятельность и приводят к потере фракции наиболее крупных и активных клеток; 4) на этапе пробоподготовки нарушается естественное окружение тромбоцитов, что не позволяет учитывать влияние на них других форменных элементов крови, специфически модулирующих функции тромбоцитов; 5) увеличивается вероятность значительного снижения концентрации лабильных медиаторов к моменту измерения [8]. Все это не позволяет создать оптимальные стандартные условия, необходимые для обеспечения полной реализации функций тромбоцитов после стимулирования индуктором. Существенным недостатком оптической агрегатометрии является невозможность исследовать кровь больных с выраженной гиперлипидемией, часто встречающейся в кардиологической практике [8].
Предложенный способ отличается тем, что определение антитромботического эффекта ацетилсалициловой кислоты (АСК) проводят in vitro путем исследования функциональной активности тромбоцитов до и после инкубации образца биологического материала с ацетилсалициловой кислотой, а агрегационную активность тромбоцитов определяют в цельной крови импедансным методом, инкубацию образцов с ацетилсалициловой кислотой в конечной концентрации 108 мкмоль/л проводят в течение 15 минут, индукцию тромбоцитов вызывают аденозиндифосфатом в конечной концентрации 1,0-5,0 мкмоль/л.
Технический результат предложенного изобретения заключается в повышении чувствительности, точности, воспроизводимости способа, сокращении времени анализа.
При этом достигается следующий положительный эффект: 1) измерения проводятся при физиологических концентрациях АСК и аденозиндифосфата; 2) воспроизводимость определений соответствует требованиям, предъявляемым к медицинским методикам; 3) время анализа сокращается до 20 минут; 4) проводятся исследования в крови больных с гиперлипидемией.
Способ осуществляется следующим образом.
Образцы крови получают из антекубитальной вены и стабилизируются 3,8% раствором цитрата натрия в объемном отношении 9:1. В процессе исследования кровь сохраняют в закрытых пластиковых пробирках при комнатной температуре, с соблюдением общепринятых мер предосторожности при работе с клетками крови.
Анализ функциональной активности тромбоцитов осуществляют не ранее чем через 15 минут и не позднее чем через 2 часа после получения крови, с помощью импедансного агрегометра АИ-300, при 37°С и перемешивании содержимого кювет со скоростью 1000 об/мин. Соотношение объемов крови и агониста при этом составляет 11:1.
Для индуцирования агрегации используют раствор АДФ из диагностических наборов фирмы «Sigma» (Sigma diagnostics, platelet aggregation reagent, США) в конечной концентрации 1,0-5,0 мкмоль/л, приготовленный в соответствии с рекомендациями фирмы.
Исследования агрегационного статуса тромбоцитов каждого пациента проводят дважды: до и после инкубирования крови с АСК.
Время инкубирования составляет 15 минут при температуре 37°С. Физиологическая конечная концентрация АСК, соотношение объемов кровь-раствор АСК на этапе инкубации определялись из условия ингибирования агрегации аспирином в крови здоровых доноров (мужчин в возрасте 25-45 лет, n=26) на 50% и составляют 108 мкмоль/л и 50:1 соответственно. При этих условиях сохраняется возможность выявлять сдвиги, в обоих направлениях при возникновении дополнительных стимулов, а также получить оптимальную воспроизводимость результатов.
Обработка агрегатограмм производится по общепринятым характерным точкам кривых агрегации [2] с определением амплитуды процесса в омах к 5-й минуте от момента ввода АДФ, когда уже ясно видны чувствительность к дозе и интенсивность агрегации.
Ингибирующая (антитромботическая) способность АСК в процентах (С) рассчитывается по формуле
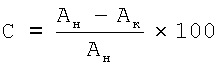 , ,
где Ан и Ак – амплитуды агрегации до и после инкубирования с АСК соответственно.
Пример обработки получаемых агрегатограмм и расчета по ним антитромботической способности АСК приведены на чертеже.
Апробацию метода осуществляли в клинике ФГУ Федеральный центр сердца, крови и эндокринологии им. В.А.Алмазова Росмедтехнологии. Обследовано 25 пациентов с ревматическими пороками сердца, контрольную группу составили 26 практически здоровых доноров (мужчины в возрасте 25-45 лет). Средняя величина ингибирующего эффекта АСК в контрольной группе составила 46,7%. В параллельной группе пациентов с ревматическими пороками сердца (n=25) 8,0% больных были абсолютно не чувствительны к АСК. Более низкий ингибирующий эффект АСК в этой группе наблюдался у больных (n=12) с тромбоэмболическими осложнениями (34,2% против 57,6%, p<0,05). Полученный результат свидетельствует о высоких диагностических возможностях способа и клинической необходимости определения антитромботического эффекта ацетилсалициловой кислоты при профилактике тромбозов и тромбоэмболии, являющихся ключевым моментом в развитии сердечно-сосудистых патологий.
Для оценки воспроизводимости и надежности предлагаемого способа мы осуществили параллельные измерения ингибирующей способности АСК в крови 28 пациентов. Коэффициент вариации теста составил 8,6% и соответствует требованиям, предъявляемым к медицинским лабораторным тестам.
Список использованной литературы
2. Гемостаз. Физиологические механизмы, принципы диагностики основных форм геморрагических заболеваний. Учеб. пособие. – СПб, 1999. – С.56.
3. Остроумова О.Д. Ацетилсалициловая кислота – препарат номер один для лечния сердечно-сосудистых заболеваний. Рус.Мед.Журнал. 2003. т.11,  5. – с.253-255. 5. – с.253-255.
5. Ушкалова Е.А. Аспиринорезистентность: механизмы развития, методы определения и клиническое значение. Фарматека. 2006.  13 (128). – с.35-41. 13 (128). – с.35-41.
Формула изобретения
Способ определения антитромботического эффекта ацетилсалициловой кислоты (АСК) in vitro путем исследования функциональной активности тромбоцитов до и после инкубации образца биологического материала с АСК, отличающийся тем, что инкубацию образцов с АСК в конечной концентрации 108 мкмоль/л проводят в течение 15 мин при температуре 37°С, индукцию тромбоцитов вызывают аденозиндифосфатом в конечной концентрации 1,0-5,0 мкмоль/л, агрегационную активность тромбоцитов определяют в цельной крови импедансным методом и по полученным агрегатограммам определяют амплитуды процесса агрегации в Омах к 5-й минуте от момента ввода аденозиндифосфата и рассчитывают антитромботическую способность АСК в процентах (С) по формуле
С=(Ан-Ак)/Ан·100,
где Ан и Ак – амплитуды агрегации до и после инкубирования с АСК.
РИСУНКИ
|