|
|
(21), (22) Заявка: 2006143571/04, 13.06.2005
(24) Дата начала отсчета срока действия патента:
13.06.2005
(30) Конвенционный приоритет:
21.06.2004 EP 04102837.4
(43) Дата публикации заявки: 27.07.2008
(46) Опубликовано: 10.01.2010
(56) Список документов, цитированных в отчете о
поиске:
RU 2197493 С2, 27.01.2003. WO 02083652 A1, 24.10.2002.
(85) Дата перевода заявки PCT на национальную фазу:
22.01.2007
(86) Заявка PCT:
EP 2005/006302 20050613
(87) Публикация PCT:
WO 2005/123738 20051229
Адрес для переписки:
191186, Санкт-Петербург, а/я 230, “АРС-ПАТЕНТ”, пат. пов. В.В.Дощечкиной
|
(72) Автор(ы):
ГЁТШИ Эрвин (CH),
ВИХМАНН Юрген (DE),
ВОЛЬТЕРИНГ Томах Йоханнес (DE)
(73) Патентообладатель(и):
Ф. ХОФФМАНН-ЛЯ РОШ АГ (CH)
|
(54) ПРОИЗВОДНЫЕ ПИРАЗОЛПИРИМИДИНА
(57) Реферат:
Изобретение относится к новым производным пиразолпиримидина формулы (I),
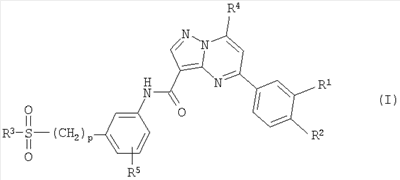
где р представляет собой 0 или 1; R1 и R2 могут независимо друг от друга представлять собой Н, галоген, низший алкил, низший алкокси, возможно замещенный одним или более чем одним галогеном или CF3; R3 представляет собой низший алкил, гидрокси-низший алкил или NRaRb; Ra и Rb независимо выбраны из группы, состоящей из Н; циклоалкила, содержащего 3-6 атомов углерода; фенила; низшего алкила, возможно замещенного одним или более чем одним гидрокси, фтором, С3-6циклоалкилом, фенилом, пиридилом или NRcRd, где Rc и Rd независимо выбраны из Н или низшего алкила; или где Ra и Rb вместе с атомом азота, к которому они присоединены, могут образовать 5- или 6-членный гетероцикл, возможно содержащий дополнительно 1 или 2 гетероатома, выбранных из О или N, и возможно замещенный низшим алкилом или гидрокси-низшим алкилом; R4 представляет собой Н, Cl, низший алкокси, циклоалкил, содержащий 3-6 атомов углерода, или неразветвленный низший алкил, который возможно замещен одним или более чем одним F; R5 представляет собой Н; галоген или низший алкил; а также к их фармацевтически приемлемым солям. Изобретение также относится к фармацевтическим композициям на основе этих соединений и их применению для изготовления лекарств для лечения или предотвращения острых и/или хронических неврологических нарушений, в которые вовлечена или играет роль активация mGluR2. 3 н. и 16 з.п. ф-лы.
Изобретение относится к производным пиразолпиримидина, способу их изготовления, их применению для лечения или предотвращения заболеваний, опосредованных метаботропными глутаматными рецепторами, их применению для приготовления лекарств для лечения таких заболеваний и содержащим их фармацевтическим композициям.
В частности, данное изобретение относится к производным пиразолпиримидина общей формулы I
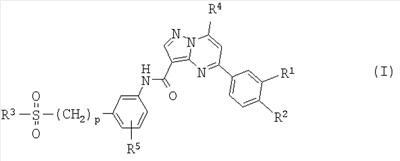
где
p представляет собой 0 или 1;
R1 и R2 могут независимо друг от друга представлять собой Н; галоген: низший алкил, возможно замещенный низшим алкокси; низший алкокси, возможно замещенный одним или более чем одним галогеном; или СF3;
R3 представляет собой низший алкил; гидрокси-низший алкил; или NRaRb;
Ra и Rb независимо выбраны из группы, состоящей из:
Н;
низший алкил, возможно замещенный одним или более чем одним гидрокси, фтором, циклоалкилом, арилом, гетероарилом или NRcRd, где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкил;
арил;
гетероарил;
или Ra и Rb могут образовать возможно замещенный 5- или 6-членный гетероцикл вместе с атомом азота, к которому они присоединены;
R4 представляет собой Н, Сl, низший алкокси, циклоалкил или неразветвленный низший алкил, который возможно замещен одним или более чем одним F:
R5 представляет собой Н; галоген или низший алкил;
а также их фармацевтически приемлемым солям,
за исключением соединений следующих формул:
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метилфенил)-N-[3-(4-морфолинилсульфонил)фенил];
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-N-[3-(4-морфолинилсульфонил)фенил]-5-фенил] и
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-мeтoкcифeнил)-N-[3-(4-мopфoлинилcyльфoнил)фeнил].
Три соединения, исключенные из объема формулы I, известны из химических библиотек. Эти три соединения никогда не упоминались в связи с метаботропными глутаматными рецепторами.
Было неожиданно обнаружено, что соединения общей формулы I являются антагонистами метаботропных глутаматных рецепторов. Соединения формулы I отличаются ценными терапевтическими свойствами.
В центральной нервной системе (ЦНС) передача стимулов происходит через взаимодействие нейромедиатора, посылаемого нейроном, с нейрорецептором.
L-глутаминовая кислота, наиболее распространенный нейромедиатор ЦНС, играет решающую роль в большом числе физиологических процессов. Рецепторы, зависящие от глутаматных стимулов, делятся на две основные группы. Первую основную группу образуют контролируемые лигандом ионные каналы. Метаботропные глутаматные рецепторы (mGluR, от metabotropic glutamate receptors) образуют вторую основную группу и, кроме того, принадлежат семейству рецепторов, связанных с G-белками.
В настоящее время известно восемь разных типов этих рецепторов mGluR, и некоторые из них еще разделены на подтипы. На основании структурных параметров, различия влияния на синтез вторичных метаболитов и различного сродства к низкомолекулярным химическим соединениям эти восемь рецепторов могут быть подразделены на три подгруппы; mGluR1 и mGluR5 принадлежат к группе I, mGluR2 и mGluR3 принадлежат к группе II, и mGluR4, mGluR6, mGluR7 и mGluR8 принадлежат к группе III.
Лиганды метаботропных глутаматных рецепторов, принадлежащих к группе II, могут быть использованы для лечения или предотвращения острых и/или хронических неврологических нарушений, таких как психоз, шизофрения, болезнь Альцгеймера, когнитивные расстройства и нарушения памяти. Другие состояния, которые можно лечить при этом, представляют собой ограниченную функцию мозга, вызванную операциями шунтирования или трансплантациями, недостаточное мозговое кровоснабжение, травмы спинного мозга, травмы головы, гипоксию, вызванную беременностью, остановку сердца и гипогликемию. Также состояния, которые можно лечить, – это хроническая и острая боль, хорея Хантингтона, боковой амиотрофический склероз (ALS, от amyotrophic lateral sclerosis), слабоумие, вызванное спидом, травмы глаз, ретинопатия, идиопатический паркинсонизм или лекарственный паркинсонизм, а также состояния, которые ведут к глутамат-недостаточным функциям, таким, например, как спазмы мышц, конвульсии, мигрени, недержание мочи, никотиновая зависимость, опиатная зависимость, тревога, рвота, дискинезия, депрессии и глиома, так как было обнаружено, что антагонисты mGluR2 снижают клеточную пролиферацию в клетках глиомы человека (J.Neurochem. March 2003, 84(6): 1288-95).
Предметом данного изобретения являются соединения формулы I и их фрамацевтически приемлемые соли сами по себе и в качестве фармацевтически активных субстанций, а также их изготовление, лекарства, основанные на соединении по изобретению, и их производство, а также применение соединений по изобретению для борьбы с заболеваниями указанного типа или их предотвращения, и соответственно, производства соответствующих лекарств.
Соединения формулы I могут также быть использованы в форме их пролекарств. Примерами являются эфиры, N-оксиды, фосфатные эфиры, гликоамидные эфиры, глицеридные конъюгаты и т.п. Пролекарства могут повысить ценность преимущества данных соединений в отношении всасывания, фрамакокинетики, распределения и транспорта в мозг.
Изобретение также относится к применению соединения формулы I по изобретению, включая соединения следующих формул:
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метилфенил)-N-[3-(4-морфолинилсульфонил)фенил];
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-N-[3-(4-морфолинилсульфонил)фенил]-5-фенил] и
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метоксифенил)-N-[3-(4-морфолинилсульфонил)фенил];
а также их фармацевтически приемлемых солей для лечения или предотвращения заболевания указанного типа, а также их применению в производстве соответствующих лекарств.
Если не указано иное, следующие термины, использованные в данном описании, имеют данные ниже определения.
Термин «низший алкил» обозначает прямоцепный или разветвленный насыщенный углеводородный остаток с 1-7 атомами углерода, предпочтительно с 1-4 атомами углерода, такими как метил, этил, н-пропил, изо-пропил, изо-бутил, трет-бутил и т.п.
Термин «гидрокси-низший алкил» обозначает остаток низшего алкила в смысле вышеприведенного определения, содержащий одну, две, три или четыре гидрокси группы, предпочтительно одну. Примеры остатков «гидрокси-низшего алкила» включают метанол, этанол, 1-пропанол, 2-пропанол, 3-пропанол, изо-бутанол и т.п.
Термин «низший алкенил» обозначает прямоцепные или разветвленные ненасыщенные углеводородные остатки с 2-7 атомами углерода, предпочтительно с 2-4 атомами углерода, такие как этенил или пропенил.
Термин «низший алкокси» обозначает остаток низшего алкила в смысле вышеприведенного определения, связанный через атом кислорода. Примеры остатков «низшего алкокси» включают метокси, этокси, изопропокси и т.п. Примеры низшего алкокси, замещенного одним или более чем одним галогеном, включают группы 2,2,2-трифторэтокси.
Термин «арил» относится к ароматической карбоциклической группе, состоящей из одного индивидуального цикла или одного или более конденсированных циклов, в которых по меньшей мере один цикл является ароматическим по своей природе. Предпочтительная арильная группа представляет собой фенил.
Термин «гетероарил» относится к ароматическому 5- или 6-членному циклу, содержащему один или более гетероатомов, выбранных из азота, кислорода или серы. Предпочтительны гетероарильные группы, содержащие азот. Примерами таких гетероарильных групп являются пиридинил, пиразинил, пиримидинил или пиридазинил.
Термин «галоген» охватывает фтор, хлор, бром и иод.
Термин «циклоалкил» означает циклоалкильную группу, содержащую 3-12, предпочтительно 3-6 атомов углерода, такую как циклопропил, циклобутил, циклопентил или циклогексил.
Термин «5- или 6-членный гетероцикл» обозначает гетероцикл, имеющий 5 или 6 членов в цикле, содержащий по меньшей мере один атом углерода в качестве члена цикла и возможно 1, 2 или 3 дополнительных гетероатома в качестве членов цикла, выбранных из N, О или S, при этом остальные члены цикла являются атомами углерода. Примеры 5- или 6-гетероцикла включают (не ограничиваясь ими) 1Н-тетразол; 2Н-тетразол; 1,2,3- и 1,2,4-триазол; имидазол; пиррол; 1,2,3-, 1,3,4- или 1,2,5-тиадиазин; 1,4-оксазин; 1,2- или 1,4-тиазин; 4-морфолинил; 1-пирролидинил; 1-пиперазинил, предпочтительно 4-морфолинил; 1-пирролидинил или 1-пиперазинил. Заместители такого 5- или 6-членного гетероцикла включают (не ограничиваясь ими) галоген, амино, нитро, циано, гидрокси, гидрокси-низший алкил, низший алкокси, низший алкенил, циклоалкил, низший алкил; или СF3, и предпочтительно низший алкил; или CF3.
Термин «фармацевтически приемлемая соль присоединения» относится к любой соли, полученной с неорганической или органической кислотой или основанием.
Предпочтительными соединениями по изобретению являются соединения, в которых:
p представляет собой 0 или 1;
R1 и R2 независимо выбраны из группы, состоящей из Н; галогена; низшего алкила, возможно замещенного низшим алкокси; низшего алкокси, возможно замещенного одним или более чем одним галогеном; или СF3;
R3 выбран из группы, состоящей из низшего алкила; гидрокси-низшего алкила; NRaRb,
где
Ra и Rb независимо выбраны из группы, состоящей из;
Н;
низшего алкила, возможно замещенного одним или более чем одним гидрокси, фтор, циклоалкил, арил, гетероарил или NRcRd,
где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкила;
арила;
гетероарила;
или Ra и Rb вместе с атомом азота, к которому они присоединены образуют 4-морфолинильную; 1-пирролидинильную или 1-пиперазинильную группу;
R4 представляет собой Н, циклопропил или неразветвленный низший алкил, который возможно замещен одним или более чем одним F;
R5 представляет собой Н; галоген или низший алкил.
Другими предпочтительными соединениями по изобретению являются те, в которых R1 и R2 независимо выбраны из группы, состоящей из Н, Сl, Me, СF3, МеО, ЕtO и СF3СН2O-, и R3, R4, R5 и p такие, как определено выше.
Другими предпочтительными соединениями по изобретению являются те, в которых R3 представляет собой низший алкил; и R1, R2, R4, R5 и p такие, как определено выше, например следующие соединения:
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а] пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-[3-2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло [1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид и
5-(4-Хлор-фенил)-7-метокси-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид.
Другими предпочтительными соединениями по изобретению являются те, в которых R3 представляет собой гидрокси-низший алкил; и R1, R2, R4, R5 и p такие, как определено выше, например следующие соединения:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амид и
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амид.
Другими предпочтительными соединениями по изобретению являются те, у которых R3 представляет собой NRaRb;
где Ra и Rb независимо выбраны из:
Н;
низшего алкила, возможно замещенного одним или более чем одним гидрокси, фтор, циклоалкил, арил, гетероарил, или NRcRd, где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкила;
арила;
гетероарила;
и R1, R2, R4, R5 и p такие, как определено выше, например следующие соединения:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил- пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил) -амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-фенилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-илметил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-илметил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-илметил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-илметил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1.5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1.5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид и
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3- карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид.
Другими предпочтительными соединениями по изобретению являются те соединения, где R3 представляет собой 4-морфолинил; и R1, R2, R4, R5 и p такие, как определено выше, например следующие соединения:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид и
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид.
Еще другими предпочтительными соединениями по изобретению являются те соединения, где R3 представляет собой пирролидин и R1, R2, R4, R5 и p являются такими, как определено выше, например следующие соединения:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид и
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((3)-2-гидроксиметил-пирролидин-1-сульфонил)-фенил]-амид и
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((3)-2-гидроксиметил-пирролидин-1-сульфонил)-фенил]-амид.
Соединения по изобретению могут быть приготовлены согласно способу, включающему в себя стадии, на которых соединение формулы VI
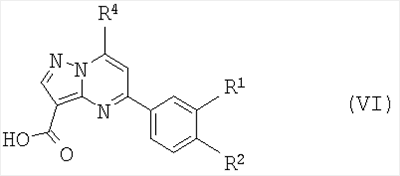
подвергают взаимодействию с соединением формулы VII,
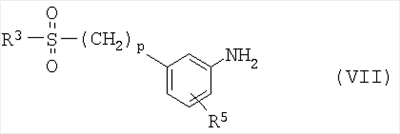
где R1, R2, R3, R4, R5 и p такие, как определено в формуле I выше;
с получением соединения формулы I, и при желании превращают соединение формулы I в его фармацевтически приемлемую соль присоединения.
Фармацевтически приемлемые соли присоединения могут быть легко изготовлены согласно известным из уровня техники методам как таковым с учетом природы соединения, которое собираются превратить в соль. Неорганические или органические кислоты, такие как, например, соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота или лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, p-толуолсульфоновая кислота и т.п., пригодны для образования фармацевтически приемлемых солей основного соединения формулы I.
Синтез промежуточного соединения формулы (VI), упомянутого выше, может быть осуществлен согласно следующим общим методам I и/или Ia, которые представлены ниже на схеме 1 и схеме 1а. Метод, приведенный на схеме 1, удобен для промежуточного соединения VI, где R4 представляет собой СF3 или CHF2, в то время как для промежуточного соединения VI, где R4 представляет собой линейный C1-3алкил или циклопропил, предпочтительным является метод, представленный на схеме 1а.
Что касается взаимодействия соединения формулы (VII) с соединением формулы (VI), оно может быть осуществлено, например, согласно следующему общему методу II, который представлен ниже на схеме 2. На этих схемах (I, Iа и II), R1, R2, R3, R4, R5 и p такие, как определено выше. Методы I/Iа и II могут быть использованы для получения всех соединений формулы I.
Общий метод I
Схема 1
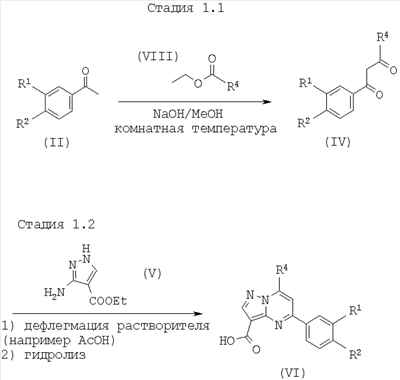
Стадия 1.1:
К перемешиваемому раствору соединения формулы (III) в органическом растворителе (например, трет-бутил-метиловом эфире) при комнатной температуре добавляют раствор метоксида натрия в метаноле, а затем раствор соединения формулы (II) в органическом растворителе (например, трет-бутил-метиловом эфире). Реакционную смесь перемешивают при комнатной температуре в течение около 19 ч, охлаждают, подкисляют и экстрагируют (например, диэтиловым эфиром). Объединенные органические слои промывают и сушат (например, с помощью MgSO4) и выпаривают с получением неочищенного соединения формулы (IV), которое может быть использовано без дальнейшей очистки.
Стадия 1.2:
Перемешиваемую смесь имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола (соединение формулы (V)) и соединения формулы (IV) в органической кислоте (например, уксусной кислоте) нагревают в условиях дефлегмации в течение около 1,5 ч. Реакционную смесь выпаривают и неочищенный продукт растворяют в смеси концентрированного основания (например, КОН в метаноле и воде). Реакционную смесь перемешивают при около 60°С в течение около 1,5 ч, охлаждают, подкисляют и концентрируют. Осадок собирают фильтрацией и очищают далее (например, кристаллизацией из диэтилового эфира/метанола) с получением соединения формулы (VI).
Общий метод Ia
Схема 1а
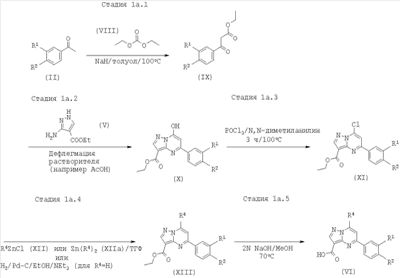
Стадия 1а.1:
К суспензии гидрида натрия в толуоле последовательно добавляют диэтилкарбонат и соединение формулы (II). Раствор медленно нагревают до 100°С, в течение чего образуется газообразный водород. Смесь перемешивают при температуре дефлегмации в течение 6-15 ч. После охлаждения смеси до 10°С добавляют уксусную кислоту, затем ледяную воду и концентрированную НСl. Смесь экстрагируют (например, этилацетатом). Органический слой последовательно промывают водным раствором NaHCO3, водой и рассолом, сушат (например, с помощью Na2SO4) и выпаривают. Оставшийся неочищенный продукт формулы (IХ) может быть использован непосредственно на следующей стадии или, возможно, очищен, например дистилляцией.
Стадия 1а.2:
Смесь соединения формулы (IХ) и 3-амино-4-этоксикарбонил-пиразола (соединение формулы (V)) нагревают либо без добавок с перемешиванием до около 150°С в течение 2-6 ч, либо, предпочтительно, в растворителе (таком, например, как уксусная кислота) в течение 8-20 ч. Продукт формулы (X) может быть выделен с помощью общепринятой процедуры обработки, например осаждением продукта водой или распределением реакционной смеси между водой и органическим растворителем, таким как дихлорметан, и неочищенный продукт может быть очищен далее, например кристаллизацией.
Стадия 1а.3:
Соединение формулы (X) нагревают при перемешивании с РОCl3 до 80-100°С в течение 1-15 ч, предпочтительно в присутствии основного катализатора (например, диметиланилина). Смесь охлаждают и выпаривают в вакууме. Остаток распределяют между водой и органическим растворителем (например, дихлорметаном или этилацетатом), органические слои промывают водой и рассолом, сушат (например, с помощью Na2SO4) и выпаривают. Оставшийся неочищенный продукт формулы (XI) может быть использован непосредственно на следующей стадии или, предпочтительно, очищен, например кристаллизацией.
Стадия 1а.4:
Для получения соединения (ХIII), где R4 представляет собой линейный C1-3-алкил или циклопропил, раствор соединения формулы (ХIII), реагента R4ZnCl (ХII) или Zn(R4)2 (XIIb) и катализатора Pd(0) (например, Рd(РРh3)4) в ТГФ нагревают до 40-70°С в течение 0,5-6 ч. К охлажденной реакционной смеси добавляют насыщенный водный хлорид аммония. Смесь экстрагируют этилацетатом, и органические слои промывают водой и рассолом, сушат (например, с помощью Na2SO4) и выпаривают. Неочищенный продукт может быть использован непосредственно на следующей стадии, или сначала очищен хроматографически и/или кристаллизацией.
Для получения соединения (ХIII), где R4 представляет собой водород, раствор соединения формулы (ХIII) в растворителе (например, в этаноле) перемешивают в атмосфере водорода в присутствии палладированного угля и основания (например, триэтиламина) при 20°С в течение 0,1-0,3 ч. Смесь фильтруют и растворитель выпаривают с получением соединения формулы (ХIII), где R4 представляет собой водород.
Стадия 1а.5:
Промежуточное соединение VI, где R4 представляет собой линейный C1-3алкил или циклопропил, может быть получено путем подвергания промежуточного соединения (ХIII) общепринятым процедурам, используемым для гидролиза этиловых эфиров, например путем обработки водным основанием, таким как 2N раствор гидроксида натрия, возможно в присутствии со-растворителя, такого как метанол, при 20-70°С.
Общий метод II
Схема 2
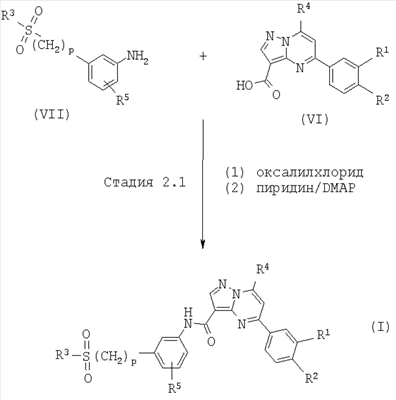
Стадия 2.1:
К перемешиваемому раствору соединения формулы (VI) в растворителе (например, ТГФ) при комнатной температуре добавляют ДМФ, раствор охлаждают до около 0°С и добавляют оксалилхлорид. Реакционную смесь перемешивают при комнатной температуре в течение около 3 ч и выпаривают досуха. Осадок растворяют в пиридине и, перемешивая при комнатной температуре, добавляют 4-диметиламино-пиридин и соединение формулы (VII). Реакционную смесь оставляют перемешиваться при комнатной температуре в течение около 16 ч, выпаривают досуха и неочищенный продукт очищают (например, флэш-хроматографией на силикагеле) с выходом продукта, который может быть далее очищен (например, кристаллизацией из метанола/гексана).
Соединения формулы I и их фармацевтически приемлемые соли являются антагонистами метаботропного глутаматного рецептора и могут быть использованы для лечения или предупреждения острых и/или хронических неврологических нарушений, таких как психоз, шизофрения, болезнь Альцгеймера, когнитивные расстройства и нарушения памяти. Другие состояния, которые можно лечить при этом, представляют собой ограниченную функцию мозга, вызванную операциями шунтирования или трансплантациями, недостаточное мозговое кровоснабжение, травмы спинного мозга, травмы головы, гипоксию, вызванную беременностью, остановку сердца и гипогликемию. Также состояния, которые можно лечить, – это острая и хроническая боль, хорея Хантингтона, боковой амиотрофический склероз (ALS), слабоумие, вызванное спидом, травмы глаз, ретинопатия, идиопатический паркинсонизм или лекарственный паркинсонизм, а также состояния, которые ведут к глутамат-недостаточным функциям, таким, например, как спазмы мышц, конвульсии, мигрени, недержание мочи, никотиновая зависимость, психозы, опиатная зависимость, тревога, рвота, дискинезия, депрессия и глиома, так как было обнаружено, что антагонисты mGluR2 снижают клеточную пролиферацию в клетках глиомы человека (J.Neurochem. March 2003, 84(6): 1288-95).
Соединения формулы I и их фармацевтически приемлемые соли могут быть использованы в качестве лекарств, например в форме фрамацевтических препаратов. Фармацевтические препараты могут вводиться перорально, например в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным также может быть ректальное введение, например в форме суппозиториев, или парентеральное, например в форме растворов для инъекций.
Соединения формулы I и их фармацевтически приемлемые соли могут быть переработаны с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических препаратов. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. могут быть использованы, например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, вески, жиры, полутвердые и жидкие полиолы и т.п.; в зависимости от природы активного вещества, однако, обычно для мягких желатиновых капсул не требуется никаких носителей. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п. Адъюванты, такие как спирты, полиолы, глицерин, растительные масла и т.п., могут быть использованы для водных инъекционных растворов водорастворимых солей соединений формулы I, но, как правило, не являются необходимыми. Подходящими носителями для суппозиториев являются, например, природные или отвержденные масла, вески, жиры, полужидкие или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, корригенты, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать и другие терапевтически ценные вещества.
Как упоминалось ранее, лекарства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный эксципиент, также являются предметом данного изобретения, равно как и способ получения таких лекарств, при котором одно или более соединений формулы I или их фармацевтически приемлемых солей и, при желании, одно или более других терапевтически ценных веществ превращают в галеновую лекарственную форму вместе с одним или более чем одним терапевтически инертным носителем.
Дозировка может варьировать в широких пределах и, конечно, должна быть подобрана по индивидуальным потребностям в каждом конкретном случае. В общем, эффективная дозировка для перорального или парентерального введения находится в интервале 0,01-20 мг/кг/день, при дозировке 0,1-10 мг/кг/день, являющейся предпочтительной для всех описанных назначений. Суточная дозировка для взрослого человека весом 70 кг, соответственно, находится в интервале 0,7-1400 мг в день, предпочтительно между 7 и 700 мг в день.
Данное изобретение также относится к применению соединения формулы I и его фармацевтически приемлемых солей для производства лекарств, особенно для борьбы или профилактики острых и/или хронических неврологических нарушений вышеуказанного типа.
Соединения по данному изобретению являются антагонистами mGlu рецепторов группы II. Соединения демонстрируют активности, как измерено в анализе, описанном ниже, в количестве 0,060 мкМ или менее, типично 0,025 мкМ или менее, и в идеальном случае 0,010 мкМ или менее. В таблице приведены некоторые специфические величины Ki предпочтительных соединений.
| Номер эксперимента |
1 |
74 |
79 |
88 |
144 |
| Кi mGlu2 (мкМ) |
0,03 |
0,067 |
0,011 |
0,015 |
0,007 |
Связывание [3H]-LY354740 на мембранах клеток СНО, трансфицированных mGlu2.
Трансфекция и клеточная культура
кДНК, кодирующая mGlu2 рецепторный белок крысы в pBluescript II, была субклонирована в эукариотический вектор экспрессии pcDNA)-amp от Invitrogen Ltd (Paisley, UK). Эта векторная конструкция (pcDlfnGR2) была котрансфицирована с плазмидой psvNeo, кодирующей ген устойчивости к неомицину, в клетки СНО модифицированным кальций-фосфатным методом, описанным Chen & Okayama (1988). Клетки поддерживали в среде Игла, модифицированной по Дульбекко, с пониженным L-глутамином (конечная концентрация 2 мМ) и 10% диализированной фетальной телячьей сывороткой от Gibco-Invitrogen (Carlsbad, CA, USA). Отбор осуществляют в присутствии G-418 (1000 мкг/мл конечная) и MCPG. Клоны идентифицируют обратной транскрипцией 5 мкг тотальной РНК, с последующей ПЦР с использованием специфичных к mGlu2 рецептору праймеров 5′-atcactgcttgggrttctggcactg-3′ и 5′-agcatcactgtgggtggcataggagc-3′ в 60 мМ Tris НСl (рН 10), 15 мМ (NH4)2SO4, 2 мМ МgСl2, 25 ед/мл Taq полимеразы в 30 циклах ренатурации при 60°С в течение 1 мин, синтеза при 72°С в течение 30 с и 1 мин денатурации при 95°С.
Приготовление мембран
Клетки, культивированные, как описано выше, собирали и промывали трижды холодным фосфатно-солевым буфером, и замораживали при -80°С. Осадок ресуспендировали в холодном 20 мМ буфере HEPES-NaOH, содержащем 10 мМ EDTA (рН 7,4), и гомогенизировали с политроном (Kinematica, AG, Littau, Switzerland) в течение 10 с при 10000 об/мин. После центрифугирования в течение 30 мин при 4°С, осадок промывали однократно тем же буфером и однократно холодным 20 мМ буфером HEPES-NaOH, содержащим 0,1 мМ EDTA, (рН 7,4). Белковое содержимое было измерено с использованием микро ВСА метода от Pierce-Perbio (Rockford, IL, USA) с использованием бычьего сывороточного альбумина в качестве стандарта.
Связывание [3H]-LY354740
После оттаивания мембраны ресуспендировали в холодном 50 мМ буфере Tris-HCl, содержащем 2 мМ МgСl2 (рН 7) (буфер для связывания). Конечная концентрация мембран в этом анализе составляла 25 мкг белка/мл. Эксперименты по ингибированию проводили с мембранами, инкубированными с 10 нМ [3H]-LY354740 при комнатной температуре в течение 1 часа в присутствии различных концентраций тестируемого соединения. После инкубации мембраны фильтровали на стекловолоконном фильтре Whatmann GF/B и промывали 5 раз холодным буфером для связывания. Неспецифичное связывание измеряли в присутствии 10 мкМ DCG IV. После переноса фильтров в пластиковые впалы, содержащие 10 мл сцинтилляционной жидкости Ultima-gold от Perkin-Elmer (Boston, MA, USA), радиоактивность была измерена жидкостной сцинтилляцией в счетчике Tri-Carb 2500 TR (Packard, Zurich, Switzerland).
Анализ данных
Кривые ингибирования выравнивали четырехпараметрическим логистическим уравнением, дающим величины ИK50 и коэффициенты Хилла.
ПРИМЕРЫ
Синтез исходных материалов
Некоторые из исходных материалов, используемых в общих методах I и II, имеются в продаже. При этом часть исходных материалов была приготовлена согласно методам, описанным ниже, и, если не указано иное, промежуточные соединения, описанные здесь, являются новыми соединениями. Иные исходные материалы, пригодные для общих методов I и II, могут быть приготовлены с учетом следующих примеров получения, используя известные способы.
Синтез производных ацетофенонов (исходный материал формулы II)
Пример А.1
4-Метил-3-трифторметил-ацетофенон
К перемешанному и охлажденному (0°С) раствору трет-бутанолята калия (1,39 г, 12 ммоль) в ДМСО (3 мл) добавляли диэтилмалонат (1,9 мл, 12 ммоль) и реакционную смесь перемешивали в течение 20 мин при комнатной температуре. К белой суспензии при комнатной температуре добавляли 4-фтор-3-трифторметил-ацетофенон (1 г, 5 ммоль) и ДМСО (2 мл). Реакционную смесь перемешивали в течение 6 ч при 60°С и в течение 16 ч при комнатной температуре. Реакционную смесь охлаждали (0°С), добавляли раствор гидроксида калия (1,09 г, 19 ммоль) в воде (2 мл) и смесь перемешивали при 100°С в течение 23 ч. Смесь выливали на лед/воду (40 мл) и экстрагировали диэтиловым эфиром (2×40 мл). Объединенные органические слои промывали водой (3×30 мл), рассолом (30 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт (0,92 г) далее был очищен колоночной хроматографией на силикагеле (гептан/этилацетат 3:1) с получением соединения, указанного в заголовке, (0,76 г, 77%) в виде светло-желтой жидкости. MS (ЕI) 202,0 [М].
Пример А.2
4-Этокси-3-трифторметил-ацетофенон
К перемешанной суспензии этанолята калия (2,36 г, 27 ммоль) в этаноле (30 мл) при комнатной температуре добавляли раствор 4-фтор-3-трифторметил-ацетофенона (2,5 г, 12 ммоль) в этаноле (10 мл). Реакционную смесь перемешивали при 60°С в течение 2 ч и выпаривали. Добавляли лед/2N НСl (50 мл) и водный слой экстрагировали диэтиловым эфиром (2×100 мл). Объединенные органические слои промывали льдом-водой (50 мл), рассолом (50 мл), высушивали (MgSO4) и выпаривали с получением соединения, указанного в заголовке, (2,9 г, 98%) в виде коричневого твердого вещества, которое использовали без дальнейшей очистки. MS (ЕI) 232,1 [М].
Пример А.3
4-(2,2,2-Трифтор-этокси)-3-трифторметил-ацетофенон
К перемешиваемому раствору 4-фтор-3-трифторметил-ацетофенона (2,5 г, 12 ммоль) в ДМСО (15 мл) при комнатной температуре добавляли 2,2,2-трифторэтанол (1,7 г, 17 ммоль) и гидроксид калия (1,74 г, 27 ммоль). Реакционную смесь перемешивали в течение 30 мин при 40°С, добавляли лед/2N НСl (50 мл) и водный слой экстрагировали диэтиловым эфиром (2×100 мл). Объединенные органические слои промывали льдом-водой (50 мл), рассолом (50 мл), высушивали (MgSO4) и выпаривали с получением соединения, указанного в заголовке, (3,6 г, 98%) в виде твердого коричневого вещества, которое использовали без дальнейшей очистки. MS (ЕI) 286,1 [М].
Пример А.4
3-Метил-4-трифторметил-ацетофенон
1-(3-метил-4-трифторметил-фенил)-этанон был получен в следующем порядке:
Стадия 1: 5-Метил-2-нитро-4-трифторметил-фениламин
В атмосфере аргона суспензию трет-бутанолята калия (71,6 г, 625 ммоль) в ДМСО (150 мл) помещали в 1,5 л колбу, снабженную механической мешалкой. Затем диэтилмалонат (97,9 мл, 625 ммоль) добавляли по каплям при 20-30°С при охлаждении на ледяной бане. К тонкой белой суспензии одной порцией добавляли твердый имеющийся в продаже 5-хлор-2-нитро-4-трифторметил-фениламин [CAS-No. 35375-74-7] (60,14 г, 250 ммоль), смесь разбавляли ДМСО (100 мл), и красный раствор нагревали до 60°С и перемешивали в течение 20 ч при 60°С. Смесь охлаждали до 23°С и по каплям добавляли раствор гидроксида калия (85%, 65,24 г, 1 моль) в воде (100 мл). Затем смесь нагревали до 100°С и перемешивали в течение еще 4 ч. Смесь охлаждали до 23°С, разбавляли водой (примерно 1000 мл), подкисляли с помощью 37% НСl до рН 3 и экстрагировали трижды трет-бутилметиловым эфиром (ТВМЕ). Органические слои промывали рассолом, высушивали над MgSO4 и выпаривали с получением твердого коричневого вещества, которое растирали с горячим гептаном, отфильтровывали и промывали гептаном с получением соединения, указанного в заголовке, в виде твердого коричневого вещества (50,0 г, 91%), которое использовали без дальнейшей очистки. MS (ISN) 218,9 [М-Н].
Стадия 2: 1-Бром-5-метил-2-нитро-4-трифторметил-бензол
К быстро перемешиваемой смеси трет-бутилнитрита (45,33 мл, 382 ммоль) и бромида меди (II) (76,1 г, 341 ммоль) в ацетонитриле (450 мл) при 65°С осторожно добавляли твердый 5-метил-2-нитро-4-трифторметил-фениламин со стадии 1 (50,0 г, 227 ммоль). После того, как закончили добавление, перемешивание продолжали в течение еще 1 ч при 65°С. Смесь охлаждали до 23°С и выливали в 1 N НСl (1000 мл), экстрагировали дважды ТВМЕ, органический слой промывали рассолом, высушивали над MgSO4. После удаления растворителя в вакууме оставалось коричневое масло, которое очищали силикагелевой колоночной хроматографией с гептаном/этилацетатом 9:1 с получением соединения, указанного в заголовке, в виде желтой жидкости (49,8 г, 77%). MS (ЕI) 283,0 [М] и 285,0 [М+2].
Стадия 3: 5-Метил-2-нитро-4-трифторметил-бензонитрил
Смесь 1-бром-5-метил-2-нитро-4-трифторметил-бензола со стадии 2 (49,80 г, 175 ммоль) и цианида меди (I) (16,5 г, 184 ммоль) в 1-метил-2-пирролидоне (NMP) (180 мл) нагревали до 150°С и перемешивали в течение 30 мин в атмосфере азота. Смесь охлаждали до 23°С и выливали в 1 N НСl, экстрагировали с помощью ТВМЕ, промывали рассолом и высушивали над Na2SO4. Удаление растворителя в вакууме давало коричневое масло, которое очищали силикагелевой колоночной хроматографией с гептаном/этилацетатом 4:1->2:1 с получением соединения, указанного в заголовке, в виде светло-желтого твердого вещества (35,48 г, 88%). MS (EI) 230,1 [М].
Стадия 4: 2-Амино-5-метил-4-трифторметил-бензонитрил
Железный порошок (37,42 г, 670 ммоль) добавляли небольшими порциями к перемешанной суспензии тонкоизмельченного 5-метил-2-нитро-4-трифторметил-бензонитрила со стадии 3 (34,58 г, 150 ммоль) в метаноле (75 мл) и 37% НСl (93 мл). Внутреннюю температуру поддерживали между 40 и 60°С внешним охлаждением на водяной бане. Полученный коричневый раствор перемешивали в течение 1 ч при 50°С, с получением зеленой суспензии. Смесь выливали в ледяную воду (600 мл), выпавшее в осадок твердое вещество отфильтровывали и промывали водой с получением твердого зеленого вещества, которое растворяли в кипящем этаноле (700 мл), добавляли активированный уголь (примерно 10 г) и смесь кипятили с обратным холодильником в течение 1 ч. Горячий раствор фильтровали, и растворитель выпаривали в вакууме, чтобы получить соединение, указанное в заголовке, в виде коричнево-желтого твердого вещества (23,55 г, 78%), которое использовали без дальнейшей очистки. MS (EI) 200,1 [М].
Стадия 5: 3-Метил-4-трифторметил-бензонитрил
К раствору 2-амино-5-метил-4-трифторметил-бензонитрила со стадии 4 (23,34 г, 117 ммоль) в сухом ТГФ (350 мл) добавляли изоамилнитрит (34,3 мл, 257 ммоль) и смесь кипятили с обратным холодильником в течение 20 ч. Добавляли дополнительный изоамилнитрит (16,6 мл, 129 ммоль) и смесь кипятили с обратным холодильником в течение еще 20 ч. Смесь охлаждали до 23°С и разбавляли ТВМЕ, органический слой промывали 1 N НСl, насыщенным раствором NaHCO3 и рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало коричневое масло (25,82 г), которое очищали пузырьковой дистилляцией (bulb to bulb) с получением желтой жидкости (20,11 г), которую окончательно очищали дистилляцией с получением соединения, указанного в заголовке, в виде желтой жидкости (17,10 г, 79%; т. кип. 38-42°С при 0,8 мбар). MS (ЕI) 185,1 [М].
Стадия 6: 3-Метил-4-трифторметил-бензойная кислота
Смесь 3-метил-4-трифторметил-бензонитрила со стадии 5 (16,25 г, 88 ммоль) и 3N NaOH (88 мл, 264 ммоль) в диоксане (90 мл) кипятили с обратным холодильником в течение 18 ч. Смесь охлаждали до 23°С, разбавляли ТВМЕ, подкисляли с помощью 1 N НСl до рН 1 и экстрагировали дважды ТВМЕ. Объединенные органические слои промывали рассолом, высушивали над MgSO4. Удаление растворителя в вакууме давало соединение, указанное в заголовке, в виде беловатого твердого вещества (14,46 г, 81%), которое использовали без дальнейшей очистки. MS (ISN) 203,1 [М-Н].
Стадия 7: N-Метокси-3,N-диметил-4-трифторметил-бензамид
К суспензии 3-метил-4-трифторметил-бензойной кислоты со стадии 6 (14,1 г, 69,1 ммоль), гидрохлорида N,O-диметилгидроксиламина (10,78 г, 111 ммоль), N-метилморфолина (12,14 мл, 111 ммоль) и 4-DMAP (844 мг, 691 ммоль) в DCM (230 мл) при 0°С добавляли 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (EDC) (15,98 г, 82,9 ммоль) и ДМФ (85 мл). Смесь нагревали до 23°С и перемешивали в течение 18 ч в атмосфере азота. Смесь разбавляли ТВМЕ, промывали водой и дважды рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало соединение, указанное в заголовке, в виде коричневого масла (16,92 г, 99%), которое использовали без дальнейшей очистки. MS (ISP) 248,0 [М+Н].
Стадия 8: 1-(3-Метил-4-трисфторметил-фенил)-этанон
К раствору N-метокси-3,N-диметил-4-трифторметил-бензамида со стадии 7 (16,90 г, 68,36 ммоль) в ТГФ (280 мл) при -5°С добавляли 3М раствор бромида метилмагния в диэтиловом эфире (45,6 мл, 136,7 ммоль). Смесь перемешивали при 0°С в течение 1 ч, затем нагревали до 23°С и продолжали перемешивание при 23°С в течение еще 1,5 ч в атмосфере азота. Затем по каплям к смеси добавляли 1N НСl (100 мл) и продолжали перемешивание в течение 30 мин. Смесь разбавляли EtOAc и водный слой отделяли, органический слой промывали рассолом и высушивали над MgSO4. Удаление растворителя в вакууме давало соединение, указанное в заголовке, в виде светло-коричневой жидкости (12,87 г, 93,1%), которое использовали без дальнейшей очистки. MS (ЕI) 202,1 [М].
Пример А.5
3-Этокси-4-трифторметил-ацетофенон
1-(3-этокси-4-трифторметил-фенил)-этанон был получен в следующей последовательности:
Стадия 1: 5-Этокси-2-нитро-4-трифторметил-фениламин
К EtOH (500 мл) добавляли металлический калий (примерно 21 г, примерно 537 ммоль), и интенсивную реакцию нужно было охлаждать на ледяной бане. Продолжали перемешивание до растворения металлического калия. Твердый имеющийся в продаже 5-хлор-2-нитро-4-трифторметил-фениламин [CAS-No. 35375-74-7] (57,74 г, 240 ммоль) добавляли одной порцией и полученную темно-красную смесь перемешивали при 55-60°С в течение 4 дней. Теплую реакционную смесь медленно выливали в Н2O (примерно 2000 мл), подводили рН с помощью конц. НСl до рН 2, отфильтровывали желтый осадок, промывали Н2O и высушивали на воздухе при 60°С с получением желтого твердого вещества (57,81 г, 96%), которое использовали без дальнейшей очистки. MS (ISN) 249 [M-H].
Стадия 2: 1-Бром-5-этокси-2-нитро-4-трифторметил-бензол
Твердый 5-этокси-2-нитро-4-трифторметил-фениламин со стадии 1 (57,81 г, 231 ммоль) медленно добавляли за 15 мин к быстро перемешиваемой смеси трет-бутилнитрита (45,8 мл, 347 ммоль) и безводного бромида меди (II) (77,4 г, 347 ммоль) в ацетонитриле (462 мл), которую нагревали до 65°С в масляной бане. Перемешивание при 65°С продолжали в течение 30 мин, реакционную смесь охлаждали до 23°С, выливали в 1N НСl, насыщенную твердым NaCl, экстрагировали с помощью ТВМЕ, высушивали над MgSO4. Удаление растворителя в вакууме давало темно-коричневое масло (74,5 г). Силикагелевая колоночная хроматография с гептаном/ЕtOАс 4:1 давала соединение, указанное в заголовке, в виде желтого твердого вещества (63,03 г, 87%). MS (ЕI) 313,0 [М] и 315,0 [М+2].
Стадия 3: 5-Этокси-2-нитро-4-трифторметил-бензонитрил
Смесь 1-бром-5-этокси-2-нитро-4-трифторметил-бензола со стадии 2 (61,81 г, 197 ммоль) и CuCN (18,51 г, 207 ммоль) в NMP (197 мл) нагревали до 150°С в течение 30 мин, охлаждали до 23°С, выливали в 1N НСl, экстрагировали с помощью ТВМЕ, промывали рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало коричневое масло. Силикагелевая колоночная хроматография с гептаном/ЕtOАс 4:1 давала соединение, указанное в заголовке, в виде желтого твердого вещества (46,73 г, 91%). MS (ЕI) 260,1 [М].
Стадия 4: 2-Амино-5-этокси-4-трифторметил-бензонитрил
Железный порошок (40,96 г, 733 ммоль) добавляли небольшими порциями за 5 мин к перемешиваемой суспензии тонкоизмельченного 5-этокси-2-нитро-4-трифторметил-бензонитрила со стадии 3 (42,79 г, 164,5 ммоль) в МеОН (85 мл) и конц. НСl (102 мл) с охлаждением на водяной бане. поддерживающей внутреннюю температуру на 40-50°С. Полученную смесь перемешивали в течение еще 1 ч при примерно 50°С и затем выливали в ледяную Н2O (700 мл). Осадок фильтровали, промывали водой, высушивали и растворяли в кипящем EtOH (800 мл), добавляли активированный уголь (примерно 10 г), смесь кипятили с обратным холодильником в течение 45 мин, горячий раствор фильтровали и выпаривали досуха с получением желтого твердого вещества (31,81 г, 84%), которое использовали без дальнейшей очистки. MS (ЕI) 230,1 [М].
Стадия 5: 3-Этокси-4-трифторметил-бензонитрил
К раствору 2-амино-5-этокси-4-трифторметил-бензонитрила со стадии 4 (31,62 г, 137,4 ммоль) в сухом ТГФ (410 мл) добавляли изоамилнитрит (40,4 мл, 302 ммоль), и смесь кипятили с обратным холодильником в течение 16 ч. Растворитель удаляли в вакууме с получением оранжевого масла, которое растворяли в насыщенном растворе NaHCO3, экстрагировали трижды диэтиловым эфиром. Объединенные органические слои промывали 1N НСl и рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало оранжевое масло, которое очищали двойной дистилляцией по Кюгельрору (Kugelrohr) (температура бани до 160°С при 1,5 мбар) с получением соединения, указанного в заголовке, в виде светло-желтого твердого вещества (25,06 г, 85%). MS (EI) 185,1 [М].
Стадия 6: 1-(3-Этокси-4-трифторметил-фенил)-этанон
К раствору 3-этокси-4-трифторметил-бензонитрила со стадии 5 (5,00 г, 23,2 ммоль), бромида меди (I) (100 мг, 0,7 ммоль), трет.-бутилдиметилхлорсилана (4,20 г, 27,9 ммоль) в сухом ТГФ (30 мл) при -70°С по каплям добавляли 3М раствор бромида метилмагния в диэтиловом эфире (13,2 мл, 39,6 ммоль). Смесь перемешивали при -70°С в течение 10 мин, затем нагревали до 0°С и продолжали перемешивание при 0°С в течение еще 2 ч в атмосфере азота. Вливали реакционную смесь на лед и насыщенный раствор NH4Cl экстрагировали трижды диэтиловым эфиром, промывали объединенные органические слои рассолом, высушивали над MgSO4. Удаление растворителя в вакууме давало коричневое масло, которое очищали силикагелевой колоночной хроматографией с гептаном/ЕtOАс 4:1 с получением соединения, указанного в заголовке, в виде желтой жидкости (1,84 г, 34%). MS (ЕI) 232 [М].
Пример А.6
3-(2,2,2-Трифтор-этокси)-4-трифторметил-ацетофенон
1-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-этанон готовили в следующей последовательности:
Стадия 1: 2-Нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-фениламин
Имеющийся в продаже 5-хлор-2-нитро-4-трифторметил-фениламин [CAS-No. 35375-74-7] (72,2 г, 300 ммоль) растворяли в ДМСО (600 мл) и 2,2,2-трифторэтанол (270 мл) добавляли при 23°С, немного экзотермичную реакцию охлаждали на ледяной бане. Медленно добавляли КОН (85%, 99,0 г, 1500 ммоль) и темно-красную реакционную смесь перемешивали при 23°С в течение 4 дней. Переносили в 3-х литровую колбу и добавляли 1500 мл Н2O при охлаждении на ледяной бане, подкисляли с помощью 3N НСl и перемешивали при 23°С в течение 3 ч, отфильтровывали желтый осадок, промывали Н2O и высушивали на воздухе при 60°С с получением соединения, указанного в заголовке, в виде желтого твердого вещества (89,47 г, 98%). MS (ISN) 303,1 [M-H].
Стадия 2: 1-Бром-2-нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензол
Твердый 2-нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-фениламин со стадии 1 (24,28 г, 80 ммоль) добавляли медленно за 15 мин к быстро перемешиваемой смеси трет-бутилнитрита (14,23 мл, 120 ммоль) и безводного бромида меди (II) (26,75 г, 120 ммоль) в ацетонитриле (160 мл), которую нагревали до 65°С в масляной бане. Перемешивание при 65°С продолжали в течение 2 ч, реакционную смесь охлаждали до 23°С, выливали в 1N HCl, насыщенную твердым NaCl, экстрагировали с помощью ТВМЕ, высушивали над MgSO4. Удаление растворителя в вакууме давало темно-коричневое масло (35,57 г). Силикагелевая колоночная хроматография с гептаном/ЕtOАс 4:1 давала соединение, указанное в заголовке, в виде твердого оранжевого вещества (30,54 г, 104%), которое использовали без дальнейшей очистки. MS (EI) 367 [M] и 369 [М+2].
Стадия 3: 2-Нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензонитрил
Смесь 1-бром-2-нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензола со стадии 2 (30,54 г, 83,0 ммоль) и CuCN (7,80 г, 87,1 ммоль) в NMP (83 мл) нагревали до 150°С в течение 30 мин. Охлаждали до 23°С, выливали в 1N НСl, экстрагировали ЕtOАс, промывали рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало темно-коричневое масло (33,9 г). Силикагелевая колоночная хроматография с гептаном/ЕtOАс 9:1->4:1 давала соединение, указанное в заголовке, в виде желтого твердого вещества (22,05 г, 85%). MS (EI) 314 [M].
Стадия 4: 2-Амино-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензонитрил
Железный порошок (15,80 г, 283,0 ммоль) добавляли небольшими порциями за 5 мин к перемешиваемой суспензии тонкоизмельченного 2-нитро-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензонитрила со стадии 3 (19,93 г, 63,4 ммоль) в МеОН (32 мл) и конц. НСl (40 мл) с охлаждением на водяной бане, поддерживающей внутреннюю температуру на 25-35°С. Полученную смесь перемешивали в течение еще 1 ч при примерно 30°С и затем выливали в ледяную Н2O (400 мл). Осадок фильтровали, промывали водой, высушивали и растворяли в кипящем ЕtOН (400 мл), добавляли активированный уголь (примерно 10 г), смесь кипятили с обратным холодильником в течение 45 мин, горячий раствор фильтровали и выпаривали досуха с получением темно-зеленого твердого вещества (15,96 г, 84%), которое далее очищали силикагелевой колоночной хроматографией с гептаном/ЕtOАс 4:1 с получением соединения, указанного в заголовке, в виде желтого твердого вещества (14,56 г, 81%). MS (ISN) 283 [M-H].
Стадия 5: 3-(2,2,2-Трифтор-этокси)-4-трифторметил-бензонитрил
К раствору 2-амино-5-(2,2,2-трифтор-этокси)-4-трифторметил-бензонитрила со стадии 4 (14,47 г, 50,9 ммоль) в сухом ТГФ (153 мл) добавляли изоамилнитрит (15,0 мл, 112,0 ммоль) и смесь кипятили с обратным холодильником в течение 20 ч. Растворитель удаляли в вакууме с получением оранжевого масла, которое растворяли в ТВМЕ, промывали 1N НСl, насыщенным раствором NaHCO3 и рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало твердое коричневое вещество (15,05 г), которое очищали дистилляцией по Кюгельрору (температура бани до 155°С при 1,2 мбар) с получением соединения, указанного в заголовке, в виде светло-желтого твердого вещества (10,83 г, 79%). MS (EI) 269 [M].
Стадия 6: 3-(2,2,2-Трифтор-этокси)-4-трифторметил-бензойная кислота
Смесь 3-(2,2,2-трифтор-этокси)-4-трифторметил-бензонитрила со стадии 5 (8,75 г, 33 ммоль) и 3М NaOH (3,9 г, 98 ммоль в 33 мл H2O) в диоксане (33 мл) кипятили с обратным холодильником в течение 7,5 ч. Выливали на лед, подкисляли с помощью конц. НСl до рН 1, насыщали твердым NaCl, экстрагировали с помощью ТВМЕ, высушивали над MgSO4. Удаление растворителя в вакууме давало соединение, указанное в заголовке, в виде беловатого твердого вещества (9,22 г, 98%), которое использовали без дальнейшей очистки. MS (ISN) 286,9 [М-Н].
Стадия 7: N-метокси-N-метил-3-(2,2,2-трифтор-этокси)-4-трифторметил-бензамид
К смеси 3-(2,2,2-трифтор-этокси)-4-трифторметил-бензойной кислоты со стадии 6 (9,22 г, 32 ммоль), гидрохлорида N,O-диметилгидроксиламина (5,00 г, 51 ммоль), N-метилморфолина (5,62 мл, 51 ммоль) и 4-DMAP (391 мг, 3,2 ммоль) в DCM (100 мл) и DMF (20 мл) при 0°С добавляли 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (EDC) (7,36 г, 38 ммоль), и смесь перемешивали при 23°С в течение 18 ч. Выливали на охлажденную на льду 1N НСl, экстрагировали с помощью ТВМЕ, промывали насыщенным раствором NaHCO3 и рассолом, высушивали над Na2SO4. Удаление растворителя в вакууме давало соединение, указанное в заголовке, в виде коричневого масла (10,555 г, 100%), которое использовали без дальнейшей очистки. MS (ЕI) 331,0 [М].
Стадия 8: 1-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-этанон
К раствору N-метокси-N-метил-3-(2,2,2-трифтор-этокси)-4-трифторметил-бензамида со стадии 7 (10,467 г, 32 ммоль) в ТГФ (100 мл) при -5°С добавляли бромид метилмагния (3М в Et2O, 21,1 мл, 64 ммоль). Смесь перемешивали при 0°С в течение 15 мин, затем нагревали до 23°С, продолжали перемешивание в течение еще 1,5 ч при 23°С. Охлаждали до 0°С, по каплям добавляли 1N НСl (150 мл), продолжали перемешивание при 23°С в течение 15 мин, смесь разбавляли ТВМЕ, фазы разделяли, органический слой промывали водой и рассолом, высушивали над MgSO4. Удаление растворителя в вакууме давало желтое твердое вещество (9,021 г, 100%), которое использовали без дальнейшей очистки. MS (ЕI) 286,1 [М].
Синтез производных анилина (исходный материал формулы VII)
Пример В.1
3-Амино-N-(2,2,2-трифтор-этил)-бензолсульфонамид
а) К перемешиваемому раствору 2,2,2-трифторэтиламина (1,17 мл, 15 ммоль) в диоксане (37 мл) при комнатной температуре добавляли 3-нитробензолсульфонилхлорид (3,0 г, 14 ммоль) и триэтиламин (2,06 мл, 15 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 4 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (3×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:1) с выходом 3-нитро-N-(2,2,2-трифтор-этил)-бензолсульфонамида (3,18 г, 83%) в виде светло-желтого твердого вещества. MS (ISP) 283,9 [(М-Н)].
б) Смесь 3-нитро-N-(2,2,2-трифтор-этил)-бензолсульфонамида (3,12 г, 11 ммоль), дитионита натрия (8,09 г, 40 ммоль), воды (21,5 мл) и 2-метоксиэтанола (21,5 мл) перемешивали при 100°С в течение 2 ч, добавляли дополнительную воду (18,5 мл) при 70°С и затем добавляли НСl (37%, 18,5 мл) за 10 мин (выделение SO2). Реакционную смесь перемешивали при 70°С в течение 20 мин, выливали в лед/воду (50 мл) и добавляли карбонат натрия до тех пор, пока не подтверждалось, что раствор является основным. Раствор экстрагировали этилацетатом (3×75 мл), объединенные органические слои промывали рассолом (80 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:1) с выходом соединения, указанного в заголовке, (2,05 г, 73%) в виде белого твердого вещества. MS (ISP) 252,9 [(М-Н)]; т. пл. 131°С.
Пример В.2
3-Амино-N-циклопропилметил-бензолсульфонамид
а) К перемешиваемому раствору циклопропилметиламина (1,28 мл, 15 ммоль) в диоксане (37 мл) добавляли при комнатной температуре 3-нитробензолсульфонилхлорид (3,0 г, 14 ммоль) и триэтиламин (2,06 мл, 15 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 4 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (3×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:1) с выходом 3-нитро-N-циклопропилметил-бензолсульфонамида (3,08 г, 89%) в виде беловатого твердого вещества. MS (ISP) 254,9 [(М-Н)]; т. пл. 91°С.
б) Гидрогенизация перемешиваемого раствора 3-нитро-N-циклопропилметил-бензолсульфонамида (2,46 г, 10 ммоль) в метаноле (167 мл) на палладий/углероде (10%, 0,25 г) в течение 1 ч при комнатной температуре давала после удаления катализатора фильтрацией и выпаривания соединение, указанное в заголовке, в виде светло-желтой жидкости. MS (ISP) 225,1 [(M-H)–].
Пример В.3
3-Амино-N-пиридин-4-илметил-бензолсульфонамид
Смесь 3-нитро-N-(пиридин-4-илметил)-бензолсульфонамида [CAS No. 332942-34-4, имеется в продаже] (1,23 г, 4,2 ммоль), дитионита натрия (3,09 г, 15,1 ммоль), воды (10 мл) и 2-метоксиэтанола (10 мл) перемешивали при 100°С в течение 2 ч, дополнительную воду (7 мл) добавляли при 70°С и затем в течение 10 мин добавляли НСl (37%, 7 мл) (выделение SO2). Реакционную смесь перемешивали при 70°С в течение 20 мин, выливали в лед/воду (50 мл) и добавляли карбонат натрия до тех пор, пока не подтвердится, что раствор стал основным. Раствор экстрагировали этилацетатом/МеОН 9:1 (3×75 мл), объединенные органические слои промывали рассолом (80 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (МеОН/этилацетат 1:9) с выходом соединения, указанного в заголовке, (0,8 г, 72%) в виде светло-желтого твердого вещества. MS (ISP) 261,9 [(М-Н)–]; т. пл. 139°С.
Пример В.4
3-Амино-N-(2,2-диметил-пропил)-бензолсульфонамид
а) К перемешиваемому раствору неопентиламина (0,86 г мл, 9,93 ммоль) в диоксане (25 мл) при комнатной температуре добавляли 3-нитробензолсульфонилхлорид (2,0 г, 9,02 ммоль) и триэтиламин (1,38 мл, 9,93 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 17 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (3×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали кристаллизацией из этилацетата/гексана с выходом 3-нитро-N-(2,2-диметил-пропил)-бензолсульфонамида (2,14 г, 87%) в виде белого твердого вещества. MS (ISP) 271,1 [(М-Н)+]; т. пл. 117°С.
б) Гидрогенизация перемешиваемого раствора 3-нитро-N-(2,2-диметил-пропил)-бензолсульфонамида (2,04 г, 7,49 ммоль) в метаноле (130 мл) на палладий/углероде (10%, 0,20 г) в течение 1 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из гексана соединение, указанное в заголовке, в виде белого твердого вещества. MS (ISP) 243,2 [(МН+Н)+]; т. пл. 99°С.
Пример В.5
3-Амино-N-пиридин-3-илметил-бензолсульфонамид
а) Гидрогенизация перемешиваемого раствора 3-нитро-N-пиридин-3-илметил-бензолсульфонамида [CAS-No.436095-43-1; имеется в продаже] (1,42 г, 4,84 ммоль) в метаноле (90 мл) и ТГФ (50 мл) на палладий/углероде (10%, 0,14 г) в течение 2 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из этилацетата/гексана соединение, указанное в заголовке, (1,15 г, 90%) в виде светло-желтого твердого вещества. MS (ISP) 264,1 [(МН+Н)+]; т. пл. 129°С.
Пример В.6
3-Амино-N-пиридин-2-ил-метил-бензолсульфонамид
а) Гидрогенизация перемешиваемого раствора 3-нитро-N-пиридин-2-ил-метил-бензолсульфонамида [CAS-No. 309726-30-5; имеется в продаже] (1,37 г, 4,67 ммоль) в метаноле (140 мл) на палладий/углероде (10%, 0,14 г) в течение 2 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из этилацетата/гексана соединение, указанное в заголовке, (1,16 г, 94%) в виде беловатого твердого вещества. MS (ISP) 262.0 [(М-Н)–]; т. пл. 124°С.
Пример В.7
3-Амино-N-(2-пиридин-4-ил-этил)-бензолсульфонамид
а) К перемешиваемому раствору 4-(2-аминоэтил)-пиридина (1,21 г, 9,93 ммоль) в диоксане (25 мл) добавляли при комнатной температуре 3-нитробензолсульфонилхлорид (2,0 г, 9,02 ммоль) и триэтиламин (1,38 мл, 9,93 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 6 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (6×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали кристаллизацией из метанола/гексана с выходом 3-нитро-N-(2-пиридин-4-ил-этил)-бензолсульфонамида (1,63 г, 59%) в виде оранжевого твердого вещества. MS (ISP) 306,1 [(М-Н)–]; т. пл. 153°С.
б) Гидрогенизация перемешиваемого раствора 3-нитро-N-(2-пиридин-4-ил-этил)-бензолсульфонамида (1,52 г, 4,95 ммоль) в метаноле (95 мл) и ТГФ (55 мл) на палладий/углероде (10%, 0,15 г) в течение 4 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из этилацетата/гексана соединение, указанное в заголовке, в виде светло-желтого твердого вещества. MS (ISP) 276,0 [(М-Н)–]; т. пл. 138°С.
Пример В.8
3-Амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамид
а) К перемешиваемому раствору 2-амино-2-метил-1-пропанола (0,95 мл, 9,93 ммоль) в диоксане (25 мл) при комнатной температуре добавляли 3-нитробензолсульфонилхлорид (2,0 г, 9,02 ммоль) и триэтиламин (1,38 мл, 9,93 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 6 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (3×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:1) с выходом 3-нитро-N-циклопропилметил-бензолсульфонамида (1,04 г, 42%) в виде светло-желтого твердого вещества. MS (ISP) 273,2 [(М-Н)–].
б) Гидрогенизация перемешиваемого раствора 3-нитро-N-циклопропилметил-бензолсульфонамида (4,37 г, 15,9 ммоль) в метаноле (300 мл) на палладий/углероде (10%, 0,44 г) в течение 2 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из этилацетата/гексана соединение, указанное в заголовке, (3,79 г, 97%) в виде белого твердого вещества. MS (ISP) 243,2 [(М-Н)–]; т. пл. 96°С.
Пример В.9
3-Амино-N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-бензолсульфонамид
а) К перемешиваемому раствору 2-амино-2-метил-1,3-пропандиола (1,04 мл, 9,93 ммоль) в диоксане (25 мл) при комнатной температуре добавляли 3-нитробензолсульфонилхлорид (2,0 г, 9,02 ммоль) и триэтиламин (1,38 мл, 9,93 ммоль). Светло-желтую суспензию перемешивали при комнатной температуре в течение 6 ч, выливали в воду (100 мл) и экстрагировали дихлорметаном (3×75 мл). Объединенные органические слои промывали водой (100 мл) и рассолом (70 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:1) с выходом N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-3-нитро-бензолсульфонамида (0,65 г, 25%) в виде белого твердого вещества. MS (ISP) 289,1 [(М-Н)–]; т. пл. 116°С.
б) Гидрогенизация перемешиваемого раствора N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-3-нитро-бензолсульфонамида (0,59 г, 2,03 ммоль) в метаноле (60 мл) на палладий/углероде (10%, 0,06 г) в течение 2,5 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из этилацетат/гексана соединение, указанное в заголовке, (0,22 г, 42%) в виде оранжевого твердого вещества. MS (ISP) 259,3 [(М-Н)–]; т. пл. 129°С.
Пример В.10
3-Амино-4-хлор-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамид
а) К перемешиваемому раствору 2-амино-2-метил-1-пропанола (3,48 г, 39 ммоль) в 1N NaOH (25 мл) при комнатной температуре добавляли 4-хлор-3-нитробензолсульфонилхлорид (5,0 г, 19,5 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч, выливали в рассол (50 мл) и экстрагировали этилацетатом (3×70 мл). Объединенные органические слои промывали рассолом (50 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:4) и последующей кристаллизацией из этилацетата/гептана с получением 4-хлор-3-нитро-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (0,93 г, 15%) в виде беловатого твердого вещества. MS (ISP) 307,0 [(М-Н)–]; т. пл. 119°С.
б) Смесь 4-хлор-3-нитро-(2-гидрокси-1,1-диметил-этил)-бензол-сульфонамида (0,89 г, 2,89 ммоль), дитионита натрия (2,13 г, 10 ммоль), воды (9 мл) и 2-метоксиэтанола (9 мл) перемешивали при 100°С в течение 2 ч, добавляли дополнительную воду (6 мл) при 70°С и затем была добавлена НСl (37%, 6 мл) за 5 мин (выделение SO2). Реакционную смесь перемешивали при 70°С в течение 20 мин, выливали в лед/воду (50 мл) и добавляли карбонат натрия до тех пор, пока не подтверждалось, что раствор является основным. Раствор экстрагировали этилацетатом (3×70 мл), объединенные органические слои промывали рассолом (50 мл), высушивали (Na2SO4) и выпаривали. Неочищенный продукт далее очищали кристаллизацией из гексана/этилацетата с выходом соединения, указанного в заголовке, (0,65 г, 81%) в виде беловатого твердого вещества. MS (ISP) 277,1 [(М-Н)–]; т. пл. 108°С.
Пример В.11
3-Амино-N-(2-гидрокси-1,1-диметил-этил)-4-метил-бензолсульфонамид
а) К перемешиваемому раствору 2-амино-2-метил-1-пропанола (3,78 г, 42 ммоль) в 1N NaOH (25 мл) при комнатной температуре добавляли 4-метил-3-нитробензолсульфонилхлорид (5,0 г, 21 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 6 ч, выливали в рассол (50 мл) и экстрагировали этилацетатом (3×70 мл). Объединенные органические слои промывали рассолом (50 мл), высушивали (MgSO4) и выпаривали. Неочищенный продукт далее очищали колоночной хроматографией на силикагеле (гептан/этилацетат 1:4) и последующей кристаллизацией из этилацетата/гептана с выходом (2-гидрокси-1,1-диметил-этил)-4-метил-3-нитро-бензолсульфонамида (1,5 г, 25%) в виде беловатого твердого вещества. MS (ISP) 287,0 [(М-Н)–]; т. пл. 109°С.
б) Гидрогенизация перемешиваемого раствора (2-гидрокси-1,1-диметил-этил)-4-метил-3-нитро-бензолсульфонамида (1,46 г, 5,06 ммоль) в метаноле (50 мл) на палладий/углероде (10%, 0,15 г) в течение 1,5 ч при комнатной температуре давала после удаления катализатора фильтрацией, выпариванием и кристаллизацией из МеОН/диэтиловый эфир/гексан соединение, указанное в заголовке, (1,15 г, 88%) в виде беловатого твердого вещества. MS (ISP) 257,2 [(М-Н)–]; т. пл. 133°С.
Пример В.12
3-Амино-N-(2-диметиламино-этил)-бензолсульфонамид
Гидрогенизация перемешиваемого раствора N-(2-диметиламино-этил)-3-нитро-бензолсульфонамида [CAS-No. 117082-97-0] (1,44 г, 5,27 ммоль) в метаноле (145 мл) на палладий/углероде (10%, 0,14 г) в течение 2,5 ч при комнатной температуре давала после удаления катализатора фильтрацией и выпариванием соединение, указанное в заголовке, (1,25 г, 98%) в виде светло-желтой жидкости, которую использовали без дальнейшей очистки. MS (ISP) 242,2 [(М-Н)–].
Пример В.13
3-Амино-N-(1-гидроксиметил-циклопентил)-бензолсульфонамид
Смесь 3-нитро-бензолсульфонилхлорида (0,89 г, 4 ммоль) и (1-амино-циклопентил)-метанола (0,46 г, 4 ммоль) в дихлорметане (4 мл)/насыщенном растворе бикарбоната натрия (4 мл) перемешивали при 20°С в течение 20 ч. Смесь разбавляли дихлорметаном (20 мл). Слои отделяли и органический слой промывали водой, высушивали (Na2SO4) и выпаривали в вакууме. Твердый остаток растворяли в этаноле (20 мл) и гидрогенизировали в присутствии 5% палладия-углерода (0,2 г) с получением соединения, указанного в заголовке, (0,64 г, 59%). Беловатое твердое вещество. MS (ISP) 271,4 [(М+Н)+]; т. пл. 130-132°С.
Пример В.14
(3)-[1-(3-Амино-бензолсульфонил)-пирролидин-2-ил]-метанол
Подвергая 3-нитро-бензолсульфонилхлорид и L-пролинол процедуре, аналогичной описанной в примере В.13, получали соединение, указанное в заголовке. Бледно-желтое масло. MS (ISP) 257,3 [(М+Н)+].
Синтез промежуточных соединений: пиразоло-пиримидин карбоновых кислот (промежуточные соединения формулы VI) из ацетофенонов
Некоторые из промежуточных соединений, например производные пиразоло-пиримидин карбоновых кислот, которые могут быть использованы согласно общим методам I и II, имеются в продаже. При этом некоторые из этих промежуточных соединений готовят из ацетофенонов согласно методам, приведенным далее, и если не указано иное, эти соединения являются новыми. Специалист способен приготовить другие производные пиразоло-пиримидин карбоновых кислот, пригодные для общих методов I и II, с учетом следующих примеров получения:
Пример С.1
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
а) К перемешиваемому раствору этилдифторацетата (5,0 мл, 21 ммоль) в трет-бутилметиловом эфире (30 мл) при комнатной температуре добавляли 5,4М раствор метанолята натрия в метаноле (4,65 мл, 25 ммоль), а затем раствор имеющегося в продаже 4-трифторметил-ацетофенона (4,0 г, 21 ммоль) в трет-бутилметиловом эфире (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 19 ч, выливали в лед/воду (50 мл), подкисляли с помощью 2N НСl (40 мл) и экстрагировали диэтиловым эфиром (2×100 мл). Объединенные органические слои промывали рассолом (2×50 мл), высушивали (MgSO4) и выпаривали с получением неочищенного 4,4-дифтор-1-(4-трифторметил-фенил)-бутан-1,3-диона (5,87 г) в виде желтой жидкости, которую использовали без дальнейшей очистки.
б) Перемешиваемую смесь имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола (3,38 г, 22 ммоль) и 4,4-дифтор-1-(4-трифторметил-фенил)-бутан-1,3-диона (5,8 г, 22 ммоль) в уксусной кислоте (45 мл) нагревали с обратным холодильником в течение 1,5 ч. Реакционную смесь выпаривали, и неочищенный продукт (желтое твердое вещество, 8,5 г, 22 ммоль) растворяли в смеси 2М КОН в метаноле (176,5 мл, 0,35 моль) и воды (85 мл). Реакционную смесь перемешивали при 60°С в течение 1,5 ч, выливали в лед/воду (200 мл), подкисляли с помощью 3N серной кислоты (рН 4) и перемешивали при комнатной температуре в течение 30 мин. Осадок собирали фильтрацией и далее очищали кристаллизацией из диэтилового эфира/метанола с получением соединения, указанного в заголовке, (4,51 г, 57%) в виде беловатого твердого вещества. MS (ISP) 356,1 [(М-Н)–]; т. пл. 261°С.
Пример С.2
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 4-трифторметил-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола, согласно общему методу. Светло-желтое твердое вещество. MS (ЕI) 374,9 [М]; т. пл. 248°С.
Пример С.3
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, имеющегося в продаже 4-хлор-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 322,2 [(М-Н)–]; т. пл. 232°С.
Пример С.4
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этил трифторацетата, имеющегося в продаже 4-хлор-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 340,0 [(М-Н)–]; т. пл. 238°С.
Пример С.5
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этил дифторацетата, 3-метил-4-трифтор-ацетофенона (пример А.4) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 370,1 [(М-Н)–]; т. пл. 217°С.
Пример С.6
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 4-хлор-3-метил-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 354,0 [(М-Н)–]; т. пл. 243°С.
Пример С.7
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, имеющегося в продаже 3,4-дихлор-ацетофенона и имеющегося в продаже 3-амино- 4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 356,0 [(М-Н)–]; т. пл. 263°С.
Пример С.8
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, 3-метил-4-трифтор-ацетофенона (пример А.4) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 388,1 [(М-Н)–]; т. пл. 250°С.
Пример С.9
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 3,4-дихлор-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-желтое твердое вещество. MS (ISP) 374,1 [(М-Н)–]; т. пл. 264°С.
Пример С.10
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-кар6оновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, 3-(2,2,2-трифторэтокси-4-трифтор-ацетофенона (Пример А.6) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 471,9 [(М-Н)–]; т. пл. 264°С.
Пример С.11
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3- карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, 3-этокси-4-трифтор-ацетофенона (Пример А.5) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 418,0 [(М-Н)–); т. пл. 264°С.
Пример С.12
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, 3-этокси-4-трифтор-ацетофенона (Пример А.5) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Желтое твердое вещество. MS (ISP) 400,2 [(М-Н)–]; т. пл. 247°С.
Пример С.13
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, имеющегося в продаже 4-хлор-3-метил-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-желтое твердое вещество. MS (ISP) 336,0 [(М-Н)–]; т. пл. 238°С.
Пример С.14
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, 3-(2,2,2-трифторэтокси-4-трифтор-ацетофенона (Пример А.6) и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 454,2 [(М-Н)–]; т. пл. 261°С.
Пример С.15
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, 3-хлор-4-трифторметил-ацетофенона [CAS-No. 129322-80-1] и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-красное твердое вещество. MS (ISP) 390,2 [(М-Н)–]; т. пл. 216°С.
Пример С.16
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, имеющегося в продаже 3-фтор-4-трифторметил-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Твердое светло-коричневое вещество. MS (ISP) 374,1 [(М-Н)–]; т. пл. 233°С.
Пример С.17
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, 3-хлор-4-трифторметил-ацетофенона [CAS-No. 129322-80-1] и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-желтое твердое вещество. MS (ISP) 408,0 [(М-Н)–]; т. пл. 244°С.
Пример С.18
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 3-фтор-4-трифторметил-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-желтое твердое вещество. MS (ISP) 392,0 [(М-Н)–]; т. пл. 212°С.
Пример С.19 5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 4-трифторметокси-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Белое твердое вещество. MS (ISP) 390,0 [(М-Н)–]; т. пл. 225°С.
Пример С.20
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилдифторацетата, имеющегося в продаже 4-трифторметокси-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Беловатое твердое вещество. MS (ISP) 372,1 [(М-Н)–); т. пл. 231°С.
Пример С.21
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Соединение, указанное в заголовке, готовили из имеющегося в продаже этилтрифторацетата, имеющегося в продаже 3,4-дифтор-ацетофенона и имеющегося в продаже 3-амино-4-этоксикарбонил-пиразола согласно общему методу I. Светло-желтое твердое вещество. MS (ISP) 342,0 [(М-Н)–]; т. пл. 274°С.
Пример С.22
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-кар6оновая кислота
а. Смесь этил 3-(4-хлор-фенил)-3-оксо-пропионата (18,1 г, 0,080 моль) и этил 5-амино-1Н-пиразол-4-карбоксилата (13,7 г, 0,088 моль) перемешивали в течение 3 ч при 160°С. Этилацетат (40 мл) и гексан (40 мл) последовательно добавляли к охлажденной смеси, и продолжали перемешивание при 0°С в течение 0,5 ч. Кристаллы отделяли фильтрацией и растирали в течение 1,2 ч с 0,2N НСl (80 мл). Твердое вещество отфильтровывали, промывали водой и высушивали с получением этил 5-(4-хлор-фенил)-7-гидрокси-пиразоло[1,5-а]пиримидин-3-карбоксилата (13,3 г, 52%). Белое твердое вещество. MS (ISP) 316.3 [(М-Н)–]; т. пл. 190-192°С.
б. Смесь 5-(4-хлор-фенил)-7-гидрокси-пиразоло[1,5-а]пиримидин-3-карбоксилата (9,53 г, 0,03 моль), оксихлорида фосфора (11,0 мл, 0,12 моль) и N,N-диметиланилина (1,3 мл, 0,01 моль) перемешивали в течение 2 ч при 100°С. Смесь выпаривали в вакууме и остаток распределяли между водой и дихлорметаном. Органическую фазу промывали водой, высушивали (Na2SO4) и выпаривали в вакууме. Оставшееся твердое вещество кристаллизовали из этилацетат/гексана с получением 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидина (6,80 г, 67%). Бледно-желтое твердое вещество. MS (ISP) 336,0 [(М+Н)+]; т. пл. 133-135°С.
в. Смесь 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидина (0,34 г, 1,0 ммоль), триэтиламина (0,28 мл, 2,0 ммоль) и 5% палладия-углерода (0,03 г) в этаноле (60 мл) перемешивали в атмосфере водорода в течение 12 мин при 20°С. Катализатор удаляли фильтрацией, и раствор выпаривали. Остаток распределяли между этилацетатом и водой, и органический слой высушивали (Na2SO4) и выпаривали в вакууме. Остаток кристаллизовали из этилацетат/циклогексана с получением этил 5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоксилата (0,18 г, 59%). Беловатое твердое вещество. MS (ISP) 301, 9. [(M+H)+].
г. Смесь этил 5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоксилата (0,12 г, 0,4 ммоль) и 0,5N раствор гидроксида натрия (4 мл) в метаноле (4 мл) нагревали до 70°С в течение 2 ч. Смесь охлаждали, разбавляли водой (8 мл) и концентрировали в вакууме. Водный раствор подкисляли до рН 2 добавлением 3N НСl. Осадок выделяли фильтрацией, промывали водой и высушивали с получением 5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (0,11 г, 100%). Беловатое твердое вещество. MS (ISP) 272,3 [(М-Н)–]; т. пл. 309-311°С.
Пример С.23
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Подвергая этил 3-(4-трифтор-фенил)-3-оксо-пропионат процедуре, аналогичной описанной в примере С.22, стадии а-г, получали соединение, указание в заголовке. Белое твердое вещество. ЯМР (ДМСО-d6): d 7.97/8.52 (2 d, 2×2H), 7.98/9.41 (2 d, 2×1Н), 8.63 (s, 1H), 12.46 (s, 1H) ppm.
Пример С.24
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
К раствору 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидина (0,34 г, 1,0 ммоль) и тетракис(трифенилфосфин)палладия (0,35 г, 0,3 ммоль) в ТГФ (15 мл) при 20°С добавляли 2М раствор диметилцинк/толуола (1,3 мл, 3,6 ммоль), и смесь кипятили с обратным холодильником в атмосфере аргона в течение 2 ч. После медленного добавления при 0°С насыщенного водного раствора хлорида аммония (10 мл) смесь разделяли между этилацетатом и водой. Органический слой выпаривали в вакууме и остаток подвергали хроматографии на силикагеле с использованием этилацетат/гексана (1:2 об./об.) в качестве элюента с получением этил 5-(4-хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоксилата (0,15 г) в виде белого твердого вещества. Этот материал омыляли с использованием процедуры, аналогичной описанной в примере С.22, стадия г), с получением соединения, указанного в заголовке. Белое твердое вещество; MS (ISP) 286,0 [(М-Н)–]; т. пл. 233-235°С.
Пример С.25
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Подвергая этил 3-(4-трифтор-фенил)-3-оксо-пропионат процедурам, аналогичным описанным в Примере С.22, стадии а-б, и применяя к полученному продукту процедуру, описанную в примере С.24, получали соединение, указанное в заголовке. Белое твердое вещество. MS (ISP) 320,3 [(М-Н)–]; т. пл. 244-245°С.
Пример С.26
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
К раствору 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидина (1,0 г, 3,0 ммоль), тетракис(трифенилфосфин)палладия (0,35 г, 0,3 ммоль) в ТГФ (5 мл) при 20°С добавляли 0.4М раствор хлорида этилцинка/ТГФ (30 мл, 12 ммоль; свежеприготовленный путем перемешивания смеси 6 мл 2М хлорида этилмагния/ТГФ и 24 мл 0,5М хлорида цинка/ТГФ в течение 1 ч при 0°С, а затем 1 ч при 20°С), и смесь кипятили с обратным холодильником в атмосфере аргона в течение 2 ч. После медленного добавления при 0°С насыщенного водного раствора хлорида аммония (8 мл) смесь распределяли между этилацетатом и 10% раствором хлорида натрия. Органический слой выпаривали в вакууме и остаток подвергали хроматографии на силикагеле с использованием этилацетат/циклогексана (1:4 об./об.) в качестве элюента с получением этил 5-(4-хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (0,53 г, 54%). Этот материал омыляли с использованием процедуры, аналогичной описанной в примере С.22, стадия г), с получением соединения, указанного в заголовке. Белое твердое вещество; MS (ISP) 330,1 [(М-Н)–]; т. пл. 227°С.
Пример С.27
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Подвергая этил 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин процедуре, аналогичной описанной в Примере С.26, но заменив раствор хлорида этилцинка/ТГФ на 0.4М раствор хлорида пропилцинка/ТГФ (свежеприготовленный из хлорида этилмагния и хлорида цинка), получали соединение, указанное в заголовке. Белое твердое вещество. MS (ISP) 314,1 [(М-Н)–]; т. пл. 208°С.
Пример С.28
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
К раствору 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидина (4,0 г, 12,0 ммоль), тетракис(трифенилфосфин)палладия (1,15 г, 1,0 ммоль) в ТГФ (20 мл) при 20°С добавляли суспензию 0,25М хлорида циклопропилцинка/ТГФ (примерно 192 мл, 48 моль; свежеприготовленную путем перемешивания смеси 96 мл 0,5 М бромида циклопропилмагния/ТГФ и 96 мл 0,5М хлорида цинка/ТГФ (96 мл) в течение 1 ч при 0°С, а затем 1 ч при 20°С), и смесь кипятили с обратным холодильником в атмосфере аргона в течение 2,5 ч. После медленного добавления при 0°С насыщенного водного раствора хлорида аммония (30 мл), смесь распределяли между этилацетатом и 10% раствором хлорида натрия. Органический слой выпаривали в вакууме и остаток подвергали хроматографии на силикагеле с использованием этилацетат/циклогексана (1:4 об./об.) в качестве элюента с получением после кристаллизации из этилацетата этил 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2,54 г, 62%) в виде беловатого твердого вещества, т. пл. 141-143°С. Этот материал омыляли с использованием процедуры, аналогичной описанной в примере С.22, стадия (г), с получением соединения, указанного в заголовке. Беловатое твердое вещество, MS (ISP) 312,3 [(М-Н)–]; т. пл. 242-243°С.
Пример С.29
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновая кислота
Повергая этил 3-(4-трифтор-фенил)-3-оксо-пропионат процедурам, аналогичным описанным в примере С.22, стадии а-б, и применяя к полученному продукту процедуру, описанную в примере С.28, получали соединение, указанное в заголовке. Беловатое твердое вещество. MS (ISP) 346,3 [(М-Н)–]; т. пл. 233-235°С.
Синтез соединений по изобретению
Следующие примеры иллюстрируют изобретение без ограничения его объема лишь этими примерами.
Пример 1
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-супьфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 600,3 [(М+Н)+]; т. пл. 233°С.
Пример 2
5-(4-Метокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-метокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [CAS 333761-72-1; имеется в продаже] и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 562.4 [(М+Н)+]; т. пл. 203°С.
Пример 3
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II, как показано далее: к перемешиваемому раствору пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (1,0 ммоль) в ТГФ (4 мл) при комнатной температуре добавляли ДМФ (2 капли), раствор охлаждали до 0°С и добавляли оксалилхлорид (1,5 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 ч и выпаривали досуха. Осадок растворяли в пиридине (6 мл) и, перемешивая при комнатной температуре, добавляли 4-диметиламинопиридин (1 ммоль) и производное анилина (1 ммоль). Реакционную смесь оставляли перемешиваться при комнатной температуре в течение 16 ч, выпаривали досуха и неочищенный продукт очищали флэш-хроматографией на силикагеле (20 г, дихлорметан/метанол) с выходом продукта в виде светло-желтого твердого вещества, которое далее очищали кристаллизацией из метанол/гексана. MS (ISP) 580,1 [(М-Н)–]; т. пл. 221°С.
Пример 4
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 584,2 [(М+Н)+]; т. пл. 241°С.
Пример 5
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 550,2 [(MH-H)+]; т. пл. 252°C.
Пример 6
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонип)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 532,2 [(М+Н)+]; т. пл. 227°С.
Пример 7
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 561,5 [(М+Н)+]; т. пл. 147°С.
Пример 8
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 548,3 [(М+Н)+]; т. пл. 253°С.
Пример 9
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 579,2 [(М+Н)+]; т. пл. 195°С.
Пример 10
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 566,1 [(М+Н)+]; т. пл. 144°С.
Пример 11
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пирммидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 580,0 [(М+Н)+]; т. пл. 226°С.
Пример 12
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 595,2 [(М+Н)+]; т. пл. 261°С.
Пример 13
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 529,0 [(М+Н)+]; т. пл. 155°С.
Пример 14
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 564,3 [(М+Н)+]; т. пл. 230°С.
Пример 15
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.6) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 580,2 [(М+Н)+]; т. пл. 251°С.
Пример 16
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 567,2 [(М+Н)+]; т. пл. 245°С.
Пример 17
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 582,1 [(М+Н)+]; т. пл. 231°С.
Пример 18
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-этил-бензолсульфонамида [CAS 56445-08-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 556,0 [(М+Н)+]; т. пл. 207°С.
Пример 19
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-(пирролидин-4-сульфонил)-фениламина [CAS 91619-38-4; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 584,1 [(М+Н)+]; т. пл. 280°С.
Пример 20
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-(морфолин-4-сульфонил)-фениламина [САS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 601,3 [(М+Н)+]; т. пл. 239°С.
Пример 21
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-диметил-бензолсульфонамид [CAS 6274-18-6; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 558,3 [(М+Н)+]; т. пл. 210°С.
Пример 22
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.6) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 593,3 [(М+Н)+]; т. пл. 143°С.
Пример 23
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 595,3 [(М+Н)+]; т. пл. 229°С.
Пример 24
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 613,3 [(М+Н)+]; т. пл. 181°С.
Пример 25
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-этил-бензолсульфонамида [CAS 56445-08-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 538,1 [(М-Н)–]; т. пл. 259°С.
Пример 26
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N,N-диметил-бензолсульфонамида [CAS 6274-18-6: имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 540,4 [(М+Н)+]; т. пл. 197°С.
Пример 27
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 614,4 [(М+Н)+]; т. пл. 272°С.
Пример 28
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 627,4 [(М+Н)+]; т. пл. 199°С.
Пример 29
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-(4-метил-пиперазин-1-сульфонил)-фениламина [CAS 436095-35-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 609,3 [(М+Н)+]; т. пл. 198°С.
Пример 30
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.10) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 642,2 [(М-Н)–]; т. пл. 235°С.
Пример 31
7-Дифторметил-5-(3-этокси-4-трмфторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-(морфолин-4-сульфонил)-фениламина [CAS 22184-97-0; имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 624,3 [(М-Н)–]; т. пл. 231°С.
Пример 32
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.11) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 572,1 [(М-Н)–]; т. пл. 253°С.
Пример 33
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 554,0 [(М-Н)–]; т. пл. 254°С.
Пример 34
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.11) и 3-амино-N-этил-бензолсульфонамида [CAS 56445-08-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 600,0 [(М-Н)–]; т. пл. 226°С.
Пример 35
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-амино-N-этил-бензолсульфонамида [CAS 56445-08-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 582,0 [(М-Н)–]; т. пл. 222°С.
Пример 36
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 524,0 [(М-Н)–]; т. пл. 252°С.
Пример 37
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 542,1 [(М-Н)–]; т. пл. 245°С.
Пример 38
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 410,1 [(М-Н)–]; т. пл. 306°С.
Пример 39
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 528,0 [(М-Н)–]; т. пл. 302°С.
Пример 40
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 476,0 [(М-Н)–]; т. пл. 278°С.
Пример 41
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-супьфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.6) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 510,2 [(М+Н)+]; т. пл. 275°С.
Пример 42
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-метил-бензолсульфонамида [CAS 459434-40-3] согласно общему методу II. Желтое твердое вещество. MS (ISP) 524,1 [(М-Н)–]; т. пл. 255°С.
Пример 43
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 550,1 [(М-Н)–]; т. пл. 252°С
Пример 44
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-изопропил-бензолсульфонамида [CAS 118837-66-4] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 552,0 [(М-Н)–]; т. пл. 229°С
Пример 45
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 510,2 [(М-Н)–]; т. пл. 258°С.
Пример 46
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 568,0 [(М-Н)–]; т. пл. 232°С.
Пример 47
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-метил-бензолсульфонамида [CAS 459434-40-3] согласно общему методу II. Желтое твердое вещество. MS (ISP) 542,0 [(М-Н)–]; т. пл. 232°С.
Пример 48
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 511,4 [(М+Н)+]; т. пл. 251°С.
Пример 49
7-Трифторметил-5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-изопропил-бензолсульфонамид [CAS 118837-66-4] согласно общему методу II. Желтое твердое вещество. MS (ISP) 570,2 [(М-Н)–]; т. пл. 222°С.
Пример 50
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 529,3 [(М+Н)+]; т. пл. 259°С.
Пример 51
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а] пиримидин-3-карбоновой кислоты (пример С.4) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 494,0 [(М-Н)–]; т. пл. 260°С.
Пример 52
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2,2,2-трифторэтил)-бензолсульфонамида [синтез: смотри в разделе, касающемся производных анилина] согласно общему методу II. Желтое твердое вещество. MS (ISP) 592,0 [(М-Н)–]; т. пл. 257°С.
Пример 53
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 495,3 [(М+Н)+]; т. пл. 305°С.
Пример 54
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2,2,2-трифторэтил)-бензолсульфонамида (пример В.1) согласно общему методу II. Желтое твердое вещество. MS (ISP) 610,0 [(М-Н)–]; т. пл. 259°С.
Пример 55
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 511,3 [(М+Н)+]; т. пл. 262°С.
Пример 56
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 529,2 [(М+Н)+]; т. пл. 263°С.
Пример 57
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3- карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Твердое светло-коричневое вещество. MS (ISP) 525,2 [(М+Н)+]; т. пл. 261°С.
Пример 58
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3- карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 543.3 [(М+Н)+]: т. пл. 233°С.
Пример 59
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 582,0 [(М-Н)–]; т. пл. 201°С.
Пример 60
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 567,9 [(М-Н)–]; т. пл. 248°С.
Пример 61
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 534,1 [(М-Н)–]; т. пл. 257°С.
Пример 62
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.6) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 548,1 [(М-Н)–]; т. пл. 244°С.
Пример 63
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.5) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 564.2 [(М-Н)–]; т. пл. 199°С.
Пример 64
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.7) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 550,0 [(М-Н)–]; т. пл. 254°С.
Пример 65
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-амино-N-циклопропил-бензолсульфонамид [CAS 459434-39-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 516,1 [(М-Н)–]; т. пл. 262°С.
Пример 66
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-изобутил-бензолсульфонамида [CAS 608523-95-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 584,1 [(М-Н)–]; т. пл. 205°С.
Пример 67
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-циклопропилметил-бензолсульфонамида (пример В.2) согласно общему методу II. Желтое твердое вещество. MS (ISP) 582,1 [(М-Н)–]; т. пл. 234°С.
Пример 68
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.11) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 573,2 [(М+Н)+]; т. пл. 215°С.
Пример 69
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 555,3 [(М+Н)+]; т. пл. 211°С.
Пример 70
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 594,1 [(М-Н)–]; т. пл. 213°С.
Пример 71
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.11) и 3-амино-N-циклопропил-бензолсульфонамида [CAS 459434-39-0] согласно общему методу II. Желтое твердое вещество. MS (ISP) 612,2 [(М-Н)–] т. пл. 225°С.
Пример 72
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-изобутил-бензолсульфонамида [CAS 608523-95-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 566,2 [(М-Н)–]; т. пл. 186°С.
Пример 73
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-циклопропилметил-бензолсульфонамида (пример В.2) согласно общему методу II. Желтое твердое вещество. MS (ISP) 564,2 [(М-Н)–]; т. пл. 238°С.
Пример 74
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-фенилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-фенил-бензолсульфонамида [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 586,2 [(М-Н)–]; т. пл. 228°С.
Пример 75
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-бензил-бензолсульфонамида [CAS No. 303780-52-1] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 600,1 [(М-Н)–]; т. пл. 230°С.
Пример 76
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-фенилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-фенил-бензолсульфонамида [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 604,0 [(М-Н)–]; т. пл. 258°С.
Пример 77
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-бензил-бензолсульфонамида [CAS No. 303780-52-1] согласно общему методу II. Желтое твердое вещество. MS (ISP) 618,1 [(М-Н)–]; т. пл. 227°С.
Пример 78
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-[3-(2,2,2-трифторэтокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.10) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 626.1 [(М-Н)–]; т. пл. 233°С.
Пример 79
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-[3-(2,2,2-трифторэтокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.13) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 607,9 [(М-Н)–]; т. пл. 241°С.
Пример 80
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.10) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ЕI) 626,3 [М]; т. пл. 227°С
Пример 81
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.13) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (EI) 608,3 [М], т. пл. 207°С.
Пример 82
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-гидрокси-этил)-бензолсульфонамида [CAS 436095-41-9] согласно общему методу II. Желтое твердое вещество. MS (ISP) 572,0 [(М-Н)–]; т. пл. 227°С.
Пример 83
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-гидрокси-этил)-бензолсульфонамида [CAS 436095-41-9] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 554.0 [(М-Н)–]; т. пл. 231°С.
Пример 84
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.14) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ЕI) 491,1 [М]; т. пл. 264°С.
Пример 85
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-метил-4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (Пример С.14) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 488,9 [(М-Н)–]; т. пл. 270°С.
Пример 86
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-трифторметансульфонил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 565,3 [(М+Н)+]; т. пл. 207°С.
Пример 87
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-трифторметансульфонил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 583,3 [(М+Н)+]; т. пл. 207°С.
Пример 88
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-4-илметил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-пиридин-4-ил-метил-бензолсульфонамида (пример В.3) согласно общему методу II. Желтое твердое вещество. MS (ISP) 601,2 [(М-Н)–]; т. пл. 221°С
Пример 89
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-4-илметил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-пиридин-4-ил-метил-бензолсульфонамида (пример В.3) согласно общему методу II. Желтое твердое вещество. MS (ISP) 619,2 [(М-Н)–]; т. пл. 251°С.
Пример 90
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-(2-гидрокси-этансульфонил)-анилина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 541,4 [(М+Н)+]; т. пл. 205°С.
Пример 91
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-(2-гидрокси-этансульфонил)-анилина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 559,4 [(М+Н)+]; т. пл. 237°С.
Пример 92
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-(2-гидрокси-этансульфонил)-анилина [CAS-Nr. 344750-15-8; приготовлен из имеющегося в продаже 3-нитро-фенилметан-сульфонилхлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 524,0 [(М-Н)–]; т. пл. 280°С.
Пример 93
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-(2-гидрокси-этансульфонил)-анилина [CAS-Nr. 344750-15-8; приготовлен из имеющегося в продаже 3-нитро-фенилметан-сульфонилхлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 542,0 [(М-Н)–]: т. пл. 298°С.
Пример 94
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2,2-диметил-пропил)-бензолсульфонамида (пример В.4) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 580,3 [(М-Н)–]; т. пл. 208°С.
Пример 95
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-трет-бутил-бензолсульфонамида [CAS 608523-94-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 566,2 [(М-Н)–]; т. пл. 228°С.
Пример 96
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2,2-диметил-пропил)-бензолсульфонамида (пример В.4) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 598,1 [(М-Н)–]; т. пл. 231°С.
Пример 97
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-трет-бутил-бензолсульфонамида [CAS 608523-94-0] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 584,1 [(М-Н)–]; т. пл. 232°С.
Пример 98
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.15) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Твердое коричневое вещество. MS (ISP) 543,9 [(М-Н)–]; т. пл. 272°С.
Пример 99
7-Дифторметил-5-(3-трифторметил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-трифторметил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.16) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 528,0 [(М-Н)–]; т. пл. 262°С.
Пример 100
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.17) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 562,1 [(М+Н)+]; т. пл. 287°С.
Пример 101
5-(3-Трифторметил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.18) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 546,1 [(М+Н)+]; т. пл. 259°С.
Пример 102
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.15) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Твердое светло-коричневое вещество. MS (ISP) 543,0 [(М+Н)+]; т. пл. 228°С.
Пример 103
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.16) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Твердое светло-коричневое вещество. MS (ISP) 527,0 [(М+Н)+]; т. пл. 238°С.
Пример 104
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.17) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 561,1 [(М+Н)+]; т. пл. 268°С.
Пример 105
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3-фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.18) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 545,1 [(М+Н)+]; т. пл. 246°С.
Пример 106
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-ил-метил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-пиридин-3-ил-метил-бензолсульфонамида (пример В.5) согласно общему методу II. Желтое твердое вещество. MS (ISP) 603,2 [(М+Н)+]; т. пл. 256°С.
Пример 107
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-илметил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-пиридин-3-ил-метил-бензолсульфонамида (пример В.5) согласно общему методу II. Желтое твердое вещество. MS (ISP) 619,2 [(М-Н)–]; т. пл. 257°С.
Пример 108
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-ил-метил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-пиридин-2-ил-метил-бензолсульфонамида (пример В.6) согласно общему методу II. Желтое твердое вещество. MS (ISP) 601,1 [(М-Н)–]; т. пл. 208°С
Пример 109
7-Трифторметил-5-(4-грифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-илметил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-пиридин-2-ил-метил-бензолсульфонамида (пример В.6) согласно общему методу II. Желтое твердое вещество. MS (ISP) 619,3 [(М-Н)–]; т. пл. 229°С.
Пример 110
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-пиридин-4-ил-этил)-бензолсульфонамида (пример В.7) согласно общему методу II. Желтое твердое вещество. MS (ISP) 615,3[(М-Н)–]; т. пл. 238°С.
Пример 111
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-пиридин-4-ил-этил)-бензолсульфонамида (пример В.7) согласно общему методу II. Желтое твердое вещество. MS (ISP) 633.0 [(М-Н)–]; т. пл. 236°С.
Пример 112
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Оранжевое твердое вещество. MS (ISP) 582,0 [(М-Н)–]; т. пл. 232°С.
Пример 113
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 600,1 [(М-Н)–]; т. пл. 227°С.
Пример 114
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.20) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 526,2 [(М-Н)–]; т. пл. 231°С.
Пример 115
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.19) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 544,2 [(М-Н)–]; т. пл. 257°С.
Пример 116
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.20) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 527,2 [(М+Н)+]; т. пл. 223°С.
Пример 117
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.19) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 545.3 [(М+Н)+]; т. пл. 245°С.
Пример 118
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.21) и 3-сульфамоил-фениламина [имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 498,2 [(М+Н)+]; т. пл. 275°С.
Пример 119
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.21) и 3-метансульфонил-фениламина [имеется в продаже в виде гидрохлорида] согласно общему методу II. Желтое твердое вещество. MS (ISP) 497,1 [(М+Н)+]; т. пл. 256°С.
Пример 120
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 566,2 [(М-Н)–]; т. пл. 271°С.
Пример 121
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.17) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 634,0 [(М-Н)–]; т. пл. 251°С.
Пример 122
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.10) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 698,3 [(М-Н)–]; т. пл. 251°С.
Пример 123
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3- карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.8) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 614,2 [(М-Н)–]; т. пл. 230°С.
Пример 124
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.11) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 646,4 [(М+Н)+]; т. пл. 268°С.
Пример 125
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3,4-дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.9) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 599,8 [(М-Н)–]; т. пл. 269°С.
Пример 126
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(3-фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.18) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 620,3 [(М+Н)+]; т. пл. 221°С.
Пример 127
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.19) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Желтое твердое вещество. MS (ISP) 618,3 [(М+Н)+]; т. пл. 212°С.
Пример 128
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.3) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 550,1 [(М+Н)+]; т. пл. 229°С.
Пример 129
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.12) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 626,6 [(М-Н)–]; т. пл. 250°С.
Пример 130
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-6-метил-бензолсульфонамида [CAS-No. 6973-09-7] согласно общему методу II. Желтое твердое вещество. MS (ISP) 526,2 [(М+Н)+]; т. пл. 249°С.
Пример 131
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-6-метил-бензолсульфонамида [CAS-No. 6973-09-7] согласно общему методу II. Желтое твердое вещество. MS (ISP) 544,0 [(М+Н)+]; т. пл. 297°С.
Пример 132
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-3-нитро-бензолсульфонамида [CAS-No. 6374-97-6; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 600,4 [(М+Н)+]: т. пл. 208°С.
Пример 133
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-3-нитро-бензолсульфонамида [CAS-No. 6374-97-6; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 618,4 [(М+Н)+]; т. пл. 209°С.
Пример 134
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-бензолсульфонамида (пример В.9) согласно общему методу II. Желтое твердое вещество. MS (ISP) 600,4 [(М+Н)+]; т. пл. 246°С.
Пример 135
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-гидрокси-1-гидроксиметил-1-метил-этил)-бензолсульфонамида (пример В.9) согласно общему методу II. Желтое твердое вещество. MS (ISP) 616,2 [(М-Н)–]; т. пл. 248°С.
Пример 136
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-4-метил-бензолсульфонамида [CAS-No. 6274-28-8; имеется в продаже] согласно общему методу II. Желтое твердое вещество. MS (ISP) 542,1 [(М-Н)–]; т. пл. 310°С.
Пример 137
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-4-метил-бензолсульфонамида [CAS-No. 6274-28-8; имеется в продаже] согласно общему методу II. Твердое светло-коричневое вещество. MS (ISP) 524,0 [(М-Н)–]; т. пл. 293°С.
Пример 138
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-4-хлор-бензолсульфонамида [CAS-No. 29092-34-0; имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 563,1 [(М-Н)–]; т. пл. 300°С.
Пример 139
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пмримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-4-хлор-бензолсульфонамида [CAS-No. 29092-34-0; имеется в продаже] согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 545,1 [(М-Н)–]; т. пл. 286°С.
Пример 140
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-4-хлор-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.10) согласно общему методу II. Желтое твердое вещество. MS (ISP) 634,0 [(М-Н)–]; т. пл. 246°С.
Пример 141
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-4-хлор-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.10) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 616,2 [(М-Н)–]; т. пл. 234°С.
Пример 142
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-4-метил-бензолсульфонамида (пример В.11) согласно общему методу II. Желтое твердое вещество. MS (ISP) 614,2 [(М-Н)–]; т. пл. 240°С.
Пример 143
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-4-метил-бензолсульфонамида (пример В.11) согласно общему методу II. Светло-желтое твердое вещество. MS (ISP) 596.1 [(М-Н)–]; т. пл. 214°С.
Пример 144
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.1) и 3-амино-N-(2-диметиламино-этил)-бензолсульфонамида (пример В.12) согласно общему методу II. Желтое твердое вещество. MS (ISP) 583,4 [(М+Н)+]; т. пл. 184°С
Пример 145
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.2) и 3-амино-N-(2-диметиламино-этил)-бензолсульфонамида (пример В.12) согласно общему методу II. Желтое твердое вещество. MS (ISP) 601,3 [(М+Н)+]; т. пл. 224°С
Пример 146
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и 3-амино-N-(1-гидроксиметил-циклопентил)-бензолсульфонамида (пример В.13) согласно общему методу II. Желтое твердое вещество. MS (ISP) 594,0 [(М+Н)+]; т. пл. 253-255°С
Пример 147
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((8)-2-гидроксиметил-пирролидин-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.4) и (S)-[1-(3-aминo-бeнзoлcyльфoнил)-пиppoлидин-2-ил]-мeтaнoлa (пример В.14) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 580,3 [(М+Н)+]; т. пл. 227-229°С.
Пример 148
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.22) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 428,3 [(М+Н)+]; т. пл. 345°С.
Пример 149
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.22) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 427,4 [(М+Н)+]; т. пл. 258-260°С.
Пример 150
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.23) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 460,1 [(М-Н)–]; т. пл. 318-320°С
Пример 151
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.23) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 461,3 [(М+Н)+]; т. пл. 254-255°С.
Пример 152
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.24) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 442,4 [(М+Н)+]; т. пл. 308-310°С.
Пример 153
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.24) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 441,3 [(М+Н)+]; т. пл. 250-251°С.
Пример 154
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.24) и 3-aминo-N-(2-гидpoкcи-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 514,5 [(М+Н)+].
Пример 155
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.25) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 476,5 [(М+Н)+]: т. пл. 270-272°С.
Пример 156
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.25) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 475,1 [(М+Н)+]; т. пл. 198-200°С.
Пример 157
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.26) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 454,3 [(М-Н)–]; т. пл. 252-253°С.
Пример 158
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.26) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 455.92 [(М+Н)+] т. пл. 230-232°С.
Пример 159
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.26) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 528,0 [(М+Н)+]; т. пл. 239-240°С.
Пример 160
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.27) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 470,5 [(М+Н)+]; т. пл. 252-254°С.
Пример 161
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.27) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 469,5 [(М+Н)+]; т. пл. 214-217°С.
Пример 162
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.27) и 3-aминo-N-(2-гидpoкcи-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 542,3 [(М+Н)+]; т. пл. 207-208°С.
Пример 163
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 468,5 [(М+Н)+].
Пример 164
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 467,4 [(М+Н)+]; т. пл. 235-238°С.
Пример 165
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 540,5 [(М+Н)+].
Пример 166
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-амино-N-трет-бутил-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 524,5 [(М+Н)+]; т. пл. 238-239°С.
Пример 167
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((3)-2-гидроксиметил-пирролидмн-1-сульфонил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и (S)-[1-(3-aминo-бeнзoлcyльфoнил)-пиppoлидин-2-ил]-мeтaнoлa (пример В.13) согласно общему методу II. Бледно-желтое твердое вещество, т. пл. 180-182°С.
Пример 168
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-амино-N-(1-гидроксиметил-циклопентил)-бензолсульфонамида (пример В.13) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 566,3 [(М+Н)+]; т. пл. 255-257°С.
Пример 169
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид
Соединение, указанное в заголовке, готовили из 5-(4-хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.28) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-4-метил-бензолсульфонамида (пример В.11) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 554,3 [(М+Н)+].
Пример 170
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.29) и 3-амино-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 502,3 [(М+Н)+]; т. пл. 249-250°С.
Пример 171
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.29) и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 501,3 [(М+Н)+]; т.пл. 231-234°С.
Пример 172
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.29) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-бензолсульфонамида (пример В.8) согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 574,5 [(М+Н)+]; т. пл. 228-230°С.
Пример 173
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.29) и 3-амино-N-трет-бутил-бензолсульфонамида согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 558,2 [(М+Н)+]; т. пл. 258-259°С.
Пример 174
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид
Соединение, указанное в заголовке, готовили из 7-циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (пример С.29) и 3-амино-N-(2-гидрокси-1,1-диметил-этил)-4-метил-бензолсульфонамида (пример В.11) согласно общему методу II. Бледно-желтое твердое вещество, т. пл. 232-233°С.
Пример 175
7-Хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили из 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбонилхлорида и 3-метансульфонил-фениламина согласно общему методу II. Бледно-желтое твердое вещество. MS (ISP) 461.3 [(М+Н)+]; т. пл. 253-255°С.
Исходный материал готовили следующим образом:
7-Хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбонилхлорид
Смесь этил 5-(4-хлор-фенил)-7-гидрокси-пиразоло[1,5-а]пиримидин-3-карбоксилата (1,59 г, 5,0 ммоль) (пример С.22, стадия а) в диметилсульфоксиде (30 мл)/2N NaOH (10 мл) нагревали до 80°С в течение 1 ч с образованием белого осадка. После добавления воды (100 мл) к охлажденной смеси образовывался прозрачный раствор, который сначала промывали диэтиловым эфиром, а затем подкисляли до рН 2 путем добавления 3N НСl. Белый осадок отделяли фильтрацией и высушивали с получением 5-(4-хлор-фенил)-7-гидрокси-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (1,44 г, 99%). Белое твердое вещество. MS (ISP) 288,0 [(М-Н)–]; т. пл. 258°С.
Этот материал нагревали вместе с оксихлоридом фосфора (4,0 мл, 0,15 моль) и N,N-диметиланилином (0,19 мл, 2 ммоль) до 100°С в течение 2 ч. Смесь выпаривали в вакууме, и остаток распределяли между водой и дихлорметаном. Органическую фазу высушивали (Na2SO4) и выпаривали в вакууме с получением неочищенного соединения, указанного в заголовке, (1,6 г) в виде бледно-желтого твердого вещества.
Пример 176
5-(4-Хлор-фенил)-7-метокси-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид
Соединение, указанное в заголовке, готовили перемешиванием 7-хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амида (пример 175) (46 мг) с раствором метоксида натрия (11 мг) в метаноле (1,5 мл) в течение 2 ч при 50°С и последующим осаждением продукта путем добавления воды (10 мл). Бледно-желтое твердое вещество. MS (ISP) 457,5 [(М+Н)+]; т. пл. 265°С.
Приготовление фармацевтических композиций, содержащих соединения по изобретению:
Пример I
Таблетки следующего состава готовят традиционным способом:
 |
мг/таблетка |
| Активный ингредиент |
100 |
| Порошкообразная лактоза |
95 |
| Белый кукурузный крахмал |
35 |
| Поливинилпирролидон |
8 |
| Na карбоксиметилкрахмал |
10 |
| Стеарат магния |
2 |
| Вес таблетки |
250 |
Пример II
Таблетки следующего состава готовят традиционным способом:
 |
мг/таблетка |
| Активный ингредиент |
200 |
| Порошкообразная лактоза |
100 |
| Белый кукурузный крахмал |
64 |
| Поливинилпирролидон |
12 |
| Na карбоксиметилкрахмал |
20 |
| Стеарат магния |
4 |
| Вес таблетки |
400 |
Пример III
Готовят капсулы следующего состава:
 |
мг/капсула |
| Активный ингредиент |
50 |
| Кристаллическая лактоза |
60 |
| Микрокристаллическая целлюлоза |
34 |
| Тальк |
5 |
| Стеарат магния |
1 |
| Вес содержимого капсулы |
150 |
Активный ингредиент с подходящим размером частиц, кристаллическую лактозу и микрокристаллическую целлюлозу смешивают друг с другом до получения однородной смеси, просеивают и затем примешивают тальк и стеарат магния. Конечной смесью заполняют твердые желатиновые капсулы подходящего размера.
Формула изобретения
1. Соединение формулы I

где р представляет собой 0 или 1;
R1 и R2 могут независимо друг от друга представлять собой Н; галоген; низший алкил; низший алкокси, возможно замещенный одним или более чем одним галогеном; или CF3;
R3 представляет собой низший алкил; гидрокси-низший алкил; или NRaRb;
Ra и Rb независимо выбраны из группы, состоящей из:
Н;
низшего алкила, возможно замещенного одним или более чем одним гидрокси, фтором, С3-6циклоалкилом, фенилом, пиридилом или NRcRd,
где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкила, содержащего 3-6 атомов углерода;
фенила;
или Ra и Rb вместе с атомом азота, к которому они присоединены, могут образовать 5- или 6-членный гетероцикл, возможно содержащий дополнительно 1 или 2 гетероатома, выбранных из О или N, и возможно замещенный низшим алкилом или гидрокси-низшим алкилом;
R4 представляет собой Н, Cl, низший алкокси, циклоалкил, содержащий 3-6 атомов углерода, или неразветвленный низший алкил, который возможно замещен одним или более чем одним F;
R5 представляет собой Н; галоген или низший алкил;
а также их фармацевтически приемлемые соли,
за исключением соединений следующих формул:
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метилфенил)-N-[3-(4-морфолинилсульфонил)фенил];
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-N-[3-(4-морфолинилсульфонил)фенил]-5-фенил]; и
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метоксифенил)-N-[3-(4-морфолинилсульфонил)фенил].
2. Соединение формулы I по п.1, где R1 и R2 независимо выбраны из группы, состоящей из Н, Cl, Me, CF3, МеО, EtO и CF3CH2O-; и R3, R4, R5 и р являются такими, как определено в п.1.
3. Соединение формулы I по п.1, где
р представляет собой 0 или 1;
R1 и R2 независимо выбраны из группы, состоящей из Н; галогена; низшего алкила; низшего алкокси, возможно замещенного одним или более чем одним галогеном; или CF3;
R3 выбран из группы, состоящей из низшего алкила; гидрокси-низшего алкила; NRaRb,
где Ra и Rb независимо выбраны из группы, состоящей из:
Н;
низшего алкила, возможно замещенного одним или более чем одним фтором, гидрокси, С3-6циклоалкилом, фенилом, пиридилом, или NRcRd,
где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкила, содержащего 3-6 атомов углерода;
фенила;
или Ra и Rb вместе с атомом азота, к которому они присоединены, образуют 4-морфолинильную; 1-пирролидинильную или 1-пиперазинильную группу;
R4 представляет собой Н, циклопропил или неразветвленный низший алкил, который возможно замещен одним или более чем одним F;
R5 представляет собой Н; галоген или низший алкил.
4. Соединение формулы I по п.3, где R3 представляет собой низший алкил и R1, R2,
R4, R5 и р являются такими, как определено в п.3.
5. Соединение формулы I по п.4, где указанное соединение выбрано из группы, состоящей из следующих соединений:
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Трифторметил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3-фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид;
7-Хлор-5-(4-хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид; и
5-(4-Хлор-фенил)-7-метокси-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метансульфонил-фенил)-амид.
6. Соединение формулы I по п.3, где R3 представляет собой гидрокси-низший алкил; и R1, R2, R4, R5 и р являются такими, как определено в п.3.
7. Соединение формулы I по п.6, где указанное соединение выбрано из группы, состоящей из:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амида; и
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоилметил-фенил)-амида.
8. Соединение формулы I по п.3, где R3 представляет собой NRaRb, причем Ra и Rb независимо выбраны из:
Н;
низшего алкила, возможно замещенного одним или более чем одним гидрокси, фтором, С3-6циклоалкилом, фенилом, пиридилом или NRcRd,
где Rc и Rd независимо выбраны из Н или низшего алкила;
циклоалкила, содержащего 3-6 атомов углерода;
фенила;
и R1, R2, R4, R5 и р являются такими, как определено в п.3.
9. Соединение формулы I по п.8, где указанное соединение выбрано из группы, состоящей из следующих соединений:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-[3-(2,2,2-трифтор-этокси)-4-трифторметил-фенил]-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этансульфонил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(4-метил-пиперазин-1-сульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-этилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-диметилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-метилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2,2-трифтор-этилсульфамоил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-циклопропилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-изобутилсульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(циклопропилметил-сульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-фенилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-бензилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трифторметансульфонил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2,2-диметил-пропилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(3-фтор-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-ил-метил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-3-ил-метил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-ил-метил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[(пиридин-2-ил-метил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-пиридин-4-ил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметокси-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(3,4-Дифтор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Хлор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-[3-(2,2,2-Трифтор-этокси)-4-трифторметил-фенил]-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(3-Фтор-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Трифторметокси-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(3-этокси-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (4-метил-3-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты {3-[бис-(2-гидрокси-этил)-сульфамоил]-фенил}-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1-гидроксиметил-1-метил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-метил-5-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (2-хлор-5-сульфамоил-фенил)-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [2-хлор-5-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид;
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-диметиламино-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-метил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Метил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-этил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-пропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(1-гидроксиметил-циклопентилсульфамоил)-фенил]-амид;
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-сульфамоил-фенил)-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(2-гидрокси-1,1-диметил-этилсульфамоил)-фенил]-амид;
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты (3-трет-бутилсульфамоил-фенил)-амид; и
7-Циклопропил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [5-(2-гидрокси-1,1-диметил-этилсульфамоил)-2-метил-фенил]-амид.
10. Соединение формулы I по п.3, где R3 представляет собой 4-морфолинил, и R1, R2, R4, R5 и р являются такими, как определено в п.3.
11. Соединение формулы I по п.10, где указанное соединение выбрано из группы, состоящей из следующих соединений:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
7-Дифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-дифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3,4-Дихлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
5-(3-Метил-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид; и
5-(3-Этокси-4-трифторметил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(морфолин-4-сульфонил)-фенил]-амид;
12. Соединение формулы I по п.3, где R3 представляет собой пирролидин, и R1, R2, R4, R5 и р являются такими, как определено в п.3.
13. Соединение формулы I по п.12, где указанное соединение выбрано из группы, состоящей из следующих соединений:
7-Трифторметил-5-(4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
7-Дифторметил-5-(3-метил-4-трифторметил-фенил)-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
5-(4-Хлор-3-метил-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-(пирролидин-1-сульфонил)-фенил]-амид;
5-(4-Хлор-фенил)-7-трифторметил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((S)-2-гидроксиметил-пирролидин-1-сульфонил)-фенил]-амид; и
5-(4-Хлор-фенил)-7-циклопропил-пиразоло[1,5-а]пиримидин-3-карбоновой кислоты [3-((S)-2-гидроксиметил-пирролидин-1-сульфонил)-фенил]-амид.
14. Фармацевтическая композиция, содержащая соединение по любому из пп.1-13, для предотвращения или лечения заболевания или состояния, в которое вовлечена или играет роль активация mGluR2.
15. Фармацевтическая композиция по п.14 для предотвращения или лечения острых и/или хронических неврологических нарушений, таких как психоз, шизофрения, болезнь Альцгеймера, когнитивные расстройства, нарушения памяти и глиома.
16. Применение соединения формулы I по любому из пп. 1-13, включая соединения следующих формул:
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метилфенил)-N-[3-(4-морфолинилсульфонил)фенил];
пиразоло[1,5-а]пиримидин-3-карбоксамид,7-(дифторметил)-N-[3-(4-морфолинилсульфонил)фенил]-5-фенил]; и
пиразоло[1,5-а]пиримидин-3-карбоксамид, 7-(дифторметил)-5-(4-метоксифенил)-N-[3-(4-морфолинилсульфонил)фенил];
для лечения или предотвращения заболевания или состояния, в которое вовлечена или играет роль активация mGluR2.
17. Применение по п.16 для лечения или предотвращения острых и/или хронических неврологических нарушений, включая психоз, шизофрению, болезнь Альцгеймера, когнитивные расстройства, нарушения памяти и глиому.
18. Применение соединения формулы I по п.16 для изготовления лекарства для лечения или предотвращения заболевания или состояния, в которое вовлечена или играет роль активация mGluR2.
19. Применение по п.18 для лечения и/или предотвращения острых и/или хронических неврологических нарушений, включая психоз, шизофрению, болезнь Альцгеймера, когнитивные расстройства, нарушения памяти и глиому.
|
|