Патент на изобретение №2378242
|
||||||||||||||||||||||||||
(54) СУЛЬФИРОВАННЫЕ НИТРОФЕНОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОЛИМЕРИЗАЦИИ
(57) Реферат:
Настоящее изобретение относится к ингибированию и замедлению полимеризации этиленненасыщенных мономеров. Описан способ ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества, по меньшей мере, одного ингибитора, который является сульфированным нитрофенолом формулы 1, где R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, углеводорода, NO2, и SO3H, при условии, что, по меньшей мере, один R1, R2 и R3 является NO2, и, по меньшей мере, один R1, R2 и R3 является SO3H. Также описан способ ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества комбинации (А), по меньшей мере, одного первого ингибитора, который является сульфированным нитрофенолом формулы 1, где R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, углеводорода, NO2 и SO3H, при условии, что, по меньшей мере, один R1, R2 и R3 является NO2, и, по меньшей мере, один R1, R2 и R3 является SO3H; и (В), по меньшей мере, одного второго ингибитора, выбранного из группы, состоящей из нитроксильных соединений, нитрозоанилинов, нитрофенолов, аминов и их смесей. Технический результат – получение высокоэффективного и недорогого ингибитора полимеризации этиленненасыщенных соединений. 2 н. и 18 з.п. ф-лы.
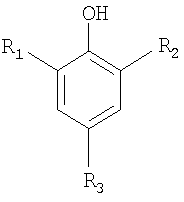
На основании Раздела 35 Кодекса законов США [секция] 120 мы испрашиваем приоритет по предварительной заявке на Патент США номер 60/614377, выданной 28 сентября 2004 года, озаглавленной СУЛЬФИРОВАННЫЕ НИТРОФЕНОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОЛИМЕРИЗАЦИИ и предварительной заявке на Патент США номер 60/632529, выданной 3 декабря 2004 года, озаглавленной СУЛЬФИРОВАННЫЕ НИТРОФЕНОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОЛИМЕРИЗАЦИИ. УРОВЕНЬ ТЕХНИКИ 1. Область техники, к которой относится изобретение Настоящее изобретение относится к ингибированию и замедлению полимеризации этиленненасыщенных мономеров путем добавления к ним сульфированных нитрофенолов. 2. Описание предшествующего уровня техники Многие этиленненасыщенные мономеры склонны к нежелательной полимеризации на различных стадиях их производства, переработки, транспортировки, хранения и применения. Полимеризация, например термическая полимеризация в процессе требующейся очистки мономера, приводит к его потере, то есть к более низкому выходу, и повышению вязкости любых получаемых далее смол. Переработка и транспортировка смол с более высокой вязкостью требует более высокой температуры и затрат (затраты энергии) для удаления остаточного мономера. Полимеризация может также приводить к забивке оборудования, особенно в случае производства акриловых мономеров. Такая полимеризация приводит к снижению эффективности производства из-за отложения полимера в или на используемом оборудовании. Эти отложения должны периодически удаляться, что приводит к дополнительным потерям при производстве мономера. Для ингибирования неконтролируемой и нежелательной полимеризации этиленненасыщенных мономеров было предложено и использовано большое разнообразие соединений. Однако многие из этих соединений были практически неприемлемыми. В Патенте США 2867672 раскрывается, что может быть сведена до минимума полимеризация конденсирующегося на поверхностях в жидком виде неингибированного стирола, содержащегося в виде пара над поверхностью основной части жидкого стирола в емкости, путем опрыскивания ингибитором полимеризации стирола поверхностей, окружающих паровое пространство. В Патенте США 4086147 описан способ дистилляции легкополимеризующихся виниловых ароматических соединений, включающий воздействие ингибитора полимеризации, содержащего м-нитро-п-крезол, на винилароматическое соединение при повышенных температурах в ректификационной системе. В Патенте США 4468343 раскрывается соединение и способ применения соединения для предотвращения полимеризации винилароматических соединений, таких как стирол, при нагревании. Композиция включает эффективные количества 2,6-динитро-п-крезола и или фенилендиамина или 4-трет-бутилкатехина соответственно, которые действуют как соингибиторная система полимеризации в присутствии кислорода. В Патенте США 4670131 описывается контролирование забивки оборудования, используемого для переработки потоков органического сырья, содержащего олефиновые соединения, путем ингибирования полимеризации олефиновых соединений за счет проведения переработки олефинов в присутствии стабильного свободного радикала, такого как нитроксид, от 20 ppb до меньше чем 1000 ppb. В Патенте США 5254760 раскрывается ингибирование полимеризации винилароматического соединения, такого как стирол, при его ректификации или очистки в результате присутствия, по меньшей мере, одного стабильного нитроксильного соединения вместе, по меньшей мере, с одним ароматическим нитросоединением. В Патенте США 5290888 описывается способ стабилизации этиленненасыщенного мономера или олигомера от преждевременной полимеризации, в соответствии с которым стабилизирующее количество N-гидроксизамещенного стерически затрудненного амина добавляют к указанному способному к полимеризации мономеру или олигомеру. К этиленненасыщенному мономеру или олигомеру относятся виниловые мономеры или олигомеры, имеющие в своей структуре, по меньшей мере, один способный к полимеризации фрагмент.Указано, что преждевременную полимеризацию в жидкой и/или паровой фазе ингибирует N-гидроксизамещенный стерически затрудненный амин. В Патенте США 5446220 раскрываются способы ингибирования полимеризации винилароматических олигомеров в системах технологического оборудования, не содержащих кислород. Эти способы включают добавление от 1 до 10000 частей комбинации динитрофенольного соединения, гидроксиламинного соединения и финилендиаминного соединения на миллион частей мономера. Предпочтительно, чтобы использовался 2-втор-бутил-4,6-динитрофенол или 4,6-динитро-o-крезол в комбинации с бис-(гидроксипропил)гидроксиламином и N,N’-ди-втор-бутил-п-фенилендиамином. В Патенте США 5545786 описывается, что нитроксильные ингибиторы в комбинации с кислородом уменьшают преждевременную полимеризацию винилароматических мономеров в процессе их производства. Также раскрывается, что даже небольшие количества воздуха, используемые в комбинации с нитроксильными ингибиторами, приводят к значительному увеличению времени ингибирования для указанных мономеров. В Патенте США 5932735 раскрывается, что выбранные производные 1-оксил-2,2,6,6-тетраметил-4-гидроксипиперидина являются эффективными в качестве ингибиторов для предотвращения преждевременной полимеризации акриловой и метакриловой кислот, их эфиров, их амидов, винилацетата и акрилонитрила в присутствии воды. В Патенте США 6143205 описывается смесь для ингибирования преждевременной полимеризации мономеров, которая содержит (A) винилсодержащие мономеры и (B) эффективное количество смеси (i) от 0,05 до 4,5% по массе от суммарной массы смеси (B), по меньшей мере, одно N-оксильное соединение вторичного амина, у которого отсутствуют атомы водорода на В Патентах России 1027150, 1139722 и 1558888 описано пониженное полимерообразование в условиях нормальной эксплуатации (истинные ингибиторы), но не обеспечивается защита системы в случаях аварийной остановки подачи сырья, то есть отсутствует эффект замедления. Упомянутые выше патенты включены в описание путем соответствующих ссылок на них. СУЩНОСТЬ ИЗОБРЕТЕНИЯ В соответствии с настоящим изобретением было обнаружено, что сульфированные нитрофенолы являются отличными ингибиторами и замедлителями для предотвращения полимеризации этиленненасыщенных соединений. Эти материалы необязательно могут быть использованы в комбинации с нитрофенолами, такими как 2,4-динитро-o-втор-бутилфенол (DNBP); соединениями типа нитроксильного радикала, такими как 4-оксо-TEMPO, с нитрофенолами и аминами, такими как N-метилпирролидинон (NMP); нитрозоанилинами, например C-нитрозоанилинами, такими как 4-нитрозо-N-(1,4-диметилпентил)-анилин, с нитрофенолами и аминами; и другими подобными соединениями и их комбинациями. Преимуществом настоящего изобретения является то, что сульфированные нитрофенолы могут быть легко получены при производстве нитрофенола путем изменения условий нитрования. Поэтому целью настоящего изобретения является разработка высокоэффективного и недорогого ингибитора полимеризации, обладающего превосходными качествами истинного ингибитора и замедлителя. Эта и другие цели достигаются настоящим изобретением, относящимся к способу ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, которое включает добавление к указанным мономерам эффективного количества, по меньшей мере, одного ингибитора, являющегося сульфированным нитрофенолом формулы:
где: R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, углеводорода, NO2, и SO3H, при условии, что, по меньшей мере, один R1, R2 и R3 является NO2 и, по меньшей мере, один R1, R2, и R3 является SO3H. В предпочтительном варианте осуществления настоящее изобретение относится к способу ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, который включает добавление к указанным мономерам эффективного количества комбинации: (A), по меньшей мере, одного первого ингибитора, являющегося сульфированным фенолом формулы:
где: R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, углеводорода, NO2 и SO3H, при условии, что, по меньшей мере, один R1, R2 и R3 является NO2 и, по меньшей мере, один R1, R2 и R3 является SO3H; и (B) по меньшей мере, одного второго ингибитора, выбранного из группы, состоящей из нитроксильных соединений, нитрозоанилинов, нитрофенолов, аминов и их смесей. ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ Как было заявлено выше, настоящее изобретение относится к ингибиторам и способу ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, который включает добавление к указанным мономерам эффективного количества, по меньшей мере, одного ингибитора, являющегося сульфированным нитрофенолом формулы:
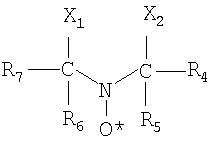
где: R1, R2 и R3 независимо выбирают из группы, состоящей из водорода, углеводорода, NO2 и SO3H, при условии, что, по меньшей мере, один R1, R2 и R3 является NO2 и, по меньшей мере, один R1, R2 и R3 является SO3H. Сульфированные нитрофенолы, применяемые в настоящем изобретении, могут быть легко получены в две стадии. Исходный фенол обрабатывают концентрированной H2SO4 с получением сульфированного производного фенола. Сульфированный фенол подвергают затем взаимодействию с HNO3. Мольное отношение HNO3:фенол должно составлять от 0,5 до 1,9, предпочтительно – от 0,9 до 1,1. Концентрация азотной кислоты должна быть от 1 до 65%, предпочтительно – от 16 до 35%. Температура должна составлять от 40 до 80°C. Конечный продукт может содержать некоторое количество нитрофенола, который также обладает хорошим замедляющим действием. В предпочтительном варианте осуществления ингибирующая система дополнительно включает один или более дополнительных ингибиторов, выбранных из группы, состоящей из нитрофенолов, нитроксильных соединений, нитрозоанилинов, аминов и их смесей. Когда один из R1, R2 и R3 является углеводородом, предпочтительно, чтобы алкил или алкенил с линейной или разветвленной цепью имел от 1 до 18 углеродных атомов, более предпочтительно – от 1 до 12 углеродных атомов, включая, но этим не ограничивая, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, 2-этилгексил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, олеил, их изомеры, такие как изопропил, втор-бутил, неопентил, и другие подобные изомеры; или циклические алкильные группы, такие как циклопентил, циклогексил, циклогептил, циклооктил и циклододецил. Нитрофенолы, которые могут быть применены в настоящем изобретении, включают, но этим не ограничивая, 2,6-динитро-4-метилфенол, 2-нитро-4-метилфенол, 2,4-динитро-1-нафтол, 2,4,6-тринитрофенол (пикриновая кислота), 2,4-динитро-6-метилфенол, 2,4-динитрофенол, 2,4-динитро-6-втор-бутилфенол, 4-циано-2-нитрофенол, 3-йод-4-циано-5-нитрофенол, м-нитро-п-крезол, 2,6-динитро-п-крезол и другие подобные нитрофенолы. 2,4-Динитро-6-втор-бутилфенол является предпочтительным. Сульфированные нитрофенолы настоящего изобретения могут также с успехом применяться с дополнительным ингибитором, которым является нитроксильное соединение, предпочтительно – стабильное стерически затрудненное нитроксильное соединение со структурной формулой:
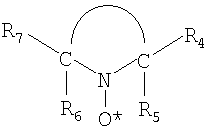
где R4 и R7 независимо выбирают из группы, состоящей из водорода, алкила и замещенного гетероатомом алкила, и R5 и R6 независимо выбирают из группы, состоящей из алкила и замещенного гетероатомом алкила; и X1 и X2 (1) независимо выбирают из группы, состоящей из галогена, циано, COOR10, -S-COR10, -OCOR10, где R10 является алкилом или арилом, амидо, -S-C6H5, карбонила, алкенила или алкила, содержащего от 1 до 15 углеродных атомов, или (2) будучи взятые вместе образуют кольцевую структуру с азотом. В конкретном предпочтительном варианте осуществления стабильное стерически затрудненное нитроксильное соединение имеет структурную формулу:
где R4 и R7 независимо выбирают из группы, состоящей из водорода, алкила и замещенного гетероатомом алкила, и R5 и R6 независимо выбирают из группы, состоящей из алкила и замещенного гетероатомом алкила, и
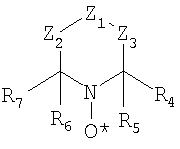
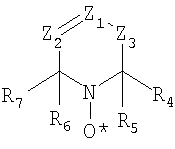
фрагмент представляет атомы, необходимые для образования пяти-, шести- или семичленного гетероциклического кольца. Соответственно, один из нескольких классов циклических нитроксидов, который может быть применен в настоящем изобретении, может быть представлен следующей структурной формулой:
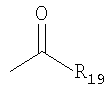
где Z1, Z2 и Z3 независимо выбирают из группы, состоящей из кислорода, серы, вторичных аминов, третичных аминов, фосфором в различных степенях окисления и замещенных или незамещенных углеродных атомов, таких как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHОH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CRSOR9, >CHNR8R9, >CCONR8R9, >C=NOH, >C=CH-C6H5, >CF2, >CCl2, >CBr2, >CI2, >CR8PR13R14R15 и других подобных, где R8 и R9 независимо выбирают из группы, состоящей из водорода, алкила, арила и ацила, и R13, R14 и R15 независимо выбирают из группы, состоящей из необобщенных электронов, алкила, арила, =О, OR16, и NR17R18, где R16, R17 и R18 независимо выбирают из группы, состоящей из водорода, алкила и арила. Когда R8 и/или R9 являются алкилом, предпочтительно, чтобы они были низшим алкилом (то есть алкилом, имеющим от одного до пяти углеродных атомов, например метилом, этилом, пропилом, бутилом, пентилом и их изомерами). Когда R8 и/или R9 являются арилом, предпочтительно, чтобы они были арилом, содержащим от 6 до 10 углеродных атомов, например, фенилом или нафтилом, которые, кроме того, могут быть замещены подходящими заместителями, например низшими алкильными группами, галогенами и другими подобными заместителями. Когда R8 и/или R9 являются ацилом, предпочтительно, чтобы они были ацилом структуры
где R19 является алкилом, арилом, OR20 или NR20R21 и где R20 и R21 являются алкилом, арилом или
где R22 является алкилом или арилом. Когда R19, R20, R21 или R22 являются алкилом, предпочтительно, чтобы они были алкилом, содержащим от 1 до 15 углеродных атомов, более предпочтительно – низшим алкилом, содержащим от 1 до 5 углеродных атомов, как описано выше. Когда R19, R20, R21 или R22 являются арилом, предпочтительно, чтобы они были арилом, содержащим от 6 до 10 углеродных атомов, как описано выше. Другие несколько классов циклических нитроксидов, которые могут быть применены в настоящем изобретении, представлены следующей структурной формулой:
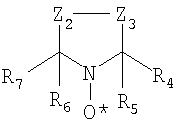
где Z1 и Z2, которые могут быть одинаковыми или различными, являются атомами азота или замещенного или незамещенного углерода, такими как=C(H)-, =C(CH3)-, =C(COOH)-, =C(COOCH3)-, =C(COOC2H5)-, =C(OH)-, =C(CN)-, =C(NR8R9)-, =C(CONR8R9)-, и другими подобными, где Z3, R8 и R9 описаны выше. Циклические нитроксиды, применяемые в настоящем изобретении, могут также быть получены из пятичленных колец. Эти соединения имеют структуру:
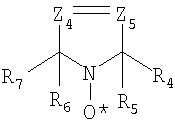
где Z2 и Z3, которые могут быть одинаковыми или различными, являются серой, кислородом, вторичными аминами, третичными аминами, фосфором в различных степенях окисления или замещенными или незамещенными углеродными атомами, такими как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHOH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CR8OR9, >CHNR8R9, >CCONR8R9, >C=NOH, >C=CH-C6H5, CF2, CCl2, CBr2, CI2, >CR8PR13R14R15, и другими подобными, где несколько R групп описаны выше. Циклические нитроксиды, применяемые в настоящем изобретении, могут также иметь структуру:
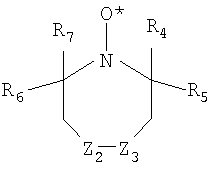
где Z4 и Z5, которые могут быть одинаковыми или различными, могут быть атомами азота или замещенными или незамещенными углеродными атомами, такими как =C(H)-, =C(CH3)-, =C(COOH)-, =C(COOCH3)-, =C(COOC2H5)-, =C(OH)-, =C(CN)-, =C(NR8R9), =C(CONR8R9)-, и другими подобными, где R8 и R9 описаны выше. Другой класс циклических нитроксидов, который может применяться в настоящем изобретении, имеет структуру:
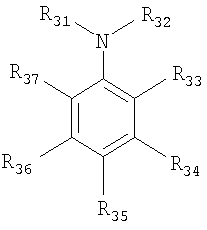
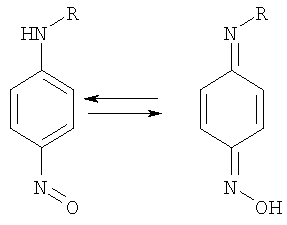
где Z2 и Z3, которые могут быть одинаковыми или различными, являются серой, кислородом, вторичными аминами, третичными аминами или замещенными или незамещенными углеродными атомами, такими как >CH2, >CHCH3, >C=O, >C(CH3)2, >CHBr, >CHCl, >CHI, >CHF, >CHOH, >CHCN, >C(OH)CN, >CHCOOH, >CHCOOCH3, >CHCOOC2H5, >C(OH)COOC2H5, >C(OH)COOCH3, >C(OH)CHOHC2H5, >CHNR8R9, >CONR8R9, >CR8OR9, >C=NOH, >C=CH-C6H5, CF2, CCl2, CBr2, CI2, >CR8PR13R14R15, и другими подобными, где несколько R групп описаны выше. Кроме того, две или более нитроксильные группы могут быть представлены в одной и той же молекуле, например, путем связывания через один или более фрагментов типа Z путем связывания группы E, как описано в Патенте США 5254760, который приводится здесь путем ссылки на него. Как было заявлено выше, для всех вышеприведенных нитроксильных структур R4 и R7 независимо выбирают из группы, состоящей из водорода, алкила и алкила, замещенного гетероатомом, и R5 и R6 независимо выбирают из группы, состоящей из алкила и алкила, замещенного гетероатомом. Алкильные (или алкильные, замещенные гетероатомом) группы от R4 до R7 могут быть одинаковыми или различными и могут предпочтительно содержать от 1 до 15 углеродных атомов, например метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, и другие подобные алкилы и их изомеры, например, т-бутил, 2-этилгексил и другие подобные изомеры. Более предпочтительно, чтобы группы от R4 до R7 были независимо выбранным низшим алкилом (или низшим алкилом, замещенным гетероатомом), содержащим от одного до пяти углеродных атомов (например, метилом, этилом, пропилом, бутилом, пентилом и их изомерами). Когда присутствуют гетероатомные заместители, они могут, например, включать галоген, кислород, серу, азот и другие подобные атомы. Наиболее предпочтительно, чтобы все группы от R4 до R7 были метилом. Примеры подходящих соединений нитроксидного свободного радикала, которые могут применяться в комбинации с сульфированными нитрофенолами в настоящем изобретении, включают, но этим не ограничивая: N,N-ди-трет-бутилнитроксид; N,N-ди-трет-амилнитроксид; N-трет-бутил-2-метил-1-фенилпропилнитроксид; N-трет-бутил-1-диэтилфосфоно-2,2-диметилпропилнитроксид; 2,2,6,6-тетраметилпиперидинилокси; 4-амино-2,2,6,6-тетраметилпиперидинилокси; 4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-оксо-2,2,6,6-тетраметилпиперидинилокси; 4-диметиламино-2,2,6,6-тетраметилпиперидинилокси; 4-этаноилокси-2,2,6,6-тетраметилпиперидинилокси; 2,2,5,5-тетраметилпирролидинилокси; 3-амино-2,2,5,5-тетраметилпирролидинилокси; 2,2,4,4-тетраметил-1-окса-3-азациклопентил-3-окси; 2,2,4,4-тетраметил-1-окса-3-пирролинил-1-окси-3-карбоновая кислота; 2,2,3,3,5,5,6,6-октаметил-l,4-диазациклогексил-l,4-диокси; 4-бром-2,2,6,6-тетраметилпиперидинилокси; 4-хлор-2,2,6,6-тетраметилпиперидинилокси; 4-йод-2,2,6,6-тетраметилпиперидинилокси; 4-фтор-2,2,6,6-тетраметилпиперидинилокси; 4-циано-2,2,6,6-тетраметилпиперидинилокси; 4-карбокси-2,2,6,6-тетраметилпиперидинилокси; 4-карбометокси-2,2,6,6-тетраметилпиперидинилокси; 4-карбэтокси-2,2,6,6-тетраметилпиперидинилокси; 4-циано-4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-метил-2,2,6,6-тетраметилпиперидинилокси; 4-карбэтокси-4-гидрокси-2,2,6,6-тетраметилпиперидинилокси; 4-гидрокси-4-(1-гидроксипропил)-2,2,6,6-тетраметилпиперидинилокси; 4-метил-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбометокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-карбэтокси-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-амино-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 4-амидо-2,2,6,6-тетраметил-1,2,5,6-тетрагидропиридин-1-оксил; 3,4-дикето-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4-оксимино-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4-бензилидин-2,2,5,5-тетраметилпирролидинилокси; 3-кето-4,4-дибром-2,2,5,5-тетраметилпирролидинилокси; 2,2,3,3,5,5-гексаметилпирролидинилокси; 3-карбоксимидо-2,2,5,5-тетраметилпирролидинилокси; 3-оксимино-2,2,5,5-тетраметилпирролидинилокси; 3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-циано-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-карбометокси-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 3-карбэтокси-3-гидрокси-2,2,5,5-тетраметилпирролидинилокси; 2,2,5,5-тетраметил-3-карбоксамидо-2,5-дигидропиррол-1-оксил; 2,2,5,5-тетраметил-3-амино-2,5-дигидропиррол-1-оксил; 2,2,5,5-тетраметил-3-карбэтокси-2,5-дигидропиррол-1-оксил; 2,2,5,5-тетраметил-3-циано-2,5-дигидропиррол-1-оксил; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)сукцинат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил) адипинат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил) себацинат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)н-бутилмалонат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)фталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)изофталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)терефталат; бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)гексагидротерефталат; N,N’-бис(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)адипамид; N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)-капролактам; N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)-додецилсукцинимид; 2,4,6-трис-[N-бутил-N-(1-оксил-2,2,6,6-тетраметилпиперидин-4-ил)]-s-триазин; 4,4′-этиленбис(1-оксил-2,2,6,6-тетраметилпиперазин-3-он) и другие подобные соединения нитроксидного свободного радикала. Применяемое здесь сокращение TEMPO означает 2,2,6,6-тетраметил-1-пиперидинилокси. Поэтому 4-амино-TEMPO является 4-амино-2,2,6,6-тетраметил-1-пиперидинилокси; 4-гидрокси-TEMPO является 4-гидрокси-2,2,6,6-тетраметил-1-пиперидинилокси (также известное в технике как HTEMPO); 4-оксо-TEMPO является 4-оксо-2,2,6,6-тетраметил-1-пиперидинилокси и так далее. Предпочтительно, чтобы одним элементом комбинации, применяемой в настоящем изобретении, был 4-амино-TEMPO, 4-оксо-TEMPO, 4-гидрокси-TEMPO или TEMPO. Могут также применяться смеси двух или более вышеупомянутых соединений, например 4-амино-TEMPO и 4-оксо-TEMPO. Такие стабильные соединения со свободным нитроксидным радикалом могут быть получены известными способами (смотрите, например, патенты США 3163677; 3334103; 3372182; 3422144; 3494930; 3502692; 3873564; 3966711 и 4665185, которые приводятся здесь путем соответствующей ссылки на них.) Они применяются в широкой области температур, но используемые температуры ректификации для этиленненасыщенных мономеров, которые стабилизируют по способу настоящего изобретения, обычно находятся в интервале от 60°C до 180°C, предпочтительно – от 70°C до 165°C и более предпочтительно – от 80°C до 150°C. Такие ректификации обычно осуществляют при абсолютном давлении в интервале от 10 до 1200 мм Hg. Когда система ингибирования настоящего изобретения включает дополнительный ингибитор, которым является нитрозоанилин, то им может быть N-нитрозоанилин или C-нитрозоанилин. Предпочтительно, чтобы соединением нитрозоанилина был C-нитрозоанилин. Соединения C-нитрозоанилина могут быть получены C-нитрозированием соответствующих аминов любым обычным способом, применяемым для C-нитрозирования ароматических аминов. Например, реакция амина с холодной азотистой кислотой дает N-нитрозосоединение, которое в результате перегруппировки под действием избытка хлористоводородной кислоты преобразуется в пара-нитрозоанилин. В некоторых случаях более удобно осуществлять нитрозирование и перегруппировку в одну стадию путем проведения реакции в растворе метанола в присутствии избытка хлористого водорода в безводных условиях. Этот метод описан в Патенте США 2046356. Специалистам в этой области известно, что производные нитрозоанилина таутомеризуются до производных хинонов иминоксимов, то есть
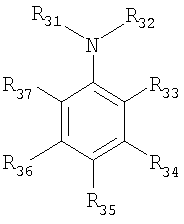
Смотрите, например, Sidgwick, N.V., The Organic Chemistry of Nitrogen, Third Edition, Clarendon Press, Oxford, 1966. Поэтому обе формы могут присутствовать в растворе, особенно при повышенных температурах, и можно ожидать, что они способствуют ингибирующей активности этих соединений. Когда система ингибирования настоящего изобретения включает C-нитрозоанилин, предпочтительно, чтобы он имел следующую структуру:
где R31 и R32 независимо выбирают из группы, состоящей из водорода, алкила, арила, ацила, гидроксила, алкокси, нитрозо и сульфонил, или R31 и R32 могут образовывать циклическое кольцо, которое является арилом, циклоалкилом, полиарилом или гетероциклом; R33 до R37 независимо выбирают из группы, состоящей из водорода, алкила, арила, ацила, гидроксила, алкокси, NR38(R39), нитро, нитрозо, галогена и сульфонила, или любые два смежных R могут образовывать циклическое кольцо, которое является арилом, циклоалкилом, полиарилом или гетероциклом, при условии, что, по меньшей мере, один из R33-R37 должен быть нитрозогруппой; и R38 и R39 независимо выбирают из группы, состоящей из водорода, алкила, арила, ацила и нитрозо. Предпочтительно, чтобы R38 был водородом и R39 был алкилом. Когда система ингибирования настоящего изобретения включает дополнительный ингибитор, которым является амин, то он может быть первичным, вторичным или третичным амином и может включать алкильные группы, арильные группы или их комбинации. Такие амины включают, но этим не ограничивая, Этиленненасыщенным мономером, преждевременная полимеризация и рост цепи которого являются предметом настоящего изобретения, может быть любым таким мономером, для которого является проблемой нежелательная полимеризация и/или рост полимерной цепи в процессе его производства, хранения и/или продажи. Среди тех мономеров, для которых применение настоящего изобретения дает положительный эффект, находятся: стирол, В результате присутствия ингибитора (ингибиторов) этиленненасыщенные мономеры не обязательно будут находиться в стабилизированном состоянии в течение бесконечно долгого времени, особенно когда мономеры нагревают в процессе ректификации, но можно считать, что они будут стабилизированы до тех пор, пока: A) имеется ощутимое увеличение времени, в течение которого они могут быть нагреты до начала полимеризации и/или роста полимерной цепи в статической системе, B) количество полимера, образующегося при постоянной температуре, остается постоянным в течение времени в динамической системе и/или C) скорость роста полимерной цепи значительно ниже, чем в случаях, когда система, ингибирующая рост цепи полимера, отсутствует. Для специалистов в этой области очевидно, что, если желательно, то могут также применяться в настоящем изобретении ловушки свободных радикалов. Например, могут быть добавлены воздух или O2, как раскрыто в Патентах США 5545782 и 5545786, также как и ароматические нитросоединения, описанные в Патенте США 5254760, дигетерозамещенные соединения бензола, имеющие, по меньшей мере, один переносимый водород, например производное хинона, такое как монометиловый эфир гидрохинона, раскрытый в европейской патентной заявке 0765856 A1, соединения железа, описанные в патентной заявке WO 98/25872, и другие ингибиторы, например фенольные смолы и определенные неорганические соли, хорошо известные специалистам в этой области. Ингибиторы полимеризации могут быть введены в защищаемый мономер любым традиционным способом. Они могут, например, быть добавлены в виде концентрированного раствора в подходящих растворителях просто в поток мономера из желательной точки ввода любым подходящим способом. Кроме того, индивидуальные ингибирующие компоненты могут быть впрыснуты раздельно в линию дистилляции наряду с поступающим сырьем и/или через раздельные и многочисленные точки ввода при условии, что ингибирующей композиции будет обеспечено эффективное распределение. Так как ингибиторы постепенно истощаются в процессе операции ректификации, обычно желательно поддерживать их соответствующее количество в ректификационной колонне путем их добавления в процессе ректификации. Для того чтобы поддерживать концентрацию ингибитора выше минимально требуемого уровня, добавление ингибиторов может осуществляться или непрерывно, или периодически. Суммарная концентрация ингибитора должна составлять от 1 до 2000 ppm по отношению к ингибируемому мономеру; предпочтительно – от 5 до 1000 ppm, в зависимости от условий применения. Предпочтительно, чтобы амин присутствовал в интервале от 1 до 500 ppm, более предпочтительно – от 1 до 300 ppm; предпочтительно, чтобы нитроксильный радикал присутствовал в интервале от 1 до 1000 ppm, более предпочтительно – от 5 до 500 ppm; предпочтительно, чтобы нитрозоанилин присутствовал в интервале от 1 до 1000 ppm, более предпочтительно – от 5 до 500 ppm, и предпочтительно, чтобы нитрофенол присутствовал в интервале от 1 до 1000 ppm, более предпочтительно – от 5 до 500 ppm. Преимущества и важные характерные черты настоящего изобретения будут более очевидны из следующих примеров. ПРИМЕРЫ Пример 1 Раствор 17% HNO3 в количестве 471 грамм помещали в круглодонную колбу, снабженную сверху мешалкой, термометром, капельной воронкой и обратным холодильником, и нагревали до 80°C. Добавляли к этой кислоте порцию (162 грамма) сульфированного o-втор-бутилфенола, полученного сульфированием 300 грамм o-втор-бутилфенола (OSBP) с помощью 280 грамм концентрированной H2SO4 при 84°C. Кислоту добавляли в глубь раствора и по каплям. В результате разделения реакционной смеси получали два слоя. Верхний (водно-кислотный) слой (509 грамм) отделяли от нижнего (2,4-динитро-o-втор-бутилфенол) слоя (104,6 грамм) и испаряли 464 грамм под вакуумом 2 мм Hg при температуре не выше 30°C в течение 75 минут. Этот остаток (173 грамма) переносили в делительную воронку. Извлечение верхнего (органического) слоя приводило к 37,1 грамм смеси, содержащей 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновую кислоту и 2-гидрокси-3-втор-бутил-5-нитробензолсульфоновую кислоту. Свойства этого материала в качестве ингибитора и замедлителя для стирола исследовали в тесте в непрерывном динамическом ребойлере, при концентрации ингибитора 500 ppm, контролируя образование полимера с помощью УФ-спектрометрии. Согласно этому тесту ингибитор добавляют к мономерному стиролу, из которого предварительно был удален ректификацией трет-бутилкатехин (TBC). Этот стирол (180 грамм) загружают в колбу, которую погружают в масляную баню. Температура стирола обычно составляет 116°C. Во время теста свежее сырье загружают в колбу при скорости три грамма в минуту и в то же самое время материал из колбы выгружают с той же скоростью. Стабильная стадия продолжается до равновесия. На стадии прекращения подачи сырья загрузку и разгрузку прекращают. Образцы отбирают каждый час на стабильной стадии и каждые 5-10 минут при прекращении подачи сырья. После 5 часов стабильной стадии было обнаружено 0,0005% полимера, в то время как 1 час прекращения подачи сырья приводил к образованию 0,03% полимера. Пример 2 Смесь 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты и 2-гидрокси-3-втор-бутил-5-нитробензолсульфоновой кислоты, полученную в промышленном масштабе, тестировали согласно методике, описанной в примере 1, при концентрации 500 ppm. Этот материал содержал также 21% динитро-втор-бутилфенола (DNBP). Во время стабильной стадии теста образовывалось 0,0004% полимера, в то время как стадия теста прекращения подачи сырья после одного часа приводила к 0,038% полимера. В качестве сравнения, когда подвергали тесту только один DNBP с использованием аналогичной методики, образование полимера на стабильной стадии составляло 0,11%, в то время как прекращение подачи сырья в течение 1 часа приводило к образованию 1,18% полимера. Пример 3 Триста грамм OSBP сульфировали 280 граммами 98% серной кислоты, как описано в примере 1. Двести грамм этого материала использовали для нитрования при мольном отношении HNO3:OSBP 1,6:1 с использованием следующей методики. Азотную кислоту (35%; 171,4 грамм) загружали в круглодонную колбу и добавляли к ней по каплям 200 грамм сульфированного OSBP в течение двух часов при 40°C. Смесь затем переносили в делительную воронку, где образовывались два слоя. 151 грамм нижнего слоя являлся 40% серной кислотой, в то время как верхнюю (органическую) фазу извлекали в виде смеси 1:1 DNBP и смеси 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты и 2-гидрокси-3-втор-бутил-5- нитробензолсульфоновой кислоты. Пример 4 Смесь 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты и 2-гидрокси-3-втор-бутил-5-нитробензолсульфоновой кислоты (250 ppm) примера 3 тестировали в присутствии 4-оксо-TEMPO/NMP/DNBP (100 ppm/90 ppm/250 ppm). Пять часов стабильной стадии приводили к образованию 0,0005% полимера, в то время как 2 часа прекращения подачи сырья давало 0,101% полимера. Пример 5 Смесь 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты и 2-гидрокси-3-втор-бутил-5-нитробензолсульфоновой кислоты (250 ppm) примера 3 тестировали в присутствии 4-нитрозо-N-(2,4-диметилпентил)-анилин/NMP/DNBP (100 ppm/90 ppm/250 ppm). Пять часов стабильной стадии приводило к 0,002% полимера, в то время как 2 часа прекращения подачи сырья давало 0,0057% полимера. Ввиду того, что может быть сделано много изменений и модификаций без отхода от принципов, лежащих в основе изобретения, объем защиты, который обеспечивает изобретение, следует определять по прилагаемой формуле изобретения.
Формула изобретения
1. Способ ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества, по меньшей мере, одного ингибитора, который является сульфированным нитрофенолом формулы: 2. Способ по п.1, в котором один из R1, R2 и R3 является углеводородом. 3. Способ по п.2, в котором углеводородом является линейный или разветвленный алкил или алкенил, имеющий от 1 до 18 углеродных атомов. 4. Способ по п.3, в котором углеводород выбирают из группы, состоящей из метила, этила, пропила, бутила, пентила, гексила, гептила, октила, 2-этилгексила, нонила, децила, ундецила, додецила, тридецила, тетрадецила, пентадецила, гексадецила, гептадецила, октадецила, олеила, их изомеров, циклопентила, циклогексила, циклогептила, циклооктила и циклододецила. 5. Способ по п.1, в котором сульфированный нитрофенол выбирают из группы, состоящей из 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты, 2-гидрокси-3-втор-бутил-5-нитробензолсульфоновой кислоты и их смесей. 6. Способ ингибирования и замедления преждевременной полимеризации и роста полимерной цепи этиленненасыщенных мономеров, включающий добавление к указанным мономерам эффективного количества комбинации 7. Способ по п.6, в котором один из R1, R2 и R3 является углеводородом. 8. Способ по п.7, в котором углеводород является линейным или разветвленным алкилом или алкенилом, имеющим от 1 до 18 углеродных атомов. 9. Способ по п.8, в котором углеводород выбирают из группы, состоящей из метила, этила, пропила, бутила, пентила, гексила, гептила, октила, 2-этилгексила, нонила, децила, ундецила, додецила, тридецила, тетрадецила, пентадецила, гексадецила, гептадецила, октадецила, олеила, их изомеров, циклопентила, циклогексила, циклогептила, циклооктила и циклододецила. 10. Способ по п.6, в котором сульфированный нитрофенол выбирают из группы, состоящей из 4-гидрокси-5-втор-бутил-3-нитробензолсульфоновой кислоты, 2-гидрокси-3-втор-бутил-5- нитробензолсульфоновой кислоты и их смесей. 11. Способ по п.6, в котором амин выбирают из группы, состоящей из N-метил-2-пирролидинона, 12. Способ по п.6, в котором нитрофенол выбирают из группы, состоящей из 2,6-динитро-4-метилфенола, 2-нитро-4-метилфенола, 2,4-динитро-1-нафтола, 2,4,6-тринитрофенола (пикриновой кислоты), 2,4-динитро-6-метилфенола, 2,4-динитрофенола, 2,4-динитро-6-втор-бутилфенола, 4-циано-2-нитрофенола, 3-йод-4-цианоо-5-нитрофенола, м-нитро-п-крезола, 2,6-динитро-п-крезола. 13. Способ по п.6, в котором нитроксильное соединение имеет структурную формулу: 14. Способ по п.6, в котором нитрозоанилин имеет структуру: 15. Способ по п.6, в котором второй ингибитор включает смесь, по меньшей мере, одного нитроксильного соединения, по меньшей мере, одного амина и, по меньшей мере, одного нитрофенола. 16. Способ по п.10, в котором второй ингибитор включает смесь, по меньшей мере, одного нитроксильного соединения, по меньшей мере, одного амина и, по меньшей мере, одного нитрофенола. 17. Способ по п.16, в котором нитроксильным соединением является 4-оксо-2,2,6,6-тетраметил-1-пиперидинилокси, амином является N-метилпирролидинон, и нитрофенолом является 2,4-динитро-о-втор-бутилфенол. 18. Способ по п.6, в котором второй ингибитор включает смесь, по меньшей мере, одного нитрозоанилина, по меньшей мере, одного амина и, по меньшей мере, одного нитрофенола. 19. Способ по п.10, в котором второй ингибитор включает смесь, по меньшей мере, одного нитрозоанилина, по меньшей мере, одного амина и, по меньшей мере, одного нитрофенола. 20. Способ по п.19, в котором нитрозоанилином является 4-нитрозо-N-(2,4-диметилпентил)-анилин, амином является N-метил-пирролидинон, и нитрофенолом является 2,4-динитро-о-втор-бутилфенол.
|
||||||||||||||||||||||||||

 -углеродных атомах, и (ii) от 99,95 до 95,5% по массе от суммарной массы смеси (B), по меньшей мере, одно нитросоединение.
-углеродных атомах, и (ii) от 99,95 до 95,5% по массе от суммарной массы смеси (B), по меньшей мере, одно нитросоединение.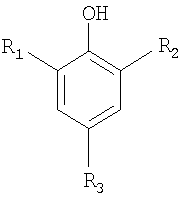

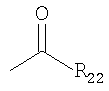
 -нафтиламин, изопропоксидифениламин, альдоль-
-нафтиламин, изопропоксидифениламин, альдоль-