Патент на изобретение №2378014
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И КОРОНАВИРУСНОЙ ИНФЕКЦИИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ
(57) Реферат:
Изобретение относится к ветеринарной вирусологии и биотехнологии. Вакцина содержит активное вещество и целевую добавку. В качестве активного вещества вакцина содержит смесь из авирулентного очищенного антигенного материала из штамма «ВГНКИ-4» вируса ПГ-3 КРС, сем. Paramyxoviridae, рода Parainfluenza, подтипа Parainfluenza virus 3, коллекция ФГУ «ВГНКИ» «ВГНКИ-4» ДЕП, из авирулентного очищенного антигенного материала из штамма «ВНИИЗЖ» вируса ИРТ КРС, сем. Herpesviridae, рода Varicellavims, коллекция ФГУ «ВГНКИ» «ВНИИЗЖ-ДЕП», и из авирулентного очищенного антигенного материала из штамма «ВНИИЗЖ» коронавируса КРС, сем. Coronaviridae, рода Coronavirus, коллекция ФГУ «ВГНКИ» «ВНИИЗЖ-ДЕП». Штаммы взяты в соотношении 1:1:1 и в количествах, обеспечивающих протективную иммунную активность каждого антигена в организме животного после введения ему целевого препарата. Вакцина индуцирует у иммунизированных животных высокий уровень антител, иммунитет у привитых животных формируется через 10-15 суток после повторного введения вакцины и сохраняется не менее 6 месяцев. 14 з.п. ф-лы, 7 табл.
Изобретение относится к области ветеринарной вирусологии и биотехнологии и касается ассоциированной вакцины для специфической профилактики респираторных и желудочно-кишечных заболеваний крупного рогатого скота (КРС), обусловленных возбудителями парагриппа-3 (ПГ-3), инфекционного ринотрахеита (ИРТ) и коронавирусной инфекции КРС. Указанные вирусы играют ведущую роль в этиологии респираторных и желудочно-кишечных заболеваний КРС, особенно в крупных животноводческих хозяйствах. ПГ-3 (транспортная лихорадка КРС, параинфлюэнца – 3) – остро протекающее контагиозное вирусное заболевание, главным образом телят, характеризующееся поражением органов дыхания, но наиболее характерной является латентная форма парагриппозной инфекции. ПГ-3 возникает у КРС как в виде моноинфекции, так и в виде смешанных вирусных и вирусно-бактериальных инфекций, которые наносят значительный экономический ущерб из-за гибели и выбраковки животных, снижения продуктивности и нарушения воспроизводства. ПГ-3 распространен повсеместно, практически во всех странах мира. ИРТ – остро протекающее вирусное контагиозное заболевание КРС, наносящее значительный экономический ущерб скотоводству. Вирус ИРТ вызывает заболевание КРС различных возрастных групп, проявляющееся пятью формами: поражением верхних дыхательных путей, вагинитами, энцефалитами, конъюнктивитами и артритами. Кроме того, у телят возможна пневмония. Экономический ущерб, наносимый ИРТ, слагается из снижения удоев в период болезни (до 50-60%), значительного увеличения сервис-периода и яловости коров, болевших вагинальной формой, слабого развития больного молодняка и значительным процентом гибели и выбраковки телят. При хронической серозно-гнойной пневмонии погибает до 20% молодняка. Болезнь широко распространена во всем мире. Коронавирусная инфекция у КРС проявляется в виде коронавирусной диареи новорожденных телят, коронавирусной зимней дизентерии взрослого КРС и коронавирусной респираторной инфекции. Чрезвычайно широкое распространение, тенденция вызывать длительную персистенцию, относительная устойчивость к воздействию разнообразных факторов обусловливают энзоотическое течение болезни в хозяйствах с неблагополучными условиями содержания и кормления. Стационарность болезни поддерживается за счет длительной персистенции возбудителя в организме животных-реконвалесцентов. Указанные инфекции возникают у КРС как в виде моноинфекций, так и смешанных вирусных и вирусно-бактериальных инфекций. В настоящее время основным средством борьбы с респираторными и желудочно-кишечными болезнями КРС является специфическая профилактика, для которой применяются живые и инактивированные вакцины как в виде моно-, так и ассоциированных препаратов (1, 2, 3). Преимущество живых вакцин из-за технологичности в производстве и простоты при применении не вызывает сомнений. Однако иммунная реакция у животных при их введении не всегда стабильна и в ряде случаев вызывает осложнения после вакцинации: вакцина может вызвать повышенную реактогенность, иммуносупрессию, а иногда и гибель до 2% животных при вакцинации в зависимости от условий содержания и наличия коинфекций, проблемы воспроизводства, длительную персистенцию и выделение вакцинного вируса во внешнюю среду. По этой причине они не нашли широкого применения. Для специфической профилактики указанных заболеваний широко используют инактивированные вакцины как сорбированные, так и эмульсионные. Известна вакцина против ПГ-3 КРС сорбированная инактивированная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3, полученного в культуре клеток ВНК-21 с инфекционной активностью не менее 6,5 Ig ТЦД50/см3, и в качестве целевой добавки адъювант-сорбент гидроокись алюминия (ГОА) в эффективном соотношении (4). Известна вакцина против ИРТ КРС эмульсионная инактивированная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток ВНК-21, из культуры клеток MDBK и из культуры клеток ЗКГ, с инфекционной активностью не менее 6,0 Ig ТЦД50/см3 и активностью в РДП не менее 4,0 log, и в качестве целевой добавки масляный адъювант в соотношении, мас.%:
Известна вакцина против коронавирусной инфекции КРС сорбированная инактивированная, содержащая в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK, из культуры клеток Таурус-1, из культуры клеток КСТ и из культуры клеток Vero, в концентрации вирусных частиц, обеспечивающей протективную иммунную активность антигена в организме животного после введения ему целевого препарата, и в качестве целевой добавки адъювант-сорбент ГОА в эффективном соотношении (6). Недостатки моновалентных инактивированных вакцин заключаются в том, что они стимулируют образование иммунитета у животных только к одной инфекции, требуют проведения профилактических обработок против каждой инфекции в отдельности, что сказывается на затратах труда, растягивает сроки формирования иммунитета у животных, способствует возникновению стрессовых явлений и осложнений. Указанные недостатки частично устранены созданием ассоциированных вакцин, содержащих отдельно или в сочетании антигены возбудителей ПГ-3, ИРТ и коронавирусной инфекции КРС различных штаммов. В ряде случаев в состав известных вакцин, особенно предназначенных для защиты телят, включают антигены возбудителей, вызывающих вторичные инфекции. Известна ассоциированная вакцина против вирусной диареи – болезни слизистых (ВД-БС), рота- и коронавирусной инфекций и эшерихиоза КРС эмульсионная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма VDV-Oregon-С24 V (САРМ V-293) вируса ВД-БС КРС, из штамма ТМ-91 (САРМ V-279) ротавируса КРС, из штамма BCV-9 (САРМ V-280) коронавируса КРС и из штаммов 3935/1 (САРМ 6233), 4804 (САРМ 6234) и 6304 (САРМ 6235) бактерий Е. coli, полученных в чувствительных биологических системах, и в качестве целевой добавки масляный адъювант в эффективных соотношениях (7). Известна ассоциированная вакцина против ИРТ, рота- и коронавирусной инфекций и эшерихиоза КРС эмульсионная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма IBR-BK-5-PTOB-8 INRV Известна ассоциированная вакцина против ПГ-3, рота- и коронавирусной инфекций и эшерихиоза КРС эмульсионная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма PI-3/T1/11 V-30 вируса ПГ-3 КРС, из штамма ТМ-91 (САРМ V-279) ротавируса КРС, из штамма BCV-9 (САРМ V-280) коронавируса КРС и из штаммов 3935/1 (САРМ 6233), 4808 (САРМ 6234) и 6304 (САРМ 6235) бактерий Е. coli, полученных в чувствительных биологических системах, и в качестве целевой добавки масляный адъювант в эффективных соотношениях (9). Известна ассоциированная вакцина против рота-, корона-, герпесвирусной и эшерихиозной диареи новорожденных телят сорбированная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма «III-1» Bovine rotavirus, из штамма «СМ-1» Bovine coronavirus, из штамма «ТКА-ВИЭВ-В-2» Bovine Herpesvirus и из штаммов бактерий Е. coli, содержащих адгезины K99 и A20, и в качестве целевой добавки адъювант-сорбент ГОА в эффективных соотношениях (10). Известна ассоциированная вакцина против рота- и коронавирусной инфекций, эшерихиоза и клостридиоза КРС эмульсионная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов их штаммов Cody 81-4, 10В223 типа G и В 641 ротавируса КРС, штамма Mebus (АТСС Известна ассоциированная вакцина против ИРТ, ПГ-3, вирусной диареи, респираторно-синцитиальной инфекции, рота- и коронавирусных заболеваний телят «КОМБОВАК» сорбированная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из 6 производственных штаммов вирусов: ИРТ, ПГ-3, ВД-БС, респираторно-синцитиальной инфекции, рота- и коронавирусных заболеваний КРС, – полученных в чувствительных биологических системах, и в качестве целевой добавки адъювант-сорбент ГОА в эффективных соотношениях (12). Известна ассоциированная вакцина против вирусных пневмогастроэнтеритов КРС и телят сорбированная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штаммов В-25 и ТК-А вируса ИРТ КРС, из штаммов ВД-N и ВД-R вируса ВД-БС КРС, из штаммов В-19 и ПТК-45/86 вируса ПГ-3 КРС, из штаммов К-88 и РП-82 ротавируса КРС, из штаммов КВ-90 и К-22 коронавируса КРС и из штаммов PC-89 и PC-71 возбудителя респираторно-синцитиальной инфекции КРС, полученных в чувствительных биологических системах, и в качестве целевой добавки адъювант-сорбент ГОА в эффективных соотношениях (13). Известен также способ количественной оценки вируссодержащих суспензий с помощью электронной микроскопии, возникший как результат многолетних опытов по электронно-микроскопическому контролю вирусных препаратов и сопоставлению его данных с показателями биологических тестов, например титром инфекционности вируса (14). Авторами данного способа установлена зависимость между титром инфекционности нативных суспензий вируса ящура и количеством физических вирусных частиц, наблюдаемых под электронным микроскопом, что послужило основанием для определения общей концентрации вирусных частиц в единице объема суспензии (степень накопления вирусных частиц в определенном объеме жидкости). Для определения общей концентрации (N) вирусных частиц в единице объема анализируемой суспензии на экране электронного микроскопа площадью S2 подсчитывают число одновременно наблюдаемых частиц n. По известному инструментальному увеличению электронного микроскопа (М) определяют размер участка пленки-подложки S1, соответствующего полезной площади экрана:
При нанесении вирусных препаратов на пленки-подложки концентрация вирусных частиц (n) на данном участке S1 соответствует суммарному количеству адсорбированных частиц и частиц, осажденных на подложку при испарении остаточной жидкости. Следовательно, наблюдаемое одновременно на экране число частиц распределяется в микрообъеме, равном: v=S1·I, где I – толщина остаточного слоя жидкости на подложке (мм). В определяемом объеме вируссодержащей суспензии число частиц равно:
а после замены значений v и S1:
где V – объем анализируемой суспензии (1 см3); N – среднее арифметическое ряда значений числа частиц, просчитанных с экрана электронного микроскопа или экспонированных фотопластинок. Толщину остаточного слоя (I) на подложке измеряют предварительно охлажденным микрометром после замораживания жидкости на подложке в парах жидкого азота. Она составляет 0.03-0.04 мм и ее принимают как постоянную величину. Электронно-микроскопическое определение концентрации физических вирусных частиц позволяет не только определять количественную характеристику вируса в анализируемых суспензиях, но и одновременно оценивать морфологическое состояние исследуемых вирусных частиц. Указанный способ оказался универсальным и пригодным для определения количественной характеристики различных вирусов в исследуемых жидкостях. Наиболее близкой к предлагаемому изобретению по совокупности существенных признаков является ассоциированная вакцина против ПГ-3 и коронавирусной инфекции КРС эмульсионная инактивированная, содержащая в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма PI-3/T1/ 11 V-30 вируса ПГ-3 КРС и из штамма BCV-9 (CAPM V-280) коронавируса КРС, полученных в чувствительных биологических системах, и в качестве целевой добавки масляный адъювант в эффективных соотношениях (9). Общим существенным недостатком известных ассоциированных вакцин, в том числе вакцины-прототипа, предназначенных для профилактики массовых инфекционных респираторных и желудочно-кишечных заболеваний КРС различных половозрастных групп, является их недостаточно высокая эффективность вследствие: 1) неполноценности (неполноты) антигенного состава входящих в них ингредиентов и сложных взаимодействий антигенов, из которых они изготовлены; 2) узости антигенного спектра действия используемых штаммов; 3) низкой иммуногенной активности препаратов. Причиной указанного недостатка может быть использование для инактивации вирусов формалина, вызывающего деструктивные изменения вирусных белков. Поэтому проблема создания ассоциированной вакцины против основных возбудителей инфекционных респираторных и желудочно-кишечных заболеваний КРС и телят продолжает оставаться актуальной и является основным направлением исследований по их совершенствованию. Задача, на решение которой направлено настоящее изобретение, заключается в получении ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионной инактивированной, создающей эффективную защиту восприимчивых животных различных половозрастных групп против возбудителей ПГ-3, ИРТ и коронавирусной инфекции КРС, циркулирующих на территории Российской Федерации. Технический результат от использования предлагаемого изобретения заключается в расширении арсенала высокоиммуногенных, безвредных и ареактогенных ассоциированных вакцин против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионных инактивированных, способных защитить поголовье КРС различных половозрастных групп от возбудителей ПГ-3, ИРТ и коронавирусной инфекции КРС, циркулирующих на территории России. Указанный технический результат достигнут созданием ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионной инактивированной, охарактеризованной следующей совокупностью признаков. Согласно изобретению предлагаемая вакцина содержит в качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма «ВГНКИ-4» (авторское наименование) вируса ПГ-3 КРС, из штамма «ВНИИЗЖ» (авторское наименование) вируса ИРТ и из штамма «ВНИИЗЖ» (авторское наименование) коронавируса КРС, полученных в культурах клеток животного происхождения, в количествах, обеспечивающих протективную иммунную активность каждого антигена в организме животного после введения ему целевого препарата, и в качестве целевой добавки масляный адъювант в эффективном соотношении. Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана: 1. Ассоциированная вакцина против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионная инактивированная. 2. Активное вещество. 3. В качестве активного вещества смесь авирулентных очищенных антигенных материалов из штамма «ВГНКИ-4» вируса ПГ-3 КРС, из штамма «ВНИИЗЖ» вируса ИРТ КРС и из штамма «ВНИИЗЖ» коронавируса КРС, полученных в культурах клеток животного происхождения, в количествах, обеспечивающих протективную иммунную активность каждого антигена в организме животного после введения ему целевого препарата. 4. Целевая добавка. 5. В качестве целевой добавки масляный адъювант. Признаками изобретения, характеризующими предлагаемую вакцину и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются: 1. Ассоциированная вакцина против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионная инактивированная. 2. Активное вещество. 3. Целевая добавка. По сравнению с вакциной-прототипом существенные отличительные признаки предлагаемой вакцины заключаются в том, что в качестве активного вещества она содержит смесь авирулентных очищенных антигенных материалов из штамма «ВГНКИ-4» вируса ПГ-3, из штамма «ВНИИЗЖ» вируса ИРТ и из штамма «ВНИИЗЖ» коронавируса КРС, полученных в культурах клеток животного происхождения, в количествах, обеспечивающих протективную иммунную активность каждого антигена в организме животного после введения ему целевого препарата. Предлагаемое изобретение характеризуется другими отличительными признаками, выражающими конкретные формы выполнения или особые условия его использования: 1. Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток почек теленка MDBK и из культуры клеток почек сирийского хомячка ВНК-21, в эффективном количестве. 2. Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток MDBK с инфекционной активностью не менее 6,5 Ig ТЦД50/см3, в количестве не менее 10,0 мас.%. 3. Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью не менее 6,5 Ig ТЦД50/см3, в количестве не менее 10,0 мас.%. 4. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток ВНК-21, из культуры клеток MDBK и из культуры клеток гонад 3-дневной козы 3КГ, в эффективном количестве. 5. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью не менее 6,0 Ig ТЦД50/см3 и активностью в реакции диффузионной преципитации (РДП) не менее 4,0 log2, в количестве не менее 10,0 мас.%. 6. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток MDBK с инфекционной активностью не менее 6,0 Ig ТЦД50/см3 и активностью в РДП не менее 4,0 log2, в количестве не менее 10,0 мас.%. 7. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ЗКГ с инфекционной активностью не менее 6,0 Ig ТЦД50/см3 и активностью в РДП не менее 4,0 log2, в количестве не менее 10,0 мас.%. 8. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK, из культуры клеток почек теленка Таурус-1, из культуры клеток коронарных сосудов теленка КСТ и из культуры клеток почек обезьяны Vero, в эффективном количестве. 9. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток MDBK со степенью накопления не менее 108 вирусных частиц/см3 и активностью в реакции гемагглютинации (РГА) не менее 7,0 log2, в количестве не менее 10,0 мас.%. 10. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Таурус-1 со степенью накопления не менее 109 вирусных частиц/см3 и активностью в РГА не менее 9,0 log2, в количестве не менее 10,0 мас.%. 11. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток КСТ со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. 12. Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Vero со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. 13. Масляный адъювант в количестве не менее 70,0 мас.%. 14. Смесь авирулентных очищенных антигенных материалов из штамма «ВГНКИ-4» вируса ПГ-3, из штамма «ВНИИЗЖ» вируса ИРТ и из штамма «ВНИИЗЖ» коронавируса КРС, полученных в культурах клеток животного происхождения, и масляный адъювант в соотношении, мас.%: Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK и из культуры клеток ВНК-21, с инфекционной активностью не менее 6,5 Iq ТЦД50/см3 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток ВНК-21, из культуры клеток MDBK и из культуры клеток ЗКГ, с инфекционной активностью не менее 6,0 Ig ТЦД50/см3 и активностью в РДП не менее 4,0 log2 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK, из культуры клеток Таурус-1, из культуры клеток КСТ и из культуры клеток Vero, в концентрации вирусных частиц, обеспечивающей протективную иммунную активность антигена в организме животного после введения ему целевого препарата – 10,0 Масляный адъювант – до 100,0, Входящие в предлагаемую вакцину штаммы вирусов известны и являются производственными при изготовлении моновакцин (15, 16, 17). В результате проведенных исследований, авторами установлено, что между антигенами, входящими в состав предлагаемой вакцины, отсутствует конкуренция. Авторами обнаружено также явление синергизма при соединении указанных антигенов в предлагаемой вакцине, что позволило снизить их количественное содержание в препарате при сохранении такой же напряженности и длительности иммунитета у вакцинированных животных, как и при использовании для иммунизации соответствующих монопрепаратов. Дополнительный технический результат от использования предлагаемого изобретения достигается за счет того, что для инактивации вируссодержащих материалов используют аминоэтилэтиленимин (АЭЭИ), что позволяет значительно снизить трудо- и энергозатраты на изготовление вакцины и повысить качество антигенных материалов. Дополнительный технический результат от использования предлагаемого изобретения в части повышения антигенной и иммуногенной активности целевого продукта достигается также за счет использования в его составе масляного адъюванта марки Montanide ISA-70 производства фирмы «Seppic» (Франция, стандарт ИСО 9001). Вирусный изолят, послуживший источником для получения производственного штамма «ВГНКИ-4» вируса ПГ-3 КРС, выделен из легких 2-3-месячных телят с респираторной патологией. Штамм «ВГНКИ-4» адаптирован к культуре клеток почек сирийского хомячка ВНК-21 и к культуре клеток теленка Таурус-1 (5). Штамм «ВГНКИ-4» вируса ПГ-3 КРС депонирован 30 сентября 1999 года во Всероссийскую государственную коллекцию штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Федерального государственного учреждения «Всероссийский государственный центр качества и стандартизации лекарственных средств для животных и кормов» (ФГУ «ВГНКИ») под регистрационным наименованием «ВГНКИ-4» ДЕП. Штамм «ВГНКИ-4» вируса ПГ-3 КРС характеризуется следующими признаками и свойствами (15). Морфологические признаки Штамм «ВГНКИ-4» вируса ПГ-3 КРС относится к семейству Paramyxoviridae, роду Parainfluenza, подтипу Parainfluenza virus 3 и по своему строению является классическим парамиксовирусом. Внешне вирус почти сферический, но часто встречаются полиморфные формы. Плавучая плотность в сахарозе составляет 1,197 г/см3. Коэффициент седиментации вирионной РНК составляет 42S. Молекулярная масса 4,5×106Д. Размер сферических форм от 80 до 300 нм, но большинство вирионов в среднем от 130 до 140 нм. Вирус ПГ-3 КРС штамма «ВГНКИ-4» имеет 7 структурных белков: 1. Фосфопротеиды (Р, м.м. 83 кД). 2. ГА-нейраминидазный гликопротеин (HN, м.м. 69 кД). 3. Главный нуклеокапсидный протеин (NP, м.м. 66 кД). 4. Гликопротеин (F, м.м. 55 Д). 5. Матричный белок (М, м.м. 38 Д). 6. Белок L-полимераза (м.м. 180 Д). 7. Клеточный активный белок А (м.м. 43 Д). В двухслойной, содержащей липиды, оболочке (толщина 10-15 нм) размещены 2 различные макромолекулы: гликопротеин гемагглютинин нейраминидаза (HN) и гликопротеин слияния (F). Оба выступают на 8 нм над оболочкой вириона с интервалом 7-8 нм. Гемагглютинин осуществляет прикрепление вириона к рецепторам клетки хозяина, содержащих нейраминовую (сиаловую) кислоту, а нейраминидаза разрушает рецепторы и тем самым помогает элюции вируса в процессе отпочковывания от клетки-хозяина. F-белок отвечает за проникновение вируса в клетку, осуществляя слияние с клеточной мембраной и неся ответственность за гемолиз, который происходит за счет точечного гидролиза молекулы неактивного предшественника F0. Известна зависимость между структурой гликопротеидов и патогенностью вируса. У патогенных штаммов оба поверхностных гликопротеида в клетках ВНК-21 включаются в вирионы только в расщепленной форме. У апатогенных штаммов гликопротеид F включается в вирионы в виде предшественника F0. Вирусы с нерасщепленными гликопротеидами обладают очень низкой биологической активностью, однако, если их обрабатывать трипсином, они проявляют полную биологическую активность. Белок F ответственен за гемолитическую активность и вирусиндуцируемый кариоцитоз. Посттрансляционное расщепление белка предшественника F0 на F1 и F2 осуществляется клеточными ферментами. Антигенные свойства Штамм «ВГНКИ-4» вируса ПГ-3 КРС агглютинирует эритроциты морской свинки, кролика, свиньи, коровы, мыши, овцы, козы, человека и белой мыши. Клетки, инфицированные вирусом ПГ-3 КРС из штамма «ВГНКИ-4», сорбируют эритроциты морской свинки, КРС, овцы, кролика и белой мыши. При вакцинации вирус индуцирует образование специфических антител на 8-14 сутки после ревакцинации, антитела достигают пика к 16-28 дню и сохраняются до одного года. Продолжительность и напряженность поствакцинального иммунитета обеспечивается преимущественно IgG и секреторными IgA, выработка которых стимулируется активным вакцинальным процессом. Привитые телята с титром гуморальных антител от 6,0 до 10,3 log2 устойчивы к заражению вирусом ПГ-3 КРС. Полевые изоляты вируса ПГ-3 КРС имеют близкое антигенное родство с вирусом ПГ-3 КРС штамма «ВГНКИ-4». Биотехнологические характеристики Штамм «ВГНКИ-4» вируса ПГ-3 КРС предназначен для приготовления живых и инактивированных вакцин против ПГ-3 КРС. Вирус штамма «ВГНКИ-4» ПГ-3 КРС репродуцируется в культурах клеток ПЭК, ПТ, MDBK и ВНК-21 и накапливается в титрах от 6,5 до 8,5 Ig ТЦД50/см3. Штамм «ВГНКИ-4» является стабильным и безвредным. Устойчивость к внешним факторам Вирус ПГ-3 КРС штамма «ВГНКИ-4» быстро разрушается под действием высокой температуры. Возбудитель чувствителен к хлороформу, эфиру, формалину и детергентам. Для получения антигенного материала из штамма «ВГНКИ-4» вируса ПГ-3 КРС в качестве чувствительной биологической системы используют преимущественно культуры клеток ВНК-21 или MDBK. Полученный вируссодержащий материал очищают от балластных примесей центрифугированием или любым другим известным методом. Для инактивации вируса ПГ-3 используют АЭЭИ, который добавляют в очищенную вируссодержащую суспензию до концентрации 0,1%. Инактивацию вируса ведут при 36-37°С и рН 7,0-7,6 в течение 24 часов. По окончании инактивации АЭЭИ нейтрализуют внесением в антигенный материал тиосульфата натрия. Для этого в охлажденную суспензию антигена добавляют 1М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Для изготовления эмульсионной формы предлагаемой вакцины используют авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3, полученного в культуре клеток MDBK или ВНК-21 с инфекционной активностью не менее 6,5 Ig ТЦД50/см3, в количестве не менее 10,0 мас.%. Вирусный изолят, послуживший источником для получения производственного штамма «ВНИИЗЖ» вируса ИРТ КРС, выделен из патологического материала телят, павших с явлениями ИРТ во время вспышки заболевания в СПК «Миневское» Нижегородской области в 1998 году. Вакцинный штамм «ВНИИЗЖ» вируса ИРТ КРС адаптирован к культурам клеток ВНК-21, MDBK и ЗКГ. Штамм «ВНИИЗЖ» вируса ИРТ КРС депонирован 12 марта 2001 года во Всероссийскую государственную коллекцию штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Федерального государственного учреждения «Всероссийский государственный центр качества и стандартизации лекарственных средств для животных и кормов» (ФГУ «ВГНКИ») под регистрационным наименованием «ВНИИЗЖ-ДЕП». Штамм «ВНИИЗЖ» вируса ИРТ КРС характеризуется следующими признаками и свойствами (16). Морфологические свойства Штамм «ВНИИЗЖ» вируса ИРТ КРС относится к семейству Herpesviridae, подсемейству Alphaherpesviridae, роду Varicellavirus, группе HPV-1, обладает морфологическими признаками, характерными для данного семейства. Штамм «ВНИИЗЖ» включает линейную 2-цепочечную ДНК с молекулярной массой 92-102 кД. Вирионы округлой формы состоят из 4-х структурных компонентов: нуклеоида, капсида диаметром 120-150 нм, окруженного содержащей липиды оболочкой, мембраны (тегумента) и наружной оболочки. Плавучая плотность вирионов в градиенте CsCl составляет 1,27-1,29 г/см3. Нуклеоид тороидальной формы содержит ДНК и окружен икосаэдрическим капсидом диаметром 100-110 нм, содержащим 162 частично полых капсомера. Капсид окружает ядро вириона, состоящее из ДНК, покрытой белком. Мембрана из глобулярного материала окружает капсид. В составе вириона определено до 32 белков с молекулярной массой до 200 кД. Вирионы имеют сложную четырехуровневую (от центра к периферии) организацию: нуклеоид, капсид, суперкапсидную структуру и оболочку. Наружная оболочка вирионов имеет типичное строение и содержит многочисленные выступы (шипы) длиной около 8 нм. Вирусы формируют характерные внутриядерные включения. При прохождении через внутренний листок ядерной мембраны в эндоплазматический ретикулум вирионы покрываются дополнительной оболочкой, содержащей гликопротеины и липиды. Антигенные свойства По своим антигенным свойствам штамм «ВНИИЗЖ» вируса ИРТ КРС относится к группе 1 герпесвирусов КРС. Вирус стабильно нейтрализуется гомологичной антисывороткой. Вирус обладает гемагглютинирующей активностью (ГА-активностью), реагируя с антителами переболевших или иммунизированных животных в реакции непрямой гемагглютинации (РНГА). При вакцинации лабораторных и естественно-восприимчивых животных вирусный антиген индуцирует образование специфических антител, выявляемых в РНГА в разведении 1:16-1:256. Биотехнологические характеристики Вирус ИРТ КРС штамма «ВНИИЗЖ» репродуцируется в культурах клеток ВНК-21, MDBK и ЗКГ, вызывая цитопатическое действие (ЦПД), и в течение 48-96 часов инкубирования накапливается в титрах от 6,5 до 8,0 Ig ТЦД50/см3. Результаты адаптации вируса ИРТ КРС штамма «ВНИИЗЖ» к указанным культурам клеток представлены в таблицах 1, 2 и 3. Штамм «ВНИИЗЖ» является стабильным и сохраняет свои свойства на протяжении 10 пассажей (срок наблюдения). Генотаксономическая характеристика Выделено и охарактеризовано 9 структурных белков вируса ИРТ штамма «ВНИИЗЖ»: VP 105, VP 90 (гемагглютинин), VP 74, VP 64, VP 54, VP 50, VP 47, VP 40 и VP 31. Гликопротеины g I, g III, g IV участвуют в формировании гуморального и клеточного иммунитета. Наиболее эффективным в этом отношении является g IV. По данным реакции нейтрализации наибольшей иммуногенностью обладают VP 90 и VP 74. Белок, маркированный как VP 8 с м.м. 96 кД, является одним из главных белков герпесвируса-1 КРС. Он участвует в модуляции экспрессии генов класса А, стимулирует пролиферацию Т-клеток и образование антител у телят как после заражения, так и после иммунизации животных очищенным белком. За индукцию вируснейтрализующих антител к герпесвирусу-1 КРС ответственны 4-х оболочечные гликопротеины, главными из которых являются g 70 и g 97, расположенные в шипиках вириона. В структуре g IV вируса ИРТ идентифицированы 3 нейтрализующих домена. Домен 1 содержит 2 перекрывающих эпитопа, домен 2 – один эпитоп. Домен 1 имеет отношение к проникновению вируса в клетки-мишени. Устойчивость к внешним факторам Штамм «ВНИИЗЖ» вируса ИРТ КРС устойчив к воздействию низких температур: при минус 60-70°С вирус выживает 7-9 месяцев, при 56°С вирус инактивируется через 20 минут, при 37°С – через 4-10 суток, при 22°С – через 50 суток, при 4°С активность вируса снижается через 30-40 суток лишь на 1,0 Ig. Раствор формалина 1:500 инактивирует вирус через 24 часа. Ацетон, эфир, хлороформ и этиловый спирт инактивируют его немедленно. В кислой среде вирус быстро теряет свою активность, но длительно (до 9 месяцев) сохраняется при рН 6-9 и в условиях 4°С. Лиофилизация почти не влияет на его активность, однако многократное замораживание и оттаивание снижают вирулентность и иммуногенность вируса. Дополнительные признаки и свойства Иммуногенная активность -100%. Патогенность – выражена. Вирулентность – выражена. Контагиозность – выражена. Онкогенность – отсутствует. Свободен от контаминации бактериями, микоплазмами и гемагглютинирующими вирусами. Для получения антигенного материала из штамма «ВНИИЗЖ» вируса ИРТ КРС в качестве чувствительной биологической системы используют преимущественно монослойные культуры клеток ВНК-21 и MDBK, выращенные в 1,5 дм3 матрасах или вращающихся сосудах объемом 3 дм3. При необходимости для получения антигенного материала из штамма «ВНИИЗЖ» вируса ИРТ КРС можно использовать культуру клеток 3 КГ. Полученный вируссодержащий материал освобождают от клеточного детрита и других балластных примесей низкоскоростным центрифугированием и производят контроль вирусного сырья. Производственная серия вируса ИРТ КРС должна иметь инфекционную активность не менее 6,0 Ig ТЦД50/см3 и активность в РДП не менее 4,0 log2. Для инактивации вируса ИРТ штамма «ВНИИЗЖ» используют АЭЭИ, который вносят в очищенную вируссодержащую суспензию до концентрации 0,1%. Инактивацию вируса проводят при температуре 36-37°С в течение 24 часов при значении рН 7,6-7,8 с периодическим перемешиванием суспензии (каждые 5-6 часов по 3-5 минут). По окончании инактивации АЭЭИ нейтрализуют внесением в антигенный материал тиосульфата натрия. Для этого в охлажденную до 2-8°С суспензию антигена добавляют 1М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Для изготовления эмульсионной формы предлагаемой вакцины используют антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС с активностью в РНГА не менее 4,0 log2 в количестве не менее 10,0 мас.%. Вирусный изолят, послуживший источником для получения производственного штамма «ВНИИЗЖ» коронавируса КРС, выделен из фекалий новорожденного теленка с нарушением функции желудочно-кишечного тракта. Производственный штамм «ВНИИЗЖ» коронавируса КРС адаптирован к культурам клеток MDBK, Таурус-1, КСТ и Vero. Штамм «ВНИИЗЖ» коронавируса КРС депонирован 12 марта 2001 года во Всероссийскую государственную коллекцию штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Федерального государственного учреждения «Всероссийский государственный центр качества и стандартизации лекарственных средств для животных и кормов» (ФГУ «ВГНКИ») под регистрационным наименованием «ВНИИЗЖ-ДЕП». Штамм «ВНИИЗЖ» коронавируса КРС характеризуется следующими признаками и свойствами (17). Морфологические признаки Штамм «ВНИИЗЖ» коронавируса КРС относится к семейству Coronaviridae, роду Coronavirus и обладает морфологическими признаками, характерными для возбудителя коронавирусной инфекции КРС: сферический или плеоморфный вирион диаметром 80-100 нм состоит из нуклеокапсида спиральной симметрии и липопротеидной оболочки, на поверхности которой имеются булавовидные выступы длиной 12-24 нм, образующие подобие солнечной короны. Плавучая плотность вирионов в градиенте сахарозы составляет 1,15-1,18 г/см3. В составе вирионов обнаружены три структурных белка: пепломерный гликопротеин Е2 (180-200 кД), нуклеокапсидный фосфопротеин N (50-60 кД) и матриксный гликопротеин Е1 (23-30 кД). Антигенные свойства Антиген коронавируса КРС штамма «ВНИИЗЖ» индуцирует в организме морских свинок и кроликов образование вирусспецифических антител, выявляемых в реакции торможения гемагглютинации (РТГА). В сыворотках крови вакцинированных кроликов уровень антител колеблется от 5,4±0,25 до 7,25±0,47 log2 (в среднем 6,32±0,39 log2), а в сыворотках крови иммунизированных морских свинок – от 5,4±0,38 до 8,2±0,8 log2 (в среднем 6,1±0,49 log2). В сыворотках крови проб, отобранных за 10-15 дней до отела, дважды вакцинированных коров выявляются антитела в РТГА в титрах от 7,9±0,35 до 8,9±0,47 log2. Своевременное скармливание такого молозива обеспечивает высокий уровень колостральных антител (до 8,0 log2) в организме новорожденных телят. Биотехнологические характеристики Коронавирус КРС штамма «ВНИИЗЖ» репродуцируется в культурах клеток почек теленка (MDBK, Таурус-1), коронарных сосудов теленка (КСТ) и в гетерологичной культуре клеток почек обезьяны (Vero). При 37°С в течение 3-4 суток инкубирования вирус накапливается в количестве до 108 частиц/см3 (данные электронно-микроскопического исследования). Результаты исследований по адаптации коронавируса КРС штамма «ВНИИЗЖ» к культурам клеток MDBK, Таурус-1, Vero и КСТ представлены в таблице 4. Штамм «ВНИИЗЖ» коронавируса КРС обладает способностью в культуре клеток MDBK репродуцироваться с такой же степенью накопления при 34°С. Срок репродукции при этой температуре увеличивается почти на сутки, однако позволяет получать двойной урожай вируса путем смены поддерживающей среды. «Слив» обладает высокой инфекционной, антигенной и иммуногенной активностью. Устойчивость к внешним факторам Штамм «ВНИИЗЖ» коронавируса КРС проявляет максимальную устойчивость в диапазоне рН 6,0-7,2. Кислая (рН 3,0) и щелочная (рН 11,0) среды оказывают на вирус инактивирующее действие. Возбудитель устойчив к воздействию трипсина. Вирус разрушается жирорастворителями: хлороформом, метиленхлоридом и трипсином Х-100. Инактивированный антиген коронавируса КРС штамма «ВНИИЗЖ» устойчив в процессе хранения при 4°С как в нативном состоянии, так и в составе инактивированных вакцин. Дополнительные признаки и свойства Антигенная активность обладает антигенностью в составе инактивированной вакцины и препарата для гипериммунизации доноров диагностических и лечебных сывороток. Реактогенность – реактогенными свойствами не обладает. Стабильность сохраняет исходные биологические (антигенные) свойства при пассировании в культуре клеток MDBK в течение 30 пассажей (срок наблюдения). Патогенность – выражена. Вирулентность – выражена. Контагиозность – выражена. Онкогенность – отсутствует. Штамм «ВНИИЗЖ» коронавируса КРС свободен от контаминации бактериями, микоплазмами и другими гемагглютинирующими вирусами. Для получения антигенного материала из штамма «ВНИИЗЖ» коронавируса КРС в качестве чувствительной биологической системы используют преимущественно культуру клеток MDBK. При необходимости для получения антигенного материала из штамма «ВНИИЗЖ» коронавируса КРС можно использовать культуру клеток Таурус-1, КСТ и Vero. Полученный вируссодержащий материал очищают от балластных примесей центрифугированием или любым другим известным методом. Для инактивации вируса используют АЭЭИ, который добавляют в очищенную вируссодержащую суспензию до концентрации 0,1%. Инактивацию вируса ведут при 37°С в течение 24 часов. По окончании инактивации АЭЭИ нейтрализуют внесением в суспензию антигена 1М раствора тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Для изготовления предлагаемой вакцины используют в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного преимущественно в культуре клеток MDBK со степенью накопления не менее 108 вирусных частиц/см3 и активностью в РГА не менее 7,0 log2, в количестве не менее 10,0 мас.%. При необходимости предлагаемая ассоциированная вакцина может содержать в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Таурус-1 со степенью накопления не менее 109 вирусных частиц/см3 и активностью в РГА не менее 9,0 log2, в количестве не менее 10,0 мас.%. При необходимости предлагаемая ассоциированная вакцина может содержать в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток КСТ со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. При необходимости предлагаемая ассоциированная вакцина может содержать в качестве активного вещества авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Vero со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. Полученный таким образом антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС используют для изготовления эмульсионной формы предлагаемой ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС. Для изготовления предлагаемой вакцины полученные антигенные материалы смешивают в соотношении 1:1:1 и смесь тщательно эмульгируют с масляным адъювантом в гомогенизаторе в соотношении, мас.%, 30,0-70,0 соответственно. Из масляных адъювантов целесообразно использовать масляный адъювант марки Montanide ISA-70 производства фирмы «Seppic» (Франция, стандарт ИСО 9001). Содержание антигенов в предлагаемой вакцине в указанном выше соотношении являются их эффективным количеством в препарате, обеспечивающим достижение технического результата. Использование предлагаемого изобретения расширяет арсенал высокоиммуногенных, безвредных и ареактогенных ассоциированных вакцин против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионных инактивированных, способных защитить поголовье КРС различных половозрастных групп от возбудителей ПГ-3, ИРТ и коронавирусной инфекции КРС, циркулирующих на территории России. Сущность предлагаемого изобретения пояснена примерами его реализации и использования. Пример 1 Для приготовления ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионной инактивированной используют производственные штаммы вирусов: штамм «ВГНКИ-4» вируса ПГ-3, штамм «ВНИИЗЖ» вируса ИРТ и штамм «ВНИИЗЖ» коронавирусной инфекции КРС. Посевной вирус производственного штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученный в монослойной культуре клеток MDBK или ВНК-21, и хранившийся при минус 20°С, дважды оттаивают-замораживают. Полученной вируссодержащей жидкостью заражают суспензионную культуру клеток ВНК-21. Множественность заражения составляет 0,1-1,0 ТЦД50/клетку. После заражения культуру клеток инкубируют в стеклянных культиваторах объемом 6,5 дм3 и 36,5 дм3 при 37°С в течение 24-32 часов до появления ЦПД более чем на 70-90% клеток. После этого полученную вируссодержащую суспензию однократно замораживают-оттаивают, сливают в емкость и отбирают пробы для контроля стерильности и инфекционной активности материала. Инфекционная активность вируса должна быть не менее 6,5 Ig ТЦД50/см3. Полученный вирус очищают от балластных примесей центрифугированием. Затем вирусную суспензию подвергают инактивации рабочим раствором АЭЭИ. Рабочий раствор АЭЭИ готовят за 30-60 минут до внесения в вирусную суспензию путем разбавления исходного препарата (15-19%-ного водного раствора АЭЭИ) стерильной деминерализованной водой до 6%-ной концентрации. Во избежание изменения рН вирусной суспензии рабочий раствор АЭЭИ предварительно доводят 5М раствором уксусной кислоты до рН 7,8-8,2. Перед внесением инактиванта вируссодержащий материал нагревают до 36-37°С и в него вносят рабочий раствор АЭЭИ до конечной концентрации 0,1%. Инактивацию вируса ведут в течение 24 часов при 36-37°С и рН 7,0-7,6 с периодическим перемешиванием (3-5 минут через 5-6 часов). По окончании инактивации антигенный материал охлаждают до 4-6°С и берут пробу для проверки на остаточную вирулентность. Для нейтрализации остаточного АЭЭИ в суспензию антигена добавляют 1М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученный антиген контролируют на стерильность и антигенную активность. Антигенная активность полученного препарата должна составлять не менее 6,5 Ig ТЦД50/см3. Полученный антигенный материал используют в количестве не менее 10,0 мас.% для изготовления эмульсионной формы предлагаемой вакцины. Посевным вирусом производственного штамма «ВНИИЗЖ» вируса ИРТ КРС заражают монослойную культуру клеток ЗКГ или MDBK, или ВНК-21, выращенных в 1,5 дм3 матрасах или во вращающихся сосудах объемом 3,0 дм3. Доза заражения должна составлять 0,1-0,01 ИЕ/клетку. Инфицированную культуру инкубируют при температуре 37°С в течение 48-96 часов до появления ЦПД вируса более, чем в 50% клеток монослоя. Полученную вируссодержащую суспензию охлаждают до 4°С и, соблюдая условия стерильности, освобождают от клеточного детрита низкоскоростным центрифугированием. Очищенная таким образом суспензия должна иметь вид прозрачной жидкости розового или вишневого цвета. Очищенную суспензию сливают в емкость, из которой отбирают пробу для производственного контроля вирусного сырья. Производственная серия вируса ИРТ КРС должна иметь инфекционную активность не менее 6,0 Ig ТЦД50/см3 и активность в РДП не менее 4,0 Iog2. Инактивацию вируса ИРТ осуществляют с помощью 6%-ного водного раствора АЭЭИ, который вносят в вируссодержащую суспензию до конечной концентрации 0,1-0,2%. В подогретую до 26-28°С суспензию вносят при постоянном перемешивании раствор АЭЭИ. рН суспензии устанавливают в пределах значений 7,6-7,8 добавлением в нее 5М раствора уксусной кислоты или аммиака. Инактивацию вируса проводят при температуре 36-37°С в течение 24 часов с периодическим перемешиванием суспензии (по 3-5 минут через каждые 5-6 часов). По окончании инактивации антигенный материал охлаждают до 2-8°С и отбирают пробы для проверки на остаточную инфекционность в культуре клеток MDBK. Для нейтрализации АЭЭИ в суспензию антигенного материала вносят 1М раствор тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученный антигенный материал используют в количестве не менее 10,0 мас.% для изготовления эмульсионной формы предлагаемой вакцины. Посевной вирус производственного штамма «ВНИИЗЖ» коронавируса КРС хранят перед использованием при температуре -20°С. Посевной вирус должен быть свободен от бактериальной и грибковой микрофлоры, специфичным, вызывать агглютинацию эритроцитов мышей, иметь активность в РГА не ниже 1:8 и концентрацию вирусных частиц (по результатам электронной микроскопии) в пределах от 105,0 до 106,5 вирусных частиц/см3 (14). Посевной коронавирус КРС дважды замораживают – оттаивают и используют для заражения культуры клеток MDBK. Перед заражением культуру клеток MDBK с качественным монослоем дважды отмывают от ростовой сыворотки раствором Хенкса, содержащим трипсин (15-20 мкг/см3). Множественность заражения составляет 0,1-1,0 вирусных частиц/клетку. После заражения культуральные сосуды инкубируют при 37°С в течение 1,5-2 часов, периодически покачивая. Затем проводят слив вируссодержащего материала и в него вносят поддерживающую среду, содержащую трипсин (15-20 мкг/см3). Сосуды инкубируют при 34°С или 37°С до появления ЦПД вируса более чем в 90% клеток. После этого культуру дважды замораживают-оттаивают. Полученный вирусный материал очищают от балластных примесей низкоскоростным центрифугированием при 2500-3000 об/мин в течение 30 минут. Инактивацию вируса проводят с помощью АЭЭИ. Для этого в вируссодержащую суспензию вносят 6%-ный рабочий раствор АЭЭИ, подкисленный ледяной уксусной кислотой до значения рН 7,8-8,2. Конечная концентрация АЭЭИ в вируссодержащей суспензии должна быть не менее 0,1%. Инактивацию вируса проводят при температуре 36-37°С в течение 24 часов с периодическим перемешиванием суспензии (по 3-5 минут через каждые 5-6 часов). Остаток АЭЭИ нейтрализуют добавлением 1М раствора тиосульфата натрия из расчета 10% к объему использованного АЭЭИ. Полученный антигенный материал исследуют на стерильность, авирулентность, содержание вирусных частиц в суспензии с помощью электронного микроскопа и активность в РГА. Для изготовления предлагаемой вакцины используют авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного преимущественно в культуре клеток MDBK со степенью накопления не менее 108 вирусных частиц/см3 и активностью в РГА не менее 7,0 log2, в количестве не менее 10,0 мас.%. При необходимости для изготовления предлагаемой вакцины можно использовать авирулентный и очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Таурус-1 со степенью накопления не менее 109 вирусных частиц/см3 и активностью в РГА не менее 9,0 log2, в количестве не менее 10,0 мас.%. При необходимости для изготовления предлагаемой вакцины можно использовать авирулентный и очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток КСТ со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. При необходимости для изготовления предлагаемой вакцины можно использовать авирулентный и очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Vero со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. Полученные таким образом антигенные материалы используют для изготовления предлагаемой вакцины. Для этого антигенные материалы смешивают в соотношении 1:1:1 и смесь тщательно эмульгируют с масляным адъювантом в гомогенизаторе в соотношении, мас.%, 30,0-70,0 соответственно. Из масляных адъювантов целесообразно использовать масляный адъювант марки Montanide ISA-70 производства фирмы «Seppic» (Франция, стандарт ИСО 9001). Предлагаемая вакцина имеет оптимальный компонентный состав, мас.%: Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK и из культуры клеток ВНК-21, с инфекционной активностью не менее 6,5 Ig ТЦД50/см3 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток ВНК-21, из культуры клеток MDBK и из культуры клеток 3КГ, с инфекционной активностью не менее 6,0 lg ТЦД50/см3 и активностью в РДП не менее 4,0 log2 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK, из культуры клеток Таурус-1, из культуры клеток КСТ и из культуры клеток Vero, в концентрации вирусных частиц, обеспечивающей протективную иммунную активность антигена в организме животного после введения ему целевого препарата – 10,0 Масляный адъювант – до 100,0 Содержание антигенных материалов в предлагаемой вакцине в указанных выше пределах является их эффективным количеством в препарате, обеспечивающим достижение технического результата от использования изобретения. Полученная вакцина представляет собой однородную эмульсию белого или бело-розового цвета слегка вязкой консистенции. При хранении вакцины допускается незначительное отслоение минерального масла на верхней поверхности эмульсии и водной фазы на дне флакона толщиной не более 1 см. Вакцину контролируют на авирулентность и стерильность, а затем фасуют в стерильные флаконы. Стерильность вакцины определяют в соответствии с ГОСТом 28085-89. Авирулентность препарата определяют методом трехкратных последовательных пассажей инактивированного антигена в культуре клеток MDBK по отсутствию ЦПД. Для проверки безвредности вакцину вводят внутримышечно в область бедра 10 белым мышам в дозе 0,1 см3. Вакцина считается безвредной, если белые мыши в течение 10 суток остаются клинически здоровыми: без каких-либо патологических изменений. На месте введения препарата допускается местная тканевая реакция. Вязкость вакцины определяют на вискозиметре ВПЖ-2 и выражают мм2/сек. Предлагаемая вакцина, содержащая в своем составе масляный адъювант марки Montanide ISA-70, образующего тип эмульсии «вода-масло», имеет вязкость 38,3±0,5 мм2/сек. Контроль вакцины на стабильность эмульсии осуществляют посредством центрифугирования при 3000 об/мин в течение 30 минут, а также в процессе хранения при 2-8°С и 37°С с последующей визуальной оценкой однородности эмульсии. Вакцина с масляным адъювантом марки Montanide ISA-70 обладает высокой стабильностью эмульсии при хранении в различных температурных условиях и при центрифугировании. Для проверки реактогенности препарата предлагаемую вакцину вводят внутримышечно в область бедра 3 кроликам и 5 морским свинкам в дозе 2,0 см3 и 1,0 см3 соответственно. За клиническим состоянием животных ведут наблюдение в течение 14 суток. После иммунизации у кроликов и морских свинок отмечено незначительное местное повышение температуры тела и образование припухлости диаметром около 1 см в месте введения. Эти признаки полностью исчезают к концу срока наблюдения. Таким образом, предлагаемая вакцина относится к типу слабореактогенных препаратов. Антигенную активность проверяют на кроликах. Для этого берут 6 кроликов массой 2,0-2,5 кг. Вакцину вводят 4 кроликам подкожно в область спины по 2,0 см3. Через 14 суток после двукратного введения вакцины с интервалом 20-25 суток у кроликов берут из ушной вены по 2,0-3,0 см3 крови, кровь выдерживают при температуре 37°С, отделяют сыворотку и исследуют на наличие антител к вирусу ПГ-3 и коронавирусу КРС в реакции торможения гемагглютинации (РТГА), к вирусу ИРТ КРС в реакции нейтрализации (рН) или в реакции непрямой гемагглютинации (РНГА). Невакцинарованных животных (2 головы) обескровливают одновременно с вакцинированными, отделяют сыворотку и ее используют для контроля. Серию вакцины считают прошедшей контроль на антигенность, если титр вирусспецифических антител к вирусу ПГ-3 и коронавирусу КРС в РТГА не ниже 5,0 log2, а к вирусу ИРТ КРС в рН не ниже 3,0 log2 или в РНГА не ниже 4,0 log2. Ассоциированная вакцина против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионная инактивированная предназначена для иммунизации коров и телят в хозяйствах, неблагополучных по данным заболеваниям. Вакцину вводят животным внутримышечно в область средней трети шеи в объеме 2,0 см3 двукратно с интервалом 21-30 дней с последующей ревакцинацией через 6 месяцев. Для поддержания благополучия по данным заболеваниям следует придерживаться следующей схемы вакцинации: 1) телят вакцинируют, начиная с 1-3-дневного возраста двукратно с интервалом 21-30 дней. Ревакцинация через 6 месяцев; 2) нетелей и коров вакцинируют двукратно с интервалом 21-30 дней. Ревакцинация через 6 месяцев; 3) телок случного периода вакцинируют двукратно с интервалом 21-30 дней за 1,0-1,5 месяца до первой случки. Ревакцинация через 6 месяцев. Иммунитет у привитых животных формируется через 10-15 суток после повторного введения вакцины и сохраняется не менее 6 месяцев. Пример 2 Проведена проверка антигенной активности ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионной инактивированной, изготовленной так, как описано в примере 1, и содержащей, мас.%: Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью 7,0 Ig ТЦД50/см3 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью 6,5 Ig ТЦД50/см3 и активностью в РДП 4,0 log2 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток MDBK со степенью накопления 108 вирусных частиц/см3 и активностью в РГА 7,0 log2 – 10,0 Масляный адъювант – до 100,0 Антигенную активность полученного препарата определяли на 10 кроликах массой 2,5-3,0 кг. В сыворотках крови вакцинированных кроликов антитела к коронавирусу КРС выявлялись в РТГА на уровне 6,0±0,44 log2, к вирусу ИРТ КРС в РНГА на уровне 6,2±0,12 log2 и вирусу ПГ-3 КРС в РТГА на уровне 6,5±0,3 log2. Вакцина была использована также для иммунизации 15-25-дневных телят в хозяйствах Нижегородской области. В таблице 5 приведены результаты исследования сывороток крови вакцинированного молодняка. Данный препарат индуцировал образование вирусспецифических антител к возбудителям ПГ-3, ИРТ и коронавирусной инфекции КРС в титрах 6,73±0,35 log2, 6,43±0,35 log2 и 6,68±0,44 log2 соответственно. Отмечено увеличение уровня антител на 1,28-1,95 log2 по сравнению с исходным. Количество иммунных животных увеличилось на 17,5-40,0%. Пример 3 Проведена проверка антигенной активности ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионной инактивированной, изготовленной так, как описано в примере 1, и содержащей, мас %: Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток ВНК-21, с инфекционной активностью 7,0 Ig ТЦД50/см3 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью 6,5 Ig ТЦД50/см3 и активностью в РДП 4,0 log2 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток MDBK со степенью накопления 108 вирусных частиц/см3 и активностью в РГА 7,0 log2 – 10,0 Масляный адъювант – до 100,0 Исследования проводились в ЗАО «Друг крестьянина» Лысковского района Нижегородской области на 5 коровах 4-8-летнего возраста и в ЗАО «Имени Лакина» Собинского района Владимирской области на 33 коровах 4-8-летнего возраста. Результаты исследований представлены в таблице 6, которые свидетельствуют о высокой антигенной активности, полученной в соответствии с изобретением вакцины. Средний уровень антител к вирусу ПГ-3 КРС составил 6,9±0,62 log2, к вирусу ИРТ КРС – 5,8±0,95 log2, к коронавирусу КРС – 6,3±0,48 log2, что является достаточным основанием для практического применения предлагаемой вакцины. При смешивании конкуренции антигенов не происходит. Пример 4 Проведена проверка эффективности ассоциированной вакцины против ПГ-3, ИРТ и коронавируса КРС эмульсионной инактивированной, изготовленной так, как описано в примере 1, и содержащей, мас.%: Авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью 7,0 Ig ТЦД50/см3 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью 6,5 Ig ТЦД50/см3 и активностью в РДП 4,0 log2 – 10,0 Авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток MDBK со степенью накопления 108 вирусных частиц/см3 и активностью в РГА 7,0 log2 – 10,0 Масляный адъювант – до 100,0 Предварительно были проведены исследования сыворотки крови молодняка КРС из неблагополучных по респираторным заболеваниям хозяйств. Полученные данные свидетельствуют о том, что антитела к вирусу ПГ-3 выявлены в 52,0% проб сывороток крови, к вирусу ИРТ КРС – в 57,9%, к коронавирусу КРС – в 47,9% и к возбудителю вирусной диареи – в 29,7%. Антитела к одному вирусу обнаружены в 11,9% сывороток, к двум – в 31,3%, к трем – в 25,8%, к четырем – в 19,5%. Полученные данные свидетельствуют о циркуляции в большинстве обследованных хозяйств нескольких возбудителей, что свидетельствует о преобладании ассоциированного течения респираторных заболеваний. В серии опытов были исследованы сыворотки крови КРС разного возраста. Полученные результаты свидетельствуют о том, что у большинства животных до 30-40 дней выявляются колостральные антитела к указанным возбудителям, а у молодняка старших возрастов – постинфекционные. Данные лабораторных исследований подтверждаются результатами клинического осмотра, которые свидетельствуют о вспышках респираторных заболеваний через 5-10 дней после перегруппировки телят в 30-45-дневном возрасте. В результате исследований парных проб сывороток крови молодняка КРС получены данные, свидетельствующие об участии коронавируса КРС в этиопатогенезе респираторных заболеваний молодняка КРС. Во вторых пробах было отмечено повышение титров антител к коронавирусу на 1,4-3,6 log2. В этих же пробах не было отмечено повышение титров антител к возбудителям ПГ-3 и ИРТ, либо они увеличились на 0,2-1,5 log2. Руководствуясь полученной информацией, был поставлен эпизоотологический эксперимент по выявлению роли коронавируса в респираторной патологии молодняка КРС. Для этого в условиях родильных отделений пяти неблагополучных по респираторным заболеваниям хозяйств были сформированы 10 групп телят 15-25-дневного возраста по 20-30 голов в каждой. В каждом хозяйстве телята одной группы были двукратно иммунизированы коммерческой ассоциированной вакциной против ПГ-3 и ИРТ КРС эмульсионной инактивированной, а животные другой группы – предлагаемой ассоциированной вакциной против ПГ-3, ИРТ и коронавирусной инфекции КРС. В результате клинического осмотра, проведенного через 10-20 дней после вакцинации у 10-20% животных, привитых коммерческой ассоциированной вакциной против ПГ-3 и ИРТ эмульсионной инактивированной были отмечены кашель и риниты. В то же время у телят, привитых предлагаемой вакциной, клинических признаков респираторных заболеваний не отмечалось. В таблице 7 приведены результаты исследований сывороток крови от КРС, привитого предлагаемой вакциной. Эти данные свидетельствуют об эффективности указанного препарата. Таким образом, показана возможность оздоровления стада от респираторных заболеваний вирусной этиологии посредством применения ассоциированной вакцины против ПГ-3, ИРТ и коронавирусной инфекции КРС. Источники информации, принятые во внимание при составлении описания изобретения к заявке на выдачу патента РФ на изобретение «Ассоциированная вакцина против ПГ-3, ИРТ и коронавирусной инфекции КРС эмульсионная инактивированная»: 1. Инфекционные болезни животных: Справочник. Под ред. Д.Ф.Осидзе. – М.: Агропромиздат, 1987, 288 с. 2. Сюрин В.Н., Самуйленко А.Я., Соловьев Б.В., Фомина Н.В. Вирусные болезни животных. – М.: ВНИИТИБН, 1998, 928 с. 3. Инфекционная патология животных: В 2 Т. / Под ред. А.Я.Самуйленко, Б.В.Соловьева, Е.А.Непоклонова, Е.С.Воронина. – М.: «Академкнига», 2006. – Т.1. – 911 с. 4. Пат. РФ 5. Пат. РФ 6. Пат. РФ 7. Пат. ЧССР 8. Пат. ЧССР 9. Пат. ЧССР 10. Пат. РФ 11. WO 2002/062 382, A61K 39/15, 39/215, 39/08, 39/108, 15.08.2002 г. 12. Наставление по применению вакцины инактивированной комбинированной против ИРТ, ПГ-3, вирусной диареи, респираторно-синцитиальной, рота- и коронавирусной болезни телят КОМБОВАК, 13. Пат. РФ 14. Пономарев А.П., Молчанова А.И. и Узюмов В.Л. Определение концентрации частиц вируса ящура в суспензиях. – Ветеринария, 1983, 15. Пат. РФ 16. Пат. РФ 17. Пат. РФ
Формула изобретения
1. Ассоциированная вакцина против парагриппа-3 (ПГ-3), инфекционного ринотрахеита (ИРТ) и коронавирусной инфекции крупного рогатого скота (КРС) эмульсионная инактивированная, содержащая активное вещество и целевую добавку, отличающаяся тем, что в качестве активного вещества она содержит смесь из авирулентного очищенного антигенного материала из штамма «ВГНКИ-4» вируса ПГ-3 КРС, сем. Paramyxoviridae, рода Parainfluenza, подтипа Parainfluenza virus 3, коллекция ФГУ «ВГНКИ» «ВГНКИ-4» ДЕП, из авирулентного очищенного антигенного материала из штамма «ВНИИЗЖ» вируса ИРТ КРС, сем. Herpesviridae, рода Varicellavirus, коллекция ФГУ «ВГНКИ» «ВНИИЗЖ-ДЕП» и из авирулентного очищенного антигенного материала из штамма «ВНИИЗЖ» коронавируса КРС, сем. Coronaviridae, рода Coronavirus, коллекция ФГУ «ВГНКИ» «ВНИИЗЖ-ДЕП», взятых в соотношении 1:1:1 и в количествах, обеспечивающих протективную иммунную активность каждого антигена в организме животного после введения ему целевого препарата. 2. Ассоциированная вакцина по п.1, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток почек теленка MDBK и из культуры клеток почек сирийского хомячка ВНК-21, в эффективном количестве. 3. Ассоциированная вакцина по п.2, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток MDBK с инфекционной активностью не менее 6,5 lg ТЦД50/см3, в количестве не менее 10,0 мас.%. 4. Ассоциированная вакцина по п.2, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВГНКИ-4» вируса ПГ-3 КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью не менее 6,5 lg ТЦД50/см3, в количестве не менее 10,0 мас.%. 5. Ассоциированная вакцина по п.1, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток ВНК-21, из культуры клеток MDBK и из культуры клеток гонад 3-дневной козы 3КГ, в эффективном количестве. 6. Ассоциированная вакцина по п.5, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток ВНК-21 с инфекционной активностью не менее 6,0 lg ТЦД50/см3 и активностью в реакции диффузной преципитации (РДП) не менее 4,0 log2, в количестве не менее 10,0 мас.%. 7. Ассоциированная вакцина по п.5, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток MDBK с инфекционной активностью не менее 6,0 lg ТЦД50/см3 и активностью РДП не менее 4,0 log2, в количестве не менее 10,0 мас.%. 8. Ассоциированная вакцина по п.5, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» вируса ИРТ КРС, полученного в культуре клеток 3КГ с инфекционной активностью не менее 6,0 lg ТЦД50/см3 и активностью в РДП не менее 4,0 log2, в количестве не менее 10,0 мас.%. 9. Ассоциированная вакцина по п.1, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток животного происхождения, взятой из группы, состоящей из культуры клеток MDBK, из культуры клеток почек теленка Таурус-1, из культуры клеток коронарных сосудов теленка КСТ и из культуры клеток почек обезьяны Vero, в эффективном количестве. 10. Ассоциированная вакцина по п.9, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток MDBK со степенью накопления не менее 108 вирусных частиц/см3 и активностью в реакции гемагглютинации (РГА) не менее 7,0 log2, в количестве не менее 10,0 мас.%. 11. Ассоциированная вакцина по п.9, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Таурус-1 со степенью накопления не менее 109 вирусных частиц/см3 и активностью в РГА не менее 9,0 log2, в количестве не менее 10,0 мас.%. 12. Ассоциированная вакцина по п.9, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток КСТ со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. 13. Ассоциированная вакцина по п.9, отличающаяся тем, что она содержит авирулентный очищенный антигенный материал из штамма «ВНИИЗЖ» коронавируса КРС, полученного в культуре клеток Vero со степенью накопления не менее 107,5 вирусных частиц/см3 и активностью в РГА не менее 6,0 log2, в количестве не менее 10,0 мас.%. 14. Ассоциированная вакцина по п.1, отличающаяся тем, что в качестве целевой добавки она содержит масляный адъювант в количестве не менее 70,0 мас.%. 15. Ассоциированная вакцина по любому из пп.1-14, отличающаяся тем, что она содержит смесь авирулентных очищенных антигенных материалов из штамма «ВГНКИ-4» вируса ПГ-3, из штамма «ВНИИЗЖ» вируса ИРТ и из штамма «ВНИИЗЖ» коронавируса КРС, полученных в культурах клеток животного происхождения, и масляный адъювант в соотношении, мас.%:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 3760 вируса ИРТ КРС, из штамма ТМ-91 (САРМ V-279) ротавируса КРС, из штамма BCV-9 (САРМ V-280) коронавируса КРС и из штаммов 3935/1 (САРМ 6234) и 6304 (САРМ 6235) бактерий Е. coli, полученных в чувствительных биологических системах, и в качестве целевой добавки масляный адъювант в эффективных соотношениях (8).
3760 вируса ИРТ КРС, из штамма ТМ-91 (САРМ V-279) ротавируса КРС, из штамма BCV-9 (САРМ V-280) коронавируса КРС и из штаммов 3935/1 (САРМ 6234) и 6304 (САРМ 6235) бактерий Е. coli, полученных в чувствительных биологических системах, и в качестве целевой добавки масляный адъювант в эффективных соотношениях (8).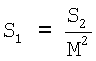
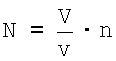 ,
,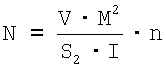 ,
,