|
|
(21), (22) Заявка: 2006115731/04, 06.05.2006
(24) Дата начала отсчета срока действия патента:
06.05.2006
(43) Дата публикации заявки: 20.11.2007
(46) Опубликовано: 27.12.2009
(56) Список документов, цитированных в отчете о
поиске:
CHEN J. ет al. Tetrahedron Lett., 43, 2002, p.3533-3535. SU 1776655 A1, 23.11.1992. SU 1583420 A1, 07.08.1990. RU 2160269 С1, 10.12.2000. FAGAN R.J. ет al. JACS, 116, 1994, р. 1880-1890.
Адрес для переписки:
450075, г.Уфа, пр-кт Октября, 141, ИНК РАН, патентная группа
|
(72) Автор(ы):
Джемилев Усеин Меметович (RU),
Ибрагимов Асхат Габдрахманович (RU),
Дьяконов Владимир Анатольевич (RU),
Зиннурова Регина Адиковна (RU),
Халилов Леонард Мухибович (RU),
Ковтуненко Ирина Анатольевна (RU)
(73) Патентообладатель(и):
ИНСТИТУТ НЕФТЕХИМИИ И КАТАЛИЗА РАН (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ 2,3,4,5-ТЕТРААЛКИЛТИОФЕНОВ
(57) Реферат:
Изобретение относится к органической химии, в частности, к способу получения 2,3,4,5-тетраалкилтиофенов, которые могут найти применение в качестве промежуточного продукта в синтезе красителей, биологически активных соединений, а также в качестве компонента усилителей аромата пищи, присадок к маслам и гидравлическим жидкостям. Описывается способ получения 2,3,4,5-тетраалкилтиофенов, заключающийся во взаимодействии дизамещенных ацетиленов с н-BuMgCl в присутствии катализатора цирконацендихлорида в атмосфере аргона при комнатной температуре в диэтиловом эфире в течение 2-4 часов с последующим добавлением элементной серы S8 в эквимольном по отношению к BuMgCl количестве и кипячением в бензоле 5 часов. Предложенный способ позволяет получить целевой продукт с высокой селективностью по упрощенной технологии за счет исключения труднодоступных 1,4-дийодбутадиенов, высокопирофорного н-бутиллития и высокотоксичного сероуглерода. 1 табл.
Предлагаемое изобретение относится к органической химии, конкретно к усовершенствованному способу получения 2,3,4,5-тетраалкилтиофенов общей формулы (1):

Замещенные тиофены могут найти применение в пищевой промышленности в качестве компонентов усилителей аромата пищи, биологически активных соединений, красителей, присадок к маслам и гидравлическим жидкостям.
 , , -диацетиленов с последующей обработкой реакционной массы бисциклопентадиенилцирконийдихлоридом (Ср2ZrСl2) и бутиллитием (n-BuLi), с полухлористой серой (S2Cl2) за 1 час по схеме: -диацетиленов с последующей обработкой реакционной массы бисциклопентадиенилцирконийдихлоридом (Ср2ZrСl2) и бутиллитием (n-BuLi), с полухлористой серой (S2Cl2) за 1 час по схеме:

Известным способом не могут быть получены 2,3,4,5-тетраалкилтиофены (1).
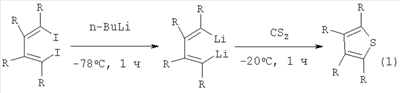
Известный способ синтеза 2,3,4,5-тетраалкилтиофенов (1) предполагает использование труднодоступных 1,4-дииодо-1,3-бутадиенов, крайне пирофорного n-BuLi и сероуглерода (СS2), представляющего собой легковоспламеняющуюся, легколетучую и высокотоксичную жидкость. Кроме того, в ходе реакции необходимо поддерживать низкую температуру -78°С.
Предлагается усовершенствованный способ синтеза 2,3,4,5-тетраалкилтиофенов (1).
Сущность способа заключается во взаимодействии дизамещенных ацетиленов формулы R- -R, где R=С2Н5, н-С3H7, н-С4Н9, с н-BuMgCl в присутствии катализатора цирконацендихлорида (Cp2ZrCl2), взятыми в мольном соотношении R- -R, где R=С2Н5, н-С3H7, н-С4Н9, с н-BuMgCl в присутствии катализатора цирконацендихлорида (Cp2ZrCl2), взятыми в мольном соотношении R- -R:н-BuMgCl:Cp2ZrCl2=10:(22-26):(1.0-1.4), предпочтительно 10:24:1.2, в среде диэтилового эфира в течение 2-4 ч при комнатной температуре (~20°С), с последующим добавлением эквивалентного к BuMgCl количества элементной серы (S8), бензола и кипячении в течение 5 ч. Реакцию проводят в атмосфере аргона и атмосферном давлении. Выход целевых продуктов 44-60%. -R:н-BuMgCl:Cp2ZrCl2=10:(22-26):(1.0-1.4), предпочтительно 10:24:1.2, в среде диэтилового эфира в течение 2-4 ч при комнатной температуре (~20°С), с последующим добавлением эквивалентного к BuMgCl количества элементной серы (S8), бензола и кипячении в течение 5 ч. Реакцию проводят в атмосфере аргона и атмосферном давлении. Выход целевых продуктов 44-60%.
Реакция протекает по схеме:
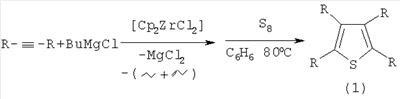
R=С2Н5, н-С3Н7, н-С4Н9
Целевые продукты (1) образуются только лишь с участием дизамещенного ацетилена, н-BuMgCl, элементной серы (S8) и катализатора Cp2ZrCl2. В присутствии других катализаторов на основе комплексов переходных металлов (например, Zr(acac)4, Cp2TiCl2, Pd(acac)2, Ni(acac)2, Fе(асас)3) целевые продукты (1) не образуются.
Проведение реакции в присутствии катализатора Ср2ZrCl2 больше 14 мол.% по отношению к ацетилену не приводит к существенному увеличению выхода целевых продуктов (1). Использование в реакции катализатора Cp2ZrCl2 менее 10 мол.% снижает выход тиофенов (1), что связано со снижением каталитически активных центров в реакционной массе. Опыты проводили при комнатной температуре ~20°С. При более высокой температуре (например, 50°С) увеличивается содержание продуктов уплотнения, при меньшей температуре (например, 0°С) снижается скорость реакции.
Изменение соотношения исходных реагентов в сторону увеличения содержания н-BuMgCl по отношению к ацетилену не приводит к значительному повышению выхода целевых продуктов (1). Снижение количества н-BuMgCl по отношению к ацетилену уменьшает выход тиофенов (1).
Существенные отличия предлагаемого способа:
В предлагаемом способе используются в качестве исходных соединений дизамещенный ацетилен, н-BuMgCl и S8 с участием катализатора Cp2ZrCl2. В известном способе тетраалкилтиофены (1) получают из 1,4-дийодбутадиенов, бутиллития и сероуглерода.
Предлагаемый способ обладает следующими преимуществами:
Способ позволяет получать с высокой селективностью 2,3,4,5-тетраалкилтиофены (1) без использования труднодоступных 1,4-дийодбутадиенов, крайне прирофорного н-BuLi и высокотоксичного сероуглерода СS2.
Способ поясняется следующими примерами:
Пример 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 1.2 ммоль Cp2ZrCl2, 10 ммоль окт-4-ина и при температуре ~0° 24 ммоль н-BuMgCl (2М раствор в Et2O). Перемешивают при комнатной температуре 3 ч, затем добавляют 24 ммоль элементной серы S8, 10 мл бензола и кипятят в течение 5 ч. Получают индивидуальный 2,3,4,5-тетрапропилтиофен (1) с выходом 54%. Спектральные характеристики 2,3,4,5-тетрапропилтиофена (1).
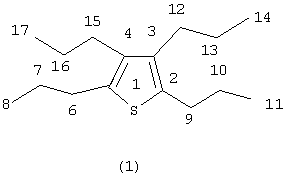 |
Спектр ЯМР 13C ( , м.д.):13.54 (С14,17), 14.25(С8,11), 21.90 (С13,16), 24.18(С7,10), 29.33(С6,9), 30.17 (С12,15), 135.25 (С2,5), 136.78 (С3,4). , м.д.):13.54 (С14,17), 14.25(С8,11), 21.90 (С13,16), 24.18(С7,10), 29.33(С6,9), 30.17 (С12,15), 135.25 (С2,5), 136.78 (С3,4). |
Другие примеры, подтверждающие способ, приведены в таблице
Формула изобретения
Способ получения 2,3,4,5-тетраалкилтиофенов общей формулы (I)
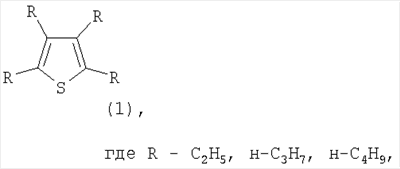
характеризующийся тем, что дизамещенный ацетилен общей формулы
R –  -R, -R,
где R – C2H5, н-С3Н7, н-С4Н9,
подвергают взаимодействию с н-BuMgCl в присутствии катализатора цирконацендихлорида (Cp2ZrCl2) в мольном соотношении R- -R: н-BuMgCl: Cp2ZrCl2=10:22-26:1,0-1,4 в атмосфере аргона при нормальном давлении в диэтиловом эфире в течение 2-4 ч с последующим добавлением элементной серы S8 в эквимольном по отношению к BuMgCl количестве и кипячением в бензоле в течение 5 ч. -R: н-BuMgCl: Cp2ZrCl2=10:22-26:1,0-1,4 в атмосфере аргона при нормальном давлении в диэтиловом эфире в течение 2-4 ч с последующим добавлением элементной серы S8 в эквимольном по отношению к BuMgCl количестве и кипячением в бензоле в течение 5 ч.
|
|