Патент на изобретение №2376020
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ
(57) Реферат:
Изобретение относится к области медицины, в частности фармации, и касается нового противоопухолевого средства, представляющего собой билигандный комплекс ванадила с яблочной кислотой – бис(L-малато)оксованадий (IV). 7 табл., 1 ил.
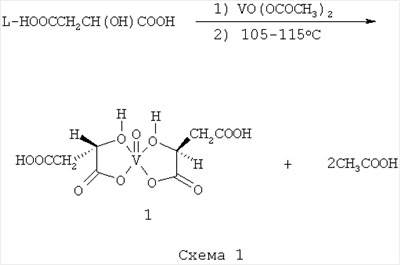
Изобретение относится к области медицины и касается расширения арсенала потенциальных противоопухолевых средств на основе комплекса оксованадия с органическим лигандом. Микроэлемент ванадий рассматривается в настоящее время как важный регулятор роста, дифференцировки и гибели клеток. Ванадийсодержащие соединения представляют интерес и как потенциальные терапевтические агенты, поскольку многие из них проявляют инсулиноподобную [1] или противоопухолевую активность [2]. Для некоторых соединений оксованадия (IV), таких как бис(мальтолато)оксованадий (IV) и бис(ацетилацетонато)оксованадий (IV), являющихся эффективными инсулиномиметиками, описана и антипролиферативная активность в отношении целого ряда линий опухолевых клеток человека [3]. Исследования последних лет показали, что как неорганические соединения четырех- или пятивалентного ванадия, так и целый ряд его комплексов с органическими лигандами, в составе которых валентность ванадия изменяется от 3 до 5, обладают цитостатической активностью, подавляя рост опухолевых клеток in vitro и in vivo [4, 2, 5]. Так, соединения ванадия проявляют выраженный противоопухолевый эффект в отношении рака печени мыши, асцитной опухоли Эрлиха, карциномы молочной железы мыши [6], гепатомы Морриса [5], лейомиосаркомы крысы [7], некоторых линий опухолевых клеток человека [8-10]. Общим для различных соединений ванадия является их способность стимулировать апоптоз в неопластических клетках. Показано, что добавление в питьевую воду животным метаванадата аммония индуцирует апоптоз в неопластических клетках, не оказывая при этом никакого влияния на нормальные пролиферирующие клетки [11]. Комплекс 4-валентного ванадия (бис(4,7-диметил-1,10-фенантролин) сульфатооксованадий (IV))-метван намного более эффективно вызывает апоптоз лейкозных клеток от пациентов с различными формами лейкемии, чем такой стандартный химиотерапевтический агент, как винкристин. Кроме того, метван высокоэффективен в отношении резистентных к цисплатину линий клеток раковых опухолей яичников и тестикул [12, 9]. Исследования, проведенные на различных клеточных линиях, позволили сделать вывод о том, что соединения ванадия проявляют противоопухолевый эффект путем ингибирования тирозинфосфатаз, участвующих в передаче внутриклеточных сигналов. Этот эффект в конечном счете приводит к усилению апоптоза или к активации генов – супрессоров опухолей. Ингибирование фосфорилирования тирозина в белках, вызываемое соединениями ванадия, может также подавлять инвазию и метастазирование опухолевых клеток. Имеющиеся в настоящее время экспериментальные данные позволяют говорить о том, что соединения ванадия могут проявлять (а) антипролиферативный эффект (т.е. подавлять скорость роста раковых клеток); (б) обладать цитотоксическим и (или) цитостатическим действием, обусловленным некрозом или апоптозом; (в) снижать инвазивный или метастатический потенциал малигнезированных клеток; (г) подавлять клеточную резистентность по отношению к химиотерапевтическим агентам [2]. Природа органического лиганда в молекуле ванадийсодержащего соединения во многом определяет его цитотоксическое (противоопухолевое) действие и в то же время цитотоксичность каждого конкретного соединения ванадия варьирует по отношению к различным видам опухолевых клеток. В этой связи актуальным является поиск новых эффективных и нетоксичных соединений ванадия, который продолжается в настоящее время во многих исследовательских центрах. Известен билигандный комплекс ванадила с яблочной кислотой – бис(L-малато)оксованадий(IV) (VO(mal)2) [Патент Яблочная кислота, входящая в состав исследуемого комплекса, является естественным метаболитом и может стать дополнительным источником накопления энергии в клетке. Сущность изобретения состоит в обнаружении противоопухолевой активности бис(L-малато)оксованадия (IV). Целевое соединение бис(L-малато)оксованадий (IV) получают в 2 стадии взаимодействием L-яблочной кислоты (2 моля) с ванадилирующим агентом (ванадилацетатом) (1 моль) в водной среде, в результате чего образуется первичный ванадильный комплекс L-яблочной кислоты в смеси со свободной L-яблочной кислотой. Реакционную смесь удалением воды переводят в твердофазное состояние, и полученный твердый раствор первичного ванадильного комплекса [(L-малато)оксованадия (IV)] в L-яблочной кислоте с целью получения целевого соединения бис(L-малато)оксованадия (IV) подвергают нагреванию при 105-115°С (Схема 1) при пониженном или атмосферном давлении. Строение полученного комплекса подтверждено результатами элементного анализа, а также данными масс-спектрометрии. Пример 1. Бис(L-малато)оксованадий (IV) (1). В раствор 50,9 г (0,38 моль) L-яблочной кислоты в 250 мл воды вносят 35,2 г (0,19 моль) ацетата ванадила. Реакционную смесь перемешивают при 40-60°С до полного растворения осадка. Темно-голубой реакционный раствор упаривают досуха на роторном испарителе и полученный промежуточный темно-синий стекловидный продукт высушивают до постоянного веса в вакуум-эксикаторе. Высушенный продукт измельчают и нагревают в той же реакционной колбе на роторном испарителе при 105-115°С (температура в массе) в вакууме водоструйного насоса в течение 1-1,5 ч, процесс сопровождается выделением воды (5-7 г). Полученный бис(L-малато)оксованадий (IV) 1 представляет собой хрупкую темно-синюю пористую массу, выход 58-61 г (96-98%), содержит 1-2% свободной яблочной кислоты. Бис(L-малато)оксованадий (IV) легко растворим в воде, слабо растворим метаноле и диметилсульфоксиде, почти не растворим в метаноле, не растворим в ацетоне. Найдено, %: V 15,35; С 28,50; Н 3,32. Брутто-формула: C8H10O11V. Вычислено, %: V 15,30: С 28,84; Н 3,03. Молекулярная масса (m/e) 333 (ионизация электроспреем). Удельное оптическое вращение [ Пример 2. Бис(L-малато)оксованадий (IV) (1). Промежуточный продукт, полученный по методу А (1,0 г), нагревают при 97-100°С в течение 24-30 часов. Выход комплекса 0,93 г (99%), который идентичен по физико-химическим характеристикам продукту, полученному в примере 1. В опытах in vitro исследовали влияние оксованадиевого комплека L-яблочной кислоты (VO(mal)2) на рост нормальных фибробластов кожи человека, трансформированных вирусом фибробластов мыши NIH 3Т3, трансформированных вирусом клеток почки человека 293, клеток фибросаркомы мыши L 929, клеток феохромоцитомы крысы PC12 и карциномы печени человека HepG2. Изучение цитотоксичности и противоопухолевой активности оксованадиевых комплексов проводили в сравнении с неорганическим соединением четырехвалентного ванадия -ванадилсульфатом (VOSO4). Культура клеток. Клетки PC12 и L929 были получены из Института морфологии человека и животных PAMH, клетки HepG2 – из Института канцерогенеза Российского онкологического научного центра им. Н.Н.Блохина РАМН, клетки NIH 3Т3 и 293 получены из коллекции клеточных культур Института цитологии РАН. Нормальные фибробласты кожи человека были получены из Института ревматологии РАМН. Клетки PC12 культивировали в среде RPMI 1640, клетки HepG2, L929, NIH 3Т3 и 293 – в среде ДМЕМ с добавлением 10% эмбриональной телячьей сыворотки, фибробласты кожи здорового человека в среде Игла с добавлением 20% бычьей сыворотки. Среды содержали 2 мМ L-глутамина и гентамицин в концентрации 50 мг/мл. Клетки культивировали в 48-луночных планшетах в СО2-инкубаторе при 37°С до состояния плотного монослоя. Цитотоксичность соединений ванадия изучали в интервале концентраций от 0,5 до 24 мкг/мл, используя МТТ-тест. Этот тест, основанный на способности митохондриальных дегидрогеназ образовывать кристаллы формазана из МТТ-реактива (3-[4,5-диметилтиа-2-ил]-2,5-дифенилтетразолий бромида), позволяет точно определить число живых клеток. Исследование действия различных концентраций VO(mal)2 на рост нормальных фибробластов кожи показало, что через 24 часа после добавление VO(mal)2 в концентрации от 0,5 до 6,0 мкг/мл жизнеспособность фибробластов не изменялась по сравнению с контролем. В то же время ванадилсульфат проявляет дозозависимое цитотоксическое действие, начиная с самой низкой концентрации (табл.1). Таким образом, VO(mal)2 не проявляет цитотоксичности по отношению к нормальным клеткам. Увеличение времени инкубации фибробластов в присутствии как VO(mal)2, так и VOSO4 приводит к некоторой стимуляции пролиферации. При исследовании действия VO(mal)2 на клетки фибросаркомы L929 обнаружено дозозависимое уменьшение числа жизнеспособных клеток по сравнению с контролем, которое усиливается с увеличением времени инкубации. Через 72 часа культивирования VO(mal)2 в концентрации 6 мкг/мл подавляет рост клеток на 74%. Такой же эффект вызывает и VOSO4 (табл.2). Клетки PC12 также чувствительны к цитотоксическому действию VO(mal)2, которое проявлялось уже через 24 часа инкубации (табл.3). Для выяснения значения органического лиганда в проявлении цитотоксического действия был исследован также монокомплекс ванадила с яблочной кислотой (L-малатооксованадий) (IV) – VO(mal). Оказалось, что в отличие от биокомплекса VO(mal) во всех исследуемых концентрациях практически не влияет на рост клеток PC12 в течение 24 часов. Через 48 часов культивирования (табл.3) в присутствии монокомплекса наблюдается стимуляция роста этих клеток. Дозозависимое снижение жизнеспособности в присутствии VO(mal)2 наблюдалось и для клеток NIH 3Т3 (табл.4). Клетки HepG2 менее чувствительны к соединениям ванадия по сравнению с другими линиями трансформированных клеток. Так, цитотоксическое действие VO(mal)2 на клетки HepG2 проявляется только через 72 часа культивирования. При инкубации в течение 96 часов число клеток снижается на 40% по сравнению с контролем. Ванадилсульфат в той же концентрации уменьшает число живых клеток приблизительно на 30% только через 96 часов инкубации (табл.5). Эти клетки оказались резистентными к действию комплексов ванадила, в состав которых входят стериоизомеры яблочной кислоты: ванадильные комплексы D-яблочной кислоты (хирального антипода L-яблочной кислоты) и рацемической формы DL-яблочной кислоты (данные не приведены). В табл.6 представлены значения IC50 для пяти линий трансформированных клеток. Из этих данных следует, что бискомплекс ванадила с яблочной кислотой эффективно подавляет рост клеток фибросаркомы (L929), феохромоцитомы (PC12) и трансформированных вирусом клеток почки человека (293). Менее чувствительными к цитотоксическому действию VO(mal)2 оказались трансформированные вирусом фибробласты мыши (NIH 3Т3). В то же время этот комплекс не проявляет цитотоксичности по отношению к нормальным клеткам (табл.1). Известно, что соединения ванадия могут осуществлять антипролиферативное и цитотоксическое действие путем ингибирования синтеза ДНК (14), а также взаимодействия ДНК с факторами транскрипции (15). Включение радиоактивного предшественника в ДНК. Для исследования пролиферации клетки синхронизовали в ростовой среде, содержащей 0,5% эмбриональной телячьей сыворотки в течение 24 часов, затем добавляли исследуемые соединения и С14-тимидин. Через 24 часа после этого клетки промывали холодным раствором Хэнкса и обрабатывали в течение ночи ледяным фиксирующим раствором для того, чтобы убрать из клеток свободный радиоактивный предшественник синтеза ДНК. Затем измеряли число клеток после их окраски кристаллвиолетом, используя мультискан “LabSystems”. Клеточный монослой лизировали в течение 12-ти часов 0.6 н. КОН, затем лизат нейтрализовали 1н. HClO4. Радиоактивность измеряли стандартными радиометрическими методами, используя сцинтилляционную жидкость Брея. Результаты рассчитывали в имп./мин на 106 клеток и в % к контролю. Результаты исследования по влиянию VO(mal)2 и VOSO4 на включение С14-тимидина в ДНК свидетельствуют о том, что синтез ДНК в клетках L929 менее чувствителен к действию оксованадиевых соединений по сравнению с клетками PC12 и его подавление наблюдается только при высоких концентрациях (табл.6). Отметим, что в клетках HepG2, которые оказались на порядок менее чувствительными к цитотоксическому действию оксованадиевых соединений, чем другие линии трансформированных клеток (см. табл.7), ингибирования синтеза ДНК в этих условиях мы не наблюдали. ЛИТЕРАТУРА 1. Badmaev V., Prakash S. and Majeed M. (1999) J. Alternat. Complement. Medicine, 5, 273-291. 2. Evangelou A.M. (2002) Crit. Rev. Oncol./Hematol., 42, 249-265. 3. U.S. Pat. 4. Bishayee A., Oinam S., Basu M. and Chatterjiee M. (2000). Brain Cancer Res. Treatment, 63, 133-145. 5. Osinska-Krolicka I., Podsiadly H., Bukietynska K. et al (2004). J. Inorg. Biochem., 98, 2087-2998. 6. Thompson H.J., Chasteen N.D. and Meeker L.D. (1984). Carcinogenes, 5, 849-851. 7. Liasko R., Kabanos T. A., Karkabounas S. et al (1998). Antycancer Res., 18, 3609-3613. 8. Kopf-Maler P. (1994) Eur. J. Clin. Pharmacol., 47, 1-16. 9. Cruz O. J D., Uckun F.M. (2002). Expert Opin. Investig. Drugs, 11, 1829-1836. 10. Ray R.S., Rana В., Swami В. et al (2006) Chem. Biolog. Interact, 163, 239-247. 11. Ray R.S., Roy S, Ghosh S. et al (2004). Biochim. Biophys. Acta, 1675, 165-73. 12. Naria R.K, Chen C.L., Dong Y, Uckun F.M. (2001). Clin. Cancer Res., 7, 2124-33. 13. Патент РФ 14. Hall I.H., Durham R.W, Tram M. et al. (2003). J Inorg. Biochem, 93, 125-131. 15. Lampronty I., Bianchi N., Borgatty M. et al. (2005). Oncol. Rep., 14, 9-15.
Формула изобретения
Средство, проявляющее противоопухолевую активность, представляющее собой бис(L-малато)оксованадий (IV).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 2101287, 1998 г.], который прошел доклинические испытания в качестве гипогликемического агента [13].
2101287, 1998 г.], который прошел доклинические испытания в качестве гипогликемического агента [13]. ]20-164° (вода), (вода, с 1,65).
]20-164° (вода), (вода, с 1,65).