Патент на изобретение №2375446
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПЛОТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ПАТОГЕННЫХ МИКОБАКТЕРИЙ И НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ
(57) Реферат:
Плотная питательная среда содержит в качестве солевой основы L-аспарагин – 4,0 г, калий фосфорнокислый двузамещенный – 0,5 г, сернокислый магний – 0,5 г, лимонную кислоту – 2,0 г, лимоннокислое аммиачное железо – 0,05 г, пируват натрия – 0,5 г, глицерин – 40,0 г, агар – 15,0 г, гумивит – 90,0-95,0 мл. В качестве яичной основы она содержит сваренный вкрутую желток куриного яйца – 50,0 г и дистиллированную воду до 1000,0 мл. Это обеспечивает сроки появления первичного роста и интенсивность роста, сравнимые с таковыми на традиционно применяемых средах, дешевизну и технологичность приготовления, а ее использование упрощает проведение бактериологических исследований. 7 табл.
Изобретение относится к микробиологическим исследованиям, касается питательной среды для культивирования микобактерий и нокардиоформных актиномицетов и может быть использовано для характеристики микобактерий по их биологической активности. Известны плотные питательные среды для выращивания первичных культур микобактерий, состоящие из яичной массы и солевой основы: Левенштейна-Йенсена, Гельберга, Петраньяни, среды Финн-2 и Мордовского /1/. Приготовленные по прописям яичные среды разливают по пробиркам по 4-5 мл, помещают в аппарат для свертывания или в аппарат Коха в наклонном положении и стерилизуют при 85°С в течение 2 дней по 40 минут или однократно при 90°С в течение 1 часа. Цель изобретения – плотная питательная среда для культивирования микобактерий и нокардиоформных актиномицетов, простая в получении и использовании. Поставленная цель достигается тем, что питательная среда, содержащая солевую основу и яичную основу, содержит в качестве солевой основы L-аспарагин, калий фосфорнокислый двузамещенный, сернокислый магний, лимонную кислоту, лимоннокислое аммиачное железо, пируват натрия, глицерин, агар, гумивит и дистиллированную воду, а в качестве яичной основы сваренный вкрутую желток куриного яйца при следующем соотношении компонентов:
Гумивит – щелочной гидролизат низинных сортов торфа (выпускается ООО Агропром), представляет собой высокодисперсный золь натриевых солей комплекса гумусных кислот – гуминовых, гуматомелановых и фульво-кислот 121. Раствор солей гумусных кислот состоит из длинных фрагментарных цепочек с различными функциональными группами, важнейшими из которых являются карбоксильные (СООН) и фенольные (ОН), способные образовывать хелатные комплексы с микроэлементами, что обеспечивает их высокую обменную емкость и транспорт в клетку микроорганизмов /3, 4/. Гумивит – жидкость от темно-коричневого до черного цвета со специфическим сладковатым запахом, благодаря чему готовая среда имеет интенсивно коричневый цвет, на фоне которого хорошо видны даже мелкие колонии в начальной фазе роста. Сущность способа поясняется примерами. Пример 1. Для приготовления среды в химически чистую стерильную колбу емкостью 2,0 л наливали 300,0 мл дистиллированной воды, прогревали на водяной бане до 75-85°С. В воде растворяли последовательно 2,0 г лимонной кислоты, 4,0 г L-аспарагина, 0,5 г сернокислого магния, 0,5 г двузамещенного фосфорнокислого калия, 0,05 г лимоннокислого аммиачного железа, 0,5 г пирувата натрия, 40,0 г глицерина и 90,0 мл гумивита. Каждый компонент добавляли после полного растворения предыдущего. После внесения всех компонентов общий объем доводили до 750,0 мл стерильной дистиллированной водой. Устанавливали pH=7,1-7,2 добавлением 1 н. NaOH или 1 н. HCl. Свежие куриные яйца хорошо промывали в проточной воде, отваривали вкрутую, извлекали желтки. Расчетное количество сваренного вкрутую желтка (250 г) растирали в ступке в полученном солевом растворе до получения однородной массы, в которую добавляли 15 г агара, перемешивали, доводили объем до 1000 мл и нагревали на водяной бане до расплавления агара. Полученную среду автоклавировали в течение 30 минут при 1 атм. Приготовленную питательную среду хранили в холодильнике при температуре +4°С и использовали по мере надобности, для чего ее расплавляли, разливали по пробиркам и сквашивали. Пример 2. В таблице 1 приведены варианты плотной питательной среды в соответствии с изобретением.
Пример 3. Для определения эффективности плотной питательной среды для культивирования микобактерий использовали референс-штаммы микобактерий M.bovis (шт.Vallee и BCG), M.tuberculosis (шт. Academia) и M.avium (шт. ГИСК, 44, 659). Все штаммы хранились на среде Левенштейна-Йенсена в холодильнике при температуре +4°С. Посевы культур производили нанесением одной капли суспензии микобактерий, содержавшей 30-60КОЕ при посеве на среду Левенштейна-Йенсена, и на все сравниваемые варианты среды в соответствии с изобретением. Посев каждого штамма проводили на 3-5 пробирок. При оценке роста культур учитывали сроки появления первичных колоний, интенсивность роста (± слабый, + средний, ++ обильный) и изучали культурально-морфологические свойства. Контроль – плотная питательная среда Левенштейна-Йенсена. Полученные результаты (таблицы 2 и 3) показали, что оптимальными являются варианты 2 и 3 плотной питательной среды в соответствии с изобретением, обеспечивавшие более ранние сроки появления первичных колоний и более высокую интенсивность роста относительно варианта 1 и сравнимые с таковыми на среде Левенштейна-Йенсена. Повышение количества гумивита (вариант 4 плотной питательной среды в соответствии с изобретением) не сокращало сроки появления роста и не повышало его интенсивность, поэтому было нецелесообразным. Культурально-морфологические свойства и цвет выросших колоний штаммов не отличались от таковых на исходной среде.
Пример 4. Для определения эффективности среды для культивирования нокардиоформных актиномицетов использовали референс-штамм Corynebacterium pseudotuberculosis и четыре штамма родококков, выделенные от свиней и идентифицированные в лабораторных условиях. Все штаммы хранились на среде Левенштейна-Йенсена в холодильнике при температуре +4°С. Посевы культур и учет результатов проводили, как в примере 3. Контроль – традиционно применяемая среда Левенштейна-Иенсена. Результаты представлены в таблицах 4 и 5.
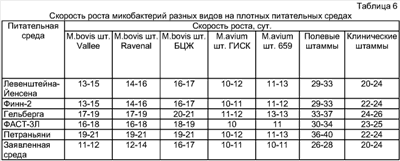
Пример 5. Для сравнительного изучения информативности среды в соответствии с изобретением (вариант 2) и сред Левенштейна-Йенсена, Финн-2, Гельберга, ФАСТ-3Л и Петраньяни использовали референс-штаммы микобактерий M.bovis (шт. Vallee, Ravenal, БЦЖ), М.avium (шт. ГИСК и 659), полевые штаммы, выделенные от положительно реагировавшего на туберкулин крупного рогатого скота неблагополучных по туберкулезу хозяйств с характерными поражениями в органах и лимфатических узлах и клинические штаммы M.tuberculosis, выделенные от больных туберкулезом. Все штаммы хранились на среде Левенштейна-Йенсена в холодильнике при температуре +4°С. Посевы культур производили нанесением одной капли суспензии микобактерий, содержавшей 30-60 КОЕ при посеве на известные среды и на среду в соответствии с изобретением. Посев каждого штамма проводили на 3-5 пробирок. При оценке роста культур учитывали сроки появления первичных колоний и изучали культурально-морфологические свойства. Интенсивность роста изучали при посеве культуры М.bovis (шт.Vallee) на все анализируемые среды. Результаты представлены в таблицах 6 и 7.
Проведенные исследования подтвердили эффективность плотной питательной среды в соответствии с изобретением для культивирования микобактерий и нокардиоформных актиномецитов (сроки появления первичного роста и интенсивность роста сравнимы с таковыми на традиционно применяемых средах). Обратимость среды позволяет использовать ее в качестве наслаиваемого компонента двухслойной питательной среды при изучении биологических свойств микобактерий. Заявляемая плотная питательная среда отличается дешевизной и технологичностью приготовления, а ее использование упрощает проведение бактериологических исследований благодаря визуализации начального роста колоний. Источники информации 1. Васильев В.Н. Микобактериозы и микозы легких. – София, 1971. – С.146-175.
3. Левинский Б.В. Все о гуматах. – Иркутск: ИП Марков С.Е., 1999. – 198 с. Формула изобретения
Плотная питательная среда для культивирования патогенных микобактерий и нокардиоформных актиномицетов, содержащая солевую и яичную основы, отличающаяся тем, что она содержит в качестве солевой основы L-аспарагин, калий фосфорнокислый двузамещенный, сернокислый магний, лимонную кислоту, лимонно-кислое аммиачное железо, пируват натрия, глицерин, агар, гумивит и дистиллированную воду, а в качестве яичной основы – сваренный вкрутую желток куриного яйца при следующем соотношении компонентов:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 3-4. – С.80-82.
3-4. – С.80-82.