|
(21), (22) Заявка: 2006103853/13, 12.07.2004
(24) Дата начала отсчета срока действия патента:
12.07.2004
(30) Конвенционный приоритет:
10.07.2003 US 60/485,717
(43) Дата публикации заявки: 20.08.2007
(46) Опубликовано: 10.12.2009
(56) Список документов, цитированных в отчете о
поиске:
WO 03024481, 27.03.2003. SCHWARZ К. et al. “Role of Toll-like receptors in costimulating cytotoxic Т cell responses”, Eur J Immunol. 2003 Jun; 33(6): 1465-70.
(85) Дата перевода заявки PCT на национальную фазу:
10.02.2006
(86) Заявка PCT:
EP 2004/007679 20040712
(87) Публикация PCT:
WO 2005/004907 20050120
Адрес для переписки:
101000, Москва, М.Златоустинский пер., д.10, кв.15, “ЕВРОМАРКПАТ”, пат.пов. И.А.Веселицкой, рег. 0011 0011
|
(72) Автор(ы):
БАХМАНН Мартин Ф. (CH),
ШВАРЦ Катрин (CH)
(73) Патентообладатель(и):
ЦИТОС БИОТЕХНОЛОГИ АГ (CH)
|
(54) УКОМПЛЕКТОВАННЫЕ ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ
(57) Реферат:
Изобретение относится к области вирусологии, иммунологии и медицины. Композиция содержит антиген, связанный или слитый с вирусоподобной частицей (VLP), укомплектованной иммуностимулирующей нуклеиновой кислотой, содержащей, по крайней мере, одну неметилированную CpG-последовательность и лиганд toll-подобного рецептора (TLR). Раскрыты также вакцинная композиция и способ усиления иммунного ответа у животного. Изобретение может быть использовано для индуцирования сильного антительного и Т-клеточного ответа и, в особенности, полезно для лечения аллергии, опухолей и хронических вирусных заболеваний, а также других хронических заболеваний. 3 н. и 22 з.п. ф-лы, 12 ил., 1 табл.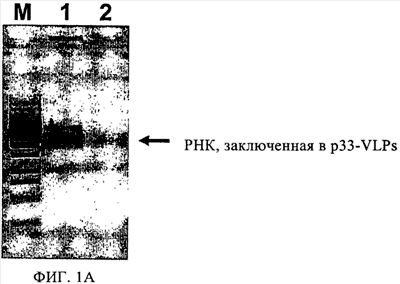
Текст описания приведен в факсимильном виде.                                                                                                    
Формула изобретения
1. Композиция для усиления иммунного ответа у животного, содержащая:
(a) вирусоподобную частицу;
(b) иммуностимулирующую нуклеиновую кислоту,
где указанная иммуностимулирующая нуклеиновая кислота является неметилированным CpG-содержащим олигонуклеотидом и где указанная иммуностимулирующая нуклеиновая кислота (b) упакована в вирусоподобную частицу (а);
(c) по крайней мере один антиген, связанный или смешанный с указанной вирусоподобной частицей (а), и
(d) по крайней мере один лиганд toll-подобного рецептора (TLR), где указанный лиганд TLR выбирают из лиганда TLR4, лиганда TLR7 или лиганда TLR8.
2. Композиция по п.1, в которой указанный лиганд TLR (d) смешан с указанной VLP.
3. Композиция по п.1, в которой указанный лиганд (d) представляет собой лиганд TLR4 и где предпочтительно указанный лиганд (d) выбирают из группы, включающей:
(a) LPS и его производные;
(b) моносфориллипид А и его производные;
(c) синтетический аналог LPS;
(d) gp96 и его производные;
(e) белки теплового шока и
(f) дефензин.
4. Композиция по п.1, в которой указанный лиганд (d) представляет собой лиганд TLR4 и где указанный лиганд (d) представляет собой LPS и его производные.
5. Композиция по п.1, в которой указанный CpG-мотив указанного неметилированного CpG-содержащего олигонуклеотида является частью палиндромной последовательности и где предпочтительно указанная палиндромная последовательность представляет собой последовательность GACGATCGTC (SEQ ID NO:39).
6. Композиция по п.5, в которой указанный неметилированный CpG-содержащий олигонуклеотид содержит или, альтернативно, по существу, состоит или альтернативно состоит из последовательности GGGGGGGGGGGACGATCGTCGGGGGGGGGG (SEQ ID NO:54).
7. Композиция по п.5, в которой указанная палиндромная последовательность фланкирована на своем 5′-концевом участке по крайней мере и максимально 9 гуанозиновыми остатками, причем такая палиндромная последовательность фланкирована на своем 3′-концевом участке по крайней мере 6 и максимально 9 гуанозиновыми остатками, где предпочтительно указанный неметилированный CpG-содержащий олигонуклеотид имеет нуклеотидную последовательность, выбранную из группы, включающей
(a) GGGGACGATCGTCGGGGGG (SEQ ID NO:40);
(b) GGGGGGACGATCGTCGGGGGG (SEQ ID NO:41);
(c) GGGGGGACGATCGTCGGGGGG (SEQ ID NO:42);
(d) GGGGGGGACGATCGTCGGGGGG (SEQ ID NO:43);
(e) GGGGGGGACGATCGTCGGGGGGG (SEQ ID NO:44);
(f) GGGGGGGGGACGATCGTCGGGGGGGG (SEQ ID NO:45);
(g) GGGGGGGGGGACGATCGTCGGGGGGGGG (SEQ ID NO:46);
(h) GGGGGGCGACGACGATCGTCGTCGGGGGGG (SEQ ID NO:47).
8. Композиция по п.1, где указанный неметилированный CpG-содержащий олигонуклеотид не стабилизирован за счет фосфоротиоатных модификаций фосфодиэфирного остова.
9. Композиция по п.1, в которой указанный лиганд (d) представляет собой лиганд TLR 7 и 8.
10. Композиция по п.9, где указанный лиганд TLR 7 и TLR 8 является имидазохинолином.
11. Композиция по п.1, в которой указанная вирусоподобная частица содержит по крайней мере один первый сайт прикрепления, а указанный антиген (с) также содержит по крайней мере один второй сайт прикрепления, выбранный из группы, включающей:
(a) сайт прикрепления антигена или антигенной детерминанты, не существующий в природе;
(b) сайт прикрепления антигена или антигенной детерминанты, существующий в природе, причем указанный второй сайт прикрепления способен к ассоциации с указанным первым сайтом прикрепления.
12. Композиция по п.11, дополнительно содержащая аминокислотный линкер, причем указанный аминокислотный линкер содержит или, альтернативно, состоит из указанного второго сайта прикрепления.
13. Композиция по п.1, в которой указанная вирусоподобная частица содержит или, альтернативно, по существу, состоит из рекомбинантных белков РНК-бактериофагов или фрагментов данных белков, причем предпочтительно указанный РНК-бактериофаг выбран из группы, включающей
(a) бактериофаг Q ; ;
(b) бактериофаг R17;
(c) бактериофаг fr;
(d) бактериофаг GA;
(e) бактериофаг SP;
(f) бактериофаг MS2;
(g) бактериофаг M11;
(h) бактериофаг МХ1;
(i) бактериофаг NL95;
(j) бактериофаг f2;
(k) бактериофаг РР7 и
(1) бактериофаг АР205.
14. Композиция по п.13, в которой указанная вирусоподобная частица содержит рекомбинантные белки РНК-бактериофагов или фрагменты данных белков, причем указанный РНК-бактериофаг представляет собой бактериофаг Q или бактериофаг АР205. или бактериофаг АР205.
15. Композиция по п.1, где указанная вирусоподобная частица включает протеин SEQ ID NO:1.
16. Композиция по п.1, в которой указанный антиген (с) выбран из группы, включающей:
(a) полипептиды;
(b) липопротеины и
(c) гликопротеины.
17. Композиция по п.1, в которой указанный антиген (с) получен из природного источника, выбранного из группы, включающей
(a) экстракт пыльцы;
(b) экстракт пыли;
(c) экстракт пылевых клещей;
(d) экстракт грибов;
(e) экстракт эпидермиса млекопитающих;
(f) экстракт перьев;
(g) экстракт насекомых;
(h) экстракт пищевых продуктов;
(i) экстракт волос;
(j) экстракт слюны и
(k) экстракт сыворотки.
18. Композиция по п.1, в которой указанный антиген (с) получен из источника, выбранного из группы, включающей
(a) вирусы;
(b) бактерии;
(c) паразитические простейшие;
(d) прионы;
(e) опухоли;
(f) аутоантигены;
(g) непептидные молекулы гаптенов;
(h) аллергены и
(i) гормоны.
19. Композиция по п.1, в которой указанный антиген (с) представляет собой опухолевый антиген, предпочтительно выбранный из группы, включающей
(а) Неr2;
(b) GD2;
(c)EGF-R;
(d) СЕА;
(e) CD52;
(f) белок gp100 меланомы человека;
(g) белок melan-A/MART-1 меланомы человека;
(h) тирозиназу;
(i) белок NA17-A nt;
(о) белок MAGE-3;
(k) белок р53;
(l) белок HPV16 E7;
(m) аналог любого из антигенов (а)-(l) и
(n) фрагмент любого из опухолевых антигенов (а)-(m).
20. Композиция по п.1, в которой указанный антиген (с) представляет собой аллерген, полученный из источника, выбранного из группы, включающей:
(a) экстракт пыльцы;
(b) экстракт пыли;
(c) экстракт пылевых клещей;
(d) экстракт грибов;
(e) экстракт эпидермиса млекопитающих;
(f) экстракт перьев;
(g) экстракт насекомых;
(h) экстракт пищевых продуктов;
(i) экстракт волос;
(j) экстракт слюны и
(k) экстракт сыворотки.
21. Композиция по п.1, в которой указанный антиген (с) представляет собой аллерген, полученный из источника, выбранного из группы, включающей
(a) деревья;
(b) травы;
(c) домашнюю пыль;
(d) домашних пылевых клещей;
(e) Aspergillus;
(f) волосы животных;
(g) перья животных;
(h) яд пчелы;
(i) животные продукты и
(j) растительные продукты.
22. Композиция по п.1, в которой указанный антиген (с) выбран из группы включающей
(a) фосфолипазу А2 яда пчелы;
(b) Amb a1 (антиген пыльцы амброзии);
(c) Bet v1 (антиген пыльцы березы);
(d) 5 Dol m V (антиген осы пятнистой);
(e) Der p 1 (антиген домашних пылевых клещей);
(f) Der f 2 (антиген домашних пылевых клещей);
(g) Der 2 (антиген домашних пылевых клещей);
(h) Lep d (антиген пылевых клещей);
(i) Alt a 1 (аллерген грибов);
(j) Asp f 1 (аллерген грибов);
(к) Asp f 16 (аллерген грибов) и
(l) аллергены арахиса.
23. Композиция по п.1, в которой указанный антиген (с) представляет собой эпитоп цитотоксических Т-клеток, эпитоп Th-клеток или комбинацию по крайней мере двух указанных эпитопов, причем по крайней мере два эпитопа связаны непосредственно между собой или посредством линкерной последовательности.
24. Способ усиления иммунного ответа у животного, включающий введение животному композиции по любому из пп.1-23.
25. Вакцинная композиция для усиления иммунного ответа у животных, содержащая иммунологически эффективное количество композиции по любому из пп.1-23 вместе с иммунологически приемлемым разбавителем, носителем или наполнителем.
РИСУНКИ
|