|
|
(21), (22) Заявка: 2006129281/04, 12.01.2005
(24) Дата начала отсчета срока действия патента:
12.01.2005
(30) Конвенционный приоритет:
13.01.2004 JP 2004-005586
(43) Дата публикации заявки: 20.02.2008
(46) Опубликовано: 20.11.2009
(56) Список документов, цитированных в отчете о
поиске:
US 2002090515, 11.07.2002. JP 2000169481 A1, 20.06.2000. RU 2060985 A, 27.05.1996. US 9676603 A, 24.08.1976. EP 842980 A, 20.05.1998. US 5508380 A, 16.04.1996. JP 2001208736 A,03.08.2001. RU 2073664 A, 10.10.1991.
(85) Дата перевода заявки PCT на национальную фазу:
14.08.2006
(86) Заявка PCT:
JP 2005/000256 20050112
(87) Публикация PCT:
WO 2005/068534 20050728
Адрес для переписки:
129090, Москва, ул. Б.Спасская, 25, стр.3, ООО “Юридическая фирма Городисский и Партнеры”, пат.пов. Е.Е.Назиной
|
(72) Автор(ы):
СИРАКАВА Дайсуке (JP),
ОХАРУ Казуя (JP),
ОКАЗОЕ Такаси (JP)
(73) Патентообладатель(и):
АСАХИ ГЛАСС КОМПАНИ, ЛИМИТЕД (JP)
|
(54) ФТОРПОЛИЭФИРНОЕ СОЕДИНЕНИЕ
(57) Реферат:
Изобретение относится к фторполиэфирному соединению, применяемому, например, в качестве модификатора поверхности или другого средства для покрытия поверхности. Фторполиэфирное соединение, представленное формулой (X-)xY(-Z)z, где Х является группой, представленной формулой HO-(CH2CH2O)a·(CH2CH(OH)CH2O)b-(CH2)c-CF2O
(CF2CF2O)d- (где “а” является целым числом от 0 до 100, b является целым числом от 0 до 100, с является целым числом от 1 до 100 и d является целым числом от 1 до 200). При этом Z является группой, представленной формулой RFO(CF2CF2O)g- (где RF является С1-20 перфторалкильной группой, имеющей эфирный атом кислорода, расположенный между атомами углерод-углерод, и g является целым числом от 3 до 200). При этом Y является, например, (x+z) валентной перфторированной насыщенной углеводородной группой, где x является целым числом, равным, по меньшей мере, 2, a z является целым числом, равным, по меньшей мере, 0, и (x+z) является целым числом, равным 3 или 4. Фторполиэфирное соединение имеет низкое давление пара и низкую вязкость и не имеет проблем ухудшения свойств при его применении. 3 н. и 5 з.п. ф-лы.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к новому фторполиэфирному соединению, применяемому, например, в качестве смазки, модификатора поверхности или поверхностно-активного вещества.
УРОВЕНЬ ТЕХНИКИ
Перфторированные полиэфирные соединения широко применяются, например, в качестве смазки, модификатора поверхности или поверхностно-активного вещества. Например, в качестве соединения с конечной группой, превращаемой в -CH2OH, известно соединение (например, Непатентный документ 1), представленное следующей формулой (I) (где каждый h и i являются целым числом, равным, по меньшей мере, 1):
HO-CH2CF2О-(CF2CF2О)h-(CF2О)i-CF2CH2OH (I)
Из этого документа известно, что поверхность, имеющая покровную пленку, образованную в результате нанесения соединения (I) на поверхность основы, имеет такое свойство (способность самообновления), что когда часть покровной пленки повреждается, соединение (I) покрывает поврежденное место, обновляя поврежденную поверхность. Кроме того, известно, что к такой способности самообновления имеет отношение -CH2OH группа, присутствующая на конце молекулы соединения (I).
Так как перфторированное полиэфирное соединение, такое как соединение (I), может применяться в условии высокой температуры, желательно, чтобы соединение имело низкое давление пара. Для достижения низкого давления пара была сделана попытка увеличить молекулярную массу соединения, но при увеличении молекулярной массы соединения (I) значительно возрастает вязкость, что затрудняет применение этого соединения. Кроме того, существует проблема в том, что при увеличении молекулярной массы становится низкой доля -CH2OH групп на единицу объема, в результате чего снижается способность самообновления.
Для решения таких проблем было предложено соединение, представленное следующей формулой (II) (в следующей формуле каждое h и i являются целым числом, равным, по меньшей мере, 1), но оно также имело недостаток из-за высокой вязкости:
HO-CH2CH(OH)CF2О-(CF2CF2О)h-(CF2О)i-CF2CH(OH)CH2-ОH (II)
Кроме того, для соединения (I) и соединения (II) характерно присутствие в их молекулярной структуре -OCF2О- фрагмента. Этот фрагмент вызывает реакцию разложения соединения и, поэтому, у соединения, содержащего такой фрагмент, при его использовании ухудшаются свойства (например, Непатентные документы 2, 3 и 4).
В качестве перфторированного полиэфирного соединения, не содержащего -OCF2О- фрагмента, сообщалось о соединении, в котором концевыми являются -COOH группы (например, Непатентный документ 5). Однако в таком соединении, в котором концевыми являются -COOH группы, при выдержке в условиях высокой температуры, в концевых -COOH группах происходит отщепление CО2, в результате чего полярные концевые группы утрачиваются, и способность самообновления снижается. Кроме того, соединение с -COOH имеет недостаток из-за высокой кислотности -COOH групп, что вызывает коррозию.
Непатентный документ 1: C. Tonelli et al., J. Fluorine Chem., Vol.95, 1999, p.51-70
Непатентный документ 2: W. Fong et al. “IEEE Transactions on Magnetics”, vol.35, No.2, March 1999, p.911-912.
Непатентный документ 3: J. Scheirs, “Modern Fluoropolymers”, John Wiley & Sons Ltd., 1997, p.466-468.
Непатентный документ 4: P.H. Kasai, “Macromolecules”, Vol.25, 1992, p.6791.
Непатентный документ 5: Kyle W. Fellling et al., J. Fluorine Chem., Vol.125, 2004, p.749-754.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЦЕЛЬ, ДОСТИГАЕМАЯ ИЗОБРЕТЕНИЕМ
Настоящее изобретение было создано для решения вышеназванных проблем, и целью настоящего изобретения является разработка нового фторполиэфирного соединения, обладающего низким давлением пара и низкой вязкостью при высокой химической стабильности и не имеющего проблем ухудшения свойств при его применении. Кроме того, целью настоящего изобретения является разработка фторполиэфирного соединения с высокой способностью самообновления и применяемого, например, в качестве смазки или вещества для покрытия, и жидкой композиции в органическом растворителе, содержащей это соединение.
СРЕДСТВА ДОСТИЖЕНИЯ ЦЕЛИ
Настоящее изобретение предлагает следующее:
1. Фторполиэфирное соединение, представленное следующей формулой (A):
где символы имеют следующие значения:
X: группа, представленная следующей формулой (X) (где “a” является целым числом от 0 до 100, b является целым числом от 0 до 100, c является целым числом от 1 до 100 и d является целым числом от 1 до 200):
HO-(CH2CH2О)a·(CH2CH(OH)CH2О)b-(CH2)c-CF2О(CF2CF2О)d– (X)
Z: группа, представленная следующей формулой (Z) (где RF является C1-20 перфторалкильной группой или группой, имеющей эфирный атом кислорода, расположенный между атомами углерод-углерод, такой как перфторалкильная группа (группа не имеет -ОCF2О- структуры), и g является целым числом от 3 до 200):
RFО(CF2CF2О)g– (Z)
Y: (x+z) валентная перфторированная насыщенная углеводородная группа, или
(x+z) валентная перфторированная насыщенная углеводородная группа, имеющая эфирный атом кислорода, расположенный между атомами углерод-углерод, не имеющая -ОCF2О- структуры;
x, z: x является целым числом, равным, по меньшей мере, 2, z является целым числом, равным, по меньшей мере, 0, и (x+z) является целым числом от 3 до 20 при условии, что когда x равен, по меньшей мере, 2, группы, представленные формулой (X), могут быть одинаковыми или различными, и когда z равно, по меньшей мере, 2, группы, представленные формулой (Z), могут быть одинаковыми или различными.
2. Соединение по п.1, где группа, представленная формулой (X), является любой группой, выбранной из групп, представленных следующими формулами от (X-1) до (X-4), при условии, что d уже определено выше:
HOCH2CF2О(CF2CF2О)d–
HОCH2CH(OH)CH2OCH2CF2О(CF2CF2О)d–
HOCH2CH2CF2О(CF2CF2О)d–
HOCH2CH2OCH2CF2О(CF2CF2О)d– |
(X-1)
(X-2)
(X-3)
(X-4) |
3. Соединение по п.2, где соединение, представленное формулой (A), является соединением, представленным следующими формулами (A-1) или (A-2), при условии что X10 является любой группой, выбранной из групп, представленных следующими формулами от (X-1) до
(X-4), Y3 является перфторалкантриильной группой и Y4 является перфторалкантетраильной группой:
(X10-)3Y3
(X10-)4Y4 |
(A-1)
(A-2) |
4. Соединение по п.2, где соединение, представленное формулой (A), является соединением, представленным следующей формулой (A-3), при условии что X10 является любой группой, выбранной из групп, представленных следующими формулами от (X-1) до (X-4), Y3 является перфторалкантриильной группой и Z уже определено выше:
(X10-)2Y3-Z (A-3)
5. Фторполиэфирное соединение по любому из пп.1-4, где соединение, представленное формулой (A), имеет молекулярную массу от 500 до 1000000, измеренную с помощью гельпроникающей хроматографии, и имеет распределение молекулярной массы от 1,0 до 1,5.
6. Жидкая композиция, содержащая фторполиэфирное соединение по любому из пп. 1-5, и органический растворитель.
7. Жидкая композиция по п.6, где концентрация фторполиэфирного соединения составляет от 0,01 до 50 мас.%.
8. Смазка, модификатор поверхности или поверхностно-активное вещество, которое содержит фторполиэфирное соединение по любому из пп.1-5, в качестве основной составной части.
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
По настоящему изобретению предлагается новое фторполиэфирное соединение, применяемое, например, в качестве смазки, модификатора поверхности или поверхностно-активного вещества. Фторполиэфирное соединение имеет низкое давление пара и низкую вязкость и имеет меньше недостатков с точки зрения ухудшения его свойств при применении. Кроме того, фторполиэфирное соединение настоящего изобретения обладает высокой способностью самообновления.
ПРЕДПОЧТИТЕЛЬНЫЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В этом описании фторполиэфирное соединение, представленное формулой (A), называют соединением (A). Кроме того, группу, представленную формулой (X), называют группой (X). Что касается других формул, они будут названы аналогичным способом.
Настоящее изобретение предлагает следующее соединение (A). Соединение (A) настоящего изобретения не имеет -OCF2О- структуры:
В соединении (A) X является одновалентной группой, представленной следующей формулой (X):
| HO-(CH2CH2О)a·(CH2CH(OH)CH2О)b-(CH2)cCF2-О(CF2CF2О)d– |
(X) |
Здесь “a” обозначает число -(CH2CH2О)- фрагментов и является целым числом, равным от 0 до 100, предпочтительно, целым числом, равным от 0 до 10, особенно предпочтительно от 0 до 2, наиболее предпочтительно от 0 до 1.
b обозначает число -(CH2CH(OH)CH2О)- фрагментов и является целым числом, равным от 0 до 100, предпочтительно, целым числом, равным от 0 до 10, особенно предпочтительно от 0 до 2, наиболее предпочтительно от 0 до 1.
Что касается комбинации “a” и b, то предпочтительными являются случаи, когда и “a” и b равны 0, случай когда “a” равно 0 и b, по меньшей мере, равно 1 (предпочтительно b равно 1), или случай, когда “a”, по меньшей мере, равно 1 (предпочтительно “a” равно 1) и b равно 0.
c обозначает число -(CH2)- фрагментов и является целым числом, равным от 1 до 100, предпочтительно целым числом, равным от 1 до 10, особо предпочтительно 1 или 2. В случае когда c, по меньшей мере, равно 2, с точки зрения эффективности производства предпочтительно, чтобы c являлось четным числом.
d обозначает число -(CF2CF2О)- фрагментов и является целым числом, равным от 1 до 200, предпочтительно целым числом, равным от 3 до 100, особенно предпочтительно целым числом, равным от 3 до 200, более предпочтительно целым числом, равным от 3 до 70, и еще более предпочтительно целым числом, равным от 5 до 50. Любое значение a, b и c, равное 0, означает, что такой фрагмент в группе не присутствует.
В формуле (X) предпочтительной является группа (X), где “a” равно 0, b равно 0, c равно 1 и d равно от 3 до 200, или группа (X), где одно из “a” и b, по крайней мере, равно 1, а другое равно 0, c равно 1 и d равно от 3 до 200.
Обозначение “-(CH2CH2О)a·(CH2CH(OH)CH2О)b-” части в формуле (X) означает, что когда присутствуют, по меньшей мере, по одному фрагменту каждого -(CH2CH2)О- фрагмента и -(CH2CH(OH)CH2О)- фрагмента, их расположение специально не ограничивается. А именно, в случае когда присутствуют по одному фрагменту каждого -(CH2CH2О)- фрагмента и -(CH2CH(OH)CH2О)- фрагмента, фрагментом, который связан с гидроксильной группой, может быть -(CH2CH2О)- фрагмент или -(CH2CH(OH)CH2О)- фрагмент.
Кроме того, в случае когда присутствуют оба, и -(CH2CH2О)- фрагмент, и -(CH2CH(OH)CH2О)- фрагмент, и, по меньшей мере, один из фрагментов присутствует во множественном числе, то есть, по меньшей мере, в количестве двух фрагментов, расположение таких фрагментов может быть поблочное или неупорядоченное, предпочтительно поблочное, более предпочтительно поблочное в порядке соответствующих фрагментов, как указано в формуле (X) от концевой гидроксильной группы.
Следующие примеры могут быть приведены для группы (X) при условии, что d уже определено выше:
HOCH2CF2О(CF2CF2О)d–
HOCH2CH(OH)CH2OCH2CF2О(CF2CF2О)d–
HOCH2CH2CF2О(CF2CF2О)d–
HOCH2CH2OCH2CF2О(CF2CF2О)d– |
(X-1)
(X-2)
(X-3)
(X-4) |
Среди них предпочтительно, чтобы, с точки зрения эффективности производства, меньшей склонности к разложению и высокой стабильности, группой (X) являлась группа (X-1) или (X-2).
В формуле (A) Z является одновалентной группой следующей формулы (Z):
Здесь, RF является C1-20 перфторалкильной группой или группой, имеющей эфирный атом кислорода, расположенный между атомами углерод-углерод такой перфторалкильной группы (при условии, что группа не имеет -OCF2О- фрагмент). Структура RF может быть линейной, разветвленной, циклической или структурой, имеющей как часть циклическую структуру, предпочтительно линейной структурой или разветвленной структурой, более предпочтительно линейной структурой. Предпочтительно, чтобы RF имел от 1 до 20, особенно предпочтительно от 1 до 16 углеродных атомов.
Следующие группы могут быть приведены в качестве конкретных примеров для RF, и предпочтительной является группа (RF1). В следующих формулах s является целым числом от 0 до 15, Cy F является перфторциклогексильной группой, t является целым числом от 0 до 15, Ad F является перфторциклогексильной группой, t является целым числом от 0 до 15, Ad F является перфторированной адамантильной группой и t является целым числом от 0 до 15: F является перфторированной адамантильной группой и t является целым числом от 0 до 15:
CF3(CF2)S-(RF1)
Cy F – (CF2)t– F – (CF2)t–
Ad F – (CF2)t– F – (CF2)t–
g является числом -(CF2CF2О)- фрагментов и является целым числом от 3 до 200, предпочтительно целым числом от 3 до 100, более предпочтительно целым числом от 3 до 70, особенно предпочтительно целым числом от 5 до 50.
Следующие примеры могут быть приведены в качестве группы (Z):
CF3-О-(CF2CF2О)g–
CF3(CF2)2-О-(CF2CF2О)g–
CF3(CF2)5-О-(CF2CF2О)g– |
(Z-1)
(Z-2)
(Z-3) |
Соединение (A) является соединением, имеющим x одновалентных групп (X) и z одновалентных групп (Y), связанных с Y, и Y является (x+z)-валентной группой.
(x+z), которая является валентностью Y, является целым числом, равным, по меньшей мере, 3, предпочтительно целым числом от 3 до 20, особенно предпочтительно целым числом от 3 до 10. Значение (x+z) удобно корректировать в зависимости от целей применения соединений (A), и в случае когда соединение (A) применяют в качестве смазки, как описано в дальнейшем, предпочтительно, чтобы
(x+z) являлась целым числом от 3 до 10, особенно предпочтительно 3 или 4, более предпочтительно 3. Соединение, в котором валентность Y равна 3 или 4 (особенно 3), легко получать, оно имеет подходящую температуру кипения и обладает высокой способностью самообновления.
(x), соответствуя числу групп (X), является целым числом, равным, по меньшей мере, 2, предпочтительно целым числом от 3 до 20, особенно предпочтительно целым числом от 3 до 10, особенно предпочтительно 3 или 4. (z), соответствуя числу групп (Z), является целым числом, равным, по меньшей мере, 0, z предпочтительно является целым числом от 0 до 17, особенно предпочтительно целым числом от 0 до 7, особенно предпочтительно 0 (то есть группа (Z) не присутствует) или 1. В случае когда x равен, по меньшей мере, 2, группы (X) могут быть одинаковыми или различными, и в случае когда z равно, по меньшей мере, 2, группы (Z) могут быть одинаковыми или различными.
Y имеет предпочтительно от 1 до 50, особенно предпочтительно от 1 до 20, особенно предпочтительно от 3 до 5 углеродных атомов. В случае когда Y является (x+z)-валентной перфторированной насыщенной углеводородной группой, группа является (x+z)-валентной насыщенной группой, состоящей только из углеродных атомов и атомов фтора. В случае когда Y является группой, содержащей эфирный атом кислорода, число эфирных атомов кислорода составляет 1 или более, предпочтительно от 1 до 3. Так как эфирный атом кислорода расположен между атомами углерод-углерод, атом эфирного кислорода не присутствует в концевых фрагментах Y, связанных с X и Z. Кроме того, так как соединение (A) не имеет -OCF2О- структуры, Y не имеет -OCF2О- структуры. Кроме того, атом эфирного кислорода в Y не связан с атомом углерода на связанном конце. Предпочтительно, чтобы Y был (x+z)-валентной перфторированной насыщенной углеводородной группой, не содержащей атом эфирного кислорода. Особенно предпочтительно, чтобы трехвалентной группой (Y) была перфторалкантриильная группа, и особенно предпочтительно, чтобы четырехвалентной группой (Y) была перфторалкантетраильная группа. Такие группы, имеющие от 1 до 20 углеродных атомов, являются особенно предпочтительными, и такие группы, имеющие от 3 до 5 углеродных атомов, являются более предпочтительными.
Соединение (A), в котором Z не присутствует и группа (Y) является трехвалентной группой (Y3), предпочтительным является следующее соединение (A-1). В следующей формуле X10 является любой группой, выбранной из групп от (X-1) до (X-4), и Y3 является перфторалкантриильной группой:
Предпочтительно, чтобы соединение (A-1) было следующими соединениям, в которых X10 является группой (X-1) или (X-2):
(HOCH2CF2О(CF2CF2О)d-)3Y3
(HOCH2CH(OH)CH2OCH2CF2О(CF2CF2О)d-)3Y3 |
(A-11)
(A-12) |
Соединение (A), в котором не присутствует Z и группа (Y) является четырехвалентной группой (Y4), предпочтительным является следующее соединение (A-2). В следующей формуле X10 является любой группой, выбранной из групп от (X-1) до (X-4), и Y4 является перфторалкантетраильной группой:
Предпочтительно, чтобы соединение (A-2) являлось следующим соединением (A-21) или (A-22), в котором X10 является группой (X-1) или (X-2):
(HOCH2CF2О(CF2CF2О)d-)4Y4
(HOCH2CH(OH)CH2OCH2CF2О(CF2CF2О)d-)4Y4 |
(A-21)
(A-22) |
В случае когда Z присутствует, предпочтительным является следующее соединение (A-3), в котором группа (Y) является трехвалентной группой (Y3). В следующей формуле X10 является любой группой, выбранной из групп, представленных формулами от (X-1) до (X-4), Y3 является перфторалкантриильной группой и Z является группой, представленной формулой (Z):
Предпочтительно, чтобы соединение (A-3) было следующим соединением (A-31) или (A-32), в котором X10 является группой (X-1) или (X-2):
(HOCH2CF2О(CF2CF2О)d-)2Y3-Z
(HOCH2CH(OH)CH2OCH2CF2О(CF2CF2О)d-)2Y3-Z |
(A-31)
(A-32) |
В вышеприведенных формулах в качестве Y3 (перфторалкантриильной группы) могут быть приведены следующие группы:

В качестве Y4 (перфторалкантетраильной группы) может быть приведена следующая группа:
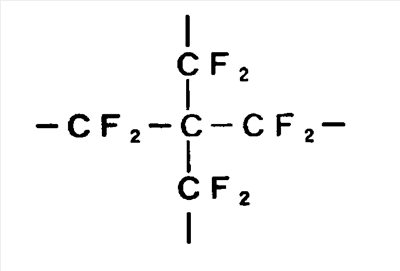
Примеры группы (Y), отличающиеся от указанных выше, приведены в примерах для соединения (A).
Соединение (A) может быть представлено в качестве единственного соединения или комбинации, по меньшей мере, двух типов соединений. В качестве примера последней, может быть упомянута композиция, содержащая два или более соединений, отличающихся в группе (X) и/или группе (Z), присутствующих в соединении (A).
В случае когда соединение (A) является композицией, содержащей два или более различных типов соединения (A), предпочтительно, чтобы среднее значение “a” в группе (X) составляло положительное число от 0 до 2, особенно предпочтительно 0. Предпочтительно, чтобы среднее значение b составляло положительное число от 0 до 2. Предпочтительно, чтобы среднее значение c составляло 1. Предпочтительно, чтобы среднее значение d составляло положительное число от 3 до 100. Предпочтительно, чтобы среднее значение g составляло положительное число от 3 до 100.
Предпочтительно, чтобы молекулярная масса соединения (A) составляла от 500 до 100000, более предпочтительно – от 1000 до 20000. Более того, в случае когда соединение (A) является смесью, по меньшей мере, двух типов соединения, предпочтительно, чтобы распределение молекулярной массы (Mw/Mn) соединения (A) составляло предпочтительно от 1,0 до 1,5, более предпочтительно от 1,0 до 1,25. Когда молекулярная масса и распределение молекулярной массы находятся внутри вышеуказанных интервалов, будут достигаться такие преимущества, как низкая вязкость, небольшое количество испаряющихся компонентов и однородность при растворении в растворителе. Молекулярная масса и распределение молекулярной массы соединения (A) могут быть измерены гельпроникающей хроматографией, и что касается условий измерений, то могут быть использованы условия, описанные в примерах, приведенных далее.
Следующие соединения могут быть приведены в качестве конкретных примеров соединения (A) в настоящем изобретении. Здесь, в следующих формулах, X и Z определены выше, и k является целым числом от 1 до 10 при условии, что в случае когда два или более k присутствуют в одной и той же молекуле, они могут быть одинаковыми или отличаться друг от друга:
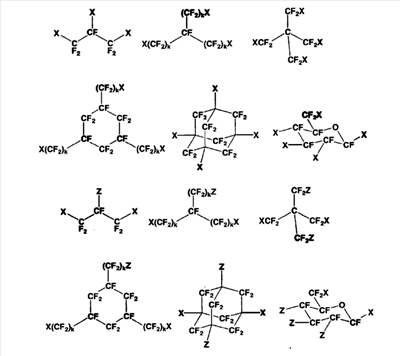
В соединении (A) настоящего изобретения фрагмент, представленный -(OCF2О)-, не присутствует. Соединение, не имеющее -(OCF2О)- фрагмент, является таким соединением, в котором фрагмент не может быть определен обычным аналитическим методом (таким как 19F-ЯМР).
Соединение (A) настоящего изобретения может быть получено способом, аналогичным способу, раскрытому в WO02/4397 авторами настоящего изобретения, или подобным способом из гидрополиэтиленгликоля, имеющего углеродный скелет, соответствующий соединению (A). Что касается гидрополиэтиленгликоля, который может быть использован в качестве сырья, то гидрополиэтиленгликоли различного строения и с различными молекулярными массами коммерчески легко доступны и недороги. В противном случае, он может быть легко синтезирован путем добавления окиси этилена к многоатомному спирту.
В частности, соединение формулы (A), в котором c равно 1, может быть получено следующим способом.
Здесь, в следующих формулах символы уже определены выше. YH является такой же группой, как Y, или группой, имеющей несколько или все атомы фтора в Y, замещенные атомами водорода. R является такой же группой, как RF, или группой, имеющей несколько или все атомы фтора в RF, замещенные атомами водорода, предпочтительно такой же группой, как RF. Rb является одновалентной фторированной органической группой, предпочтительно перфторалкильной группой или перфторалкильной группой, содержащей атом эфирного кислорода (группа не имеет -OCF2О- фрагмента). RbF является одновалентной перфторированной органической группой, предпочтительно такой же перфторалкильной группой, как Rb, или такой же перфторалкильной группой, содержащей атом эфирного кислорода, как Rb. Rc является алкильной группой. X1 является атомом хлора или атомом фтора.
А именно, следующее соединение (D1) взаимодействует со следующим соединением (D2) с получением следующего соединения (D3), и соединение (D3) перфторируют с получением следующего соединения (D4). В соединении (D4), эфирную связь подвергают реакции разложения с получением следующего соединения (D5). Затем, соединение (D5) взаимодействует со следующим соединением (D6) с получением следующего соединения (D7) или соединение (D5) гидролизуют с получением следующего соединения (D8). Затем, соединение (D7) подвергают восстановлению и реакции разложения эфирной связи или соединение (D8) восстанавливают с получением следующего соединения (A-4). В противном случае соединение (D7) может также быть получено путем проведения реакции эфирного обмена между соединением (D4) и соединением формулы Rc-OH (где Rc уже определено выше). Таким соединением (A-4) является соединение формулы (A), где c равно 1 и каждое “a” и b равно 0.
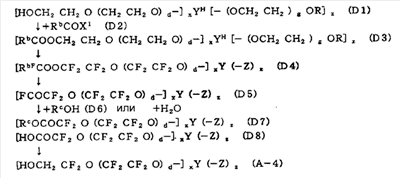
Следующее соединение (A-5), которое соответствует соединению (A), в котором c равно, по меньшей мере, 2, и каждое “a” и b равно 0, может быть получено следующим способом. А именно, соединение (D5) в вышеуказанном способе взаимодействует с йодом (I2) или LiI для превращения концевой -COF группы в -I (атом йода), в результате получая соединение (D9). Затем, выбираемое мольное количество этилена взаимодействует по реакции присоединения с соединением (D9) с получением соединения (D10). Затем, концевой атом йода в соединении (D10) подвергают реакции модификации спирта с помощью дымящей серной кислоты или бетаина с получением соединения (A-5).
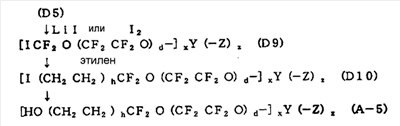
Соединение (A), где “a” равно, по меньшей мере, 1, может быть получено путем добавления этиленкарбоната и/или окиси этилена к соединению (A-4) или соединению (A-5), полученным вышеупомянутым методом. Кроме того, соединение (1), где b равно, по меньшей мере, 1, может быть получено добавлением глицидилового спирта к соединению (A-4) или соединению (A-5).
Реакция присоединения этиленкарбоната и/или окиси этилена может быть проведена в соответствии с известными способами и условиями. Здесь, в случае когда содержание фтора в соединении (A-4) или соединении (A-5) является высоким, совместимость с этиленкарбонатом и/или окисью этилена, которые используют для реакции присоединения, является низкой, в силу чего реакционная система для реакции присоединения может подвергаться фазовому расслоению на две фазы. Если такое фазовое расслоение происходит, время реакции будет продолжительным, что неэффективно, и предпочтительно проводить реакцию при добавлении растворителя для повышения совместимости в реакционной системе. В качестве такого растворителя может применяться гидрофторуглерод (HCFC).
В качестве соединения (D1), являющегося сырьем для способа получения, обычно легко доступно соединение, которое является смесью, по меньшей мере, двух типов, отличающихся по числу -(CH2CH2О)- фрагментов. В случае когда вышеуказанный способ получения проводят с использованием соединения (D1) в виде такой смеси, образующееся соединение (A) будет также представлять собою смесь.
Соответствующие реакционные стадии способа получения соединения (A) могут быть проведены в соответствии со способами и условиями для известных реакций (например, способ, раскрытый в патентной заявке WO02/4397). Кроме того, реакционные стадии от соединения (D5) до соединения (D7) и соединения (D8) могут также быть проведены в соответствии с известными способами. Например, стадия восстановления при получении соединения (D7) и соединения (D8) может быть проведена в соответствии со способом, раскрытым, например, в JP-A-10-72568 (paragraph 0021). Такую стадию восстановления предпочтительно проводить с использованием восстановителя, такого как NaBH4, боргидрид-ТГФ или литийалюминийгидрида.
Продукт, содержащий соединение (A), полученный вышеприведенным способом, в зависимости от конкретной цели обычно предпочтительно подвергать очистке для получения соединения (A) высокой чистоты, после чего его применяют соответствующим образом.
Предпочтительно очисткой удалять примеси металлов, примеси анионов и побочные продукты реакции (такие как побочные продукты, отличающиеся числом гидроксильных групп), содержащиеся в продукте. В качестве способов очистки могут быть упомянуты известный способ удаления, например, примесей металлов и примесей анионов, абсорбирующим ионы полимером или способом суперкритической экстракции.
Кроме того, с промышленной точки зрения выгодно применять для очистки колоночную хроматографию для очистки, так как в результате, например, могут быть эффективно удалены побочные продукты. Неподвижной фазой в колоночной хроматографии может, например, быть силикагель, активированный оксид алюминия, оксид магния, силикат алюминия или силикат магния (такой как торговой марки Forisil,), и предпочтительной является фаза, имеющая средний размер диаметра пор менее чем 200 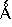 . В качестве подвижной фазы может быть использован обычный неполярный растворитель или полярный растворитель, и, в случае необходимости, предпочтительно изменять полярность путем изменения соотношения таких растворителей. Кроме того, соединение (A) настоящего изобретения является фторированным соединением и обычно обладает отличной растворимостью во фторированном растворителе, но фторированный растворитель не является характерным для использования в качестве подвижной фазы в колоночной хроматографии. . В качестве подвижной фазы может быть использован обычный неполярный растворитель или полярный растворитель, и, в случае необходимости, предпочтительно изменять полярность путем изменения соотношения таких растворителей. Кроме того, соединение (A) настоящего изобретения является фторированным соединением и обычно обладает отличной растворимостью во фторированном растворителе, но фторированный растворитель не является характерным для использования в качестве подвижной фазы в колоночной хроматографии.
Неполярным растворителем может, например, быть углеводородный растворитель, такой как гексан или октан, или галогенированный углеводородный растворитель, такой как R-113 или R-225. Полярным растворителем может, например, быть спиртовой растворитель, такой как метанол, этанол или пропанол; галогенированный спирт, такой как гексафторизопропанол; кетонный растворитель, такой как ацетон или метилэтилкетон; растворитель из карбоновой кислоты, такой как уксусная кислота, нитрильный растворитель, такой как ацетонитрил; амидный растворитель, такой как диметилформамид; эфирный растворитель, такой как метилацетат или этилацетат; или алкилсульфоксид, такой как диметилсульфоксид.
Соединение (A), получаемое способом настоящего изобретения, является соединением, применяемым в качестве смазки, модификатора поверхности или поверхностно-активного вещества. А именно, настоящее изобретение предлагает смазку, модификатор поверхности или поверхностно-активное вещество, содержащие фторполиэфирное соединение (A) в качестве основного компонента.
Смазкой может быть смазка, применяемая для защитной пленки из алмазоподобного углерода (DLC пленка) для магнитных дисков. Модификатор поверхности может быть использован для регулирования показателя преломления полимера или улучшения устойчивости полимера к химическому воздействию путем его нанесения на поверхность полимера.
В случае когда соединение (A) применяют в качестве смазки или модификатора поверхности, соединение (A) используют предпочтительно в виде жидкой композиции. В случае когда оно применяется в виде жидкой композиции, растворителем предпочтительно является перфторамин, такой как перфтортрипропиламин или трибутиламин, или перфторалкан, такой как Vertrel (производимый фирмой DuPont). Концентрация соединения (A) в жидкой композиции может быть, соответственно, скорректирована в зависимости от цели использования, и она предпочтительно составляет от 0,01 до 50 мас.%, более предпочтительно от 0,01 до 20 мас.%.
Жидкой композицией, содержащей соединение (А), может быть любой раствор, суспензия или эмульсия, предпочтительно раствор. Кроме того, предпочтительно, чтобы растворителем был растворитель, имеющий температуру кипения, соответствующую процессу покрытия (такого как покрытие при нанесении покрытия погружением), описанному далее. Жидкая композиция может содержать компонент (далее называемой другим компонентом), отличный от соединения (A) и растворителя. В случае когда соединение (A) применяют в качестве смазки, другим компонентом может, например, быть акцептор радикалов (такой как торговой марки X-1p, производимый фирмой Dow Chemicals). В случае когда соединение (A) применяют в качестве материала для покрытия, другим компонентом может быть силан, эпоксид, титан, алюминий или другое повышающее адгезию вещество, которое будет улучшать адгезивные свойства соединения (A) к основе.
В случае когда соединение (A) применяют в качестве смазки или модификатора поверхности, предпочтительно разработать специальный подход для нанесения соединения (A) или жидкой композиции, содержащей соединение (A), на поверхность основы с последующей сушкой для образования тонкой мембраны соединения (A).
Способом нанесения покрытия может, например, быть нанесение покрытия с помощью валка, поливом, погружением, центрифугированием, с помощью водного покрытия, штампованием, методом Лангмюра-Блоджетта или методом вакуумного осаждения и предпочтительно методом центрифугирования, погружения или вакуумного осаждения.
В случае когда покрытие наносят центрифугированием или погружением, предпочтительно применять жидкую композицию. Для жидкой композиции предпочтительно выбирать растворитель, соответственно принимая во внимание, например, эффективность применения, температуру кипения и доступность.
Тонкая мембрана, образованная при использовании соединения (A) настоящего изобретения, является прозрачной, имеет низкий показатель преломления или является превосходной с точки зрения теплостойкости или устойчивости к химическому воздействию. Кроме того, тонкая мембрана имеет высокую смазывающую способность и имеет способность самовосстановления. Предпочтительно, чтобы толщина тонкой мембраны обычно составляла от 0,001 до 50 мкм. Форма и материал основы специально не ограничиваются. Основа, покрытая жидкой композицией, содержащей соединение (A) настоящего изобретения, может быть использована, например, для основы для накопителя на жестком диске, оптических волокон, зеркала, солнечной батареи, оптического диска, сенсорной панели, фотокопировального или термобарабана, пленочного конденсатора или пленки, такой как лучепоглощающая пленка для оконного стекла.
Примером использования соединения (A) в качестве поверхностно-активного вещества является добавка или выравнивающее средство для понижения поверхностного натяжения покрытия или выравнивающее средство для полировочной жидкости. При добавлении к покрытию, предпочтительно добавлять его столько, чтобы количество соединения (A) составляло от 0,01 до 5 мас.% к покрытию.
Соединение (A) является полезным также для применений, отличных от вышеуказанных. В случае когда соединение (A) используют для другого применения, соединение (A) может быть использовано, как оно есть или в форме, например, жидкой композиции. Другим применением может быть, например, добавка к материалу кабельного покрытия, материал, отталкивающий чернила (например, для покрытия или для принтера, такого как струйный принтер), адгезив для полупроводникового устройства (такой как адгезив для LOC (вывод на чипе) ленты, защитное покрытие для полупроводника (такое как средство для влагонепроницаемого покрытия или ингибитор повышения температуры для пайки) или тонкая мембрана (такая как пленочная мембрана), применяемая в оптике, смазка для неотражающей пленки для дисплеев и неотражающей пленки для фоторезистов.
Когда соединение (A) настоящего изобретения используют для этих приложений, преимущество может быть получено за счет того, что обеспечивается стабильная эксплуатация в течение долгого периода времени.
ПРИМЕРЫ
Сейчас настоящее изобретение будет подробно описано со ссылкой на примеры. Однако следует понимать, что настоящее изобретение ни в коей мере этим не ограничивается.
Далее тетраметилсилан обозначается как ТМС, CCl2FCClF2 – как R-113, дихлорпентафторпропан – как R-225, и CClF2CF2CCl2CF2CF3 – как R-419.
Кроме того, Mw обозначает средневзвешенную молекулярную массу и Mn обозначает среднечисленную молекулярную массу. Среднюю молекулярную массу означает Mn, и распределение молекулярной массы означает Mw/Mn.
Молекулярную массу измеряли гельпроникающей хроматографией (далее обозначаемой как ГПХ). Способ измерения с помощью ГПХ проводили в соответствии со способом, раскрытым в JP-A-2001-208736. А именно соединяли последовательно две колонки торговой марки PLgel MIXED-E (производимые фирмой Polymer Laboratories Ltd.) для получения колонки для анализа, используя в качестве подвижной фазы (99:1) смесь растворителей R-225 (торговой марки Asahiklin AK-225SEC Grade 1, производимый фирмой Asahi Glass Company, Limited) и гексафторизопропилового спирта (ГФИП). Анализ проводили путем использования в качестве стандартных образцов для измерения молекулярных масс четырех типов перфторполиэфиров, имеющих молекулярные массы от 2000 до 10000 и Mw/Mn меньше чем 1,1 и одного типа перфторполиэфира, имеющего молекулярную массу 1300 и
Mw/Mn, по меньшей мере, 1,1. Объемную скорость потока подвижной фазы устанавливали 1,0 мл/мин, температуру в колонке устанавливали 37°C, и в качестве детектора применяли испарительный детектор по рассеиванию света.
ТМС использовали в качестве стандартного вещества для 1H-ЯМР (300,4 MГц), и CFCl3 использовали в качестве стандартного вещества для 19F-ЯМР (282,7 MГц).
R-113 использовали в качестве растворителя для ЯМР, если не было указано иначе.
ПРИМЕР 1: ПРИМЕР РЕАКЦИИ ЭТЕРИФИКАЦИИ
Оксид этилена добавляют известным способом к триолу, представленному формулой HC(CH2OH)3, и затем вносят в колбу R-225 (50 г) и NaF (2,88 г), и барботируют азот при интенсивном перемешивании при внутренней температуре 25°C с получением следующего соединения (D2-1). Добавляют туда по каплям в течение 1,0 часа FCOCF(CF3)OCF2CF(CF3)O(CF2)3F (34,3 г) при внутренней температуре не более 10°C. После завершения добавления по каплям смесь перемешивают при комнатной температуре в течение 24 часов, в результате чего получают неочищенную жидкость. Далее неочищенную жидкость подвергают фильтрации при пониженном давлении, и полученную жидкость сушат в течение 12 часов в вакуумной сушилке (100°C, 666,5 Пa (абсолютное давление)). Полученную таким образом неочищенную жидкость растворяют в R-225 (100 мл) и промывают три раза насыщенным раствором карбоната натрия (1000 мл) для получения органической фазы.
К полученной органической фазе далее добавляют сульфат магния (1,0 г) с последующим перемешиванием в течение 12 часов. Затем сульфат магния удаляют фильтрацией под давлением и отгоняют с помощью испарителя R-225 с получением полимера (52,8 г), который при комнатной температуре является жидкостью. Результаты 1H-ЯМР и 19F-ЯМР подтверждают, что полученный полимер является следующим соединением (D3-1). Здесь среднее значение (k+r+p) равно 27,0. Rf является -CF(CF3)OCF2CF(CF3)OCF2CF2CF3. Mn равна 2600, и Mw/Mn равно 1,15.
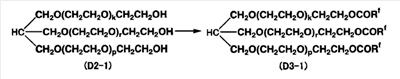
1H-ЯМР (растворитель: CDCl3)  (м.д.): от 3,4 до 3,8, 4,5. (м.д.): от 3,4 до 3,8, 4,5.
19F-ЯМР (растворитель: CDCl3)  (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7. (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7.
ПРИМЕР 2: ПРИМЕР ФТОРИРОВАНИЯ СОЕДИНЕНИЯ (D3-1), ПОЛУЧЕННОГО В ПРИМЕРЕ 1
ПРИМЕР 2-1: Пример, в котором растворителем для реакции является R-113
В 500 мл автоклав, сделанный из сплава Хастелой, добавляют R-113 (312 г), перемешивают при 25°C. На выходе автоклава для газа устанавливают последовательно холодильник, в котором поддерживается температура 20°C, слой гранул NaF и холодильник, в котором температура поддерживается на уровне -20°C. Здесь от холодильника, работающего при -20°C, устанавливают линию возврата жидкости для возврата сконденсированной жидкости в автоклав. После продувки газообразным азотом в течение 1,0 часа продувают в течение одного часа при объемной скорости 16,97 л/час газообразный фтор, разбавленный до 20 мол.% газообразным азотом (далее обозначаемый как 20% газообразный фтор).
Затем при продувке 20% газообразным фтором при той же самой объемной скорости вводят в течение 11 часов раствор, содержащий продукт (D3-1) (15 г), полученный в примере 1, растворенный в R-113 (200 г).
Затем вводят 6 мл раствора R-113 при продувке 20% газообразным фтором при той же самой объемной скорости. Далее в течение 1,0 часа продувают газообразным азотом.
После завершения реакции получают неочищенную жидкость, и отгоняют растворитель вакуумной сушкой (60°C, 6,0 часов) с получением продукта (21,4 г), который является жидкостью при комнатной температуре. В результате анализа продукта подтверждается, что он является следующим соединением (D4-1), имеющим практически все атомы водорода соединения (D3-1), полученного в примере 1, замещенные на атомы фтора. Отношение числа атомов фтора в соединении (D4-1) к числу атомов водорода в соединении (D3-1) составляет, по меньшей мере, 99,9 мол.%. Mn равен 4600, таким образом (k+r+p) в следующей формуле равняется значению, при котором Mn равна 4600. Кроме того, Mw/Mn равно 1,20.

1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0, от -181,5 до -184,5. (м.д.): от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0, от -181,5 до -184,5.
ПРИМЕР 2-2: Пример, в котором растворителем для реакции является R-419
Реакцию проводят аналогично, за исключением того, что R-113 в примере 2-1 заменяют на R-419. Результаты анализа образовавшегося продукта подтверждают образование такого же соединения (D4-1), как продукт в примере 2-1.
ПРИМЕР 2-3: Пример, в котором растворителем для реакции является FCOCF(CF3)OCF2CF(CF3)OCF2CF2CF3
Реакцию проводят аналогично, за исключением того, что R-113 в примере 2-1 заменяют на FCOCF(CF3)OCF2CF(CF3)OCF2CF2CF3. Результаты анализа продукта подтверждают образование такого же соединения (D4-1), как продукт в примере 2-1.
ПРИМЕР 3: ПРИМЕР ТЕРМИЧЕСКОГО РАЗЛОЖЕНИЯ СОЕДИНЕНИЯ (D4-1), ПОЛУЧЕННОГО В ПРИМЕРЕ 2-1
Круглодонную колбу объемом 50 мл, содержащую крошку для перемешивания, тщательно продувают азотом. В круглодонную колбу добавляют 1,1,3,4-тетрахлоргексафторбутан (25 г), KF (0,20 г) и соединение (D4-1) (20 г), полученное в примере 2-1, энергично перемешивают при 120°C. На выходе круглодонной колбы устанавливают последовательно холодильник, в котором поддерживается температура 20°C, и охлаждаемую смесью сухой лед/этанол трубку и проводят герметизацию азотом.
Через восемь часов внутреннюю температуру понижают до комнатной температуры и затем подсоединяют вакуумный насос к охлаждающей трубке, при поддержании внутри пониженного давления, отгоняют растворитель и побочные продукты. Через три часа получают продукт (13,3 г), который является жидкостью при комнатной температуре.
Анализ продукта подтверждает образование следующего соединения (D5-1). Отношение числа -COF групп в продукте к общему числу эфирных связей в соединении (D4-1) составляет, по меньшей мере, 99 мол.%.
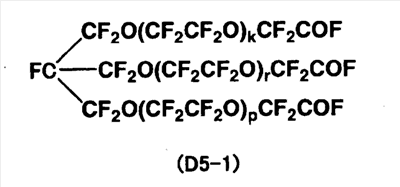
1H-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): 12,7, -78,1, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): 12,7, -78,1, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 4: ПРИМЕР ПОЛУЧЕНИЯ МЕТИЛОВЫХ ЭФИРОВ ЭТЕРИФИКАЦИЕЙ СОЕДИНЕНИЯ (D5-1), ПОЛУЧЕННОГО В ПРИМЕРЕ 3
ПРИМЕР 4-1: Пример получения продукта реакцией этерификации
В круглодонную колбу, содержащую соединение (D5-1), полученное в примере 3, добавляют KF (0,9 г) и R-113 (5,0 г), с последующим интенсивным перемешиванием при внутренней температуре 25°C. Далее медленно по каплям добавляют метанол (0,5 г) при внутренней температуре 25°C или выше.
Через восемь часов перемешивание прекращают и неочищенную жидкость фильтруют на установке для фильтрования под давлением для удаления KF. Затем при помощи испарителя полностью удаляют R-113 и избыток метанола с получением продукта (13,5 г), который является жидкостью при комнатной температуре.
Анализ продукта подтверждает образование следующего соединения (D7-1). Найдено, что все -COF группы в соединении (D5-1) этерифицированы метилом. Mn равна 3200, и Mw/Mn равно 1,17.

1H-ЯМР  (м.д.): 3,95, от 5,9 до 6,4. (м.д.): 3,95, от 5,9 до 6,4.
19F-ЯМР  (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 4-2: Пример получения реакцией переэтерификации
Круглодонную колбу объемом 50 мл, содержащую крошку для перемешивания, тщательно продувают азотом. Добавляют соединение (D4-1) (20,0 г), полученное также как в примере 2-1, и метанол (1,0 г), затем проводят интенсивное перемешивание путем барботирования при комнатной температуре. Выходное отверстие круглодонной колбы герметизируют с помощью азота.
Через восемь часов подсоединяли вакуумный насос к охлаждающей трубке для создания внутри колбы пониженного давления и отгоняли избыток метанола и побочные продукты реакции. Через три часа получали продукт (13,6 г), который при комнатной температуре является жидкостью.
Анализ продукта подтверждает образование следующего соединения (D7-1). Mn продукта равна 3200. Отношение числа -COOCH3 групп в продукте к числу эфирных связей в соединение (D4-1) составляет 99,9 мол.%.
1H-ЯМР  (м.д.): 3,95, от 5,9 до 6,4. (м.д.): 3,95, от 5,9 до 6,4.
19F-ЯМР  (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 5: ПРИМЕР КОНВЕРСИИ СОЕДИНЕНИЯ (D7-1), ПОЛУЧЕННОГО В ПРИМЕРЕ 4
Смешивают соединение (D7-1) (13,0 г), полученное способом в примере 4-2, R-225 (240 мл) и тетрагидрофуран (240 мл), и добавляют комплекс боргидрид/тетрагидрофуран (4,0 г) в токе азота с последующим перемешиванием при комнатной температуре в течение ночи. Растворитель отгоняют в испарителе и к остатку добавляют 2 моль/л хлористоводородной кислоты с последующей экстракцией при помощи R-225. Экстракт концентрируют с получением неочищенного продукта (11,95 г). Неочищенный продукт очищают в колонке с силикагелем (элюент: R-225/гексафторизопропиловый спирт). Образование следующего соединения (A-11a) подтверждают с помощью 1H-ЯМР и 19F-ЯМР. Кроме того, подтверждено, что в соединении практически не содержится -(OCF2О)- фрагментов. Mn равна 3000, и Mw/Mn равно 1,12.
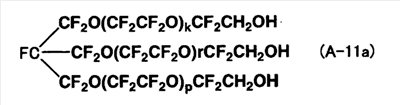
1H-ЯМР  (м.д.): 3,94. (м.д.): 3,94.
19F-ЯМР  (м.д.): -80,1, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): -80,1, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 6: ПРИМЕРЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ ЭТИЛЕНКАРБОНАТА К СОЕДИНЕНИЮ (A-11a), ПОЛУЧЕННОМУ В ПРИМЕРЕ 5
Соединение (A-11a) (10,0 г), полученное в примере 5, R-419 (10 мл) и этиленкарбонат (1,0 г) помещают в круглодонную колбу (50 мл) с последующим перемешиванием. Затем в атмосфере азота добавляют фторид калия (0,9 г), в верхней части колбы устанавливают обратный холодильник, охлаждающий до 20°, и смесь перемешивают в течение 36 часов при нагревании до 150°C при герметизации выхода холодильника азотом с получением в качестве продукта реакции неочищенной жидкости. Жидкость подвергают фильтрации под давлением на фильтре (диаметр пор 0,1 мкм, сделанный из тефлона), и растворитель в полученном фильтрате отгоняют в испарителе с получением в качестве продукта соединения бледно-желтого цвета (10,80 г), которое является жидкостью при 25°C.
В результате анализа продукта методом 1H-ЯМР и 19F-ЯМР подтверждается образование следующего соединения (A-11b), в котором -CF2CH2OH группы в соединении (A-11a) превращены в -CF2CH2OCH2CH2OH группы. Отношение -CF2CH2OCH2CH2OH групп в продукте к -CF2CH2OH группам в соединении (A-11a), используемом для реакции, составляет 97,3 мол.%, и продукт является смесью двух или более типов, отличающихся концевыми группами. Mn равна 3050, и Mw/Mn равно 1,25. Кроме того, подтверждено методом 19F-ЯМР, что -(ОCF2О)- структура в соединении (A-lib) не присутствует.
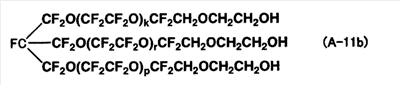
1H-ЯМР  (м.д.): 4,31, 3,9, 3,76. (м.д.): 4,31, 3,9, 3,76.
19F-ЯМР  (м.д.): -77,0, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): -77,0, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 7: ПРИМЕРЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ 2,3-ЭПОКСИ-1-ПРОПАНОЛА К СОЕДИНЕНИЮ (A-11a), ПОЛУЧЕННОГО В ПРИМЕРЕ 5
Соединение (A-11a) (10 г), полученное таким же способом, как и в примере 5, и 2-метил-2-пропанол (5,0 г) помещают в круглодонную колбу (250 мл) в атмосфере азота с последующим перемешиванием до тех пор, пока смесь не станет однородной. Обратный холодильник в виде трубки, у которой выходное отверстие герметизируют газообразным азотом при 20°C устанавливают на выходе круглодонной колбы.
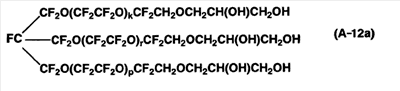
Затем трет-бутоксид калия (0,20 g) загружают в автоклав и нагревают при 70°C с последующим перемешиванием в течение 30 минут. Далее при поддержании внутренней температуры 70°C добавляют туда по каплям 2,3-эпокси-1-пропанол (0,8 г) в течение 2 часов с последующим перемешиванием в течение 12 часов. Круглодонную колбу охлаждают до 25°C и герметизируют газообразным азотом и добавляют по каплям 0,2 г/л хлористоводородной кислоты (50 мл) с получением жидкости, разделенной на два слоя. Органический слой жидкости отделяют и добавляют R-225 (50 мл) с получением раствора, который промывают дважды дистиллированной водой (500 мл) и обезвоживают сульфатом магния, и растворитель отгоняют в испарителе с получением в качестве продукта бледно-желтого соединения (10,68 г), которое является жидкостью при 25°C.
В результате анализа продукта методом 1H-ЯМР и 19F-ЯМР подтверждается образование следующего соединения (A-12a), в котором -CF2CH2OH группы в соединении (A-11b) превращены в -CF2CH2OCH2CH(OH)CH2ОH. Отношение -CF2CH2OCH2CH(OH)CH2OH в продукте к -CF2CH2OH группам в соединении (A-11b), использованном для реакции, составляет 92,5 мол.%, и продукт является смесью двух или более типов, отличающихся концевыми группами. Методом 19F-ЯМР подтверждается, что продукт является соединением, в котором структура -(ОCF2О)- не присутствует. Кроме того, Mn равна 3060, и Mw/Mn равно 1,28.
1H-ЯМР  (м.д.): 3,45, 3,67, 4,67. (м.д.): 3,45, 3,67, 4,67.
19F-ЯМР  (м.д.): -77,1, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5. (м.д.): -77,1, от -88,2 до -90,5, от -135,0 до -139,0, от -181,5 до -184,5.
ПРИМЕР 8: ПРИМЕРЫ ПОКРЫТИЯ НА ОСНОВЕ СОЕДИНЕНИЯ (A-11a)
Соединение (A-11a) (1 г), полученное в примере 5, и перфтортретбутиламин (99 г, IL-263, выпускаемый фирмой Tokuyama Corporation) загружают в стеклянную колбу с последующим перемешиванием в течение 2 часов с получением бесцветного и прозрачного однородного раствора. Раствор наносят на алюминиевую пластину центрифугированием при скорости вращения 700 об/мин в течение 20 секунд с последующей тепловой обработкой при 80°C в течение 1 часа с образованием на алюминиевой пластине однородной и прозрачной мембраны толщиной 0,05 мкм. Коэффициент трения на поверхности алюминиевой пластины значительно понижается.
ПРИМЕР 9: ПРИМЕРЫ ТЕСТИРОВАНИЯ СТАБИЛЬНОСТИ СОЕДИНЕНИЯ (A-11a)
В атмосфере азота (100 мл/мин) повышают температуру от 25 до 500°C при скорости 10°C/мин, в результате чего измеряют дифференциальными термовесами потерю массы соединения (A-11a) (25 мг), полученного в примере 5. В результате, потеря массы не наблюдается до 300°C, и кривая потери массы является постоянной, демонстрируя тем самым высокую стабильность.
Кроме того, также в случае когда тест на стабильность вышеуказанного соединения (25 мг) проводят в присутствии тонкодисперсных частиц  -оксида алюминия (0,5 г, N-611N, производимые фирмой Nikki Chemical Co., Ltd), кривая потери массы является такой же, как и в случае когда тонкодисперсные частицы -оксида алюминия (0,5 г, N-611N, производимые фирмой Nikki Chemical Co., Ltd), кривая потери массы является такой же, как и в случае когда тонкодисперсные частицы  -оксида алюминия отсутствуют, тем самым, демонстрируя высокую стабильность даже в присутствии катализатора типа кислоты Льюиса. -оксида алюминия отсутствуют, тем самым, демонстрируя высокую стабильность даже в присутствии катализатора типа кислоты Льюиса.
ПРИМЕР 10: ТЕСТ НА СТАБИЛЬНОСТЬ ИЗВЕСТНОГО ПЕРФТОРПОЛИЭФИРА (СРАВНИТЕЛЬНЫЙ ПРИМЕР)
Используя перфторполиэфир, содержащий в основном -OCF2О- структуру (FOMBLIN Z DiOL4000, выпускаемый фирмой Ausimont Inc.), проводили тест на стабильность так же, как в примере 9. В результате, в присутствии тонкодисперсных частиц  -оксида алюминия эфир подвергался разложению полностью при температуре от 240 до 250°C и испарялся, так как превращался в низкомолекулярные соединения. -оксида алюминия эфир подвергался разложению полностью при температуре от 240 до 250°C и испарялся, так как превращался в низкомолекулярные соединения.
ПРИМЕР 11
ПРИМЕР 11-1: пример получения и оценки соединения (A-11d)
Соединение (A-11d) получали проведением таких же реакций, что и в примерах 1, 2-1, 3, 4-1 и 5, за исключением того, что соединение (D2-1) в примере 1 заменяли на коммерческий глицериновый эфир полиоксиэтилена (Uniox G1200, выпускаемый фирмой NOF Corporation). Структуры и ЯМР спектры соединений, полученных в соответствующих примерах, являются следующими. Было подтверждено, что соединение (A-11d) не содержит -(OCF2О)- фрагмент. Mn соединения (A-11d) составляла 3000. Кроме того, используя соединение (A-11d), были проведены такие же оценки, как в примерах 8 и 9, в результате чего был получен такой же вывод, как и для соединения (A-11a). Соединение (A-11d) имело Mn, равную 2600, и Mw/Mn, равное 1,14.
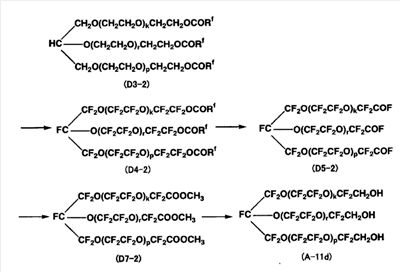
Спектры ЯМР соединения (D3-2)
1Н-ЯМР (растворитель: CDCl3)  (м.д.): от 3,4 до 3,8, 4,5. (м.д.): от 3,4 до 3,8, 4,5.
19F-ЯМР (растворитель: CDCl3)  (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7. (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7.
Спектры ЯМР соединения (D4-2)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0. (м.д.): от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0.
Спектры ЯМР соединения (D5-2)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): 12,7, -78,1, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): 12,7, -78,1, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (D7-2)
1Н-ЯМР  (м.д.): 3,95, от 5,9 до 6,4. (м.д.): 3,95, от 5,9 до 6,4.
19F-ЯМР  (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): -78,3, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (A-11d)
1Н-ЯМР  (м.д.): 3,94. (м.д.): 3,94.
19F-ЯМР  (м.д.): -80,1, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): -80,1, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕРЫ 11-2
Следующее соединение (A-11e) было получено так же, как в примере 6, за исключением того, что соединение (A-11a) в примере 6 было заменено на соединение (A-11d), полученное в примере 11-1. Mn соединения (A-11e) составляла 3050. Mw/Mn равнялось 1,26. Методом 19F-ЯМР было подтверждено, что соединение (A-11e) не содержит -(OCF2О)- структуру.
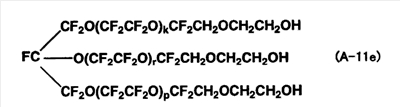
1Н-ЯМР  (м.д.): 4,31, 3,9, 3,76. (м.д.): 4,31, 3,9, 3,76.
19F-ЯМР  (м.д.): -77,0, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): -77,0, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕР 11-3
Следующее соединение (A-12b) получали так же, как и в примере 7, за исключением того, что соединение (A-11a) в примере 7 было заменено на соединение (A-11d), полученное в примере 11-1. Mn соединения (A-12b) составляла 3060. Mw/Mn было 1,29.
Методом 19F-ЯМР было подтверждено, что соединение (A-12b) не содержит -(OCF2О)- структуру.
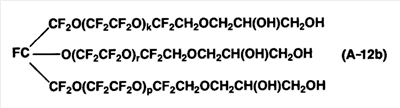
1Н-ЯМР  (м.д.): 3,45, 3,67, 4,67. (м.д.): 3,45, 3,67, 4,67.
19F-ЯМР  (м.д.): -77,1, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): -77,1, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕР 12
ПРИМЕР 12-1: Примеры получения соединения (A-21a)
Соединение (A-21a) получали проведением таких же реакций, что и в примерах 1, 2-1, 3, 4-1 и 5, за исключением того, что соединение (D3-1) в примере 1 заменяли на следующее соединение (D3-3). Структуры и ЯМР спектры соединений, полученных в соответствующих примерах, являются следующими. Было подтверждено, что соединение (A-21a) не содержит -(OCF2О)- фрагмент. Mn соединения (A-21a) составляла 26003600. Кроме того, используя соединение (A-21a), были проведены такие же оценки, как в примерах 8 и 9, в результате чего был получен такой же вывод, как и для соединения (A-2la). Соединение (A-21a) имело Mw/Mn, равное 1,21.
Спектры ЯМР соединения (D3-3)
1Н-ЯМР (растворитель: CDCl3)  (м.д.): от 3,4 до 3,8, 4,5. (м.д.): от 3,4 до 3,8, 4,5.
19F-ЯМР (растворитель: CDCl3)  (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7. (м.д.): от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -128,0 до -129,2, -131,1, -144,7.
Спектры ЯМР соединения (D4-3)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -65,2 до -68,8, от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0. (м.д.): от -65,2 до -68,8, от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0.
Спектры ЯМР соединения (D5-3)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): 12,7, от -60,2 до -68,8, -78,1, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): 12,7, от -60,2 до -68,8, -78,1, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (D7-3)
1Н-ЯМР  (м.д.): 3,95, от 5,9 до 6,4. (м.д.): 3,95, от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -63,2 до -65,8, -78,3, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): от -63,2 до -65,8, -78,3, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (A-21a)
1Н-ЯМР  (м.д.): 3,94. (м.д.): 3,94.
19F-ЯМР  (м.д.): от -64,2 до -65,8, -80,1, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): от -64,2 до -65,8, -80,1, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕР 12-2
Следующее соединение (A-21b) было получено так же, как в примере 6, за исключением того, что соединение (A-11a) в примере 6 было заменено на соединение (A-21a), полученное в примере 12-1. Mn соединения (A-21b) составляла 2670. Mw/Mn равнялось 1,30.
Методом 19F-ЯМР было подтверждено, что соединение (A-21b) не содержит -(OCF2О)- структуру.
| C(CF2О(CF2CF2О)FCF2CH2ОCH2CH2ОH)4 |
(A-21b) |
1Н-ЯМР  (м.д.): 4,31, 3,9, 3,76. (м.д.): 4,31, 3,9, 3,76.
19F-ЯМР  (м.д.): от -64,2 до -65,8, -77,0, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): от -64,2 до -65,8, -77,0, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕР 12-3
Следующее соединение (A-22а) было получено так же, как в примере 7, за исключением того, что соединение (A-11a) в примере 7 было заменено на соединение (A-21a), полученное в примере 12-1. Mn соединения (A-22а) составляла 2650. Mw/Mn равнялось 1,34.
Методом 19F-ЯМР было подтверждено, что соединение (A-22а) не содержит -(OCF2О)- структуру.
| C(CF2О(CF2CF2О)kCF2CH2OCH2CH(OH)CH2ОH)4 |
(A-22a) |
1Н-ЯМР  (м.д.): 3,45, 3,67, 4,67. (м.д.): 3,45, 3,67, 4,67.
19F-ЯМР  (м.д.): от -64,2 до -65,8, -77,1, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): от -64,2 до -65,8, -77,1, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕР 13
ПРИМЕР 13-1: Пример получения и оценки соединения (A-31a)
Соединение (A-31а) получали проведением таких же реакций, что и в примерах 1, 2-1, 3, 4-1 и 5, за исключением того, что соединение (D3-1) в примере 1 заменяли на следующее соединение (D3-4). Глицериновый эфир полиоксиэтилена (D2-4) в качестве материала соединения (D3-4) получали добавлением 2,3-эпокси-1-пропанола к соединению (D0-4), полученному способом, раскрытым в патентном документе (PERFECT Basic Patent), известным способом с получением (D1-4), и далее добавлением оксида этилена. Структуры и ЯМР спектры соединений, полученных в соответствующих примерах, являются следующими. Было подтверждено, что соединение (A-31а) не содержит -(OCF2О)- фрагмент. Mn соединения (A-31а) составляла 2900. Кроме того, используя соединение (A-11d), были проведены такие же оценки, как в примерах 8 и 9, в результате чего был получен такой же вывод, как и для соединения (A-11a). Соединение (A-31а) имело Mw/Mn, равное 1,13.
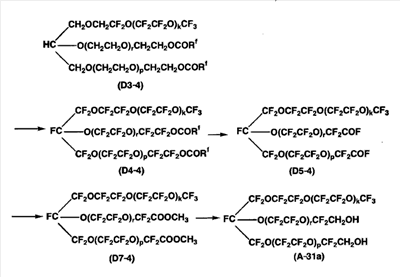
Спектры ЯМР соединения (D3-4-2)
1Н-ЯМР (растворитель: CDCl3)  (м.д.): от 3,4 до 3,8, 3,95, 4,5. (м.д.): от 3,4 до 3,8, 3,95, 4,5.
19F-ЯМР (растворитель: CDCl3)  (м.д.): от -54,0 до -56,0, от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -87,0 до -92,0, от -128,0 до -129,2, -131,1, -144,7. (м.д.): от -54,0 до -56,0, от -76,0 до -81,0, от -81,0 до -82,0, от -82,0 до -82,5, от -82,5 до -85,0, от -87,0 до -92,0, от -128,0 до -129,2, -131,1, -144,7.
Спектры ЯМР соединения (D4-4-2)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -54,0 до -56,0, от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0. (м.д.): от -54,0 до -56,0, от -77,5 до -86,0, от -88,2 до -92,0, от -120,0 до -139,0, от -142,0 до -146,0.
Спектры ЯМР соединения (D5-4-2)
1Н-ЯМР  (м.д.): от 5,9 до 6,4. (м.д.): от 5,9 до 6,4.
19F-ЯМР  (м.д.): 12,7, от -54,0 до -56,0, -78,1, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): 12,7, от -54,0 до -56,0, -78,1, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (D7-4-2)
1Н-ЯМР  (м.д.): 3,95, от 5,9 до 6,4. (м.д.): 3,95, от 5,9 до 6,4.
19F-ЯМР  (м.д.): от -54,0 до -56,0, -78,3, от -88,2 до -92,0, от -135,0 до -139,0. (м.д.): от -54,0 до -56,0, -78,3, от -88,2 до -92,0, от -135,0 до -139,0.
Спектры ЯМР соединения (A-11d)
1Н-ЯМР  (м.д.): 3,94. (м.д.): 3,94.
19F-ЯМР  (м.д.): от -54,0 до -56,0, -80,1, от -88,2 до -90,5. (м.д.): от -54,0 до -56,0, -80,1, от -88,2 до -90,5.
ПРИМЕРЫ 13-2
Следующее соединение (A-31b) было получено так же, как в примере 6, за исключением того, что соединение (A-11a) в примере 6 было заменено на соединение (A-31a), полученное в примере 13-1. Mn соединения (A-31b) составляла 2950. Mw/Mn равнялось 1,19.
Методом 19F-ЯМР было подтверждено, что соединение (A-31b) не содержит -(OCF2О)- структуру.
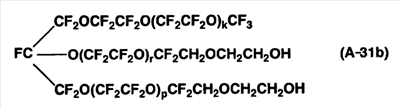
1Н-ЯМР  (м.д.): 4,31, 3,9, 3,76. (м.д.): 4,31, 3,9, 3,76.
19F-ЯМР  (м.д.): от -54,0 до -56,0, -77,0, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): от -54,0 до -56,0, -77,0, от -88,2 до -90,5, от -135,0 до -139,0.
ПРИМЕРЫ 11-3
Следующее соединение (A-32а) было получено так же, как в примере 7, за исключением того, что соединение (A-11a) в примере 7 было заменено на соединение (A-31a), полученное в примере 13-1. Mn соединения (A-32а) составляла 2960. Mw/Mn равнялось 1,21.
Методом 19F-ЯМР было подтверждено, что соединение (A-32а) не содержит -(OCF2О)- структуру.
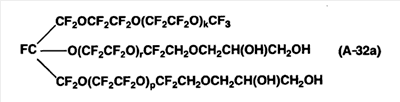
1Н-ЯМР  (м.д.): 3,45, 3,67, 4,67. (м.д.): 3,45, 3,67, 4,67.
19F-ЯМР  (м.д.): от -54,0 до -56,0, -77,1, от -88,2 до -90,5, от -135,0 до -139,0. (м.д.): от -54,0 до -56,0, -77,1, от -88,2 до -90,5, от -135,0 до -139,0.
ВОЗМОЖНОСТЬ ПРОМЫШЛЕННОГО ИСПОЛЬЗОВАНИЯ
Настоящее изобретение предлагает новое фторполиэфирное соединение, применяемое, например, в качестве смазки, модификатора поверхности или поверхностно-активного вещества. Фторполиэфирное соединение настоящего изобретения имеет низкое давление пара и низкую вязкость, имеет высокую химическую стабильность и не имеет проблем ухудшения свойств при его применении. Кроме того, фторполиэфирное соединение настоящего изобретения обладает высокой способностью самообновления и в связи с этим является полезным для вышеуказанного применения.
Полное раскрытие заявки на японский патент No. 2004-5586, зарегистрированной 13 января 2004 года, включая описание, формулу изобретения и реферат, включено в описание путем ссылки на соответствующий источник.
Формула изобретения
1. Фторполиэфирное соединение, представленное следующей формулой
(А)
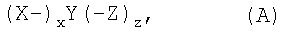
где символы имеют следующие значения:
X: группа, представленная следующей формулой (X) (где “а” является целым числом от 0 до 100, b является целым числом от 0 до 100, с является целым числом от 1 до 100, и d является целым числом от 1 до 200)
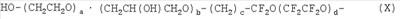
причем в случае, когда присутствуют по одному фрагменту каждого -(CH2CH2O)-фрагмента и -(СН2СН(ОН)CH2O)-фрагмента, то фрагментом, который связан с гидроксильной группой может быть -(CH2CH2O)- или -(СН2СН(ОН)CH2O)-фрагмент; и в случае когда присутствуют оба фрагмента, и -(СН2СН2О)-фрагмент, и -(СН2СН(ОН)CH2O)-фрагмент, и, по меньшей мере один из них присутствует в количестве по меньшей мере двух фрагментов, то расположение таких фрагментов может быть блочное или неупорядоченное;
Z: группа, представленная следующей формулой (Z), где RF является C1-20перфторалкильной группой и g является целым числом от 3 до 200
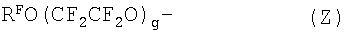
Y: (x+z) валентная перфторированная насыщенная углеводородная группа, такая как
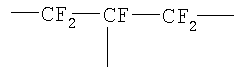 , , 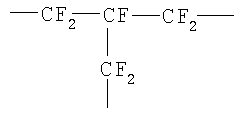 или или 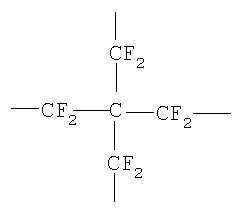
необязательно содержащая эфирный атом кислорода, расположенный между атомами углерод – углерод, но не содержащая -OCF2O- фрагмент; x, z: x является целым числом, равным, по меньшей мере, 2, z является целым числом, равным, по меньшей мере, 0, и (x+z) является целым числом, равным 3 или 4, при условии, что когда х равен, по меньшей мере, 2, группы, представленные формулой (X), могут быть одинаковыми или различными, и когда z равно, по меньшей мере, 2, группы, представленные формулой (Z), могут быть одинаковыми или различными.
2. Соединение по п.1, где группа, представленная формулой (X), является любой группой, выбранной из групп, представленных следующими формулами от (Х-1) до (Х-4), при условии, что d уже определено выше


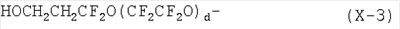
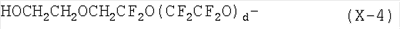
3. Соединение по п.2, где соединение, представленное формулой (А), является соединением, представленным следующими формулами (А-1) или (А-2), при условии, что X10 является любой группой, выбранной из групп, представленных следующими формулами от (X-1) до (X-4), Y3 является перфторалкантриильной группой, и Y4 является перфторалкантетраильной группой


4. Соединение по п.2, где соединение, представленное формулой (А), является соединением, представленным следующей формулой (А-3), при условии, что X10 является любой группой, выбранной из групп, представленных следующими формулами от (X-1) до (X-4), Y3 является перфторалкантриильной группой, и Z уже определено выше

5. Фторполиэфирное соединение по п.1, где соединение, представленное формулой (А) имеет молекулярную массу от 500 до 1000000, измеренную с помощью гельпроникающей хроматографии, и имеет распределение молекулярной массы от 1,0 до 1,5.
6. Композиция в виде раствора, предназначенная для модифицирования поверхности, содержащая фторполиэфирное соединение по п.1, и органический растворитель.
7. Композиция по п.6, в которой концентрация фторполиэфирного соединения составляет от 0,01 до 50 мас.%.
8. Средство для покрытия поверхности, содержащее фторполиэфирное соединение по п.1, в качестве обязательной составной части.
|
|