Патент на изобретение №2373215
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 1-ТРИМЕТИЛСИЛИЛПРОПАРГИЛОВОГО СПИРТА И ДИПРОПАРГИЛОВОГО ЭФИРА ЩАВЕЛЕВОЙ КИСЛОТЫ
(57) Реферат:
Изобретение относится к получению 1-триметилсилилпропаргилового спирта, широко применяемого в качестве исходного компонента в технологии тонкого органического синтеза. Техническая задача – разработка простого, безопасного способа получения 1-триметилсилилпропаргилового спирта, исключающего применение металлоорганического синтеза и дорогостоящих защитных групп, при одновременном снижении себестоимости получаемого продукта путем использования более дешевых и доступных реагентов. Предложено получение 1-триметилсилилпропаргилового спирта силилированием дипропаргилового эфира щавелевой кислоты под действием N-триметилсилилдиэтиламина и хлорида цинка в среде растворителя при температуре его кипения с последующим гидролизом соляной кислотой, экстрагированием и перегонкой в вакууме. Дипропаргиловый эфир щавелевой кислоты предложено получать взаимодействием щавелевой кислоты с пропаргиловым спиртом в среде бензола при температуре его кипения и постоянном водоотделении. 2 н.п. ф-лы.
Изобретение относится к органической химии, точнее к получению кремнийорганических соединений, а именно 1-триметилсилилпропаргилового спирта, формулы 1
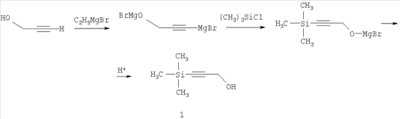
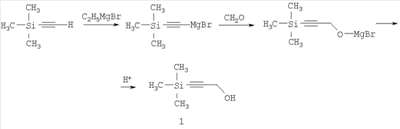
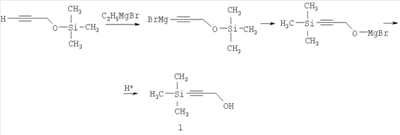
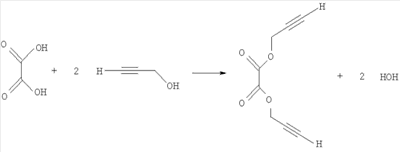
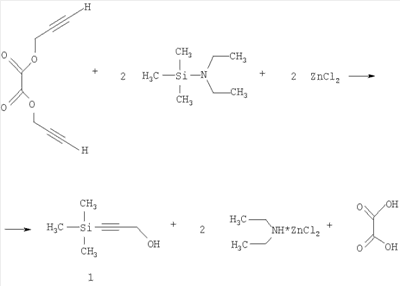
нашедшего широкое применение в технологии тонкого органического синтеза, в качестве исходного вещества. Известен способ получения 1-триметилсилилпропаргилового спирта с выходом 43,5%, основанный на взаимодействии пропаргилового спирта с избытком этилмагнийбромида и последующей обработке триметилхлорсиланом. [Комаров Н.В., Шостаковский М.Ф. Синтез первичных Известен способ получения 1-триметилсилилпропаргилового спирта с выходом 69,7% взаимодействием триметилсилилэтинилмагний бромида с формальдегидом. Однако труднодоступность и дороговизна триметилсилилэтинилмагний бромида делает ограниченным использование этого способа [Шостаковский М.Ф., Комаров Н.В., Ярош О.Г. Синтез триалкилэтинилсиланов и кремнеацетиленовых спиртов. Изв. АН СССР. Сер. химическая, 1966, с.101-104]. Наиболее близким аналогом к заявляемому является способ получения 1-триметилсилилпропаргилового спирта взаимодействием 1-триметилсилокси-2-пропинола-1 с этилмагний бромидом и последующим гидролизом разбавленным раствором соляной кислоты по схеме: В данном способе требуется кипячение реакционной массы в течение 9 часов [Medvedeva A.S., Novokshonov V.V., Demina М.М., Voronkov M.G. An unusual rearrangement of 1-trimethylsiloxy-3-bromomagnesium-2-propyne. J. Organomet. Chem. 553 (1998), 481-482]. Описанные способы требуют использования металлоорганических реагентов – реактивов Гриньяра, которые получают с использованием металлического магния и алкилбромида в среде эфирного растворителя, что сопряжено с более жесткими требованиями безопасности и длительны в исполнении. Технической задачей заявляемого способа является разработка безопасного простого способа получения 1-триметилсилилпропаргилового спирта из пропаргилового спирта, исключающего применение металлоорганического синтеза и дорогостоящих защитных групп, при одновременном снижении себестоимости получаемого продукта, путем использования более дешевых и доступных реагентов. Поставленная техническая задача решается путем использования дипропаргилового эфира щавелевой кислоты, который получают при азеотропной этерификации щавелевой кислоты пропаргиловым спиртом по схеме: Выход дипропаргилового эфира щавелевой кислоты достигает 78%. Из уровня техники не известно соединение дипропаргиловый эфир щавелевой кислоты, используемое нами для получении 1-триметилсилилпропаргилового спирта. Силилирование пропаргилового эфира щавелевой кислоты под действием N-триметилсилилдиэтиламина и хлорида цинка в среде органического растворителя при температуре кипения, с последующим гидролизом реакционной массы водным раствором соляной кислоты протекает в соответствии со схемой:
Пример получения дипропаргилового эфира щавелевой кислоты В прибор, состоящий из колбы, снабженной насадкой Дина-Старка с обратным холодильником, помещают 500 мл бензола, 1 моль (90 г) щавелевой кислоты и 3 моль (168,18 г) пропаргилового спирта. Нагревают при интенсивном кипении растворителя до прекращения отделения воды. После охлаждения реакционной массы продукт закристаллизовывается, его отфильтровывают, промывают бензолом и сушат. Выход 78%. Тпл 103-104°С ЯМР 1Н (CDCl3, Масс-спектр (ЭУ, 70эВ), m/z(Ioтн(%)): 137 [М+-29] (0,5), 39 (100). Пример получения 1-триметилсилилпропаргилового спирта В прибор для синтеза, состоящий из колбы, снабженной мешалкой и обратным холодильником, помещают 300 мл абсолютного 1,4-диоксана, 1,08 моль (146 г) безводного хлорида цинка и 0,9 моль (130 г) N-триметилсилилдиэтиламина, нагревают при перемешивании до 50°С и прибавляют раствор 0,3 моль (49,8 г) дипропаргилового эфира щавелевой кислоты, растворенный в 150 мл 1,4-диоксана. Реакционную массу нагревают, поддерживая равномерное кипение растворителя в течение 2 часов. После охлаждения реакционную массу выливают в делительную воронку, содержащую 1000 мл 15%-ного раствора соляной кислоты, встряхивают, органическую фазу отделяют, водную фазу экстрагируют хлороформом. Органические фазы объединяют, растворитель отгоняют, остаток перегоняют в вакууме. Получают 58,5 г вещества с Ткип 49°С/3 мм рт.ст. Выход 76%. ИК-спектр (KBr), ЯМР 1Н (CDCl3,
Формула изобретения
1. Способ получения 1-триметилсилилпропаргилового спирта, включающий получение из пропаргилового спирта его производного с последующим силилированием и гидролизом соляной кислотой, экстрагированием и перегонкой в вакууме, отличающийся тем, что в качестве производного пропаргилового спирта используют дипропаргиловый эфир щавелевой кислоты и силилирование проводят под действием N-триметилсилилдиэтиламина и хлорида цинка в среде растворителя при температуре его кипения. 2. Способ получения дипропаргилового эфира щавелевой кислоты путем взаимодействия щавелевой кислоты с пропаргиловым спиртом в среде бензола при температуре его кипения и постоянном водоотделении.
|
||||||||||||||||||||||||||

 3, p.421-424. SU 1766923 A1, 07.10.1992. Шостаковский М.Ф., Комаров Н.В.,Ярош О.Г. «Синтез триалкилэтинилсиланов и кремнеацетиленовых спиртов». Известия Академии Наук СССР, сер. Химическая, 1966, 1, с.101-104. Миронов В.Ф., Максимова Н.Г. «Синтез непредельных кремнеорганических соединений на основе пропаргилового спирта». Известия Академии Наук СССР, сер. Химическая, 1960, 11, с.2059-2061, Комаров Н.В., Шостаковский М.Ф. «Синтез первичных
3, p.421-424. SU 1766923 A1, 07.10.1992. Шостаковский М.Ф., Комаров Н.В.,Ярош О.Г. «Синтез триалкилэтинилсиланов и кремнеацетиленовых спиртов». Известия Академии Наук СССР, сер. Химическая, 1966, 1, с.101-104. Миронов В.Ф., Максимова Н.Г. «Синтез непредельных кремнеорганических соединений на основе пропаргилового спирта». Известия Академии Наук СССР, сер. Химическая, 1960, 11, с.2059-2061, Комаров Н.В., Шостаковский М.Ф. «Синтез первичных  -кремнеорганических ацетиленовых спиртов». Известия Академии Наук СССР, сер. Химическая, 1960, 7, с.1300-1302. ЕР 0550195 А2, 07.07.1993.
-кремнеорганических ацетиленовых спиртов». Известия Академии Наук СССР, сер. Химическая, 1960, 7, с.1300-1302. ЕР 0550195 А2, 07.07.1993.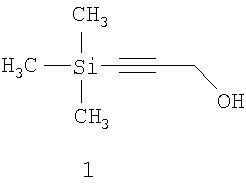
 м.д., J/Гц):2.59 (т, 2Н); 4,90 (д., 4Н).
м.д., J/Гц):2.59 (т, 2Н); 4,90 (д., 4Н). /cm-1: 3344 (ОН), 2177(С
/cm-1: 3344 (ОН), 2177(С С).
С).