|
|
(21), (22) Заявка: 2006101722/04, 18.06.2004
(24) Дата начала отсчета срока действия патента:
18.06.2004
(30) Конвенционный приоритет:
24.06.2003 US 60/480,900
24.06.2003 US 60/482,147
07.05.2004 US 60/569,356
(43) Дата публикации заявки: 27.07.2007
(46) Опубликовано: 20.11.2009
(56) Список документов, цитированных в отчете о
поиске:
DE 4142514 A1, 24.06.1993. WO 9324442 A1, 09.12.1993. WO 2004012656 A2, 12.02.2004. DE 2842243 A, 10.04.1980. WO 97/39748 A, 30.10.1997. RU 2002109234 A, 27.11.2003.
(85) Дата перевода заявки PCT на национальную фазу:
24.01.2006
(86) Заявка PCT:
EP 2004/006611 20040618
(87) Публикация PCT:
WO 2005/000781 20050106
Адрес для переписки:
101000, Москва, М.Златоустинский пер., 10, кв.15, “ЕВРОМАРКПАТ”, пат.пов. И.А.Веселицкой, рег.  11 11
|
(72) Автор(ы):
ЧУ Чан Ань (US),
ДЖИЛЛЕСПАЙ Пол (US),
ТИЛЛИ Джефферсон Райт (US)
(73) Патентообладатель(и):
Ф.ХОФФМАНН-ЛЯ РОШ АГ (CH)
|
(54) БИАРИЛОКСИМЕТИЛАРЕНОВЫЕ КАРБОНОВЫЕ КИСЛОТЫ
(57) Реферат:
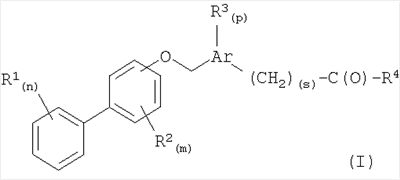
Изобретение относится к новым соединениям формулы (I), в которой Ar представляет собой фенил, фуранил, тиофенил, тиазолил, пиридинил; R1 независимо выбирают из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена и нитро; R2 независимо выбирают из группы, состоящей из водорода и галогена; R4 представляет собой гидрокси или остаток пирролидин-2-карбоновой кислоты, пиперидин-2-карбоновой кислоты или 1-аминоциклопентанкарбоновой кислоты, присоединенных через атом азота аминокислотного остатка; n означает 0, 1, 2, 3, 4 или 5; m означает 0, 1, 2, 3 или 4; р означает 0, и s означает 0, или к их фармацевтически приемлемым солям, при условии, что соединение не представляет собой S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]
пирролидин-2-карбоновую кислоту, 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту, 3-(бифенил-4-илоксиметил)бензойную кислоту, 2-(бифенил-3-илоксиметил)бензойную кислоту, 4-(бифенил-3-илоксиметил)бензойную кислоту, 4-(бифенил-4-илоксиметил)бензойную кислоту, 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту. Изобретение также относится к фармацевтической композиции на основе соединений формулы (I), стимулирующей активность гликогенсинтазы.
2 н. и 25 з.п. ф-лы.
Настоящее изобретение относится к новым биарилоксиметилареновым карбоновым кислотам и к их фармацевтически приемлемым солям, к их получению, а также к применению биарилоксиметилареновых карбоновых кислот и их фармацевтически приемлемых солей в качестве лекарственных средств, более конкретно к применению биарилоксиметилареновых карбоновых кислот и их фармацевтически приемлемых солей в качестве лекарственных средств для лечения или профилактики диабета, в частности диабета типа 2. Настоящее изобретение, кроме того, относится к фармацевтическим композициям, содержащим эти соединения.
Более подробно, настоящее изобретение относится к новым биарилоксиметилареновым карбоновым кислотам формулы (I):
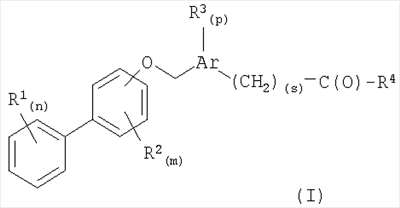
в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой группу гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4;
p означает 0, 1 или 2, и s означает 0, 1 или 2;
или к их фармацевтически приемлемым солям,
при условии, что
а) в том случае, когда Ar представляет собой фуранил, p и s означают ноль, соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой тиофенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
Было обнаружено, что соединения формулы I могут применяться при лечении и профилактике диабета, в особенности диабета типа 2.
Сахарный диабет является распространенным и довольно серьезным заболеванием, которым страдают 10 миллионов человек в США [Harris, M.I. Diabetes Care 1998, 21 (3S) Supplement, 11C], это заболевание приводит к повышенному риску возникновения инсульта, сердечно-сосудистых заболеваний, болезней почек, слепоты и может привести к ампутации. Диабет характеризуется снижением секреции инсулина и/или недостаточной способностью периферических тканей реагировать на инсулин, что приводит к повышению содержания глюкозы в крови. Сфера воздействия диабета расширяется, и это связывают с распространением ожирения и сидячим образом жизни. Существует две формы диабета: инсулинзависимый диабет и инсулиннезависимый диабет, большая часть диабетиков страдает от инсулиннезависимого диабета, называемого диабетом типа 2 или инсулиннезависимым сахарным диабетом (NIDDM). Вследствие серьезных последствий этого заболевания существует острая необходимость в контроле диабета.
Лечение диабета типа 2, как правило, начинают с похудения, здоровой диеты и программы физических упражнений. Однако эти факторы часто не способны обеспечить контроль заболевания, и имеется ряд доступных лекарственных средств, включая инсулин, метформин, сульфонилмочевины, акарбозу и тиазолидиндионы. Каждый из этих видов лечения имеет свои недостатки, и существует реальная необходимость в новых лекарственных средствах для лечения диабета.
Метформин представляет собой эффективное средство, которое снижает содержание глюкозы в плазме натощак и повышает чувствительность периферических тканей к инсулину, главным образом, посредством повышения синтеза гликогена [De Fronzo, R.A. Drugs 1999, 58 Suppl. 1, 29]. Метформин также приводит к понижению содержания ЛНП холестерина и триглицеридов [Inzucchi, S.Е. JAMA 2002, 287, 360]. Однако это лекарственное средство теряет свою эффективность в течение нескольких лет [Turner, R.С. et al. JAMA 1999, 281, 2005].
Тиазолидиндионы являются активаторами ядерного рецептора – гамма-рецептора, активируемого пролифератором пероксисомы. Эти соединения эффективны для снижения содержания глюкозы в крови, и их эффективность в первую очередь связывают со снижением резистентности к инсулину в скелетной мускулатуре [Tadayyon, M., Smith, S.A. Expert Opin. Investig. Drugs 2003, 12, 307]. Одним из недостатков, связанных с применением тиазолидиндионов, является увеличение массы тела.
Сульфонилмочевины связываются с рецепторами сульфонилмочевины панкреатических бета-клеток, стимулируют секрецию инсулина и таким образом снижают содержание глюкозы в крови. Увеличение массы тела также связывают с применением сульфонилмочевин [Inizucchi, S.E. JAMA 2002, 287, 360], и, кроме того, эти лекарственные средства, как и метформин, теряют эффективность с течением времени [Turner, R.С. et al. JAMA 1999, 281, 2005]. Дополнительной проблемой, которая часто возникает у пациентов, получающих лечение препаратами сульфонилмочевины, является гипогликемия [Salas, М. и Саго, J.J. Adv. Drug React. Tox. Rev. 2002, 21, 205-217].
Акарбоза представляет собой ингибитор фермента альфа-глюкозидаза, который расщепляет дисахариды и сложные углеводороды в кишечнике. Это средство имеет меньшую эффективность, чем метформин или сульфонилмочевины, и при этом вызывает дискомфорт в кишечнике и диарею, которые часто приводят к прекращению использования этого лекарственного средства [Inzucchi, S.E. JAMA 2002, 287, 360].
Поскольку ни один из этих видов лечения не обладает эффективностью в течение длительного периода действия без серьезных побочных эффектов, существует необходимость в новых лекарственных средствах для лечения диабета типа 2.
В скелетной мускулатуре и печени существует два основных вида метаболического пути утилизации глюкозы: гликолиз (расщепление глюкозы), или окислительный метаболизм, согласно которому глюкоза окисляется до пирувата; и гликогенезис, или депонирование, согласно которому глюкоза накапливается в полимерной форме как гликоген. Ключевой стадией синтеза гликогена является присоединение производного глюкозы UDP-глюкозы к растущей гликогеновой цепи, и эту стадию катализирует фермент гликогенсинтаза [Cid, E. et al. J. Biol. Chem. 2000, 275, 33614]. Существует две изоформы гликогенсинтазы, обнаруженные в печени [Bai, G. et al. J. Biol. Chem. 1990, 265, 7843] и в других периферических тканях, включая мышцы [Browner, М.F. et al. Proc. Nat. Acad. Sci. U.S.A. 1989, 86, 1443]. Имеются клинические и генетические данные, непосредственно связывающие гликогенсинтазу с диабетом типа 2. Как базальная, так и инсулин-стимулированная активность гликогенсинтазы в клетках мышц больных диабетом значительно ниже, чем в клетках худощавых, не страдающих диабетом субъектов [Henry, R.R. et al. J. Clin. Invest. 1996, 98, 1231-1236; Nikoulina, S.E. et al. J. Clin. Enocrmol. Metab. 2001, 86, 4307-4314]. Кроме того, некоторые исследования показали, что содержание гликогена ниже у пациентов с диабетом, чем у контрольных испытуемых [Eriksson, J. et al. N. Engl. J. Med. 1989, 331, 337; Schulman, R.G. et al. N. Engl. J. Med. 1990, 332, 223; Thorbum, A.W. et al. J. Clin. Invest. 1991, 87, 489], и в дополнение, данные генетических исследований выявляют связь у некоторых популяций между диабетом типа 2 и мутацией гена GYS 1, кодирующего мышечную изоформу гликогенсинтазы [Orhu-Melander, M. et al. Diabetes 1999, 48, 918].
Гликогенсинтаза является субъектом сложного регулирования, которое включает фосфорилирование, протекающее на по меньшей мере девяти участках [Lawrence, J.С., Jr. и Roach, Р.J. Diabetes 1997, 46, 541]. Дефосфорилированная форма фермента является активной. Гликогенсинтаза фосфорилируется при воздействии ряда ферментов, среди которых наиболее изучена Гликогенсинтаза киназа 3 (GSK3 (GSK3 ) [Tadayyon, M., Smith, S.A. Expert Opin. Investig. Drugs 2003, 12, 307]. Гликогенсинтаза дефосфорилируется при воздействии белков вида фосфатазы типа I (РР1) и протеинфосфатазы типа 2А (РР2А). В дополнение, Гликогенсинтаза подвергается регулированию при воздействии эндогенного лиганда, глюкоза-6-фосфата, который аллостерически стимулирует активность гликогенсинтазы, вызывая изменения конформации фермента, которые делают его более восприимчивым к дефосфорилированию под действием протеинфосфатаз, приводя к получению активной формы фермента [Gomis, R.R. et al. J. Biol. Chem. 2002, 277, 23246]. ) [Tadayyon, M., Smith, S.A. Expert Opin. Investig. Drugs 2003, 12, 307]. Гликогенсинтаза дефосфорилируется при воздействии белков вида фосфатазы типа I (РР1) и протеинфосфатазы типа 2А (РР2А). В дополнение, Гликогенсинтаза подвергается регулированию при воздействии эндогенного лиганда, глюкоза-6-фосфата, который аллостерически стимулирует активность гликогенсинтазы, вызывая изменения конформации фермента, которые делают его более восприимчивым к дефосфорилированию под действием протеинфосфатаз, приводя к получению активной формы фермента [Gomis, R.R. et al. J. Biol. Chem. 2002, 277, 23246].
Было предложено несколько механизмов для объяснения воздействия инсулина на снижение содержания глюкозы в крови, каждый из которых приводит к повышению количества накопления глюкозы в виде гликогена. Во-первых, поглощение глюкозы повышается посредством рекрутмента транспортера глюкозы GLUT4 в плазматической мембране [Holman, G.D. и Kasuga, M. Diabetologia 1997, 40, 991]. Во-вторых, происходит повышение концентрации глюкоза-6-фосфата, аллостерического активатора гликогенсинтазы [Villar-Palasi, С., Guinovart, J.J. FASEB J. 1997, 11, 544]. В-третьих, каскад киназных реакций, начинающийся с проявления тирозинканазной активности инсулинового рецептора, приводит к фосфорилированию и инактивации GSK3 , тем самым предотвращая деактивацию гликогенсинтазы [Cohen, P. Biochem. Soc. Trans. 1993, 21, 555; Yeaman, S.J. Biochem. Soc. Trans. 2001, 29, 537]. , тем самым предотвращая деактивацию гликогенсинтазы [Cohen, P. Biochem. Soc. Trans. 1993, 21, 555; Yeaman, S.J. Biochem. Soc. Trans. 2001, 29, 537].
Поскольку у пациентов с диабетом было обнаружено значительное снижение активности гликогенсинтазы, а также вследствие ключевой роли гликогенсинтазы в утилизации глюкозы, активация фермента гликогенсинтаза является терапевтической поддержкой при лечении диабета типа 2. Единственными известными аллостерическими активаторами этого фермента является глюкоза-6-фосфат [Leioir, L.F. et al. Arch. Biochem. Biophys. 1959, 81, 508] и глюкозамин-6-фосфат [Virkamaki, A., Yki-Jarvinen, H. Diabetes 1999, 48, 1101].
Вкратце, биарилоксиметилареновые карбоновые кислоты, описанные в тексте настоящей заявки, как было обнаружено, являются активаторами гликогенсинтазы. Таким образом, соединения согласно настоящему изобретению могут быть использованы для лечения и/или профилактики диабета типа 2, и/или пониженной толерантности к глюкозе, а также других состояний, при которых активация фермента гликогенсинтаза дает терапевтический эффект.
Некоторые биарилоксиметилареновые карбоновые кислоты известны из предшествующего уровня техники. Однако ни одно из этих известных соединений не связывают ни с лечением заболеваний, опосредованных активацией фермента гликогенсинтаза, ни с фармацевтическими композициями для лечения заболеваний, опосредованных активацией фермента гликогенсинтаза. В опубликованной международной заявке: Andersen, H.S. et al., WO 9740017, раскрыта структура и способ получения 3-(бифенил-4-илоксиметил)бензойной кислоты в качестве промежуточного соединения в синтезе ингибиторов SH2. В документе: Winkelmann, E. et al., DE 2842243, описана 5-(бифенил-4-илоксиметил)тиофен-2-карбоновая кислота в качестве гиполипидемического агента. В документе: Mueller, Т. et al., DE 4142514, описана 2-(бифенил-3-илоксиметил)бензойная кислота в качестве фунгицида.
Следующие соединения являются коммерчески доступными, производятся фирмой  ChemBridge Corporation ChemBridge Corporation , г.Сан Диего, Калифорния, США или фирмой , г.Сан Диего, Калифорния, США или фирмой  ChemDiv, Inc. ChemDiv, Inc. , г.Сан Диего, Калифорния, США. Относительно их применения информация отсутствует (примечание , г.Сан Диего, Калифорния, США. Относительно их применения информация отсутствует (примечание  chiral chiral указывает на хиральное соединение). указывает на хиральное соединение).
В соответствии с одним из аспектов настоящего изобретения предлагается соединение формулы (I):

в которой R1, R2, R3, R4, n, m, p и s являются такими, как указано ниже.
В соответствии с другим аспектом настоящего изобретения предлагается фармацевтическая композиция, включающая соединение формулы (I) или его фармацевтически приемлемые соли и фармацевтически приемлемый носитель и/или вспомогательное вещество.
Кроме того, в соответствии с еще одним аспектом настоящего изобретения предлагается способ лечения или профилактики заболеваний, которые связаны с активацией фермента гликогенсинтаза, способ включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I).
Эти и другие признаки, особенности и преимущества настоящего изобретения иллюстрируются в описании настоящего изобретения и понятны из формулы изобретения.
Если не указано иное, то для того, чтобы показать и установить значение и объем различных терминов, используемых для описания изобретения в тексте настоящей заявки, используются следующие определения.
В тексте настоящей заявки термин “низший” используют для обозначения группы, состоящей из от одного до семи атомов углерода, предпочтительно от одного до четырех атомов углерода
Термин “галоген” относится к фтору, хлору, брому и иоду, предпочтительно к фтору и хлору.
Термин “алкил”, по отдельности или в комбинации с другими группами, относится к моновалентному насыщенному алифатическому радикалу с разветвленной или линейной цепью, содержащему от одного до двадцати атомов углерода, предпочтительно от одного до шестнадцати атомов углерода, более предпочтительно от одного до десяти атомов углерода.
Алкильные группы могут быть необязательно замещенными, например, такими радикалами, как галоген, гидрокси, низший алкокси, (низший алкокси)-карбонил, NH2, N(H, низший алкил) и/или N(низший алкил)2. Незамещенные алкильные группы являются предпочтительными.
Термин “низший алкил”, по отдельности или в комбинации с другими группами, относится к моновалентному алкильному радикалу с разветвленной или линейной цепью, содержащему от одного до семи атомов углерода, предпочтительно от одного до четырех атомов углерода. Значение этого термина дополнительно иллюстрируют такие радикалы, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил и подобные радикалы. Группа  низший алкил низший алкил может быть необязательно замещенной таким образом, как описано выше в отношении термина “алкил”. Незамещенные низшие алкильные группы являются предпочтительными. может быть необязательно замещенной таким образом, как описано выше в отношении термина “алкил”. Незамещенные низшие алкильные группы являются предпочтительными.
Термин “алкокси” относится к группе R’-O-, в которой R’ представляет собой алкил. Термин “низший алкокси” относится к группе R’-O-, в которой R’ представляет собой низший алкил. Примерами групп  низший алкокси низший алкокси являются, например, группы метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и гексилокси. Группы являются, например, группы метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и гексилокси. Группы  алкокси алкокси и и  низший алкокси низший алкокси могут быть необязательно замещенными таким образом, как описано выше в отношении термина “алкил”. Незамещенные группы могут быть необязательно замещенными таким образом, как описано выше в отношении термина “алкил”. Незамещенные группы  алкокси алкокси и и  низший алкокси низший алкокси являются предпочтительными. являются предпочтительными.
Термин “аминокислота” относится как к природным аминокислотам, к их энантиомерам, так и к синтетическим аминокислотам. Природные аминокислоты включают аланин (Ala), аргинин (Arg), аспарагин (Asn), аспарагиновую кислоту (Asp), цистеин (Cys), глутамин (Gin), глутаминовую кислоту (Glu), глицин (Gly), гистидин (His), изолейцин (Ilе), лейцин (Leu), лизин (Lys), метионин (Met), фенилаланин (Phe), пролин (Pro), серин (Ser), треонин (Thr), триптофан (Trp), тирозин (Tyr) и валин (Val). Синтетические аминокислоты включают, но не ограничиваясь указанным, азетидинкарбоновую кислоту, 2-аминоадипиновую кислоту, 3-аминоадипиновую кислоту, бета-аланин, 2-аминомасляную кислоту, 4-аминомасляную кислоту, 6-аминокапроновую кислоту, 2-аминогептановую кислоту, 2-аминоизомасляную кислоту, 3-аминоизомасляную кислоту, 2-аминопимелиновую кислоту, 2,4 диаминоизомасляную кислоту, 2,2′-диаминопимелиновую кислоту, 2,3-диаминопропионовую кислоту, N-этилглицин, N-этиласпарагин, гидроксилизин, алло-гидроксилизин, 3-гидроксипролин, 4-гидроксипролин, алло-изолейцин, N-метилглицин, N-метилизолейцин, N-метилвалин, норвалин, норлейцин, орнитин и пипеколиновую кислоту (пиперидин-N-карбоновую кислоту).
Термин “арил” относится к ароматической карбоциклической или гетероциклической кольцевой системе, предпочтительно содержащей от 5 до 6 атомов углерода. Примеры арильных групп включают фенил, фуранил, тиофенил, пиридинил, тиазолил и оксазолил, эти группы могут быть необязательно моно- или мультизамещенными радикалами низший алкил, низший алкокси, галоген, CN, CF3, гидрокси, NO2, NH2, N(H, низший-алкил) и/или N(низший-aлкил)2. Предпочтительными заместителями являются низший алкил, низший алкокси, галоген и/или NO2.
Термин “гетероцикл” относится к 5- или 6-членной кольцевой системе, которая может включать 1, 2 или 3 атома, выбранных из азота, кислорода и/или серы, например, такие как тетрагидропиридин, дигидрофуран, дигидропиран, фурил, пирролил, пиридил, 1,2-, 1,3- и 1,4-диазинил, тиенил, оксазолил, оксадиазолил, изооксазолил, тиазолил, изотиазолил или имидазолил. Гетероциклическая группа может быть необязательно замещенной арильной группой или быть замещенной таким образом, как указано выше в отношении термина “арил”.
Термин “фармацевтически приемлемые соли” относится к солям соединений формулы (I), образованным с неорганическими или органическими кислотами, например, такими как хлороводородная кислота, бромоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, малеиновая кислота, уксусная кислота, фумаровая кислота, янтарная кислота, винная кислота, метансульфоновая кислота, n-толуолсульфоновая кислота, и подобными кислотами, которые нетоксичны для живых организмов. Предпочтительными солями, образованными с кислотами, являются формиаты, малеинаты, цитраты, гидрохлориды, гидробромиды и соли метансульфоновой кислоты.
Этот термин также относится к солям – карбоксилатам, содержащим органические и неорганические катионы, например, такие как катионы щелочных и щелочноземельных металлов (например, катионы лития, натрия, калия, магния, бария и цезия); аммоний; или органические катионы, например дибензиламмоний, бензиламмоний, 2-гидроксиэтиламмоний, бис(2-гидрокси-этил)аммоний, фенилэтилбензиламмоний подобные катионы. Другие катионы, которые подразумевает вышеуказанный термин, включают протонированную форму прокаина, хинина и N-метилглюкоз амина, и протонированные формы аминокислот основного характера, например, таких как глицин, орнитин, гистидин, фенилглицин, лизин и аргинин.
Термин “отщепляемая группа” относится к группе, которая удаляется или замещается в процессе реакции. Примерами отщепляемых групп являются галоген, мезилат и тозилат.
Более конкретно, настоящее изобретение относится к соединениям формулы (I):

в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4;
p означает 0, 1 или 2, и s означает 0, 1 или 2;
или к их фармацевтически приемлемым солям,
при условии, что
а) в том случае, когда Ar представляет собой фуранил, p и s означают ноль, и соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой тиофенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
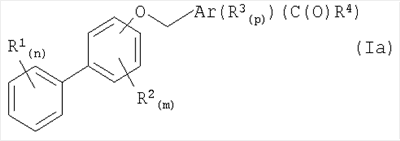
В соответствии с другим вариантом осуществления настоящее изобретение относится к соединениям формулы (Iа):
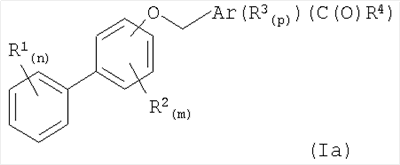
в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметил, галоген, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1,2,3 или 4; и
p означает 0, 1 или 2;
или к их фармацевтически приемлемым солям, при условии, что
а) в том случае, когда Ar представляет собой фуранил, p означает ноль и соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой тиофенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к соединениям формулы (I) или формулы (Iа), в которой R1, R2 и R3 представляют собой атомы водорода.
В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к соединениям формулы (I) или формулы (Iа), как определено выше, где R4 представляет собой гидроксильную группу.
В дополнение, соединения формулы (I) или формулы (Iа), как определено выше, где R4 представляет собой остаток пролина, присоединенный через атом азота, представляют собой еще один предпочтительный вариант осуществления настоящего изобретения.
Соединения формулы (I) или формулы (Iа), в которой Ar представляет собой арил, предпочтительно фенильную группу, представляют собой еще один предпочтительный вариант осуществления настоящего изобретения.
Другой предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы (I) или формулы (Iа), как определено выше, в которой Ar представляет собой фуранил.
Еще один предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы (I) или формулы (Iа), как определено выше, в которой Ar представляет собой тиофенил.
Кроме того, еще один предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы (I) или формулы (Ia), как определено выше, в которой Ar представляет собой тиазолил.
Соединения формулы (I) или формулы (Iа) представляют предпочтительный вариант осуществления настоящего изобретения, а фармацевтически приемлемые соли соединений формулы (I) или формулы (Iа) по отдельности также представляют предпочтительные варианты осуществления настоящего изобретения.
Предпочтительными соединениями общей формулы (I) или формулы (Iа) являются такие соединения, которые выбирают из группы, состоящей из следующих соединений:
3-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-3-илоксиметил)бензойная кислота;
3-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
3-(4′-бромбифенил-4-илоксиметил)бензойная кислота;
3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота;
5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-бромбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
2-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
2-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
2-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
2-(бифенил-4-илоксиметил)бензойная кислота;
5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновая кислота;
6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-3-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-бром-бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
4-(бифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота;
(рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота; и
1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота.
Необходимо отметить, что соединения общей формулы (I) или формулы (Iа) согласно настоящему изобретению могут быть переведены в производные по функциональным группам, с получением при этом производных, которые способны претерпевать обратное превращение в исходное соединение in vivo.
Соединения формулы (I) или формулы (Iа) могут быть получены с использованием методов, приведенных ниже, с использованием методов, указанных в примерах, и с использованием аналогичных методов. Подходящие условия проведения взаимодействия на отдельных стадиях реакции известны специалисту в данной области техники. Исходные вещества являются либо коммерчески доступными, либо могут быть получены с использованием методов, аналогичных методам, приведенным ниже, или представленным в примерах, или известных из предшествующего уровня техники.
В соответствии с одним из вариантов осуществления настоящее изобретение относится к способу получения соединений формулы I (или формулы Iа), указанный способ включает:
взаимодействие соединения формулы (II):
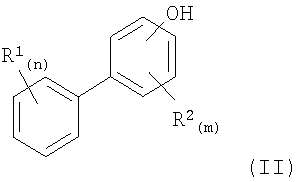
в которой R1, R2, m и n являются такими, как определено выше в тексте настоящей заявки,
в присутствии основания с соединением формулы (III):

в которой Ar, R3, p и s являются такими, как определено выше в тексте настоящей заявки, LG представляет собой отщепляемую группу, например, такую как хлор, бром или иод, и R5 представляет собой защитную группу,
и последующее отщепление защитной группы с получением при этом соединения формулы (I):

в которой R4 означает гидрокси, и Ar, R1-R3, m, n, p и s являются такими,
как определено выше в тексте настоящей заявки, и
необязательно взаимодействие этого соединения со сложным эфиром аминокислоты в присутствии EDC (1-3(диметиламинопропил)-3-этилкарбодиимид гидрохлорид) и DMAP (4-диметиламинопиридин) и последующее отщепление сложноэфирной группы, с получением при этом соединения формулы I, в которой R4 представляет собой остаток аминокислоты, присоединенный через атом азота остатка аминокислоты.
В соответствии с другим вариантом осуществления настоящее изобретение относится к способу, который описан выше, при условии, что не получают соединения:
S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновая кислота,
5-(бифенил-4-илоксиметил)фуран-2-карбоновая кислота,
3-(бифенил-4-илоксиметил)бензойная кислота,
2-(бифенил-3-илоксиметил)бензойная кислота и
5-(бифенил-4-илоксиметил)тиофен-2-карбоновая кислота.
Как описано выше, соединения формулы (I) или формулы (Iа) согласно настоящему изобретению могут быть использованы в качестве лекарственных средств для лечения и/или профилактики заболеваний, опосредованных активацией фермента гликогенсинтаза. Предпочтительно соединения согласно настоящему изобретению могут быть использованы для лечения диабета типа 2.
Таким образом, настоящее изобретение также относится к фармацевтическим композициям, включающим соединение, как определено выше, и фармацевтически приемлемый носитель и/или вспомогательное вещество.
В соответствии с одним из вариантов осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I):

в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемую соль; и
фармацевтически приемлемый носитель и/или вспомогательное вещество.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (Iа):

в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемую соль; и
фармацевтически приемлемый носитель и/или вспомогательное вещество.
В соответствии с еще одним предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I):

в которой
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемую соль; при условии, что
а) в том случае, когда Ar представляет собой фуранил, p означает ноль, и соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой фенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
В соответствии с еще одним предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 представляют собой атомы водорода;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемую соль; и
фармацевтически приемлемый носитель и/или вспомогательное вещество.
В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где n означает 1, и R1 выбирают из группы, состоящей из следующих радикалов: метильная группа, метоксигруппа, галоген и нитрогруппа.
Особенно предпочтительной является фармацевтическая композиция, включающая соединение формулы (I), как определено выше, где n означает 1, и R1 представляет собой хлор или бром.
В соответствии с еще одним предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где m означает 1, и R2 представляет собой атом хлора.
Согласно еще одному предпочтительному варианту осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где p означает 0.
В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где Ar выбирают из группы, состоящей из фенила, фуранила, тиофенила, пиридинила и тиазолила.
Согласно еще одному предпочтительному варианту осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где R4 представляет собой гидроксильную группу.
В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где R4 представляет собой остаток пролина, присоединенный к соединению через атом азота.
Согласно еще одному особенно предпочтительному варианту осуществления настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), как определено выше, где соединение выбирают из группы, состоящей из следующих соединений:
3-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-3-илоксиметил)бензойная кислота;
3-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
3-(4′-бромбифенил-4-илоксиметил)бензойная кислота;
3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-4-илоксиметил)бензойная кислота;
2-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
2-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
2-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
2-(бифенил-4-илоксиметил)бензойная кислота;
5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-бром-бифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновая кислота;
5-(бифенил-4-илоксиметил)тиофен-2-карбоновая кислота;
6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-3-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-бром-бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
4-(бифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-L-пирролидин-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота;
(рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота; и
1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота.
Кроме того, согласно еще одному варианту осуществления настоящее изобретение относится к способу лечения или профилактики заболевания, опосредованного активацией фермента гликогенсинтаза, способ включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения следующей формулы (I):

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли.
В соответствии с предпочтительным вариантом осуществления заболевание представляет собой диабет.
Согласно другому варианту осуществления настоящее изобретение относится к способу лечения или профилактики заболевания, опосредованного активацией фермента гликогенсинтаза, способ включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения следующей формулы (Iа):
где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к способу лечения или профилактики диабета, способ включает введение пациенту, нуждающемуся в этом, терапевтически эффективного количества соединения следующей формулы (Iа):

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли.
В соответствии с другим вариантом осуществления настоящее изобретение относится к соединению формулы (I):

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли;
для применения в качестве лекарственного средства.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к соединению формулы (Iа):

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли;
для применения в качестве лекарственного средства.
Кроме того, согласно еще одному варианту осуществления настоящее изобретение относится к применению соединения формулы I:

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли;
для получения лекарственных средств для лечения или профилактики заболеваний, опосредованных активацией фермента гликогенсинтаза и к применению таких лекарственных средств.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к применению соединения формулы (Iа):

где
Ar представляет собой ароматическую карбоциклическую или гетероциклическую кольцевую систему;
R1, R2 и R3 независимо выбирают из группы, состоящей из низшего алкила, низшего алкокси, трифторметила, галогена, гидрокси, амино, алкиламино, диалкиламино, циано и нитро;
R4 представляет собой гидрокси или остаток аминокислоты, присоединенный через атом азота остатка аминокислоты;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
p означает 0, 1 или 2;
или его фармацевтически приемлемой соли;
для получения лекарственных средств для лечения или профилактики заболевания, опосредованного активацией фермента гликогенсинтаза и к применению таких лекарственных средств.
Более предпочтительно настоящее изобретение относится к применению соединения, выбранного из группы, состоящей из следующих соединений:
3-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-3-илоксиметил)бензойная кислота;
3-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
3-(4′-бром-бифенил-4-илоксиметил)бензойная кислота;
3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-4-илоксиметил)бензойная кислота;
2-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
2-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
2-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
2-(бифенил-4-илоксиметил)бензойная кислота;
5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-бром-бифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновая кислота;
5-(бифенил-4-илоксиметил)тиофен-2-карбоновая кислота;
6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота;
2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-3-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-бром-бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
4-(бифенил-4-илоксиметил)тиазол-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-L-пирролидин-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота;
(рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота; и
1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота, для получения лекарственных средств для лечения или профилактики заболевания, опосредованного активацией фермента гликогенсинтаза, и к применению таких лекарственных средств.
В соответствии с предпочтительным вариантом осуществления настоящее изобретение относится к применению соединения формулы (I) для получения лекарственных средств для лечения или профилактики диабета.
Соединения формулы I или формулы (Iа) и/или их фармацевтически приемлемые соли могут быть использованы в качестве лекарственных средств, например, в виде фармацевтических препаратов для энтерального, парентерального или местного применения. Фармацевтические препараты могут быть введены перорально, например, в виде таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Кроме того, введение эффективно может быть осуществлено ректально, например, в виде суппозиториев, парентерально, например, в виде растворов для инъекций или для вливания, или местно, например, в виде мазей, кремов или масел. Пероральное введение является предпочтительным.
Получение фармацевтических препаратов может быть осуществлено таким образом, как известно специалисту в данной области техники, посредством введения соединения формулы (I) или формулы (Iа) и/или их фармацевтически приемлемых солей, необязательно в комбинации с другим терапевтически значимым соединением в состав фармацевтической формы вместе с подходящим нетоксичным, инертным, терапевтически совместимым твердым или жидким носителем и, если необходимо, с обычными фармацевтическими вспомогательными веществами.
Подходящие вещества носители представляют собой не только неорганические вещества, но и органические вещества. Так, в качестве носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул могут быть использованы, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и тому подобные соединения. Подходящие носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобные соединения. Однако в зависимости от природы активного соединения в случае мягких желатиновых капсул носитель может и не использоваться. Подходящие носители для получения растворов и сиропов представляют собой, например, воду, полиолы, сахарозу, инвертный сахар и тому подобные соединения. Подходящие носители для получения растворов для инъекций представляют собой, например, воду, спирты, полиолы, глицерин и растительные масла. Подходящие носители для суппозиториев представляют собой, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы. Подходящие носители для препаратов, предназначенных для местного применения, представляют собой глицериды, полусинтетические и синтетические глицериды, гидрогенизированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы.
В качестве фармацевтических вспомогательных веществ могут быть использованы обычные стабилизаторы, консерванты, агенты, улучшающие смачиваемость, эмульгаторы, агенты, улучшающие консистенцию, агенты, улучшающие вкус и запах, соли для регулирования осмотического давления, буферы, солюбилизаторы, подкрашивающие агенты, маскирующие агенты или антиоксиданты.
Дозировка соединений формулы (I) или формулы (Iа) может варьироваться в широких пределах в зависимости от вида заболевания, подлежащего контролю, возраста и индивидуального состояния пациента и способа введения и будет, безусловно, регулироваться в зависимости от индивидуальных требований в каждом конкретном случае. Для взрослых пациентов следует рассматривать дневную дозировку, которая составляет приблизительно от 1 до 1000 мг, в частности приблизительно от 1 до 100 мг. В зависимости от степени выраженности симптомов заболевания и определенного фармакокинетического профиля соединение можно вводить в виде одной или нескольких дневных доз, например вводить от одной до четырех единичных дозировок.
Фармацевтически препараты подходящим образом содержат приблизительно 1-500 мг, предпочтительно 1-100 мг соединения формулы (I) или формулы (Iа).
Приведенные ниже примеры служат для более подробной иллюстрации настоящего изобретения. Однако предполагается, что эти примеры не ограничивают каким-либо образом объем настоящего изобретения.
Соединения согласно настоящему изобретению могут быть получены с использованием любых известных средств. Подходящие способы синтеза этих соединений приводятся в примерах. Как правило, соединения формулы (I) или формулы (Iа) могут быть получены согласно одному из приведенных ниже методов синтеза: посредством нуклеофильного замещения или посредством конденсации Сузуки. Источники исходных веществ для проведения этих реакций описаны ниже.
Нуклеофильное замещение
Как показано на схеме 1, соединения согласно настоящему изобретению могут быть получены посредством нуклеофильного замещения отщепляемой группы LG соединения формулы 5 при воздействии гидроксибиарила формулы 4 с получением при этом соединения формулы 6, в которой R5 представляет собой защитную группу, обычно используемую для защиты карбоксильной группы. Защитную группу затем отщепляют, получая при этом соединение согласно настоящему изобретению, формулы 1, где R4 представляет собой гидрокси.
Специалисту в области органического синтеза известно множество защитных групп R5. Например, некоторые подходящие защитные группы перечислены в: “Protective Groups in Organic Synthesis” [Greene, T.W., Wuts, P.G.M., 2nd Edition, John Wiley & Sons, N.Y. 1991]. Предпочтительными защитными группами являются такие группы, которые совместимы с условиями проведения взаимодействий для получения соединений согласно настоящему изобретению. Примерами таких защитных групп являются группы сложных низших алкиловых эфиров с линейной или разветвленной цепью (например, группа метилового (R5=CH3), этилового (R=CH2CH3) или трет-бутилового (R5=С(CH3)3) сложного эфира) или бензилового сложного эфира (R5=CH2C6H5).
Схема 1
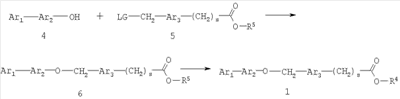
Нуклеофильное замещение отщепляемой группы LG в соединении 5 может быть осуществлено с использованием любых известных средств. Например, в том случае, когда LG представляет собой такую отщепляемую группу, как хлор, бром или иод, взаимодействие удобно проводить посредством обработки соединения 5 соединением 4 в присутствии основания, например, такого как гидрид щелочного металла (например, гидрида натрия) или карбонат щелочного металла (например, карбонат калия) в инертном растворителе (например, в N,N-диметилформамиде) при температуре между приблизительно комнатной температурой и приблизительно 100 градусами.
Превращение соединения 6, в котором R5 представляет собой защитную группу, обычно используемую для защиты карбоксильной группы, в соединение 1 посредством удаления защитной группы для карбоксильной группы проводят в условиях, хорошо известных специалисту в области органической химии, различные возможные условия описаны в: “Protective Groups in Organic Synthesis” [Greene, T.W., Wuts, P.G. M., 2nd Edition, John Wiley & Sons, N.Y. 1991]. Например, в том случае, когда R представляет собой метил или этил, взаимодействие удобно проводить посредством обработки соединения одним эквивалентом гидроксида щелочного металла, например, такого как гидроксид калия, гидроксид натрия или гидроксид лития, предпочтительно гидроксид лития, в подходящем растворителе, например, таком как смесь тетрагидрофурана, метанола и воды. Взаимодействие можно проводить при температуре от приблизительно 0 градусов и до приблизительно комнатной температуры, предпочтительно при приблизительно комнатной температуре. В качестве другого примера, в том случае, когда R5 представляет собой группу, которая отщепляется в кислой среде, например, такую как трет-бутильная группа, сложный эфир может быть подвергнут обработке сильной неорганической кислотой, например галогенводородной кислотой, например, такой как хлороводородная кислота или бромоводородная кислота, или сильной органической кислотой, например, такой как галогенированная алканкарбоновая кислота, такая как трифторуксусная кислота, и подобными кислотами. Взаимодействие удобно проводить в присутствии инертного органического растворителя (например, такого как дихлорметан) при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. В качестве заключительного (но не ограничивающего) примера, в том случае, когда R5 представляет собой группу, которая может быть подвергнута отщеплению посредством каталитического гидрирования, и при дополнительном условии, что остальная часть молекулы стабильна в таких условиях, взаимодействие может быть проведено посредством гидрирования в присутствии катализатора на основе благородного металла, например, такого как палладий на углероде в присутствии инертного растворителя (например, в присутствии спирта, такого как этанол) при приблизительно комнатной температуре и при атмосферном давлении.
Конденсация Сузуки (Suzuki)
Как показано на схеме 2, соединения согласно настоящему изобретению могут быть получены в результате последовательности реакций, начинающейся с нуклеофильного замещения отщепляемой группы LG соединения формулы 5 при воздействии соединения формулы 7, в котором Х представляет собой группу, которая может выполнять функцию отщепляемой группы в реакциях конденсации, катализируемых катализаторами на основе благородных металлов, например, таких как реакция Сузуки или реакция Штилле (Stille), с получением при этом соединения формулы 9, в которой R5 представляет собой защитную группу, обычно используемую для защиты карбоксильной группы. Соединение формулы 9 затем может быть подвергнуто взаимодействию с металлоорганическим реагентом формулы 10 (например, таким как бороновая кислота или оловоорганический реагент) с использованием катализаторов на основе благородных металлов и получением при этом биарильного соединения формулы 6. Защитную группу затем отщепляют, получая при этом соединение согласно настоящему изобретению, соответствующее формуле 1, где R4 представляет собой группу гидрокси.
Множество различных защитных групп R5 известно специалисту в области органического синтеза. Например, некоторые подходящие защитные группы перечислены в: “Protective Groups in Organic Synthesis” [Greene, T.W., Wuts, P.G. M., 2nd Edition, John Wiley & Sons, N.Y. 1991]. Предпочтительными защитными группами являются такие группы, которые совместимы с условиями реакции, используемыми для получения соединений согласно настоящему изобретению. Примерами таких защитных групп являются группы сложных низших алкиловых эфиров с линейной или разветвленной цепью (например, группы метилового (R=CH3), этилового (R=CH2CH3) или трет-бутилового (R5=С(CH3)3) сложных эфиров) или группа бензилового эфира
(R5=СCH2C6H5).
Схема 2
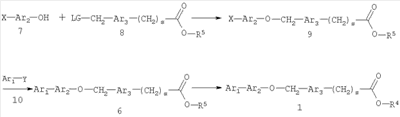
Нуклеофильное замещение отщепляемой группы LG в соединении 5 может быть осуществлено любыми общепринятыми методами. Например, в том случае, когда LG представляет собой такую отщепляемую группу, как хлор, бром или иод, взаимодействие удобно проводить посредством обработки соединения 5 соединением 7 в присутствии основания, например, такого как гидрид щелочного металла (например, гидрид натрия) или карбонат щелочного металла (например, карбонат калия) в инертном растворителе (например, таком как N,N-диметилформамид) при температуре между приблизительно комнатной температурой и приблизительно 100 градусами.
Взаимодействие соединения формулы 9, где Х представляет собой отщепляемую группу, например, такую как иод, бром или трифлат, с соединением формулы 10, в котором Y представляет собой группу бороновой кислоты, группу сложного эфира – бороната, триметилолово или три-н-бутилолово, с получением при этом соединения формулы 6, может быть осуществлено в условиях конденсации Сузуки или конденсации Штилле, которые хорошо известны обычному специалисту в данной области техники. Например, реакцию удобно проводить посредством взаимодействия соединения формулы 9, где Х представляет собой иод, с соединением формулы 10, где Y представляет В(ОН)2, в подходящем инертном растворителе, например, таком как полярный апротонный растворитель (например, N,N-диметилформамид) или простой эфир (например, диоксан) или вода, в присутствии каталитического количества комплекса палладия(0) (например, такого как тетракис(трифенил-фосфин)палладий(0)) или в присутствии соединения, которое может быть восстановлено in situ с получением при этом палладия(0) (например, такого как палладий(II) ацетат или бис(трифенилфосфин)-палладий(II) хлорид), при необязательном дополнительном присутствии каталитического количества фосфинового лиганда, например, такого как три-о-толилфосфин или три-трет-бутилфосфин, и также в присутствии неорганического основания, например, такого как карбонат щелочного металла, бикарбонат щелочного металла или фосфат щелочного металла (например, в присутствии фосфата калия или карбоната натрия) при температуре между приблизительно комнатной температурой и приблизительно 100 градусами и предпочтительно при температуре между приблизительно комнатной температурой и приблизительно 50 градусами.
Превращение соединения 6, в котором R5 означает защитную группу, обычно используемую для защиты карбоксильной группы, в соединение 1 посредством удаления защитной карбоксильной группы проводят с использованием таких условий реакции, которые хорошо известны специалисту в области органического синтеза, и множество вариантов приведено в: “Protective Groups in Organic Synthesis” [Greene, T.W., Wuts, P.G. M., 2nd Edition, John Wiley & Sons, N.Y. 1991]. Например, в том случае, когда R представляет собой метил или этил, взаимодействие удобно проводить посредством обработки соединения одним эквивалентом гидроксид щелочного металла, например, такого как гидроксид калия, гидроксид натрия или гидроксид лития, предпочтительно с использованием гидроксида лития, в подходящем растворителе, например, таком как смесь тетрагидрофурана, метанола и воды. Взаимодействие можно проводить при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. В качестве другого примера, в том случае, когда R5 представляет собой группу, которая может быть подвергнута отщеплению в кислотных условиях, например, такую как трет-бутильная группа, сложный эфир может быть обработан сильной неорганической кислотой, например галогеноводородной кислотой, такой как хлороводородная кислота или бромоводородная кислота, или может быть обработан сильной органической кислотой, например, такой как галогенированная алканкарбоновая кислота, например трифторуксусной кислотой и подобными кислотами. Взаимодействие удобно проводить в присутствии инертного органического растворителя (например, такого как дихлорметан) и при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. В качестве заключительного (но не ограничивающего) примера в том случае, когда R5 представляет собой группу, которая может быть отщеплена посредством каталитического гидрирования, и при дополнительном условии, что остальная часть молекулы стабильна в таких условиях, взаимодействие может быть проведено посредством гидрирования в присутствии катализатора на основе благородного металла, например, такого как палладий на углероде, в присутствии инертного растворителя (например, в присутствии спирта, такого как этанол) при приблизительно комнатной температуре и при атмосферном давлении.
Исходные вещества: соединения формулы 4
Многие соединения формулы 4 являются известными соединениями и могут быть синтезированы в соответствии с методиками, описанными в литературе. Некоторые примеры приведены в таблице.
| Химическое наименование |
Ссылка |
| 3-Аллилбифенил-4-ол |
White et al. J. Amer. Chem. Soc. 1958, 80, 3271 |
| 4′-Бромбифенил-4-ол |
Bell et al. J. Chem. Soc. 1927, 1131 |
| 2-(4-Бромфенил)пиримидин-5-ол |
Kizner, Т.A. et al. Khim. Geterotsikl. Soedin. 1990, 801 |
| 4′-Бутоксибифенил-4-ол |
Pollino, Joel M. Synthesis 2002, 1277 |
| 3-трет-Бутилбифенил-4-ол |
Davis В.R. et al. J. Chem. Soc. Perkin Trans. 1 1982, 1499 |
| 5-(4-отреот-Бутилфенил)тиофен-3-ол |
Hunter, G.A. et al. J. Chem. Soc. Perkin Trans. 11995,1209 |
| 2-Хлорбифенил-4-ол |
Mattingly, P.G. et al. US 5,145,790 |
| 3-Хлорбифенил-4-ол |
Burckhalter et al. J. Am. Chem. Soc. 1946, 68, 1894 |
| 4′-Хлорбифенил-4-ол |
Abernethy et al. J. Am. Chem. Soc. 1943, 65, 1464 |
| 2′,5′-Дихлорбифенил-4-ол |
Reich, I.L. et al. J. Org. Chem. 1981, 46, 3721 |
| 3,4′-Дихлорбифенил-4-ол |
Abernethy et al. J. Am. Chem. Soc. 1943, 65, 1464 |
| 3,5-Дихлорбифенил-4-ол |
Colbert et al. J. Am. Chem. Soc. 1934, 56, 2128 |
| 3,2′-Диэтилбифенил-4-ол |
Schroetter, E. et al. Pharmazie 1974, 29, 374 |
| 2′,4′-Дифторбифенил-4-ол |
Hannah, J. et al. J. Med. Chem. 1978, 21, 1093 |
| 4′-Этилбифенил-4-ол |
Leigh, Т. et al. GB 1121722 |
| 4′-Фторбифенил-4-ол |
Takatsu, H. et al. Mol. Cryst. Liq. Cryst. 1984, 108, 157 |
| 4′-Фтор-3-метилбифенил-4-ол |
Hannah, J. et al. J. Med. Chem. 1978, 21, 1093 |
| 6-(4-Фторфенил)пиридин-3-ол |
Walford, G.L. et al. J. Med. Chem. 1971, 14,339 |
| 4′-Гидроксибифенил-4-карбальдегид |
Revell, J.D. Org. Lett. 2002, 4, 3071 |
| 1-(4′-Гидроксибифенил-4-ил)-этанон |
Boy, P.J. Org. Chem. 1994, 59, 4482 |
| 4′-Иодбифенил-4-ол |
Angeletti et al. Gazz. Chim. Ital. 1928, 58, 634 |
| 4′-Метоксибифенил-4-ол |
Sakurai, H. et al. J. Org. Chem. 2002, 67, 2721 |
| 5-(4-Метоксифенил)тиофен-3-ол |
Pinkin, L.D. et al. Chem. Heterocycl. Compd. (Engl. Transl.) 1987, 23, 345 |
| 3-Метилбифенил-4-ол |
Colbert et al. J. Am. Chem. Soc. 1946, 68, 270 |
| 4′-Метилбифенил-4-ол |
Colbert et al. J. Am. Chem. Soc. 1946, 68, 270 |
| 2′-Нитробифенил-4-ол |
Schultz et al. Justus Liebigs Ann. Chem. 1881, 209, 351 |
| 3-Нитробифенил-4-ол |
Behre, H. WO 0177061 |
| 4′-Нитробифенил-4-ол |
Bell et al. J. Chem. Soc. 1926, 3047 |
| 2-(4-Нитрофенил)пиримидин-5-ол |
Kizner, Т.A. et al. Khim. Geterotsikl. Soedin. 1990, 801 |
| 6-Фенилпиридин-3-ол |
Kurita, J. Chem. Pharm. Bull. 1987, 35, 3166 |
| 2-Фенилпиримидин-5-ол |
Maurer, F. et al. US 5,010,193 |
| 5-Фенил-тиофен-3-ол |
Friedlaender et al. Chem. Ber. 1912, 45, 3391 |
| 3,5,4′-Трихлорбифенил-4-ол |
Abemethy et al. J. Am. Chem. Soc. 1943, 65, 1464 |
| 4′-Трифторметилбифенил-4-ол |
Le Barny, Р. et al. Mol. Cryst. Liq. Cryst. 1985, 127, 413 |
| 2′,4′,6′-Триметилбифенил-4-ол |
Haefelinger, G. et al. Chem. Ber. 1978, 111, 1323 |
В дополнение, многие соединения формулы 4 являются коммерчески доступными, включая следующие соединения:
| Химическое наименование |
Поставщик |
| 2-Амино-4-фенилфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Бром-4-фенилфенол |
фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 4-Хлор-4′-гидроксибифенил |
фирма  TCI America TCI America , г.Портленд, Орегон (штат США) , г.Портленд, Орегон (штат США) |
| 4,4′-Дигидроксибифенил |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3,4′-Диметилбифенил-4-ол |
фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 2-Фторбифенил-4-ол |
фирма  Bionet Research Ltd. Bionet Research Ltd. , Корнуолл, Великобритания , Корнуолл, Великобритания |
| 4-Фтор-4′-гидроксибифенил |
фирма  Apin Chemicals Ltd. Apin Chemicals Ltd. , Эбингдон, Оксон, Великобритания , Эбингдон, Оксон, Великобритания |
| 4-Гидрокси-2′-нитробифенил |
фирма  TCI America TCI America , г.Портленд, Орегон (штат США) , г.Портленд, Орегон (штат США) |
| 4-Гидрокси-4′-аминобифенил |
фирма  Apin Chemicals Ltd. Apin Chemicals Ltd. , Эбингдон, Оксон, Великобритания , Эбингдон, Оксон, Великобритания |
| 4′-Гидрокси-4-бифенилкарбонитрил |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4′-Гидрокси-4-бифенилкарбоновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Гидрокси-4′-метоксибифенил |
фирма  TCI America TCI America , г.Портленд, Орегон (штат США) , г.Портленд, Орегон (штат США) |
| 4-Гидрокси-4′-нитробифенил |
фирма  TCI America TCI America , г.Портленд, Орегон (штат США) , г.Портленд, Орегон (штат США) |
| 2-Иод-4-фенилфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-(4′-Иодфенил)фенол |
фирма  Apin Chemicals Ltd. Apin Chemicals Ltd. , Эбингдон, Оксфордшир, Великобритания , Эбингдон, Оксфордшир, Великобритания |
| 4-(4-Метилфенил)фенол |
фирма  Maybridge pie Maybridge pie , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 4′-Гидроксибифенил-4-карбоновая кислота, метиловый эфир |
фирма  Bionet Research Ltd. Bionet Research Ltd. , Корнуолл, Великобритания , Корнуолл, Великобритания |
| 2-Нитро-4-фенилфенол |
фирма  Lancaster Synthesis Ltd. Lancaster Synthesis Ltd. , Ланкашир, Великобритания , Ланкашир, Великобритания |
| 4-Фенилфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
Соединения формулы 4, известные из литературы, могут быть получены с использованием реакций, которые сами по себе известны. Например, эти соединения могут быть подходящим образом получены в соответствии со схемой 3.
Схема 3
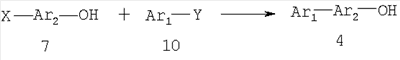
Взаимодействие соединения формулы 7, где Х означает отщепляемую группу, такую как иод, бром, хлор или трифлат, с соединением формулы 10, где Y означает группу бороновой кислота, группу сложного эфира – бороната, триметилолово или три-н-бутил-олово, с получением при этом соединения формулы 6 может быть осуществлено в условиях конденсации Сузуки или конденсации Штилле, которые хорошо известны обычному специалисту в данной области техники. Например, взаимодействие соединения формулы 7, где X означает иод с соединением формулы 10, где Y означает B(OH)2, удобно проводить в подходящем инертном растворителе, например, таком как полярный апротонный растворитель (например, N,N-диметилформамид) или простой эфир (например, диоксан) или вода, в присутствии каталитического количества комплекса палладия(0) (например, такого как тетракис-(трифенилфосфин)-палладий(0)) или соединения, которое может быть восстановлено in situ с получением при этом соединения палладия(0) (например, такого как палладий(II) ацетат или бис(трифенилфосфин)-палладий(II) хлорид), при необязательном дополнительном присутствии каталитического количества фосфинового лиганда, например три-о-толилфосфин или три-трет-бутилфосфин, и также в присутствии неорганического основания, например карбонат щелочного металла, бикарбонат или фосфат (например, фосфат калия или карбонат натрия), при температуре между приблизительно комнатной температурой и приблизительно 100 градусами и предпочтительно при между приблизительно комнатной температурой и приблизительно 50 градусами. В качестве дополнительных примеров взаимодействие можно проводить в условиях, описанных в: Sakurai, H. et al. J. Org. Chem. 2002, 67, 2721, или взаимодействие можно проводить в условиях, описанных в: Revell, J.D., Ganesan, A. Org. Lett. 2002, 4, 3071.
Исходные вещества: соединения формулы 5
Многие соединения формулы 5, в которых R5 означает защитную группу, обычно используемую для защиты карбоксильной группы, представляют собой известные соединения и могут быть синтезированы в соответствии с методиками, описанными в литературе. Некоторые примеры приведены в таблице.
| Химическое наименование |
Ссылка |
| 3-(Бромметил)фенилуксусная кислота, бензиловый эфир |
A.Dorville et al., J. Med. Chem. 1992, 35, 2551 |
| 4-(Бромметил)фенилуксусная кислота, бензиловый эфир |
К.Shen et al., J. Biol. Chem. 2001, 276, 47311 |
| 2-(Бромметил)фенилуксусная кислота, трет-бутиловый эфир |
С.L.Newton et al., WO 2003011222 |
| 2-(Бромметил)фенилуксусная кислота, этиловый эфир |
A.Peyman et al. US 5242908 |
| 3-(Бромметил)фенилуксусная кислота, этиловый эфир |
S.R.Kasibhatla et al. J. Med. Chem. 2000, 43,1508 |
| 2-(Бромметил)фенилуксусная кислота, метиловый эфир |
J.S.Sawyer et al., J. Med. Chem. 1992, 35, 1200 |
| 2-(Бромметил)фенилуксусная кислота, метиловый эфир |
F.Roussi et al., Tetrahedron 1998, 54, 10363 |
| 3-(Бромметил)фенилуксусная кислота, метиловый эфир |
J.H.Musser et al. J. Med. Chem. 1987, 30, 96 |
| 4-(Бромметил)фенилуксусная кислота, метиловый эфир |
К.С.Santhosh et al. J. Med. Chem. 2001, 44, 703 |
| 3-[3-(Бромметил)фенил]-пропановая кислота, трет-бутиловый эфир |
A.G.Caldwell, N.Whittaker, US 4204068 |
| 3-[4-(Бромметил)фенил]-пропановая кислота, этиловый эфир |
M.Babej et al., DE 2331081 |
| 3-[3-(Бромметил)фенил]-пропановая кислота, метиловый эфир |
N.A.Norman, US 4084058 |
| 3-[4-(Бромметил)фенил]-пропановая кислота, метиловый эфир |
D.V.Patel et al. WO 9623813 |
| 4-(Бромметил)-1Н-1,2,3-триазол-1-уксусная кислота, этиловый эфир |
F.Palacios et al., Org. Prep. Proc. Intl. 1995, 27, 603 |
| 2-Бромметилбензойная кислота, трет-бутиловый эфир |
Ziegler, Т. et al. Tetrahedron Lett. 2001, 42, 569-572 |
| 3-Бромметилбензойная кислота, трет-бутиловый эфир |
Danho, W. et al. US 5,508,437 |
| 2-Бромметилбензойная кислота, метиловый эфир |
Dvomikovs, V. et al. J. Org. Chem. 2002, 67, 2160-2167 |
| 3-Бромметилбензойная кислота, метиловый эфир |
Dvomikovs, V. et al. J. Org. Chem. 2002, 67, 2160-2167 |
| 5-Бромметил-2-фуранкарбоновая кислота, этиловый эфир |
Tsuboi, S. et al. Bull. Chem. Soc. Japan 1987, 60,1807-1812 |
| 5-Бромметил-2-фуранкарбоновая кислота, метиловый эфир |
Wityak, J. et al. Bioorg. Med. Chem. Lett. 1995,5,2097-2100 |
| 6-Бромметилпиридин-2-карбоновая кислота, метиловый эфир |
Scopes, D.I.C. et al. J. Med. Chem. 1992, 35, 490-501 |
| 2-Бромметилтиазол-4-карбоновая кислота, этиловый эфир |
Hallinan, E.A. et al. Bioorg. Med. Chem. 2001, 9, 1-6 |
| 5-Бромметилтиофен-2-карбоновая кислота, метиловый эфир |
Curtin, M.L. et al. J. Med. Chem. 1998, 41, 74-95 |
| 3-Хлорметилбензойная кислота, бензиловый эфир |
Chen, D.-W. et al. J. Chem. Soc. Perkin Trans. 12001, 2796-2803 |
| 2-Хлорметилбензойная кислота, этиловый эфир |
Gadient, F. et al. Helv. Chim. Acta 1962, 45, 1860-1870 |
| 3-Хлорметилбензойная кислота, метиловый эфир |
Matsukawa, Т. et al. Yakugaku Zasshi 1950, 70, 535-537. Chem. Abs. 45:36092 (1951) |
| 4-(Хлорметил)-2-фуран-уксусная кислота, этиловый эфир |
K.-T.Tang et al. Bull. Korean Chem. Soc. 2002, 23, 1333 |
| 5-Хлорметил-2-фуран карбоновая кислота, н-бутиловый эфир |
Bremner, J.G.M. et al. US 2,450,108 |
| 5-Хлорметил-2-фуранкарбоновая кислота, этиловый эфир |
Chakraborty, T.K. et al. Tetrahedron Lett. 2002, 43, 1317-1320 |
| 4-(Хлорметил)-2-фуранпропановая кислота, метиловый эфир |
J.S.U and К.Т.Kang, Bull. Korean Chem. Soc. 1994, 15, 1019 |
| 5-(Хлорметил)-2-фуранпропановая кислота, метиловый эфир |
J.W.Patterson, J.H.Fried, US 3922289 |
| 4-(Хлорметил)-1H-имидазол-1-уксусная кислота, 2-пропениловый эфир, моногидрохлорид |
V.M.Girijavallabhan et al., J. Antibiot, 1986, 39, 1182 |
| 2-(Хлорметил)-5-метил-4-оксазолуксусная кислота, метиловый эфир |
S.Shibata et al., WO 9401433 |
| 5-(Хлорметил)-2-метил-3-тиофенуксусная кислота, метиловый эфир |
M.C.Van Zandt, L.Geraci, Leo. WO 2003044015 |
| 3-(3-Хлорметил-1,2,4-оксадиазол-5-ил)пропионовая кислота, метиловый эфир |
G.Beaton et al., WO 2003015785 |
| 4-(Хлорметил)-2-оксазолпропановая кислота, этиловый эфир |
Y.Momose et al., WO 9803505 |
| 2-(Хлорметил)фенилуксусная кислота метиловый эфир |
К.Hirai et al., WO 9700850 |
| 4-(Хлорметил)фенилуксусная кислота метиловый эфир |
S.H.Park et al. EP 889020 |
| 3-[4-(Хлорметил)фенил]-пропановая кислота, этиловый эфир |
Т.Mase et al. EP 214732 |
| 3-[4-(Хлорметил)фенил]-пропановая кислота, 1-метилэтиловый эфир |
Y.Fukuda et al. WO 9747581 |
| 6-Хлорметилпиридин-2-карбоновая кислота, этиловый эфир |
Fornasier, R. et al. J. Chem. Soc. Perkin Trans. 2 1986, 233-238 |
| 6-(Хлорметил)-3-пиридинпропановая кислота, этиловый эфир |
Т.H.Brown, EP 39989 |
| 5-Хлорметил-тиофен-2-карбоновая кислота, метиловый эфир |
Kozmik, V. et al. Collect. Czech. Chem. Commun. 1992, 57, 1483-1486 |
| 4-(Хлорметил)-2-тиофенуксусная кислота, этиловый эфир |
K.-T.Tang et al. Bull. Korean Chem. Soc. 2002, 23,1333 |
| 4-(Хлорметил)-2-тиофен-уксусная кислота, метиловый эфир |
М.С.Van Zandt, L.Geraci, Leo. WO 2003044015 |
| 4-(Хлорметил)-2-тиофенпропановая кислота, метиловый эфир |
К.Т.Kang and J.S.U, Synth. Commun. 1995, 25, 2647 |
| 5-(Хлорметил)-2-тиофенпропановая кислота, метиловый эфир |
J.W.Patterson, J.H.Fried, US 3922289 |
| 3-Иодметилбензойной кислоты метиловый эфир |
Fuson, R.C. et al. J. Am. Chem. Soc. 1940, 62, 1180-1183 |
| 4-(Иодметил)-2-фурануксусная кислота, этиловый эфир |
K.-T.Tang et al. Bull. Korean Chem. Soc. 2002, 23 ,1333 |
| 5-Иодметил-2-фуранкарбоновая кислота аллиловый эфир |
Greenspan, P.D. et al. J. Med. Chem. 2001, 44, 4524-4534 |
| 4-(Иодметил)-2-тиофенуксусная кислота, этиловый эфир |
K.-T.Tang et al. Bull. Korean Chem. Soc. 2002, 23, 1333 |
| 5-Метансульфонилоксиметил-фуран-2-карбоновая кислота, этиловый эфир |
Summers, J.В., Jr. et al., патент США 5486525 |
В дополнение, некоторые соединения формулы 5 являются коммерчески доступными, включая следующие соединения:
| Химическое наименование |
Поставщик |
| 6-Бромметилпиридин-2-карбоновая кислота, метиловый эфир |
фирма  ChemPacific ChemPacific , г.Балтимор, Мэрилэнд (штат США) , г.Балтимор, Мэрилэнд (штат США) |
| 5-Хлорметил-2-фуранкарбоновая кислота, этиловый эфир |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 5-Хлорметил-2-фуранкарбоновая кислота, метиловый эфир |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Бромметилбензойная кислота, этиловый эфир |
фирма  Pfaltz & Bauer, Inc Pfaltz & Bauer, Inc ., г.Уотербери, Коннектикут (штат США) ., г.Уотербери, Коннектикут (штат США) |
| 2-Бромметилбензойная кислота, метиловый эфир |
Фирма  ChemPacific ChemPacific , г.Балтимор, Мэрилэнд (штат США) , г.Балтимор, Мэрилэнд (штат США) |
| 3-Бромметилбензойная кислота, метиловый эфир |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
Соединения формулы 5, которые не известны из литературы и не являются коммерчески доступными, могут быть подходящим образом получены с использованием реакций, которые хорошо известны специалисту в области органического синтеза, такие реакции представлены в общем виде на схеме 4.
Схема 4
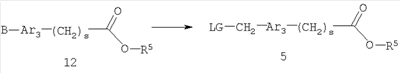
Три примера реакций, представленных схемой 4, описаны ниже. Как будет понятно специалисту в данной области техники, не все реакции могут быть использованы для получения всех соединений формулы 5, а только реакции, подходящие для получения конкретного соединения формулы 5, что будет вполне понятно специалисту в области органического синтеза.
Например, соединение формулы 5, где LG означает хлор, может быть получено из соединения формулы 12, где В означает водород, посредством реакции электрофильного ароматического замещения при обработке соединения формулы 12, где В означает водород, формальдегидом и хлористым водородом в присутствии катализатора – кислоты Льюиса, предпочтительно такого как хлорид цинка, в подходящем инертном растворителе, например, таком как галогенированный алкан (например, таком как метиленхлорид, хлороформ, 1,2-дихлорэтан или подобный растворитель), при температуре между приблизительно комнатной температурой и температурой кипения растворителя, предпочтительно при приблизительно 35 градусах Цельсия. Очевидно, что эта реакция ограничивается случаями, при которых соединение формулы 12 допускает проведение электрофильного ароматического замещения в необходимой точке присоединения, и дополнительно ограничивается случаями, при которых соединение формулы 5 стабильно к действию минеральных кислот и кислот Льюиса. Примеры соединений формулы 5, которые удовлетворяют этим условиям, известны обычному специалисту в области органической химии. Примеры таких реакций можно найти в: Moldenhauer, О. et al. Justus Liebigs Ann. Chem. 1953, 580, 176.
Соединения формулы 5, где LG означает бром, могут быть получены посредством обработки соединения формулы 12, где В означает CH3, N-бромсукцинимидом или 3,3-диметил-N,N’-дибромгидантоином в инертном растворителе, например, таком как галогенированный алкан (например, четыреххлористый углерод) или ацетонитрил, необязательно дополнительно в присутствии катализатора, например, такого как азобис(изобутиронитрил) или бензоилпероксид, при подходящей температуре, вполне удобно при температуре кипения растворителя, и необязательно при дополнительном присутствии источника света; или посредством обработки соединения формулы 12, где В означает CH3, бромом в инертном растворителе, например, таком как смесь воды и ароматического углеводорода (например, такого как бензол) или галогенированный алкан (например, хлороформ) при облучении лампами накаливания. Соединения формулы 5, где LG означает хлор, могут быть получены посредством обработки соединения формулы 12, где В означает CH3, N-хлорсукцинимидом или сульфурилхлоридом в инертном растворителе, например, таком как галогенированный алкан (например, четыреххлористый углерод) или ацетонитрил необязательно при дополнительном присутствии катализатора, например, такого как азобис(изобутиронитрил) или бензоилпероксид при подходящей температуре, вполне удобно при температуре кипения растворителя и при дополнительном присутствии источника света; или посредством обработки соединения формулы 12, где В означает CH3, хлором в инертном растворителе, например, таком как смесь воды и ароматического углеводорода (например, бензола) или галогенированный алкан (например, хлороформ или четыреххлористый углерод) при облучении лампами накаливания.
Соединение формулы 5, где LG означает бром, могут быть получены посредством обработки соединения формулы 12, где В означает CH2OH, трибромидом фосфора или смесью N-бромсукцинимида и трифенилфосфина в инертном растворителе, например, таком как галогенированный алкан (например, метиленхлорид или четыреххлористый углерод) при температуре между приблизительно 0 градусов и температурой кипения растворителя, удобно при температуре приблизительно 0 градусов. Соединение формулы 5, где LG означает хлор, могут быть получены посредством обработки соединения формулы 12, где В означает CH2OH, тионилхлоридом или смесью N-хлорсукцинимида и трифенилфосфина в инертном растворителе, например, таком как галогенированный алкан (например, метиленхлорид или четыреххлористый углерод), при температуре между приблизительно 0 градусов и температурой кипения растворителя, удобно при приблизительно 0 градусов. Соединение формулы 5, в которой LG означает OSO2E, где Е означает низший алкил или арил, могут быть получены посредством обработки соединения формулы 12, где В означает CH2OH, сульфонилхлоридом ESO2Cl (например, таким как метансульфонилхлорид или n-толуолсульфонилхлорид) в присутствии основания, например, такого как третичный амин (например, в присутствии триэтиламина или диэтилизопропиламина) в инертном растворителе, например, таком как галогенированный углеводород (например, метиленхлорид), при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно 0 градусов. Соединение формулы 5, где LG означает иод, могут быть получены посредством обработки соединения формулы 5, где LG означает хлор, бром или OSO2E, где Е означает низший алкил или арил, иодидом щелочного металла (например, таким как иодид натрия) в инертном растворителе, например, таком как кетон (например, ацетон или метилэтилкетон), при температуре между приблизительно 50 градусами и приблизительно 80 градусами, удобно при приблизительно температуре кипения растворителя.
Исходные вещества: соединения формулы 7
Многие соединения формулы 7, где Х означает отщепляемую группу, такую как хлор, иод бром или трифлат, представляют собой известные соединения и могут быть синтезированы в соответствии с методиками, описанными в литературе. Некоторые примеры приведены в таблице.
| Химическое наименование |
Ссылка |
| 3-Бром-4-хлорфенол |
Liedholm, В. Acta Chem. Scand Series В 1984, В38, 877-894 |
| 4-Бром-2-хлорфенол |
Jaeger, R. et al. US 4,223,166 |
| 6-Бром-5-хлорпиридин-3-ол |
Koch, V. et al. Synthesis 1990, 499-501 |
| 4-Бром-2,6-дихлорфенол |
Malm, J. et al. WO 02/62780 |
| 5-Бром-2-гидроксибензол-сульфонамид |
Meyer, W. et al. US 4,479,821 |
| 4-Бром-3-нитрофенол |
Lavoie, E.J. et al. US 6,486,167 |
| 3-Бром-4-метилфенол |
Jacquesy, J.C. J. Chem. Soc. Chem. Commun. 1980, 110-111 |
| 5-Бром-2-нитрофенол |
Makosza, M. et al. J. Org. Chem. 1998, 63, 4199-4208 |
| 3-Бромфенол |
Matarasso-Tchiroukhine, E. Ann. Chim. (Paris) 1958, 3, 405-459 Chem. Abs. 53: 34694 |
| 2-трет-Бутил-4-иодфенол |
Tashiro, M. et al. J. Org. Chem. 1977, 42, 835-838 |
| 3,5-Диметил-4-иодфенол |
Lu, Y. et al. Synthesis 2001, 1639-1644 |
| 3-Иодфенол |
Noelting and Stricker Chem. Ber. 1887, 20, 3019 |
| 5-Бром-2-гидрокситиазол-4-карбоновая кислота, этиловый эфир |
Serra, G. et al. Heterocycles 1995, 41, 2701-2712 |
| 5-Бром-3-гидрокси-тиофен-2-карбонитрил |
Binder, D. et al. Arch. Pharm. (Weinheim) 1988, 321, 391-395 |
| 6-Бромпиридин-2-ол |
Wibaut, J.P. et al. Reel. Trav. Chim. Pays-Bas 1940, 59, 202-206 |
| 6-Бромпиридин-3-ол |
den Hertog, H.J. et al. Reel. Trav. Chim. Pays-Bas 1950, 69, 1281-1288 |
| 2-Хлор-4,6-диметил-пиримидинол |
Hurst, D.Т. Heterocycles 1984, 22, 79-84 |
| 2-Хлор-4-метокси-6-метилпиримидин-5-ол |
Dohmori, R. et al. Chem. Pharm. Bull. 1970, 18, 1908-1914 |
| 2-Хлорпиримидин-5-ол |
Hurst, D.Т. et al. J. Chem. Soc. 1965, 7116-7119 |
| 6-Иодпиридин-3-ол |
Edgar, К.J. et al. J. Org. Chem. 1990, 55, 5287-5291 |
В дополнение, многие соединения формулы 7 являются коммерчески доступными, включая следующие соединения:
| Химическое наименование |
Поставщик |
| 4-Бром-2-хлорфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Бром-2-хлор-6-метилфенол |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 5-Бром-2,3-дифторфенол |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 4-Бром-3,5-диметилфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 5-Бром-2-гидроксибензамид |
поставщик – фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 5-Бром-2-гидрокси-бензонитрил |
фирма  Oakwood Products Oakwood Products , Западная Колумбия, Южная Каролина (штат США) , Западная Колумбия, Южная Каролина (штат США) |
| 5-Бром-2-гидрокси-3-нитро-пиридин |
фирма  Oakwood Products Oakwood Products , Западная Колумбия, Южная Каролина (штат США) , Западная Колумбия, Южная Каролина (штат США) |
| 3-Бром-5-гидроксипиридин |
фирма  Specs and Biospecs Specs and Biospecs , Райсвайк, Нидерланды , Райсвайк, Нидерланды |
| 4-Бромфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Хлор-3-фтор-5-гидрокси-пиридин |
фирма  Asymchem International, Inc. Asymchem International, Inc. , Дарем, Северная Каролина (штат США) , Дарем, Северная Каролина (штат США) |
| 5-Хлор-2-гидрокси-4,6-диметилникотинонитрил |
фирма  Maybridge plc Maybridge plc , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 2-Хлор-5-гидроксипиридин |
фирма  Asymchem International, Inc. Asymchem International, Inc. , Дарем, Северная Каролина (штат США) , Дарем, Северная Каролина (штат США) |
| 2-Гидрокси-5-бромпиримидин |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 4-Иод-2-метилфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-Иодфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Иодфенол |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
Соединения формулы 7, которые не известны из литературы и не являются коммерчески доступными, могут быть подходящим образом получены с использованием реакций, которые хорошо известны специалисту в области органического синтеза, такие реакции представлены в общем виде на схеме 5.
Схема 5

Соединения формулы 7 могут быть получены из соединения формулы 13, где G и Х представляют собой одни и те же заместители, выбранные из хлора, брома и иода, и Y означает метил, с использованием реакций, которые хорошо известны специалисту в области органического синтеза. Некоторые из этих методик приведены в: “Protective Groups in Organic Synthesis” (Greene, T.W., Wuts, P.G. M., 2nd Edition, John Wiley & Sons, N.Y. 1991). Например, соединение формулы 7 может быть получено при обработке триметилсилилиодидом соединения формулы 13, где G и Х представляют собой одни и те же заместители, выбранные из хлора, брома и иода, и Y означает метил. Взаимодействие удобно проводить в инертном растворителе, например, таком как галогенированный алкан (например, хлороформ) или ацетонитрил, при температуре между приблизительно комнатной температурой и температурой кипения растворителя, предпочтительно при температуре приблизительно 50 градусов. В качестве альтернативы, соединение формулы 7 может быть получено посредством нагревания соединения формулы 13, где G и Х представляют собой одни и те же заместители, выбранные из хлора, брома и иода, и Y означает метил, бромистым водородом в уксусной кислоте или воде при кипячении с обратным холодильником. В качестве третьей альтернативы соединение формулы 7 может быть получено посредством обработки соединения формулы 13, где G и Х представляют собой одни и те же заместители, выбранные из хлора, брома и иода, и Y означает метил, трибромидом бора в инертном растворителе, например, таком как галогенированный алкан (например, хлороформ или метиленхлорид), при температуре между приблизительно 0 градусов и приблизительно 40 градусами, удобно при приблизительно комнатной температуре.
Соединения формулы 7, где Х означает хлор и положение присоединения заместителя Х представляет собой пара-положение по отношению к гидроксигруппе, могут быть получены посредством обработки соединения формулы 13, где G означает водород и Y означает водород, сульфурилхлоридом в инертном растворителе, например, таком как простой эфир галогенированный углеводород (например, хлороформ), при температуре между приблизительно 0 градусов и приблизительно 35 градусами, предпочтительно при приблизительно комнатной температуре. Соединения формулы 7, где Х означает бром и положение присоединения заместителя Х представляет собой пара-положение по отношению к гидроксигруппе, могут быть получены посредством обработки соединения формулы 13, где G означает водород и Y означает водород, бромом в инертном растворителе, например, таком как вода или четыреххлористый углерод, или уксусная кислота, при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. В качестве альтернативы, те же самые соединения 7, где Х означает бром и положение присоединения Х представляет собой пара-положение по отношению к гидроксигруппе, могут быть получены посредством обработки соединения формулы 13, где G означает водород и Y означает водород, солью – трибромидом (например, такой как тетрабутиламмоний трибромид или бензилтриметиламмоний трибромид) в инертном растворителе, например, таком как галогенированный углеводород (например, в метиленхлориде или хлороформе) при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. Соединения формулы 7, где Х означает иод и положение присоединения заместителя Х представляет собой пара-положение по отношению к гидроксигруппе, могут быть получены посредством обработки соединения формулы 13, где G означает водород и Y означает водород, иодом или монохлоридом иода в инертном растворителе, например, таком как вода, в присутствии неорганического основания, например, такого как гидроксид щелочного металла (например, гидроксид натрия) или карбонат щелочного металла (например, карбонат натрия) при температуре между приблизительно 0 градусов и приблизительно комнатной температурой, предпочтительно при приблизительно комнатной температуре. Те же самые соединения формулы 7 где Х означает иод и положение присоединения заместителя Х представляет собой пара-положение по отношению к гидроксигруппе, могут быть получены посредством обработки соединения формулы 13, где G означает водород и Y означает водород, иодидом натрия и гипохлоритом натрия в инертном растворителе, например, таком как смесь воды и спирта (например, такого как метанол), при температуре, близкой к 0 градусов. Эта последняя реакция и некоторые возможные альтернативы описаны в: Edgar, К.J., Falling, S.N. J. Org. Chem. 1990, 55, 5287-5291.
Соединение формулы 7, где Х означает хлор, бром или иод, могут быть получены посредством обработки соединения формулы 13, где G означает NH2 и Y означает водород, в соответствии с реакцией Зандмейера (Sandmeyer), которая хорошо известна специалисту в области органической химии. Подробности относительно этой реакции можно найти в: Hodgson, H.H. Chem. Rev. 1947, 40, 251-277, и также в: Nonhebel, D.C., Copper-catalyzed Single-electron Oxidations and Reductions, Special Publication-Chemical Society (London) 1970, 24, 409-437 ISSN: 0577-618X. Например, соединение формулы 13, где G означает NH2 и Y означает водород, может быть превращено в диазониевое промежуточное соединение формулы 13, где G означает N2 + и Y означает водород, посредством обработки нитритом натрия в присутствии минеральной кислоты (например, такой как хлороводородная кислота или серная кислота) в воде при температуре между приблизительно -10 градусами и приблизительно 10 градусами, предпочтительно приблизительно при 0 градусов. Без выделения это диазониевое промежуточное соединение затем может быть превращено в соединение формулы 7, где Х означает хлор, посредством обработки хлоридом меди(I), а также в соединение формулы 7, где Х означает бром, посредством обработки бромидом меди(I), или в соединение формулы 7, где Х означает иод, посредством обработки иодидом калия. + и Y означает водород, посредством обработки нитритом натрия в присутствии минеральной кислоты (например, такой как хлороводородная кислота или серная кислота) в воде при температуре между приблизительно -10 градусами и приблизительно 10 градусами, предпочтительно приблизительно при 0 градусов. Без выделения это диазониевое промежуточное соединение затем может быть превращено в соединение формулы 7, где Х означает хлор, посредством обработки хлоридом меди(I), а также в соединение формулы 7, где Х означает бром, посредством обработки бромидом меди(I), или в соединение формулы 7, где Х означает иод, посредством обработки иодидом калия.
Исходные вещества: соединения формулы 10
Многие соединения формулы 10, где Y означает остаток бороновой кислоты, сложного эфира – бороната, триметилолово или три-н-бутил-олово, представляют собой известные соединения и могут быть синтезированы в соответствии с методиками, описанными в литературе. Некоторые примеры приведены в таблице.
| Химическое наименование |
Ссылка |
| 4-Ацетил-3-фторфенилбороновая кислота |
Holmes-Fariey, S.R. et al. US 2003064963 |
| (5-трет-Бутоксифуран-2-ил)-триметилстаннан |
Pearce, В.С. Syn. Commun. 1992, 22, 1627-1643. |
| 4-н-Бутилфенилбороновая кислота |
Glende, С. et al. Mutation Res. 2002, 515, 15-38 |
| (5-Циано-2-тиенил)бороновая кислота |
Fensome, A. et al. US 6,355,648 |
| 4-[(Диэтиламино)карбонил]фенил-бороновая кислота |
Gravel, M. et al. J. Org. Chem 2002, 67, 3-15 |
| 3,5-Диметокси-4-метил-фенилбороновая кислота |
Ishiwata, H. et al. US 2003027814 |
| 2-(2,6-Диметилфенил)-4,4,5,5-тетраметил-[1,3,2]диоксаборолан |
Baudoin, 0. et al. J. Org. Chem. 2000, 65, 9268-9271 |
| Диметил-[4-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)фенил]амин |
Murata, M.. J. Org. Chem. 1997, 62, 6458-6459 |
| 2,6-Диметил-4-(4,4,5,5-тетраметил-[1,3,2]диоксаборолан-2-ил)пиридин |
Cho, J.-Y. et al. J. Am. Chem. Soc. 2000, 122, 12868-12869 |
| 2-(1-Этоксиэтил)фенилбороновая кислота |
Dale, W.J. et al. J. Org. Chem. 1962, 27, 2598-2603 |
| 2-Этокси-5-трибутилстаннил-тиазол |
Wang, Т. et al. WO 02/062423 |
| (5-Этилфуран-2-ил)триметил-станнан |
Sasabe, M. et al. Perkin 1 2000, 3786-3790 |
| 3-Гидроксифенилбороновая кислота |
Bean, F.R., Johnson, J.R. J. Am. Chem. Soc. 1932,54,4421 |
| 6-Метокси-4-метил-3-пиридинилбороновая кислота |
Arvanitis, A.G. Bioorg. Med. Chem. Lett. 2003, 13, 289-291 |
| 2-Метокси-фенилбороновая кислота |
Rocca, P. et al Tetrahedron 1993, 49, 49-64 |
| 2-(4-Метоксифенил)-4,4,5,5-тетраметил-[1,3,2]диоксаборолан |
Ishiyama, Т. et al. Tetrahedron Lett. 1997, 38, 3447-3450 |
| (5-Метил-фуран-2-ил)бороновая кислота |
Florentin, D. et al. J. Heterocycl. Chem. 1976, 13 ,1265-1272 |
| 2-Метил-5-(триметилстаннил)тиазол |
Wentland, M. P. et al. J. Med. Chem. 1993, 36, 1580-1596 |
| 2-Нитрофенилбороновая кислота |
Groziak, M.P. et al. J. Am. Chem. Soc. 1994, 116, 7597-7605 |
| 3-Пиридилбороновая кислота |
Fischer, F.С. et al. Reel. Trav. Chim. Pays-Bas 1974, 93, 21-24 |
| 3-(4,4,5,5-Тетраметил-[1,3,2]диоксаборолан-2-ил)-бензонитрил |
Sebo, L. et al. Helv. Chim. Acta 2000, 83, 93-113 |
| 4-(4,4,5,5-Тетраметил-[1,3,2]диоксаборолан-2-ил)-бензонитрил |
Murata, M.J. Org. Chem. 1997, 62, 6458-6459 |
| 1-[4-(4,4,5,5-Тетраметил-[1,3,2]диоксаборолан-2-ил)фенил]этанон |
Fuerster, A. et al. Org. Lett. 2002, 4, 541-544 |
| 2-(4,4,5,5-Тетраметил-1,3,2-диоксаборолан-2-ил)тиазол |
Marcuccio, S. et al. US 6399779 |
| 4,4,5,5-Тетраметил-2-(4-нитро-фенил)-[1,3,2]диоксаборолан |
Ishiyama, Т. et al. Tetrahedron Lett. 1997, 38, 3447-3450 |
| 3-Тиофенилбороновая кислота |
Li, W. et al. J. Org. Chem. 2002, 67, 5394-5397 |
В дополнение, многие соединения формулы 10, где Y означает остаток бороновой кислоты, сложного эфира – бороната, триметилолово или три-н-бутилолово, являются коммерчески доступными, включая следующие соединения:
| Химическое наименование |
Поставщик |
| 3-Бромфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-(2-Карбоксиэтил)-фенилбороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 4-Карбоксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Хлорфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Хлорфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-Цианофенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2,6-Дифторфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3,5-Дифтор-(три-н-бутилстаннил)бензол |
фирма  Maybridge plc Maybridge plc , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 2,4-Диметоксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2,5-Диметоксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-(Диметиламино)фенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Этоксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Фторбифенил-4-бороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 3-Фторфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин(штат США) , г.Милуоки, Висконсин(штат США) |
| 4-Фтор-2-метилфенилбороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 4-Фтор-(три-н-бутилстаннил)бензол |
Компания  фирма фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 3-Формилфуран-2-бороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| Фуран-2-бороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-(Гидроксиметил)-фенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-(Гидроксиметил)-фенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Иодфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| (3-Изопропилфенил)бороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| (2-Метилфенил)бороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-Метилфенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Метоксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| [(4-Метилсульфонил)-фенил]бороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 5-Метилтиофен-2-бороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Метил(три-н-бутилстаннил)бензол |
фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| 1-Нафталинбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-Нитрофенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 4-Феноксифенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 2-Тиофенбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| Тиофен-3-бороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| Три-н-бутил(2-фурил)олово |
фирма  Aldrich Chemical Company, Inc. Aldrich Chemical Company, Inc. |
| Трибутил(2-метоксифенил)станнан |
фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| Три-н-бутил(2-пиридил)олово |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . |
| 2-(Трифторметил)-фенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3-(Трифторметокси)-фенилбороновая кислота |
фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) , г.Милуоки, Висконсин (штат США) |
| 3,4,5-Трифторфенилбороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| 3,4,5-Триметоксифенил-бороновая кислота |
фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd ., Ланкашир, Великобритания ., Ланкашир, Великобритания |
| Триметил(фенил)олово |
фирма  Aldrich Chemical Company, Inc. Aldrich Chemical Company, Inc. |
| 3-(Три-н-бутилстаннил)-пиридин |
фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Великобритания , Тинтэйгел, Великобритания |
| Три-н-бутил-(2-тиенил)олово |
фирма  Aldrich Chemical Company, Inc. Aldrich Chemical Company, Inc. |
Соединения формулы 10, где Y означает остаток бороновой кислоты, сложного эфира – бороната, триметилолово или три-н-бутилолово, которые не известны из литературы и не являются коммерчески доступными, могут быть подходящим образом получены с использованием реакций, которые хорошо известны специалисту области органического синтеза. Например, соединение этого типа можно удобным образом синтезировать согласно схеме б из соединения формулы 11, в котором Х означает бром или иод, посредством обработки алкиллитием (например, н-бутиллитием) или магнием (в виде реактива Гриньяра) в подходящем инертном растворителе, например, таком как простой эфир (например, в тетрагидрофуране или диэтиловом эфире), при температуре, подходящей для проведения взаимодействия (например, при температуре приблизительно -78°С для взаимодействия с алкиллитием, или при приблизительно комнатной температуре для взаимодействия с магнием), с последующей обработкой триалкилборатом или хлоридом триалкилолова с получением при этом соединения формулы 10, где Y означает B(OH)z или триалкилолово соответственно.
Схема 6
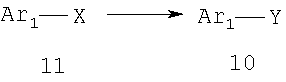
Дополнительно, взаимодействие можно проводить с использованием катализатора на основе благородного металла. Согласно такому подходу соединение формулы 11 удобно подвергать взаимодействию с гексаалкил-дистаннаном (например, таким как гексаметилдистаннан или гекса-н-бутилди-станнан) или 4,4,5,5-тетраметил-[1,3,2]диоксаборолан или 4,4,5,5,4′,4′,5′,5′-октаметил-[2,2′]би[[1,3,2]диоксабороланил] в присутствии катализатора на основе благородного металла (предпочтительно с использованием палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0) или палладий(II) хлорид или палладий(II) ацетат) и при необязательном дополнительном присутствии каталитического количества фосфинового лиганда, например, такого как три-о-толилфосфин или три-трет-бутилфосфин. В случае взаимодействия с гексаалкилдистаннаном взаимодействие необязательно проводят в присутствии органического основания, например, такого как третичный амин (например, триэтиламин), в то время как в случае взаимодействия с диоксабороланом такое взаимодействие проводят в присутствии неорганического основания (например, такого как фторид цезия или ацетат калия, предпочтительно в присутствии ацетата калия). Взаимодействие удобно проводить в подходящем инертном растворителе, таком как полярный апротонный растворитель (например, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид или ацетонитрил) или ароматический углеводород (например, толуол), при температуре между приблизительно комнатной температурой и приблизительно 100 градусами и предпочтительно при температуре между приблизительно комнатной температурой и приблизительно 50 градусами. В качестве дополнительного примера можно указать конкретные условия реакции, описанные в следующих публикациях: Baudoin, О. et al. J. Org. Chem. Soc. 2000, 65, 9268-9271; Ishiyama, Т. et al. Tetrahedron Lett. 1997, 38, 3447-3450; Hylarides, M.D. J. Organomet. Chem. 1989, 367, 259-265; Read, M.W. et al. Org. Lett. 2000, 2, 3201-3204; Ishiyama, Т. et al. Tetrahedron 1997, 57, 9813-9816; Fuerster, A. et al. Org. Lett. 2002, 4, 541-544.
Получение соединений согласно настоящему изобретению, в которых s означает 2
В добавление к способам, описанным выше для получения соединений согласно настоящему изобретению, доступны и другие способы получения соединений формулы 1, в которой s означает 2, как показано на схеме 7. В соответствии с этим способом соединения формулы 5В превращают в соединения формулы 15 или прямо посредством нуклеофильного замещения с использованием соединения формулы 4, или посредством конденсации Сузуки, проходящей через образование промежуточного соединения 9В. Проведение реакции нуклеофильного замещения и конденсации Сузуки аналогично проведению реакций, описанных выше.
Схема 7
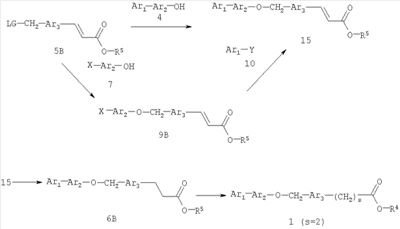
Соединения формулы 15 могут быть превращены в соединения формулы 6В посредством гидрирования с использованием катализатора – благородного металла. Такое взаимодействие проводят посредством обработки соединения формулы 15 газообразным водородом в присутствии катализатора – благородного металла, например, такого как палладий на углероде в присутствии инертного растворителя (например, в присутствии спирта, такого как этанол), при приблизительно комнатной температуре и при атмосферном давлении.
Соединение формулы 6В может быть превращено в соединение формулы 1, где s означает 2, посредством отщепления защитной группы R5. Условия, подходящие для проведения этого взаимодействия, описаны выше для превращения соединения формулы 6 в соединение формулы 1.
Исходные вещества: соединения формулы 5В
Некоторые соединения формулы 5В представляют собой известные соединения и могут быть синтезированы в соответствии с методиками, описанными в литературе. Примеры представлены в виде таблицы.
| Химическое наименование |
Ссылка |
| (2Е)-3-[2-(Бромметил)фенил]-2-акриловая кислота, метиловый эфир |
Н.Juteau et al. Bioorg. Med. Chem. Lett. 2001, 11, 747 |
| (2Е)-3-[2-(Бромметил)фенил]-2-акриловая кислота, трет-бутиловый эфир |
D.A.Price Synlett 1999,1919 |
| (2Е)-3-[3-(Бромметил)-2-пиридинил]-2-акриловая кислота, этиловый эфир |
Y.Gareau et al. WO 9947497 |
| (2Е)-3-[4-(Бромметил)фенил]-2-акриловая кислота, метиловый эфир |
P.L.Beaulieu et al. WO 2003010141 |
| (2Е)-3-[4-(Хлорметил)-5-метил-2-оксазолил]-2-акриловая кислота, этиловый эфир |
Y.Momose et al., WO 2004024705 |
| (2Е)-3-[4-(Хлорметил)фенил]-2-акриловая кислота, этиловый эфир |
H.U.Blaser et al. EP 40177 |
| (2Е)-3-[5-(Бромметил)-3-фуранил]-2-акриловая кислота, метиловый эфир |
L.M.Pevzner et al. Zhumal Obshchei Khimii 1997, 67, 1710 |
| 3-[3-(Бромметил)фенил]-2-акриловая кислота, метиловый эфир |
D.A.R.Happer J. Chem. Soc. Perkin Trans. 2 1983, 843 |
| 3-[3-(Хлорметил)фенил]-2-акриловая кислота, метиловый эфир |
D.A.R. Happer, J. Chem. Soc. Perkin Trans. 2 1983, 843 |
| 3-[4-(Бромметил)фенил]-2-акриловая кислота, метиловый эфир |
H.Ohnishi et al. EP 501876 |
| 3-[4-(Бромметил)фенил]-2-акриловая кислота, метиловый эфир |
D.V.Patel et al. WO 9623813 |
| 3-[4-(Хлорметил)фенил]-2-акриловая кислота, метиловый эфир |
D.A.R.Happer J. Chem. Soc. Perkin Trans. 2 1983, 843 |
Соединения формулы 5В, которые не известны из литературы, могут быть получены с использованием любых общеизвестных средств. Например, такие соединения удобно получать согласно схеме 8, используя в качестве исходного соединения арилкарбоксальдегид формулы 16, или из галогеноароматического соединения формулы 17.
Схема 8
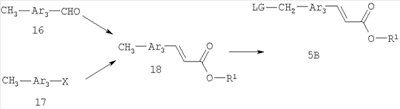
Соединение формулы 16 может быть превращено в соединение формулы 18 посредством взаимодействия с илидом фосфора по реакции Виттига (Wittig) или со сложным эфиром – фосфонатом по реакции Хорнера-Вадсворфа-Эммонса (Homer-Wadsworth-Emmons). Обе эти реакции хорошо известны из предшествующего уровня техники, дополнительную информацию можно найти, например, в: “Comprehensive Organic Transformations: A Guide to Functional Group Preparations” [R.C.Larock, VCH Publishers, Inc., N.Y. 1989, pages 173-184]; а также в: “Advanced Organic Chemistry” [J. March, 3rd Edition, Wiley biterscience, NY, 1985]. Например, соединение формулы 16 может быть обработано алкил (трифенилфосфоранилиден)ацетатом, например, таким как метил-(трифенилфосфоранилиден)ацетат, в инертном растворителе, например, таком как дихлорметан, или тетрагидрофуран, или бензол, при температуре, приблизительно равной комнатной температуре, с получением при этом соединения формулы 18. В качестве дополнительного примера соединение формулы 16 может быть подвергнуто обработке сложным эфиром – фосфоноацетатом, например, таким как триэтилфосфоноацетат, в присутствии основания, например, такого как гидрид натрия, или карбонат цезия, или карбонат калия, или этоксид натрия, в инертном растворителе, например, таком как N,N-диметилформамид, или диоксан, или тетрагидрофуран, при температуре, приблизительно равной комнатной температуре, с получением при этом соединения формулы 18.
Соединение формулы 17, где Х означает группу, которая может выполнять функцию отщепляемой группы в реакции конденсации, катализируемой катализатором на основе благородного металла, например, такой как реакция Хека (Heck), может быть превращено в соединение формулы 18 посредством взаимодействия со сложным эфиром – акрилатом при использовании катализатора на основе благородного металла. Например, взаимодействие можно проводить посредством обработки соединения структуры 17 сложным эфиром – акрилатом, например, таким как метилакрилат или этилакрилат, в присутствии источника палладия(0), например, такого как палладий(II) ацетат, при необязательном присутствии фосфина, такого как трифенилфосфин или три-орто-толилфосфин, предпочтительно три-орто-толилфосфин, в присутствии основания, которое может представлять собой органическое основание (например, триэтиламин) или не органическое основание (например, карбонат калия, гидрокарбонат натрия, таллий(I) ацетат или ацета серебра) при необязательном дополнительном присутствии катализатора фазового переноса, например, такого как тетра-н-бутилхлорид аммония, в инертном растворителе (например, в N,N-диметилформамиде или N,N-диметилацетамиде или ацетонитриле) при температуре между приблизительно комнатной температурой и приблизительно 110 градусами, предпочтительно при приблизительно 100 градусах.
Соединение формулы 18 может быть превращено в соединение формулы 5b посредством обработки галогенирующим агентом, например, таким как N-бромсукцинимид, в присутствии каталитического количества бензоилпероксида или азобисизобутиронитрила (AIBN), в инертном растворителе, например, таком как галогенированный углеводород или галогеноуглерод, например, такой как четыреххлористый углерод. Взаимодействие удобно проводить при температуре вблизи температуры кипения растворителя или при приблизительно 80 градусах, какая ниже.
Активация in vitro гликогенсинтазы при воздействии соединений согласно настоящему изобретению может быть установлена с помощью следующего теста:
Раствора субстрата, содержащего гликоген (4,32 мг/мл), 21,6 мМ UDP-глюкозы, 21,6 мМ фосфо(енол)пирувата и 2,7 мМ NADH в 30 мМ глицилглицина, буфер с рН 7,3, добавляют в количестве двенадцать мл на лунку в 384-луночные планшеты из полистирола, используемые для проведения исследования (фирма  BD Biosciences BD Biosciences ). В планшет (колонки 5-24) добавляют раствор соединения (8 мкл/лунка) различных концентраций (0-57 мМ) в 30 мМ глицилглицина, рН 7,3, 40 мМ KCl, 20 мМ MgCb плюс 9,2% ДМСО. В планшет (колонки 3-24) добавляют раствор фермента (12 мкл/лунка), содержащий гликогенсинтазу (16,88 мг/мл), пируваткиназу (0,27 мг/мл), лактат дегидрогеназу (0,27 мг/мл) в 50 мМ Трис-HCl, рН 8,0, 27 мМ DTT (дитиотреитол) и бычий сывороточный альбумин (БСА, 0,2 мг/мл). В качестве контроля (холостой опыт) раствор ферментов без гликогенсинтазы добавляют в верхнюю половину лунок колонок 1-2. В нижнюю половину лунок колонок добавляют известный активатор, глюкоза-6-фосфат (18,9 мМ) в добавление к раствору фермента. Реакционную смесь инкубируют при 37°С. Затем регистрируют поглощение при 340 нм, используя устройство для прочтения планшетов ). В планшет (колонки 5-24) добавляют раствор соединения (8 мкл/лунка) различных концентраций (0-57 мМ) в 30 мМ глицилглицина, рН 7,3, 40 мМ KCl, 20 мМ MgCb плюс 9,2% ДМСО. В планшет (колонки 3-24) добавляют раствор фермента (12 мкл/лунка), содержащий гликогенсинтазу (16,88 мг/мл), пируваткиназу (0,27 мг/мл), лактат дегидрогеназу (0,27 мг/мл) в 50 мМ Трис-HCl, рН 8,0, 27 мМ DTT (дитиотреитол) и бычий сывороточный альбумин (БСА, 0,2 мг/мл). В качестве контроля (холостой опыт) раствор ферментов без гликогенсинтазы добавляют в верхнюю половину лунок колонок 1-2. В нижнюю половину лунок колонок добавляют известный активатор, глюкоза-6-фосфат (18,9 мМ) в добавление к раствору фермента. Реакционную смесь инкубируют при 37°С. Затем регистрируют поглощение при 340 нм, используя устройство для прочтения планшетов  Tecan Ultra reader Tecan Ultra reader , каждые 3 минуты до окончания суммарно 30 минутного периода. , каждые 3 минуты до окончания суммарно 30 минутного периода.
Активность фермента (с соединением и без соединения) вычисляют по скорости реакции и представляют как изменение оптической плотности (AOD) в минуту. Стимулирование (в процентах) активности гликогенсинтазы при воздействии соединения в различной концентрации рассчитывают по следующей формуле:
% стимулирования=100*Rs/Rt,
где Rs означает скорость реакции фермента в присутствии соединения, a Rt означает скорость реакции фермента в отсутствие соединения.
SC2.0 определяют как концентрацию соединения, которая необходима для стимулирования 200% активности фермента. Предпочтительные соединения согласно настоящему изобретению характеризуются значениями SC2.0, которые находятся в интервале от 0,1 до 100 мкМ, предпочтительно в интервале от 0,1 до 20 мкМ.
Результаты, полученные в описанном выше тесте для типичных соединений формулы I как тестируемых соединений, приведены в следующей таблице.
| Химическое наименование |
SC2.0 |
| 1-[5-(Бифенил-4-илоксиметил)фуран-2-карбонил]-L-пирролидин-2-карбоновая кислота |
1,4 мкМ |
| 1-{[5-(Бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота |
16,3 мкМ |
| 2-(3-Хлорбифенил-4-илоксиметил)бензойная кислота |
10,3 мкМ |
| 2-(3-Хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота |
14,9 мкМ |
| 2-(4′-Хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота |
3,1 мкМ |
| 3-(4′-Бромбифенил-4-илоксиметил)бензойная кислота |
3,8 мкМ |
| 3-(4′-Метоксибифенил-4-илоксиметил)бензойная кислота |
9,6 мкМ |
| 5-(4′-Хлорбиф енил-4-илоксиметил)фуран-2-карбоновая кислота |
0,8 мкМ |
| 5-(Бифенил-3-илоксиметил)фуран-2-карбоновая кислота |
14,9 мкМ |
| 5-(Бифенил-4-илоксиметил)тиофен-2-карбоновая кислота |
12,7 мкМ |
Примеры
Приведенные ниже примеры иллюстрируют предпочтительные способы синтеза соединений и композиций согласно настоящему изобретению.
Промежуточное соединение 1: метиловый эфир 2-бромметилбензойной кислоты

Обозначения: NBS- N-бромсукцинимид, benzoylperoxide – бензоилпероксид
Смесь метилового эфира о-толуиловой кислоты (13,5 г, 89,9 ммоль), NBS (N-бромсукцинимид) (17,6 г, 98,9 ммоль) и бензоилпероксида (50 мг, 0,2 ммоль) в четыреххлористом углероде (250 мл) кипятят с обратным холодильником в течение двух дней. Полученную реакционную смесь охлаждают и затем фильтруют. Растворители упаривают при пониженном давлении, полученный остаток очищают хроматографией, элюируя смесью 3% этилацетат/гексан, получая при этом метиловый эфир 2-бромметилбензойной кислоты (7,7 г, выход 37%) в виде белого твердого вещества. 1Н ЯМР (CDCl3):  7,97 (dd, J=1,5 Гц, 8,0 Гц, 1Н), 7,49 (m, 2Н), 7,38 (dt, J=1,5 Гц, 8,0 Гц, 1H), 4,96 (s, 2H), 3,94 (s, 3Н). Масс-спектр (APCI+): 231 (100), 229 (93). 7,97 (dd, J=1,5 Гц, 8,0 Гц, 1Н), 7,49 (m, 2Н), 7,38 (dt, J=1,5 Гц, 8,0 Гц, 1H), 4,96 (s, 2H), 3,94 (s, 3Н). Масс-спектр (APCI+): 231 (100), 229 (93).
Промежуточное соединение 2: метиловый эфир 6-бромметилпиридин-2-карбоновой кислоты
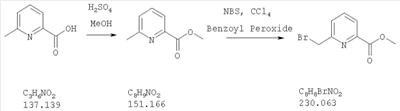
Обозначения: NBS – N-бромсукцинимид, benzoylperoxide – бензоилпероксид
Стадия 1: метиловый эфир 6-метилпиридин-2-карбоновой кислоты
Смесь 6-метилпиридин-2-карбоновой кислоты (10 г, 72,9 ммоль) и концентрированной серной кислоты (3,5 мл) в метаноле (300 мл) кипятят с обратным холодильником в течение ночи. Реакционную смесь охлаждают до комнатной температуры и концентрируют при пониженном давлении. Полученный остаток выливают в насыщенный водный раствор гидрокарбоната натрия (250 мл) и экстрагируют этилацетатом (3×100 мл), объединенные органические слои высушивают (сульфат магния), фильтруют и упаривают, получая при этом метиловый эфир 6-метилпиридин-2-карбоновой кислоты (6,5 г, выход 59%) в виде бесцветного маслянистого вещества. 1Н ЯМР (CDCl3):  7,97 (d, J=7,6 Гц, 1Н), 7,73 (dd, J=7,6 Гц, 1Н), 7,36 (d, J=7,6 Гц, 1Н), 4,01 (s, 3Н), 2,67 (s, 3Н). 7,97 (d, J=7,6 Гц, 1Н), 7,73 (dd, J=7,6 Гц, 1Н), 7,36 (d, J=7,6 Гц, 1Н), 4,01 (s, 3Н), 2,67 (s, 3Н).
Стадия 2: метиловый эфир 6-бромметилпиридин-2-карбоновой кислоты
Метиловый эфир 6-бромметилпиридин-2-карбоновой кислоты получают по методике, описанной в: Wells, G.J. et al. (WO 94/11398): Смесь метилового эфира 6-метилпиридин-2-карбоновой кислоты (6,5 г, 43,0 ммоль), бензоилпероксида (25 мг, 0,1 ммоль) и NBS (N-бромсукцинимид, 8,5 г, 47,8 ммоль) в четыреххлористом углероде (250 мл) кипятят с обратным холодильником в течение ночи. Реакционную смесь охлаждают до комнатной температуры, фильтруют, упаривают и очищают экспресс-хроматографией на силикагеле, элюируя смесью 15% этилацетат/гексан и получая при этом метиловый эфир 6-бромметилпиридин-2-карбоновой кислоты (2,0 г, выход 20%) в виде белого твердого вещества. 1H ЯМР (CDCl3):  8,06 (d, J=8,0 Гц, 1Н), 7,87 (dd, J=8,0 Гц, 1Н), 7,70 (d, J=8,0 Гц, 1H), 4,65 (s, 2H), 4,02 (s, 3Н). Масс-спектр 8,06 (d, J=8,0 Гц, 1Н), 7,87 (dd, J=8,0 Гц, 1Н), 7,70 (d, J=8,0 Гц, 1H), 4,65 (s, 2H), 4,02 (s, 3Н). Масс-спектр
(APCI+): 231 (45), 235 (42).
Промежуточное соединение 3: этиловый эфир 2-бромметилтиазол-4-карбоновой кислоты
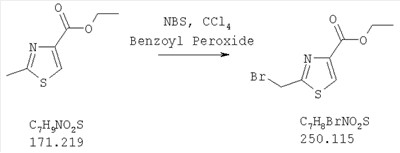
Обозначения: NBS – N-бромсукцинимид, benzoylperoxide – бензоилпероксид
Этиловый эфир 2-бромметилтиазол-4-карбоновой кислоты получают по методике, описанной в: Kindon, N et al. (патент США 6162808). Смесь 2-метилтиазол-4-карбоновой кислоты (коммерчески доступное соединение, фирма «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания; 9,8 г, 57,2 ммоль), бензоилпероксида (40 мг, 0,165 ммоль) и NBS (10,6 г, 60,0 ммоль) в четыреххлористом углероде (250 мл) кипятят с обратным холодильником в течение двух дней. Реакционную смесь охлаждают до комнатной температуры и упаривают при пониженном давлении. Неочищенное вещество разделяют между этилацетатом и водой. Органический слой высушивают (сульфат магния), фильтруют, упаривают и очищают экспресс-хроматографией на силикагеле, элюируя смесью 20% этилацетат/гексан и получая при этом этиловый эфир 2-бромметилтиазол-4-карбоновой кислоты (4,4 г, выход 31%) в виде оранжевого маслянистого вещества. 1Н ЯМР (CDCl3): », Тинтэйгел, Великобритания; 9,8 г, 57,2 ммоль), бензоилпероксида (40 мг, 0,165 ммоль) и NBS (10,6 г, 60,0 ммоль) в четыреххлористом углероде (250 мл) кипятят с обратным холодильником в течение двух дней. Реакционную смесь охлаждают до комнатной температуры и упаривают при пониженном давлении. Неочищенное вещество разделяют между этилацетатом и водой. Органический слой высушивают (сульфат магния), фильтруют, упаривают и очищают экспресс-хроматографией на силикагеле, элюируя смесью 20% этилацетат/гексан и получая при этом этиловый эфир 2-бромметилтиазол-4-карбоновой кислоты (4,4 г, выход 31%) в виде оранжевого маслянистого вещества. 1Н ЯМР (CDCl3):  9,23 (s, 1H), 4,77 (s, 2H), 4,44 (q, J=7,0 Гц, 2H), 1,41 (t, J=7,0 Гц, 3Н). Масс-спектр (APCI+): 252 (100), 250 (90). 9,23 (s, 1H), 4,77 (s, 2H), 4,44 (q, J=7,0 Гц, 2H), 1,41 (t, J=7,0 Гц, 3Н). Масс-спектр (APCI+): 252 (100), 250 (90).
Промежуточное соединение 4: этиловый эфир 4-хлорметилтиазол-2-карбоновой кислоты
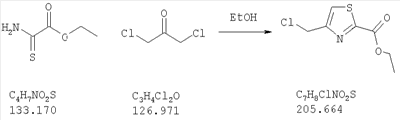
Этиловый эфир 4-хлорметилтиазол-2-карбоновой кислоты получают по методике, описанной в: Summers, J.В., Jr. et al. (патент США 5 486 525): Смесь этил тиооксамата (7,0 г, 52,6 ммоль) и 1,3-дихлорацетона (7,0 г, 55,1 ммоль) в этаноле (300 мл) кипятят с обратным холодильником в течение ночи. Растворитель упаривают при пониженном давлении и неочищенное вещество разделяют между метиленхлоридом и водным раствором гидрокарбоната натрия. Органический слой высушивают (сульфат магния), фильтруют, упаривают и очищают экспресс-хроматографией на силикагеле, элюируя смесью 15% этилацетат/гексан и получая при этом этиловый эфир 4-хлорметилтиазол-2-карбоновой кислоты (4,0 г, выход 37%) в виде оранжевого маслянистого вещества. 1H ЯМР (CDCl3):  7,64 (s, 1H), 4,78 (s, 2H), 4,51 (q, J=7,0 Гц, 2Н), 1,46 (t, J=7,0 Гц, 3Н). Масс-спектр (APCI+): 206 (100). 7,64 (s, 1H), 4,78 (s, 2H), 4,51 (q, J=7,0 Гц, 2Н), 1,46 (t, J=7,0 Гц, 3Н). Масс-спектр (APCI+): 206 (100).
Промежуточное соединение 5: 4′-метилбифенил-4-ол
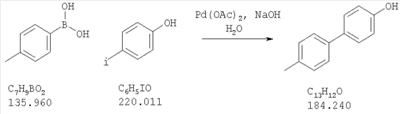
Палладий (II) ацетат (52 мг, 0,23 ммоль) добавляют к смеси 4-иодфенола (5,00 г, 22,7 ммоль), 4-метилфенилбороновой кислоты (3,4 г, 25,0 ммоль), гидроксида натрия (3,6 г, 90 ммоль) и воды (9 мл). Полученную смесь разбавляют два раза водой (9 мл) для облегчения перемешивания. Происходит выделение тепла и через 15 минут температура внутри колбы составляет 50°С. Реакционную смесь охлаждают до комнатной температуры и перемешивают в течение ночи, затем твердое вещество отфильтровывают, промывают водой и растворяют в этилацетате. Органический раствор промывают водой, три раза, используя 1 М раствор NaOH, и затем опять водой до нейтральной реакции промывных вод. Затем раствор высушивают (сульфат натрия), фильтруют и упаривают, получая при этом 4′-метилбифенил-4-ол (2 г, выход 48%).
Промежуточное соединение 6: метиловый эфир 5-(4-иодфеноксиметил)фуран-2-карбоновой кислоты
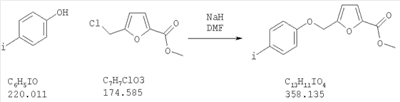
Обозначения: DMF – диметилформамид
Раствор 4-иодфенола (10,08 г, 45,8 ммоль) в N,N-диметилформамиде (30 мл) добавляют к охлаждаемой на бане со льдом суспензии гидрида натрия (60%-ная; 1,65 г, 41,2 ммоль) в N,N-диметилформамиде (30 мл). Баню со льдом убирают и полученную смесь перемешивают в течение 1 ч. После этого полученную смесь охлаждают опять до ~5°С и добавляют раствор метилового эфира 5-(хлор-метил)фуран-2-карбоновой кислоты (4,00 г, 22,9 ммоль) в N,N-диметилформамиде (60 мл). Реакционную смесь перемешивают в течение ночи при комнатной температуре, затем растворители упаривают при пониженном давлении и добавляют воду. Полученную смесь экстрагируют три раза этилацетатом и объединенные органические слои промывают два раза, используя 1 М раствор NaOH и по одному разу водой и насыщенным раствором соли. Органический раствор высушивают (сульфат магния), фильтруют, упаривают и очищают, используя систему для очистки  Biotage 65 L purification system Biotage 65 L purification system , элюируя смесью 3% метиленхлорид/толуол и получая при этом метиловый эфир 5-(4-иод-феноксиметил)фуран-2-карбоновой кислоты (2,3 г, выход 28%) в виде белого твердого вещества, вместе с некоторыми смешанными фракциями. , элюируя смесью 3% метиленхлорид/толуол и получая при этом метиловый эфир 5-(4-иод-феноксиметил)фуран-2-карбоновой кислоты (2,3 г, выход 28%) в виде белого твердого вещества, вместе с некоторыми смешанными фракциями.
Промежуточное соединение 7: метиловый эфир 5-бромметилтиофен-2-карбоновой кислоты
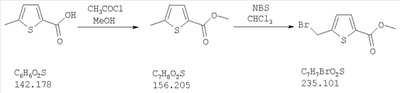
Обозначения: NBS- N-бромсукцинимид
Стадия 1. Метиловый эфир 5-метилтиофен-2-карбоновой кислоты
Ацетилхлорид (5 мл) добавляют к охлажденному до 0°С раствору метанола (40 мл) и дают раствору нагреться до комнатной температуры. Добавляют 5-метилтиофен-2-карбоновую кислоту (фирма  Lancaster Lancaster ; 1,58 г, 11,1 ммоль) и полученный раствор перемешивают при комнатной температуре в течение двух дней. Растворители упаривают при пониженном давлении и добавляют этилацетат. Затем раствор экстрагируют водным раствором гидрокарбоната натрия и водный слой подвергают обратной экстракции этилацетатом. Объединенные органические слои высушивают (сульфат натрия), фильтруют и упаривают, получая при этом метиловый эфир 5-метилтиофен-2-карбоновой кислоты (1,40 г, выход 81%) в виде желтого маслянистого вещества. ; 1,58 г, 11,1 ммоль) и полученный раствор перемешивают при комнатной температуре в течение двух дней. Растворители упаривают при пониженном давлении и добавляют этилацетат. Затем раствор экстрагируют водным раствором гидрокарбоната натрия и водный слой подвергают обратной экстракции этилацетатом. Объединенные органические слои высушивают (сульфат натрия), фильтруют и упаривают, получая при этом метиловый эфир 5-метилтиофен-2-карбоновой кислоты (1,40 г, выход 81%) в виде желтого маслянистого вещества.
Стадия 2. Метиловый эфир 5-бромметилтиофен-2-карбоновой кислоты
N-Бромсукцинимид (фирма  Aldrich Aldrich ; 1,70 г, 9,6 ммоль) и каталитическое количество бензоилпероксида добавляют к раствору метилового эфира 5-метил-тиофен-2-карбоновой кислоты (1,40 г, 9,0 ммоль) в хлороформе (15 мл). Полученную реакционную смесь перемешивают в атмосфере аргона при кипячении с обратным холодильником (~60°С) в течение 3 ч, затем фильтруют через целит (Celite ; 1,70 г, 9,6 ммоль) и каталитическое количество бензоилпероксида добавляют к раствору метилового эфира 5-метил-тиофен-2-карбоновой кислоты (1,40 г, 9,0 ммоль) в хлороформе (15 мл). Полученную реакционную смесь перемешивают в атмосфере аргона при кипячении с обратным холодильником (~60°С) в течение 3 ч, затем фильтруют через целит (Celite ) и упаривают при пониженном давлении, получая при этом метиловый эфир 5-бромметилтиофен-2-карбоновой кислоты (2 г) в виде желтого маслянистого вещества, которое непосредственно используют на последующей стадии без дополнительной очистки. ) и упаривают при пониженном давлении, получая при этом метиловый эфир 5-бромметилтиофен-2-карбоновой кислоты (2 г) в виде желтого маслянистого вещества, которое непосредственно используют на последующей стадии без дополнительной очистки.
Промежуточное соединение 8: 5-(бифенил-4-илоксиметил)фуран-2-карбоновая кислота
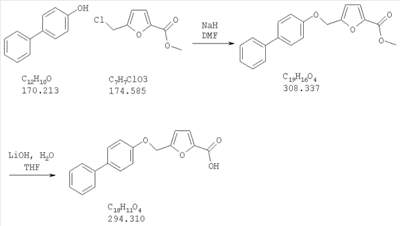
Обозначения: DMF – диметилформамид
Стадия 1: метиловый эфир 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты
N,N-Диметилформамид (400 мл) добавляют к гидриду натрия (60%-ная дисперсия; ~16 г, 0,4 моль), промытому гексаном. Полученную смесь охлаждают до ~5°С и затем добавляют раствор 4-фенилфенола (73,12 г, 0,43 ммоль) в N,N-диметилформамиде (150 мл). Полученную смесь перемешивают при комнатной температуре в течение 2,5 ч и затем добавляют раствор метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (25 г, 0,14 ммоль) в N,N-диметилформамиде (100 мл). Реакционную смесь нагревают при ~105°С в течение 2 ч, затем дают остыть, после чего упаривают при пониженном давлении, после чего добавляют воду. Полученную смесь экстрагируют три раза этилацетатом, объединенные органические слои промывают насыщенным раствором соли, высушивают (сульфат магния), фильтруют, упаривают и очищают, используя систему для очистки  Biotage 75L purification system Biotage 75L purification system , при элюировании смесью 0-10% метиленхлорид/толуол с получением при этом метилового эфира 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (20,5 г, выход 46%). , при элюировании смесью 0-10% метиленхлорид/толуол с получением при этом метилового эфира 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (20,5 г, выход 46%).
Стадия 2: 5-(бифенил-4-илоксиметил)фуран-2-карбоновая кислота
Раствор моногидрата гидроксида лития (5,10 г, 121,5 ммоль) в воде (50 мл) добавляют к раствору метилового эфира 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (15,00 г, 48,6 ммоль) в тетрагидрофуране (450 мл). Реакционную смесь перемешивают при комнатной температуре в течение 72 ч. Растворители упаривают и добавляют воду. Полученную смесь экстрагируют три раза эфиром. Отфильтровывают нерастворимое белое твердое вещество. Значение рН водного раствора доводят до 3 и затем полученную смесь экстрагируют этилацетатом (3×500 мл). Объединенные органические слои промывают 50%-ным насыщенным раствором соли и затем упаривают при пониженном давлении, получая при этом 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту (12,0 г, выход 84%) в виде белого твердого вещества.
Общая методика А получения биарилоксиметиларенкарбоновых кислот
Карбонат калия (150 мг, 1,09 ммоль) добавляют к раствору фенола (0,30 ммоль) в ДМФ (0,7 мл) и полученную смесь перемешивают в течение 15 минут. Добавляют иодид калия (4,5 мг, 0,093 ммоль) и раствор сложного эфира хлор- или бромметиларенкарбоновой кислоты (0,41 ммоль) в ДМФ (0,7 мл). Полученную смесь перемешивают при 80°С в течение 2 дней. Реакционную смесь охлаждают до комнатной температуры и затем разделяют между этилацетатом (15 мл) и водным раствором гидроксида калия (1 М, 15 мл). Органический слой пропускают через слой ( подушку подушку ) сульфата магния и высушивают в вакууме, получая при этом сложный низший алкиловый эфир. ) сульфата магния и высушивают в вакууме, получая при этом сложный низший алкиловый эфир.
Полученный сложный низший алкиловый эфир растворяют в смеси (в соотношении 3:1:1) тетрагидрофуран: метанол: вода. Добавляют моногидрат гидроксида лития (4 экв.). Полученную смесь перемешивают при 75°С в течение 2 дней и затем упаривают при пониженном давлении, полученный остаток разделяют между этиловым эфиром (15 мл) и водным раствором гидроксида калия (0,5 М, 15 мл). Водный слой отделяют, подкисляют до значения рН 1 посредством добавления 1 М раствора HCl и экстрагируют дважды этилацетатом. Органический слой пропускают через слой ( подушку подушку ) сульфата магния и высушивают в вакууме. ) сульфата магния и высушивают в вакууме.
Общая методика Б получения биарилоксиметиларенкарбоновых кислот
Карбонат калия (150 мг, 1,09 ммоль) добавляют к раствору фенола (0,30 ммоль) в ДМФ (0,7 мл) и затем полученную смесь перемешивают в течение 15 минут. Добавляют иодид калия (4,5 мг, 0,093 ммоль) и раствор сложного эфира хлор- или бромметиларенкарбоновой кислоты (0,41 ммоль) в ДМФ (0,7 мл). Затем полученную смесь перемешивают при 80°С в течение 2 дней. Реакционную смесь охлаждают до комнатной температуры и разделяют между этилацетатом (15 мл) и водным раствором гидроксида калия (1 М, 15 мл). Органический слой пропускают через слой ( подушку подушку ) сульфата магния и высушивают в вакууме, получая при этом сложный низший алкиловый эфир. ) сульфата магния и высушивают в вакууме, получая при этом сложный низший алкиловый эфир.
Полученный сложный низший алкиловый эфир растворяют в смеси тетрагидрофуран: метанол: вода (в соотношении 3:1:1). Добавляют моногидрат гидроксида лития (4 экв.). Полученную смесь перемешивают при 75°С в течение 2 дней и затем разделяют между этиловым эфиром (15 мл) и водным раствором гидроксида калия (0,5 М, 15 мл). Водный слой отделяют, подкисляют до значения рН 1 посредством добавления 1 М раствора HCl и экстрагируют дважды этилацетатом. Органический слой пропускают через слой ( подушку подушку ) сульфата магния и высушивают в вакууме. ) сульфата магния и высушивают в вакууме.
Пример 1: 3-(3-хлорбифенил-4-илоксиметил)бензойная кислота
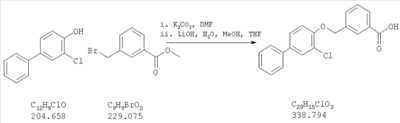
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(3-Хлорбифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 2-хлор-4-фенилфенола (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 76 мг. Масс-спектр: МН+=339. , Моркамбе, Ланкашир, Великобритания). Выход: 76 мг. Масс-спектр: МН+=339.
Пример 2: 3-(бифенил-3-илоксиметил)бензойная кислота
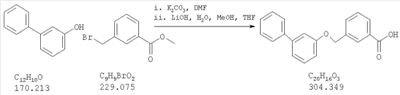
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(Бифенил-3-илоксиметил)бензойную кислоту получают, используя общую методику А, из 3-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , г.Милуоки, Висконсин (штат США)) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 76 мг. Масс-спектр (ES): MH+=305. , Моркамбе, Ланкашир, Великобритания). Выход: 76 мг. Масс-спектр (ES): MH+=305.
Пример 3: 3-(4′-метилбифенил-4-илоксиметил)бензойная кислота
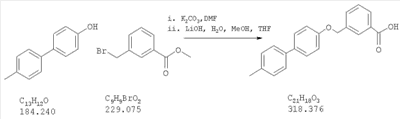
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(4′-Метилбифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4′-метилбифенил-4-ола (поставляется компанией  фирма фирма  Maybridge plc Maybridge plc  , Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 66 мг. Масс-спектр (ES): MH+=319. , Моркамбе, Ланкашир, Великобритания). Выход: 66 мг. Масс-спектр (ES): MH+=319.
Пример 4: 3-(4′-бром-бифенил-4-илоксиметил)бензойная кислота
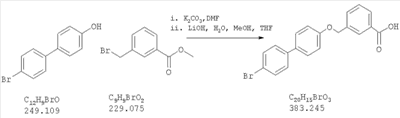
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(4′-Бром-бифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4-бром-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 91 мг. Масс-спектр (ES): MH+=383. , Моркамбе, Ланкашир, Великобритания). Выход: 91 мг. Масс-спектр (ES): MH+=383.
Пример 5: 3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота
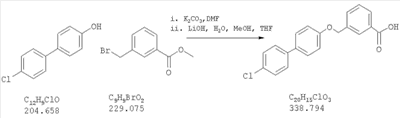
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(4′-Хлорбифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4-хлор-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и 3-(бромметил)бензойной кислоты метиловый эфир (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и 3-(бромметил)бензойной кислоты метиловый эфир (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 80 мг. Масс-спектр (ES): MH+=339. , Моркамбе, Ланкашир, Великобритания). Выход: 80 мг. Масс-спектр (ES): MH+=339.
Пример 6: 3-(2′-нитробифенил-4-илоксиметил)бензойная кислота
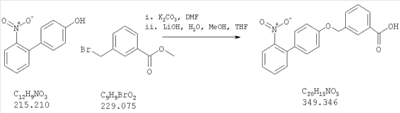
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(2′-Нитробифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4-гидрокси-2′-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 82 мг. Масс-спектр (ES): MH+=350. , Моркамбе, Ланкашир, Великобритания). Выход: 82 мг. Масс-спектр (ES): MH+=350.
Пример 7: 3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота
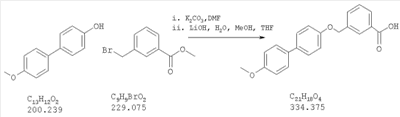
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
3-(4′-Метоксибифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4-гидрокси-4′-метоксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 3-(бромметил)бензойной кислоты (коммерчески доступное соединение, фирма  фирма фирма  Lancaster Synthesis Ltd Lancaster Synthesis Ltd . . , Моркамбе, Ланкашир, Великобритания). Выход: 73 мг. Масс-спектр (ES): MH+=335. , Моркамбе, Ланкашир, Великобритания). Выход: 73 мг. Масс-спектр (ES): MH+=335.
Пример 8: 5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота
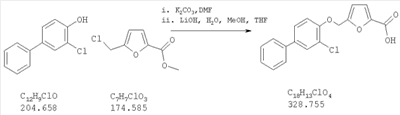
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(3-Хлорбифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 2-хлор-4-фенилфенола (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, штат Висконсин, (США), или компания «фирма , г.Милуоки, штат Висконсин, (США), или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 66 мг. Масс-спектр (ES): MH+=329. », Тинтэйгел, Великобритания). Выход: 66 мг. Масс-спектр (ES): MH+=329.
Пример 9: 5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота
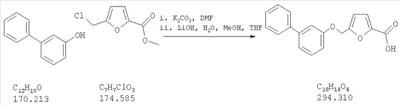
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(Бифенил-3-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 3-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Милуоки, Висконсин (штат США)) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США), или компания «фирма , г.Милуоки, Висконсин (штат США), или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 67 мг. Масс-спектр (ES): MH+=295. », Тинтэйгел, Великобритания). Выход: 67 мг. Масс-спектр (ES): MH+=295.
Пример 10: 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота
Способ 1. Из 4′-метилбифенил-4-ола и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты
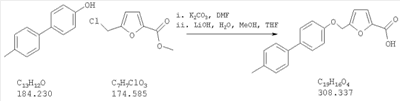
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(4′-Метилбифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 4′-метилбифенил-4-ола (поставляется компанией «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма », Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) или компания «фирма , г.Милуоки, Висконсин (штат США) или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 47 мг. Масс-спектр (ES): МН+=309. », Тинтэйгел, Великобритания). Выход: 47 мг. Масс-спектр (ES): МН+=309.
Способ 2.
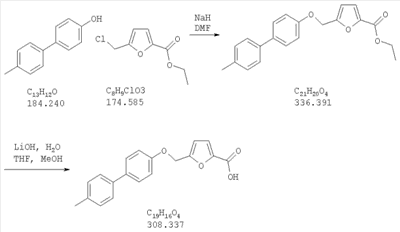
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
Стадия 1: этиловый эфир 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновой кислоты
4′-Метилбифенил-4-ол (промежуточное соединение 5; 2,0 г, 10,9 ммоль) добавляют к суспензии гидрида натрия (60%-ная дисперсия; 384 мг, 9,6 ммоль) в N,N-диметилформамиде (30 мл) и затем полученную смесь перемешивают при -5°С в течение 20 минут. Добавляют раствор этилового эфира 5-(хлор-метил)фуран-2-карбоновой кислоты (1,6 г, 8,5 ммоль) в N,N-диметилформамиде (60 мл) и затем реакционную смесь перемешивают в течение ночи при комнатной температуре. Растворители упаривают при пониженном давлении и полученный остаток разделяют между водой и этилацетатом. Водный слой экстрагируют дважды этилацетатом и затем объединенные органические слои промывают водой и насыщенным раствором соли, высушивают (сульфат натрия), фильтруют, упаривают и хроматографируют, элюируя смесью 0-50% метиленхлорид/гексан, получая при этом этиловый эфир 5-(4′-метил-бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (2,4 г, выход 84%).
Стадия 2: 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота
Раствор этилового эфира 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновой кислоты (2,00 г, 5,9 ммоль) в тетрагидрофуране (30 мл) и метаноле (10 мл) добавляют к раствору моногидрата гидроксида лития (0,476 г, 11,3 ммоль) в воде (15 мл). Добавляют метанол (5 мл) и тетрагидрофуран (10 мл) и затем реакционную смесь перемешивают при комнатной температуре в течение ночи. Растворители упаривают, затем полученный остаток суспендируют в воде и подкисляют до рН 2,5, используя 1 М раствор HCl. Полученное белое твердое вещество отфильтровывают и затем два раза суспендируют в этилацетате и упаривают, получая при этом 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновую кислоту (1,6 г, выход 88%) в виде белого твердого вещества.
Способ 3. Из метилового эфира 5-(4-иод-феноксиметил)фуран-2-карбоновой кислоты и 4-метилфенилбороновой кислоты
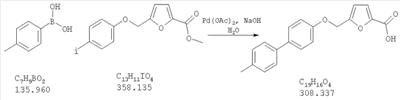
Смесь метилового эфира 5-(4-иод-феноксиметил)фуран-2-карбоновой кислоты (промежуточное соединение 6; 100 мг, 0,28 ммоль), 4-метилфенилбороновой кислоты (42 мг, 0,31 ммоль), гидроксида натрия (45 мг, 1,13 ммоль), ацетата палладия (II) (2 мг, 0,01 ммоль) и воды (10 мл) нагревают при ~50°С в течение ночи. Полученную смесь фильтруют и затем полученный остаток промывают водой, этилацетатом, метиленхлоридом и метанолом. Водный слой подкисляют и экстрагируют три раза этилацетатом. Объединенные органические слои промывают водой и насыщенным раствором соли, высушивают (сульфат магния), фильтруют и упаривают, получая при этом 5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновую кислоту (80 мг, выход 84%) в виде белого твердого вещества.
Пример 11: 5-(4′-бромбифенил-4-илоксиметил)фуран-2-карбоновая кислота
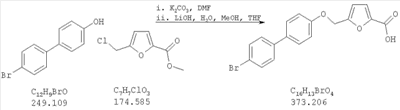
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(4′-Бром-бифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 4-бром-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США), или компания «фирма , г.Милуоки, Висконсин (штат США), или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 86 мг. Масс-спектр (ES): MH+=373. », Тинтэйгел, Великобритания). Выход: 86 мг. Масс-спектр (ES): MH+=373.
Пример 12: 5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота
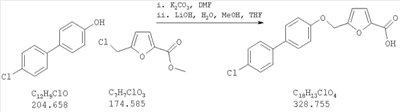
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран 5-(4′-Хлорбифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 4-хлор-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США), или компания «фирма , г.Милуоки, Висконсин (штат США), или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 72 мг. Масс-спектр (ES): MH+=329. », Тинтэйгел, Великобритания). Выход: 72 мг. Масс-спектр (ES): MH+=329.
Пример 13: 5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота
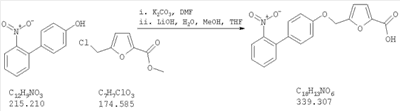
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(2′-Нитробифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 4-гидрокси-2′-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США) или компания «фирма , г.Милуоки, Висконсин (штат США) или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 82 мг. Масс-спектр (ES): MH+=340. », Тинтэйгел, Великобритания). Выход: 82 мг. Масс-спектр (ES): MH+=340.
Пример 14: 5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота
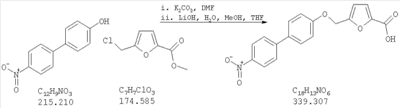
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(4′-Нитробифенил-4-илоксиметил)фуран-2-карбоновую кислоту получают, используя общую методику А, из 4-гидрокси-4′-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма , г.Портленд, штат Орегон, США) и метилового эфира 5-хлорметилфуран-2-карбоновой кислоты (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США), или компания «фирма , г.Милуоки, Висконсин (штат США), или компания «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Великобритания). Выход: 40 мг. Масс-спектр (ES): MH+=340. », Тинтэйгел, Великобритания). Выход: 40 мг. Масс-спектр (ES): MH+=340.
Пример 15: 2-(3-хлорбифенил-4-илоксиметил)бензойная кислота
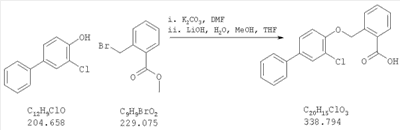
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран 2-(3-Хлорбифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 2-хлор-4-фенилфенола (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 45 мг. Масс-спектр (ES): MH+=339. , г.Портленд, штат Орегон, США) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 45 мг. Масс-спектр (ES): MH+=339.
Пример 16: 2-(4′-метилбифенил-4-илоксиметил)бензойная кислота
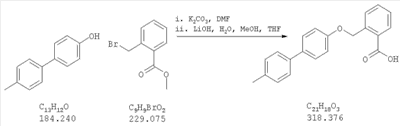
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(4′-Метилбифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4′-метилбифенил-4-ола (поставляется компанией «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 54 мг. Масс-спектр (ES): MH+=319. », Тинтэйгел, Корнуолл, Великобритания) или из промежуточного соединения 5 и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 54 мг. Масс-спектр (ES): MH+=319.
Пример 17: 2-(2′-нитробифенил-4-илоксиметил)бензойная кислота
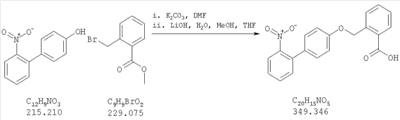
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(2′-Нитробифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4′-гидрокси-2-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 69 мг. Масс-спектр (ES): MH+=350. , г.Портленд, штат Орегон, США) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 69 мг. Масс-спектр (ES): MH+=350.
Пример 18: 2-(бифенил-4-илоксиметил)бензойная кислота
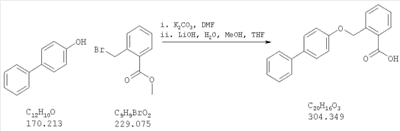
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(Бифенил-4-илоксиметил)бензойную кислоту получают, используя общую методику А, из 4-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 50 мг. Масс-спектр (ES): MH+=305. , г.Милуоки, Висконсин (штат США)) и метилового эфира 2-бромметилбензойной кислоты (промежуточное соединение 1). Выход: 50 мг. Масс-спектр (ES): MH+=305.
Пример 19: 5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновая кислота
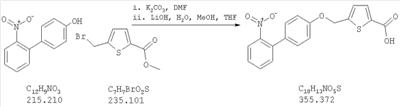
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
5-(2′-Нитробифенил-4-илоксиметил)тиофен-2-карбоновую кислоту получают, используя общую методику А, из 4-гидрокси-2′-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 5-бромметил-тиофен-2-карбоновой кислоты (промежуточное соединение 7). Выход: 80 мг. Масс-спектр (ES): MH+=356. , г.Портленд, штат Орегон, США) и метилового эфира 5-бромметил-тиофен-2-карбоновой кислоты (промежуточное соединение 7). Выход: 80 мг. Масс-спектр (ES): MH+=356.
Пример 20: 6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота
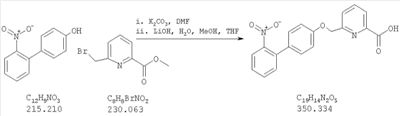
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
6-(2′-Нитробифенил-4-илоксиметил)пиридин-2-карбоновую кислоту получают, используя общую методику Б, из 4-гидрокси-2′-нитробифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и метилового эфира 6-бромметилпиридин-2-карбоновой кислоты (промежуточное соединение 2). Выход: 62 мг. Масс-спектр (ES): MH+=351. , г.Портленд, штат Орегон, США) и метилового эфира 6-бромметилпиридин-2-карбоновой кислоты (промежуточное соединение 2). Выход: 62 мг. Масс-спектр (ES): MH+=351.
Пример 21: 6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота
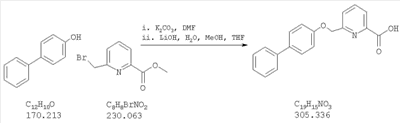
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
6-(Бифенил-4-илоксиметил)пиридин-2-карбоновую кислоту получают, используя общую методику Б, из 4-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и метилового эфира 6-бромметилпиридин-2-карбоновой кислоты (промежуточное соединение 2). Выход: 68 мг. Масс-спектр (ES): MH+=306. , г.Милуоки, Висконсин (штат США)) и метилового эфира 6-бромметилпиридин-2-карбоновой кислоты (промежуточное соединение 2). Выход: 68 мг. Масс-спектр (ES): MH+=306.
Пример 22: 2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота
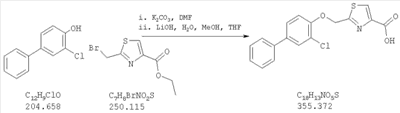
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(3-Хлорбифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 2-хлор-4-фенилфенола (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=346. , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=346.
Пример 23: 2-(бифенил-3-илоксиметил)тиазол-4-карбоновая-кислота
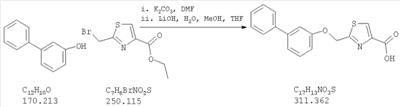
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(Бифенил-3-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 3-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 65 мг. Масс-спектр (ES): MH+=312. , г.Милуоки, Висконсин (штат США)) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 65 мг. Масс-спектр (ES): MH+=312.
Пример 24: 2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота
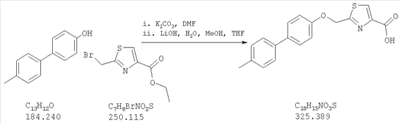
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(4′-Метилбифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4′-метилбифенил-4-ол (поставляется компанией «фирма  Maybridge plc Maybridge plc », Тинтэйгел, Корнуолл, Великобритания или из промежуточного соединения 5) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 70 мг. Масс-спектр (ES): MH+=326. », Тинтэйгел, Корнуолл, Великобритания или из промежуточного соединения 5) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 70 мг. Масс-спектр (ES): MH+=326.
Пример 25: 2-(4′-бромбифенил-4-илоксиметил)тиазол-4-карбоновая кислота
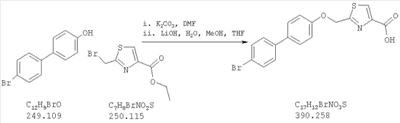
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(4′-Бром-бифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4-бром-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=390. , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=390.
Пример 26: 2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота
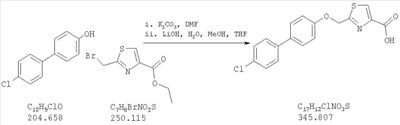
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(4′-Хлорбифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4-хлор-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=346. , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=346.
Пример 27: 2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота
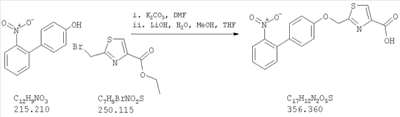
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(2′-Нитробифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4-гидрокси-4′-метоксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=357. , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 82 мг. Масс-спектр (ES): MH+=357.
Пример 28: 2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота
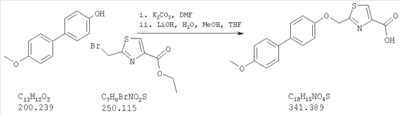
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(4′-Метоксибифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4-хлор-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 60 мг. Масс-спектр (ES): MH+=342. , г.Портленд, штат Орегон, США) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 60 мг. Масс-спектр (ES): MH+=342.
Пример 29: 2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота
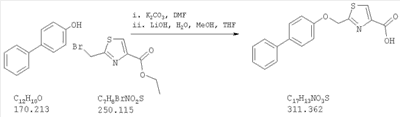
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
2-(Бифенил-4-илоксиметил)тиазол-4-карбоновую кислоту получают, используя общую методику Б, из 4-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 56 мг. Масс-спектр (ES): MH+=312. , г.Милуоки, Висконсин (штат США)) и этилового эфира 2-бромметилтиазол-4-карбоновой кислоты (промежуточное соединение 3). Выход: 56 мг. Масс-спектр (ES): MH+=312.
Пример 30: 4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота
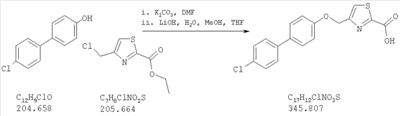
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
4-(4′-Хлорбифенил-4-илоксиметил)тиазол-2-карбоновую кислоту получают, используя общую методику Б, из 4-хлор-4′-гидроксибифенила (коммерчески доступное соединение, фирма  TCI America TCI America , г.Портленд, штат Орегон, США) и этилового эфира 4-хлорметилтиазол-2-карбоновой кислоты (промежуточное соединение 4). Выход: 71 мг. Масс-спектр (ES): MH+=346. , г.Портленд, штат Орегон, США) и этилового эфира 4-хлорметилтиазол-2-карбоновой кислоты (промежуточное соединение 4). Выход: 71 мг. Масс-спектр (ES): MH+=346.
Пример 31: 4-(Бифенил-4-илоксиметил)тиазол-2-карбоновая кислота
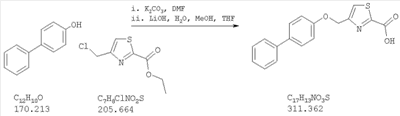
Обозначения: DMF – диметилформамид, THF – тетрагидрофуран
4-(Бифенил-4-илоксиметил)тиазол-2-карбоновую кислоту получают, используя общую методику Б, из 4-фенилфенола (коммерчески доступное соединение, фирма  Aldrich Aldrich , г.Милуоки, Висконсин (штат США)) и этилового эфира 4-хлорметилтиазол-2-карбоновой кислоты (промежуточное соединение 4). Выход: 54 мг. Масс-спектр (ES): М-ОН=294 , г.Милуоки, Висконсин (штат США)) и этилового эфира 4-хлорметилтиазол-2-карбоновой кислоты (промежуточное соединение 4). Выход: 54 мг. Масс-спектр (ES): М-ОН=294
Пример 32: 1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота
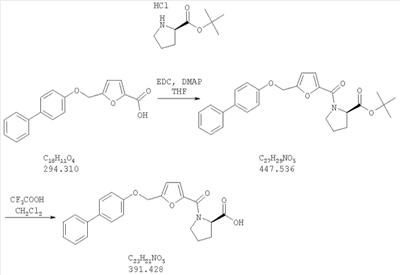
Обозначения: EDC – 1-3(диметиламинопропил)-3-этилкарбодиимид гидрохлорид), DMAP – 4-диметиламинопиридин, THF – тетрагидрофуран
Стадия 1: метиловый эфир 1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновой кислоты
Раствор 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (промежуточное соединение 8; 0,134 г, 0,46 ммоль), гидрохлорид D-пролин трет-бутилового эфира (фирма  Bachem Bachem ; 0,22 г, 1,1 ммоль), гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (фирма ; 0,22 г, 1,1 ммоль), гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида (фирма  Avocado Avocado ; 0,18 г, 0,95 ммоль) и N,N-диметиламинопиридина (0,166 г, 1,36 ммоль) в тетрагидрофуране (10 мл) перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении и затем добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом, объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки ; 0,18 г, 0,95 ммоль) и N,N-диметиламинопиридина (0,166 г, 1,36 ммоль) в тетрагидрофуране (10 мл) перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении и затем добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом, объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки  Biotage Flash 40 purification system Biotage Flash 40 purification system , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом трет-бутиловый эфир 5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновой кислоты в виде белого твердого вещества (0,115 г, выход 56%). , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом трет-бутиловый эфир 5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновой кислоты в виде белого твердого вещества (0,115 г, выход 56%).
Стадия 2: 1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-В-пирролидин-2-карбоновая кислота
Трифторуксусную кислоту (1 мл) добавляют к раствору трет-бутилового эфира 5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновой кислоты (0,115 г, 0,26 ммоль) в дихлорметане (4 мл) при 0°С. Раствору дают нагреться до комнатной температуры и затем перемешивают в течение ночи. Растворители упаривают при пониженном давлении и добавляют этилацетат. Осторожно добавляют водный раствор гидрокарбоната натрия, слои разделяют и затем отбрасывают органический слой. Водный слой подкисляют до значения рН 2, используя 1 М раствор HCl, после чего полученную смесь экстрагируют три раза этилацетатом. Органический слои объединяют, высушивают (сульфат натрия), фильтруют и упаривают. Полученный остаток растирают с эфиром и затем твердое вещество фильтруют, получая при этом 5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновую кислоту (64 мг, выход 64%) в виде белого твердого вещества.
Пример 33: (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота
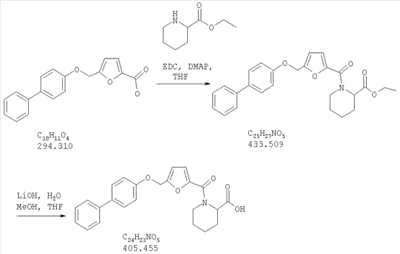
Обозначения: EDC – 1-3(диметиламинопропил)-3-этилкарбодиимид гидрохлорид), DMAP – 4-диметиламинопиридин, THF – тетрагидрофуран
Стадия 1: этиловый эфир (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил] пиперидин-2-карбоновой кислоты
Раствор 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислоты (промежуточное соединение 8; 0,098 г, 0,33 ммоль), этилпипеколинат (фирма  Aldrich Aldrich ; 0,139 г, 0,88 ммоль), 1-этил-3-(3-диметиламинопропил)-карбодиимид гидрохлорид (фирма ; 0,139 г, 0,88 ммоль), 1-этил-3-(3-диметиламинопропил)-карбодиимид гидрохлорид (фирма  Avocado Avocado ; 0,13 г, 0,68 ммоль) и N,N-диметил-аминопиридин (0,083 г, 0,68 ммоль) в тетрагидрофуране (10 мл) перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении и затем добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом, после чего объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки ; 0,13 г, 0,68 ммоль) и N,N-диметил-аминопиридин (0,083 г, 0,68 ммоль) в тетрагидрофуране (10 мл) перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении и затем добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом, после чего объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки  Biotage Flash 40 purification system Biotage Flash 40 purification system , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом этиловый эфир (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновой кислоты в виде бесцветного маслянистого вещества (0,085 г, выход 59%). , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом этиловый эфир (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновой кислоты в виде бесцветного маслянистого вещества (0,085 г, выход 59%).
Стадия 2: (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота
Раствор моногидрата гидроксида лития (0,027 г, 0,64 ммоль) в воде (1 мл) добавляют к раствору этилового эфира (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновой кислоты (0,085 г, 0,2 ммоль) в тетрагидрофуране (3 мл) и метаноле (1 мл). Полученную смесь перемешивают в течение ночи при комнатной температуре и затем растворители упаривают при пониженном давлении. Добавляют воду и этилацетат и затем полученную смесь подкисляют до значения рН 2, используя 1 М раствор HCl, после чего полученную смесь экстрагируют три раза этилацетатом. Объединенные органические слои высушивают (сульфат натрия), фильтруют и упаривают. Полученный остаток растирают с эфиром. Эфир и растворенные примеси отбирают пипеткой Пастера, получая при этом (рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновую кислоту (66 мг, выход 83%) в виде белого твердого вещества.
Пример 34: 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота
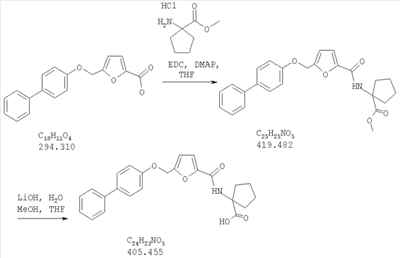
Обозначения: EDC – 1-3(диметиламинопропил)-3-этилкарбодиимид гидрохлорид), DMAP – 4-диметиламинопиридин, THF – тетрагидрофуран
Стадия 1: метиловый эфир 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}циклопентан карбоновой кислоты
Ацетилхлорид (1 мл) добавляют к охлажденному раствору метанола (10 мл) и затем раствору дают нагреться до комнатной температуры. Добавляют циклолейцин (фирма  Aldrich Aldrich ; 0,3 г, 2,3 ммоль) и затем раствор перемешивают в течение ночи при комнатной температуре. Растворитель упаривают, получая при этом гидрохлорид метилового эфира циклолейцина в виде не совсем белого твердого вещества, которое затем объединяют с 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислотой (промежуточное соединение 8; 0,085 г, 0,29 ммоль), гидрохлоридом 1-этил-3-(3-диметиламинопропил)-карбодиимида (фирма ; 0,3 г, 2,3 ммоль) и затем раствор перемешивают в течение ночи при комнатной температуре. Растворитель упаривают, получая при этом гидрохлорид метилового эфира циклолейцина в виде не совсем белого твердого вещества, которое затем объединяют с 5-(бифенил-4-илоксиметил)фуран-2-карбоновой кислотой (промежуточное соединение 8; 0,085 г, 0,29 ммоль), гидрохлоридом 1-этил-3-(3-диметиламинопропил)-карбодиимида (фирма  Avocado Avocado ; 0,128 г, 0,67 ммоль), и N,N-диметиламинопиридином (0,16 г, 1,3 ммоль) в тетрагидрофуране (5 мл). Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении, добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом и затем объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки ; 0,128 г, 0,67 ммоль), и N,N-диметиламинопиридином (0,16 г, 1,3 ммоль) в тетрагидрофуране (5 мл). Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. Растворители упаривают при пониженном давлении, добавляют воду и этилацетат. Водную фазу экстрагируют три раза этилацетатом и затем объединенные органические слои высушивают (сульфат натрия), фильтруют, упаривают и очищают, используя систему для очистки  Biotage Flash 40 purification system Biotage Flash 40 purification system , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом метиловый эфир 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновой кислоты в виде бесцветного маслянистого вещества (0,085 г, выход 59%). , с элюированием смесью метиленхлорид/ацетон в соотношении 9:1, получая при этом метиловый эфир 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновой кислоты в виде бесцветного маслянистого вещества (0,085 г, выход 59%).
Стадия 2: 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота
Раствор моногидрата гидроксида лития (0,085 г, 2,0 ммоль) в воде (1 мл) добавляют к раствору метилового эфира 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновой кислоты (0,092 г, 0,22 ммоль) в тетрагидрофуране (3 мл) и метаноле (1 мл). Полученную смесь перемешивают в течение ночи при комнатной температуре и затем растворители упаривают при пониженном давлении. Добавляют 0,5 М раствор NaOH, после чего раствор экстрагируют эфиром. Водный слой подкисляют, используя 1 М раствор HCl, полученную смесь экстрагируют три раза этилацетатом. Объединенные органические слои высушивают (сульфат натрия), фильтруют и упаривают, получая при этом 1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновую кислоту (61 мг, выход 69%) в виде белого твердого вещества.
Тест с гликогенсинтазой
Следующее тестирование проводят для того, чтобы определить активность соединений формулы (I).
Раствор субстрата, содержащего гликоген (4,32 мг/мл), 21,6 мМ UDP-глюкозы, 21,6 мМ фосфо(енол)пирувата и 2,7 мМ NADH в 30 мМ глицилглицина, буфер с рН 7,3, добавляют в количестве двенадцать мл на лунку в 384-луночные планшеты из полистирола, используемые для проведения исследования (фирма  BD Biosciences BD Biosciences ). В планшет (колонки 5-24) добавляют раствор соединения (8 мкл/лунка) различных концентраций (0-57 мМ) в 30 мМ глицилглицина, рН 7,3, 40 мМ KCl, 20 мМ MgCl2 плюс 9,2% ДМСО. В планшет (колонки 3-24) добавляют раствор фермента (12 мкл/лунка), содержащий гликогенсинтазу (16,88 мг/мл), пируваткиназу (0,27 мг/мл), лактатдегидрогеназу (0,27 мг/мл) в 50 мМ Трис-HCl, рН 8,0, 27 мМ DTT (дитиотреитол) и бычий сывороточный альбумин (БСА, 0,2 мг/мл). В качестве контроля (холостой опыт) раствор ферментов без гликогенсинтазы добавляют в верхнюю половину лунок колонок 1-2. В нижнюю половину лунок колонок добавляют известный активатор, глюкоза-6-фосфат (18,9 мМ) в добавление раствору фермента. Реакционную смесь инкубируют при 37°С. Затем регистрируют поглощение при 340 нм, используя устройство для прочтения планшетов ). В планшет (колонки 5-24) добавляют раствор соединения (8 мкл/лунка) различных концентраций (0-57 мМ) в 30 мМ глицилглицина, рН 7,3, 40 мМ KCl, 20 мМ MgCl2 плюс 9,2% ДМСО. В планшет (колонки 3-24) добавляют раствор фермента (12 мкл/лунка), содержащий гликогенсинтазу (16,88 мг/мл), пируваткиназу (0,27 мг/мл), лактатдегидрогеназу (0,27 мг/мл) в 50 мМ Трис-HCl, рН 8,0, 27 мМ DTT (дитиотреитол) и бычий сывороточный альбумин (БСА, 0,2 мг/мл). В качестве контроля (холостой опыт) раствор ферментов без гликогенсинтазы добавляют в верхнюю половину лунок колонок 1-2. В нижнюю половину лунок колонок добавляют известный активатор, глюкоза-6-фосфат (18,9 мМ) в добавление раствору фермента. Реакционную смесь инкубируют при 37°С. Затем регистрируют поглощение при 340 нм, используя устройство для прочтения планшетов  Tecan Ultra reader Tecan Ultra reader , каждые 3 минуты до окончания суммарного 30 минутного периода. , каждые 3 минуты до окончания суммарного 30 минутного периода.
Активность фермента (с соединением и без соединения) вычисляют по скорости реакции и представляют как изменение оптической плотности (AOD) в минуту. Стимулирование (в процентах) активности гликогенсинтазы при воздействии соединения в различной концентрации рассчитывают по следующей формуле:
% стимулирования=100*Rs/Rt,
где Rs означает скорость реакции фермента в присутствии соединения, a Rt означает скорость реакции фермента в отсутствие соединения.
SC2.0 определяют как концентрацию соединения, которая необходима для стимулирования 200% активности фермента.
Необходимо отметить, что изложенное выше относится к предпочтительным вариантам осуществления настоящего изобретения и что возможны различные модификации изобретения в пределах объема настоящего изобретения, который определяет приведенная далее формула изобретения.
Формула изобретения
1. Соединение формулы (I)
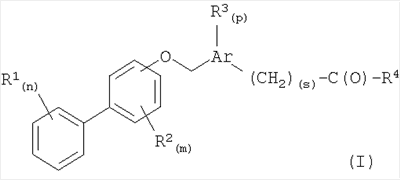
где Ar представляет собой фенил, фуранил, тиофенил, тиазолил, пиридинил;
R1 независимо выбирают из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена и нитро;
R2 независимо выбирают из группы, состоящей из водорода и галогена;
R4 представляет собой гидрокси или остаток пирролидин-2-карбоновой кислоты, пиперидин-2-карбоновой кислты или 1-аминоциклопентанкарбоновой кислоты, присоединенных через атом азота аминокислотного остатка;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4;
р означает 0, и s означает 0;
или его фармацевтически приемлемую соль, при условии, что
а) в том случае, когда Ar представляет собой фуранил, р и s означают ноль, причем соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, либо 4-(бифенил-3-илоксиметил)бензойную кислоту, либо 4-(бифенил-4-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой тиофенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
2. Соединение по п.1, где R1 и R2 представляют собой атомы водорода.
3. Соединение по п.1, где n означает 1, и R1 выбирают из группы, состоящей из метильной группы, метоксигруппы, галогена и нитрогруппы.
4. Соединение по п.3, где галоген представляет собой хлор или бром.
5. Соединение по п.1, где m означает 1 и R2 представляет собой атом хлора.
6. Соединение по п.1, где R4 представляет собой гидроксильную группу.
7. Соединение по п.1 или 2, где R4 представляет собой остаток пролина, присоединенный к соединению через атом азота.
8. Соединение по п.1, где соединение выбирают из группы, состоящей из следующих соединений:
3-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-3-илоксиметил)бензойная кислота;
3-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
3-(4′-бромбифенил-4-илоксиметил)бензойная кислота;
3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота;
2-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
2-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
2-(2′-нитробифенил-4-илоксиметил)бензойная кислота; и
2-(бифенил-4-илоксиметил)бензойная кислота.
9. Соединение по п.1, где соединение выбирают из группы, состоящей из следующих соединений:
5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-бромбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота; и
5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота.
10. Соединение по п.1, где соединение представляет собой 5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
11. Соединение по п.1, где соединение выбирают из группы, состоящей из следующих соединений:
6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота; и
6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота.
12. Соединение по п.1, где соединение выбирают из группы, состоящей из следующих соединений:
2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-3-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-бромбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота; и
4-(бифенил-4-илоксиметил)тиазол-2-карбоновая кислота.
13. Соединение по п.1, где соединение выбирают из группы, состоящей из следующих соединений:
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота;
(рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота; и
1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота.
14. Фармацевтическая композиция, стимулирующая активность гликогенсинтазы, включающая эффективное количество соединения формулы (I)
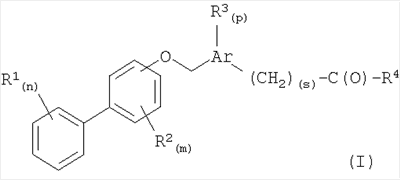
где Ar представляет собой фенил, фуранил, тиофенил, тиазолил, пиридинил;
R1 независимо выбирают из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена и нитро;
R2 независимо выбирают из группы, состоящей из водорода и галогена;
R4 представляет собой гидрокси или остаток пирролидин-2-карбоновой кислоты, пиперидин-2-карбоновой кислоты или 1-аминоциклопентанкарбоновой кислоты, присоединенных через атом азота аминокислотного остатка;
n означает 0, 1, 2, 3, 4 или 5;
m означает 0, 1, 2, 3 или 4; и
р означает 0; и
s означает 0,
или его фармацевтически приемлемую соль, при условии, что
соединение не представляет собой
5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
4-(бифенил-4-илоксиметил)бензойную кислоту, или
5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту; и фармацевтически приемлемый носитель и/или вспомогательное вещество.
15. Фармацевтическая композиция по п.14, при условии, что
а) в том случае, когда Ar представляет собой фуранил, р означает ноль, причем соединение не представляет собой либо S-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пирролидин-2-карбоновую кислоту, либо 5-(бифенил-4-илоксиметил)фуран-2-карбоновую кислоту,
б) в том случае, когда Ar представляет собой фенил, соединение не представляет собой либо 3-(бифенил-4-илоксиметил)бензойную кислоту, либо 2-(бифенил-3-илоксиметил)бензойную кислоту, и
в) в том случае, когда Ar представляет собой тиофенил, соединение не представляет собой 5-(бифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
16. Фармацевтическая композиция по п.14, где R1 и R2 представляют собой атомы водорода.
17. Фармацевтическая композиция по п.14, где n означает 1, и R1 выбирают из группы, состоящей из метила, метоксигруппы, галогена и нитрогруппы.
18. Фармацевтическая композиция по п.17, где галоген представляет собой хлор или бром.
19. Фармацевтическая композиция по п.14, где m означает 1, и R2 представляет собой атом хлора.
20. Фармацевтическая композиция по п.14, где R4 представляет собой гидроксильную группу.
21. Фармацевтическая композиция по п.14, где R4 представляет собой остаток пролина, присоединенный через атом азота.
22. Фармацевтическая композиция по п.14, где соединение выбирают из группы, состоящей из следующих соединений:
3-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-3-илоксиметил)бензойная кислота;
3-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
3-(4′-бромбифенил-4-илоксиметил)бензойная кислота;
3-(4′-хлорбифенил-4-илоксиметил)бензойная кислота;
3-(2′-нитробифенил-4-илоксиметил)бензойная кислота;
3-(4′-метоксибифенил-4-илоксиметил)бензойная кислота;
3-(бифенил-4-илоксиметил)бензойная кислота;
2-(3-хлорбифенил-4-илоксиметил)бензойная кислота;
2-(4′-метилбифенил-4-илоксиметил)бензойная кислота;
2-(2′-нитробифенил-4-илоксиметил)бензойная кислота; и
2-(бифенил-4-илоксиметил)бензойная кислота.
23. Фармацевтическая композиция по п.14, где соединение выбирают из группы, состоящей из следующих соединений:
5-(3-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(бифенил-3-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-метилбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-бромбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-хлорбифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(2′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота;
5-(4′-нитробифенил-4-илоксиметил)фуран-2-карбоновая кислота.
24. Фармацевтическая композиция по п.14, где соединение представляет собой
5-(2′-нитробифенил-4-илоксиметил)тиофен-2-карбоновую кислоту.
25. Фармацевтическая композиция по п.14, где соединение выбирают из группы, состоящей из следующих соединений:
6-(2′-нитробифенил-4-илоксиметил)пиридин-2-карбоновая кислота; и
6-(бифенил-4-илоксиметил)пиридин-2-карбоновая кислота.
26. Фармацевтическая композиция по п.14, где соединение выбирают из группы, состоящей из следующих соединений:
2-(3-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-3-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метилбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-бромбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-хлорбифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(2′-нитробифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(4′-метоксибифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
2-(бифенил-4-илоксиметил)тиазол-4-карбоновая кислота;
4-(4′-хлорбифенил-4-илоксиметил)тиазол-2-карбоновая кислота; и
4-(бифенил-4-илоксиметил)тиазол-2-карбоновая кислота.
27. Фармацевтическая композиция по п.14, где соединение выбирают из группы, состоящей из следующих соединений:
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-L-пирролидин-2-карбоновая кислота;
1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]-D-пирролидин-2-карбоновая кислота;
(рац)-1-[5-(бифенил-4-илоксиметил)фуран-2-карбонил]пиперидин-2-карбоновая кислота; и
1-{[5-(бифенил-4-илоксиметил)фуран-2-карбонил]амино}-циклопентанкарбоновая кислота.
|
|