Патент на изобретение №2372338
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 4,5-ДИЗАМЕЩЕННЫХ 2,4-ДИГИДРО-3H-1,2,4-ТРИАЗОЛ-3-ТИОНОВ
(57) Реферат:
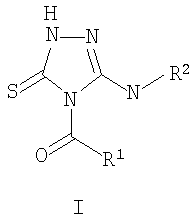
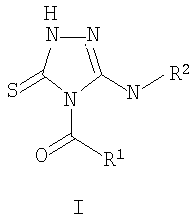
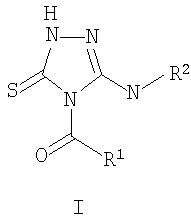
Описывается новый способ получения новых производных в ряду 5-амино-2,4-дигидро-3Н-1, 2, 4-триазол-3-тионов, а именно способ получения 4,5-дизамещенных 2,4-дигидро-3Н-1,2,4-триазол-3-тионов общей формулы I:
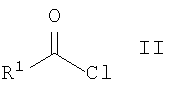
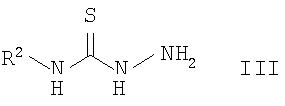
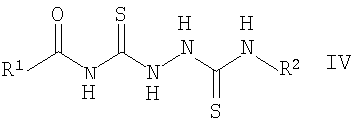
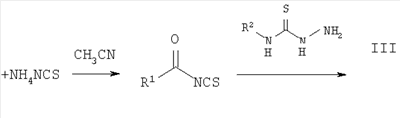
где R1=C1-C6 алкилфенил, галоидфенил, тиенил, фуранил или пирролил; R2 = фенил C1-С6 алкил, нафтил С1-С6 алкил, антрил C1-С6 алкил, С1-С6 алкоксифенил, который заключается во взаимодействии соответствующих ацилизотиоцианатов, полученных из ацилхлоридов R1-C(O)Cl и роданида аммония, с 4-R2 -тиосемикарбазидами R2-NH-C(S)-NH-NH2 и последующей циклизацией N-[2-(R2-карбамотиоил)гидразинокарбонотиоил]ациламидов в среде высококипящих алифатических спиртов. Целевой продукт, полученный с высоким выходом и чистотой, может найти применение в медицине.
Изобретение относится к способу получения производных в ряду 5-амино -2,4-дигидро-3Н-1,2,4-триазол-3-тионов, а именно к 4,5-дизамещенным 2,4-дигидро-3Н-1,2,4-триазол-3-тионам общей формулы I:
где R1=C1-С6 алкилфенил, галоидфенил, тиенил(фуранил, пирролил); R2 = фенил C1-С6 алкил, нафтил C1-С6 алкил, антрил C1-С6 алкил, C1-С6 алкокси-фенил, среди которых описано соединение, где R1=4-фторфенил, a R2 = бензил. 1,2,4-Триазольная система является важным классом органических соединений, применяемых, например, в медицине (Y.A.Al-Soud, M.N.Аl-Dweri, N.A.Al-Masoudi, Synthesis, antitumor and antiviral properties of some 1, 2, 4-triazole derivatives, II Farmaco, 2004, 59, p.775-783); в электрохимии (М.А.Quraishi, Н.К.Sharma, 4-Amino-3-butyl-5-mercapto – 1, 2, 4-triazole: a new corrosion inhibitor for mild steel in sulphuric acid. Materials Chemistry and Physics, 2002, 78, p.18-21), в качестве: катализаторов (Е.Di ez-Barra, J.Guerra, V.Homillos, S.Merino, J.Tejeda, 1, 2, 4-Triazole-based palladium pincer complexes. A new type of catalyst for the heck reaction, Organometallics 2003, Существуют разнообразные пути и методы синтеза, а также модификации производных 1, 2, 4-триазольной системы (Comprehensive heterocyclic chemistry. The structure, reactions, synthesis and uses of heterocyclic compounds, Ed. A.R.Katritzky, C.W.Rees, vol.5, Five-membered rings with two or more nitrogen atoms, Ed. K.T. Potts, 1, 2, 4-Triazoles, J.B.Polya, NY, Pergamon Press, 1984,p.734-790). Одним из примеров одностадийного синтеза 3-тио-1,2,4-триазольной системы является взаимодействие гидразидов бензойных кислот с различными изотиоцианатами в среде тетрагидрофурана при 30°С (М. – Е.Theoclitou, N.G.J.Delaet, L.A.Robinson, Rapid parallel synthesis of combinatorial libraries of substituted 3-thio-l,2,4-triazoles and 2-thioimidazoles, J. Comb. Chem., 2002, Известен также способ получения производных в ряду 3-тио-1, 2, 4-триазолов, заключающийся во взаимодействии 4-алкилтиосемикарбазидов с арилцианамидами с образованием 4-алкил-5-ариламино-1,2,4-триазол-3-тионов. Однако полученные триазолы оказываются загрязненными побочным продуктом циклизации – 1, 3, 5-трифенил-1, 2, 4, 6-трииминогексагидро-1, 3, 5-триазинами (С.Р.Joshua, К.Lissamma, К.M.Joseph, Interaction of 4-alkylthiosemicarbazide hydrochlorides with arylcyanamides: formation of 4-alkyl-3-arylamino l,2,4-triazoline-5-thiones, Indian J. Chem., Sect B, 1990, Наиболее близким по выполнению является способ получения незамещенных 5-амино-2,4-дигидро-3Н-1,2,4-триазол-3-тионов, заключающийся в циклизации этил(2-[этоксикарбониламино]карбонотиоилгидразино)карбонотиоилкарбамата в спиртовом растворе NaOH (F.Kurzer, J.L.Seeker, Addition-cyclisation of ethoxycarbonyl isothiocyanate with hydrazine derivatives as a source of thiadiazoles and triazoles, J.Heterocycl. Chem., 26 (2), p.355-360, 1989). Техническим результатом изобретения является способ получения новых производных в ряду 5-амино -2, 4-дигидро-3Н-1, 2, 4-триазол-3-тионов. Технический результат достигается способом получения соединений формулы I, синтез которых заключается во взаимодействии ацилизотиоцианатов, полученных из ацилхлоридов общей формулы II и роданида аммония, с 4-R2-тиoceмикapбaзидaми общей формулы III и последующей циклизацией N-[2-(R2-карбамотиоил) гидразинокарбонотиоил] ациламидов общей формулы IV в среде высококипящих алифатических спиртов, таких как 1-бутанол, 2-бутанол, 2-метил-1-пропанол, 2-метил-2-бутанол, 3-метил-2-бутанол, 3-метил-1-бутанол, 2,2-диметил-1-пропанол или 1-пентанол до искомых 5-(R2-амино)-4-ацил-2, 4-дигидро-3Н-1, 2, 4-триазол-3-тионов (I). Изобретение обладает изобретательским уровнем, так как не известна циклизация N-[2-(R2-карбамотиоил) гидразинокарбонотиоил] ациламидов (IV), полученных из ацилизотиоцианатов и 4-R2-тиoceмикapбaзидoв (III) до 4,5-дизамещенных 2,4-дигидро-3Н-1, 2, 4-триазол-3-тионов (I). Состав и строение всех синтезированных соединений доказано результатами элементного анализа, данными ИК- и ЯМР Н1 спектров. Структура промежуточных продуктов при получении производных 1, 2, 4-триазолов (I а-з), а именно N-(2-(R2-кapбaмoтиoил) гидpaзинoкapбoнoтиoил)aцилaмидoв (III), была доказана на примере N-(2-(бензилкарбамотиоил)гидразинокарбонотиоил)-4-метилбензамида, который удалось очистить и охарактеризовать спектральными методами. Во всех остальных случаях при попытке очистки N-(2-(R2-кapбaмoтиoил)гидpaзинoкapбoнoтиoил)aцилaмидoв они подвергались циклизации и охарактеризовать их как индивидуальные вещества не удалось. В спектре ЯМР 1Н N-(2-(бензилкарбамотиоил) гидразинокарбонотиоил)-4-метилбензамида присутствуют характеристические сигналы от четырех амидных протонов – при 8,76; 10,38; 11,37; 13,72 м.д. соответственно, а также сигнал от СН2-протонов в виде дублета ( Ниже приведена методика синтеза предлагаемых соединений. Исходные 4-R2-тиoceмикapбaзиды получены по ранее описанной методике (В.Я.Казаков, И.Я.Постовский, Получение 4-алкил- и 4-арилтио-семикарбазидов, Изв. Высш. Учеб. Зав. СССР «Хим. и хим. технология». 1961, Пример 1. Стадия 1 N-(2-(Бензилкарбамотиоил)гидразинокарбонотиоил)-4-метилбензамид Растворяют при нагревании до 60-70°С 1,37 г (0,018 моль) NH4NCS в 100 мл ацетонитрила. Раствор охлаждают до 35-40°С и при перемешивании добавляют 1,6 мл (0,012 моль) 4-метилбензоилхлорида. Суспензию перемешивают 15-20 минут. Добавляют раствор 1,81 г 4-бензилтиосемикарбазида в 50 мл ацетонитрила и продолжают перемешивать в течение 30 минут. Разбавляют холодной водой, выпавший осадок N-(2-(бензилкарбамотиоил)гидразинокарбонотиоил)-4-метилбезамида отфильтровывают, промывают водой и сушат на воздухе. Кристаллизуют из ацетонитрила. Выход 2,91 г (81,3%), т. пл. свыше 120°С циклизация. ИК-спектр, Стадия 2 5-(Бензиламино)-4-(4-метилбензоил)-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Ia) Растворяют 1,8 г (0,005 моль) N-(2-(бензилкарбамотиоил)гидразинокарбонотиоил)-4-метилбензамида в 100 мл 1-бутанола, нагревают в течение 12 часов при температуре 80°С и охлаждают до комнатной температуры. Выпавший осадок отфильтровывают, промывают горячим метанолом, сушат на воздухе. Выход 1,10 г (67,4%), т.пл. 260-261°С (1-ВuОН-ДМФА – 4:1). ИК-спектр, Аналогичные результаты получают при кипячении N-(2-(бензилкарбамотиоил)гидразинокарбонотиоил)-4-метилбензамида в 50 мл 1-бутанола в течение 4 часов. Выход 1,20 г (73,4%), т.пл. 260-261°С. Данные элементного анализа, ИК- и ЯМР 1H-спектроскопии полученного вещества совпадают с представленными выше. Аналогичные результаты получают при кипячении в среде 2-бутанола, 2-метил-1-пропанола, 2-метил-2-бутанола, 3-метил-2-бутанола, 3-метил-1-бутанола, 2,2-диметил-1-пропанола, 1-пентанола. Пример 2. 5-(Бензиламино)-4-(4-фторбензоил)-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Iб) Получают аналогично примеру 1 исходя из 1,9 г (0,012 моль) 4-фторбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,81 г (0,01 моль) 4-бензилтиосемикарбазида, без проведения очистки промежуточного продукта – N-(2-(бензилкарбамотиоил)гидразинокарбонотиоил)-4-фторбензамида, т.к. при его перекристаллизации происходит частичная циклизация. Выход 78,8%, т. пл. 272-273°С (1-ВuОН-ДМФА – 4:1). ИК-спектр, Пример 3. 5-(Бензиламино)-4-(4-хлорбензоил)-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Iв) Получают аналогично примеру 1 исходя из 2,1 г (0,012 моль) 4-хлорбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,81 г (0,01 моль) 4-бензилтиосемикарбазида. Выход 81,1%, т.пл. 258-259°С (1-ВuОН-ДМФА – 4:1). ИК-спектр, Пример 4. 5-[(9-Антрилметил)амино]-4-(4-хлорбензоил)-2, 4-дигидро-3Н-1,2,4-триазол-3-тион (Iг) Получают аналогично примеру 1 исходя из 2,1 г (0,012 моль) 4-хлорбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 2,81 г (0,01 моль) 4-(9-антрил)тиосемикарбазида. Выход 67,1%, т.пл. 290-291°С (1-BuOH-ДМФА – 4:1). ИК-спектр, Пример 5. 4-(3-фторбензоил)-5-[(2-фенилэтил)амино]-2,4-дигидро-ЗН-1,2,4-триазол-3-тион (Iд) Получают аналогично примеру 1 исходя из 1,9 г (0,012 моль) 3-фторбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,95 г (0,01 моль) 4-(2-фенилэтил)тиосемикарбазида. Выход 75,6%, т.пл. 235-236°С (1-BuOH). ИК-спектр, Пример 6. 4-(4-хлорбензоил)-5-[(2-фенилэтил)амино]-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Ie) Получают аналогично примеру 1 исходя из 2,1 г (0,012 моль) 4-хлорбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,95 г (0,01 моль) 4-(2-фенилэтил)тиосемикарбазида. Выход 75,7%, т.пл. 165-166°С (1-BuOH). ИК-спектр, Пример 7. 4-(4-трет-бутилбензоил)-5-[(2-метоксифенил)амино]-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Iж) Получают аналогично примеру 1 исходя из 2,36 г (0,012 моль) 4-трет-бутилбензоилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,97 г (0,01 моль) 4-(2-метоксифенил)тиосемикарбазида. Выход 72,4%, т. пл. 242-243°С (1-ВuОН-ДМФА – 4:1). ИК-спектр, Пример 8. 5-[(2-метоксифенил)амино]-4-(тиен-2-илкарбонил)-2,4-дигидро-3Н-1, 2, 4-триазол-3-тион (Iз) Получают аналогично примеру 1 исходя из 1,76 г (0,012 моль) тиофен-2-карбонилхлорида, 1,37 г (0,018 моль) роданида аммония и 1,97 г (0,01 моль) 4-(2-метоксифенил)тиосемикарбазида. Выход 77,8%, т. пл. 257-258°С (1-ВuОН-ДМФА – 4:1). ИК-спектр, Таким образом, разработан новый способ получения производных 1, 2, 4-триазола.
Формула изобретения
Способ получения 4,5-дизамещенных 2,4-дигидро-3Н-1,2,4-триазол-3-тионов общей формулы I:
|
||||||||||||||||||||||||||

 22, p.4610-4612), хемосенсоров (В. Du, R.Liu, Y.Zhang, W.Yang, W.Sun, M.Sun, J.Peng, Y.Cao, Novel chemosensory materials based on polyfluorenes with 2-(2
22, p.4610-4612), хемосенсоров (В. Du, R.Liu, Y.Zhang, W.Yang, W.Sun, M.Sun, J.Peng, Y.Cao, Novel chemosensory materials based on polyfluorenes with 2-(2 -pyridyl)benzimidazole and 5-methyl-3-(pyridin-2-yl)-1, 2, 4 – triazole groups in the side chain, Polymer, 2007, 48, p.1245-1254), лигандов (L.M.Field, P.M.Lahti, Coordination complexes of l-(4-[N-tert-butyl-N-aminoxyl]phenyl)-1H-1,2,4-triazole with paramagnetic transition metal dications, Inorg. Chem. 2003,
-pyridyl)benzimidazole and 5-methyl-3-(pyridin-2-yl)-1, 2, 4 – triazole groups in the side chain, Polymer, 2007, 48, p.1245-1254), лигандов (L.M.Field, P.M.Lahti, Coordination complexes of l-(4-[N-tert-butyl-N-aminoxyl]phenyl)-1H-1,2,4-triazole with paramagnetic transition metal dications, Inorg. Chem. 2003, 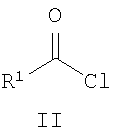
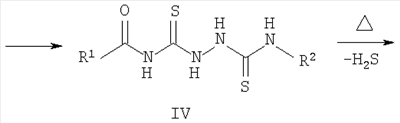
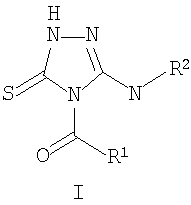
 4,74; J 5,7 Гц). В спектрах ЯМР 1Н 5(R2-амино)-4-ацил-2,4-дигидро-3Н-1,2,4-триазол-3-тионов (I а-з) присутствуют только одиночный сигнал от амидного протона в области 12-13 м.д., а сохранение сигнала от СН2-группы (в случае бензильного, 2-фенилэтильного и 9-антрилметилного производных) в виде дублета в области 3-6 м.д. однозначно свидетельствует о направлении циклизации с образованием (R2-амино)-4-ацил-2,4-дигидро-3Н-1, 2, 4-триазол-3-тионов (I а-з).
4,74; J 5,7 Гц). В спектрах ЯМР 1Н 5(R2-амино)-4-ацил-2,4-дигидро-3Н-1,2,4-триазол-3-тионов (I а-з) присутствуют только одиночный сигнал от амидного протона в области 12-13 м.д., а сохранение сигнала от СН2-группы (в случае бензильного, 2-фенилэтильного и 9-антрилметилного производных) в виде дублета в области 3-6 м.д. однозначно свидетельствует о направлении циклизации с образованием (R2-амино)-4-ацил-2,4-дигидро-3Н-1, 2, 4-триазол-3-тионов (I а-з). , см-1: 3400, 1640, 1500, 1460. Спектр ЯМР 1Н,
, см-1: 3400, 1640, 1500, 1460. Спектр ЯМР 1Н,