|
|
(21), (22) Заявка: 2008123126/15, 10.06.2008
(24) Дата начала отсчета срока действия патента:
10.06.2008
(46) Опубликовано: 10.11.2009
(56) Список документов, цитированных в отчете о
поиске:
RAO ТА, MAIYA В.G. Spectroscopic, redox and emission properties of 2-nitro-substituted free base- and metallo-tetra-aryl porphyrins, Polyhedron, 1994, vol.13,  12, p.1863-1873 Найдено из: STN International, США, номер доступа N 121:194201. SURIYANARAYANAN Р. and KRISHNAN V. SINGLET EMISSION STUDIES ON PORPHYRINS APPENDED WITH HETEROCYCLICBASES. – Photochemistry and Photobiology, 1994, vol.38 issue 5, p.533-536. Найдено из: STN International, США, номер доступа N 100:138464. Сырбу С.А., Агеева Т.А., Семейкин А.С., Койфман О.И. Синтез мезофенилзамещенных порфиринов как исходных соединений для получения порфиринсодержащих полимеров. – Изв. АН. Серия химич, 2007, 12, p.1863-1873 Найдено из: STN International, США, номер доступа N 121:194201. SURIYANARAYANAN Р. and KRISHNAN V. SINGLET EMISSION STUDIES ON PORPHYRINS APPENDED WITH HETEROCYCLICBASES. – Photochemistry and Photobiology, 1994, vol.38 issue 5, p.533-536. Найдено из: STN International, США, номер доступа N 100:138464. Сырбу С.А., Агеева Т.А., Семейкин А.С., Койфман О.И. Синтез мезофенилзамещенных порфиринов как исходных соединений для получения порфиринсодержащих полимеров. – Изв. АН. Серия химич, 2007,  4, с.680-703. 4, с.680-703.
Адрес для переписки:
141190, Московская обл., г. Фрязино, пл. Введенского, 1, ФИРЭ РАН, патентный отдел
|
(72) Автор(ы):
Румянцева Валентина Дмитриевна (RU),
Маркушев Валерий Михайлович (RU),
Панас Андрей Иванович (RU),
Шилов Игорь Петрович (RU),
Нечаев Андрей Валерьевич (RU),
Шевелева Екатерина Владимировна (RU),
Миронов Андрей Федорович (RU),
Иванов Андрей Валентинович (RU),
Барышников Анатолий Юрьевич (RU)
(73) Патентообладатель(и):
Учреждение Российской академии наук Институт радиотехники и электроники им. В.А. Котельникова РАН (RU),
Московская государственная академия тонкой химической технологии им. М.В. Ломоносова. Государственное образовательное учреждение высшего профессионального образования (RU),
Государственное учреждение Российский онкологический научный центр им. Н.Н. Блохина Российской академии медицинских наук (РОНЦ) (RU)
|
(54) ИТТЕРБИЕВЫЕ КОМПЛЕКСЫ ТЕТРАПИРАЗОЛИЛПОРФИРИНОВ КАК ФЛУОРЕСЦЕНТНЫЕ МЕТКИ ДЛЯ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ
(57) Реферат:
Изобретение относится к области лекарственных средств, в частности к иттербиевым комплексам порфиринов (ИКП), которые могут быть использованы в экспериментальной онкологии, а именно при изучении малигнизации тканей у экспериментальных животных. В качестве флуоресцентных меток для диагностики злокачественных новообразований используют Yb-комплексы замещенных 5,10,15,20-тетрапиразолилпорфиринов
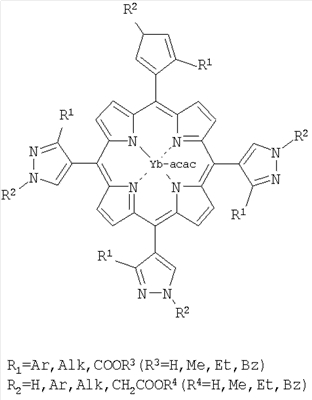
2 ил., 1 табл.
Изобретение относится к химии металлоорганических комплексов, в частности к иттербиевым комплексам порфиринов (ИКП), которые могут быть использованы в экспериментальной онкологии, а именно при изучении малигнизации тканей у экспериментальных животных, что основано на способности соединений порфиринового ряда избирательно накапливаться в злокачественных клетках и затем люминесцировать при освещении светом определенной длины волны.
 4. С.684-690], что комплексы порфиринов с иттербием обладают люминесценцией в ближней ИК-области спектра (960-1040 нм), соответствующей переходам 2F5/2 4. С.684-690], что комплексы порфиринов с иттербием обладают люминесценцией в ближней ИК-области спектра (960-1040 нм), соответствующей переходам 2F5/2 2F7/2 2F7/2 3. С.364-367]. 3. С.364-367].
В патенте США [Mody T.D., Galanter J. / Патент США  7112671, кл. МПК С07D 487/22, НКИ 540/145, опубл. 26.09.06] синтезированы водорастворимые металлокомплексы тексафиринов (расширенные порфирины с 5 атомами азота) с рядом лантаноидных элементов. В патенте США [Sessler J.L, Gregory W.H., Mody T.D. / Патент США 7112671, кл. МПК С07D 487/22, НКИ 540/145, опубл. 26.09.06] синтезированы водорастворимые металлокомплексы тексафиринов (расширенные порфирины с 5 атомами азота) с рядом лантаноидных элементов. В патенте США [Sessler J.L, Gregory W.H., Mody T.D. / Патент США  5994535, кл. МПК С07D 487/22, НПК 540/472, опубл. 30.11.1999]. Gd – комплексы тексафиринов использовали для ФДТ и ЯМР-томографии, а также испытывали их in vivo в дозе 10 мг/кг веса мышей и in vitro на культуре клеток. Вещества селективно накапливались в опухоли, и через 7 дней ее облучали. 5994535, кл. МПК С07D 487/22, НПК 540/472, опубл. 30.11.1999]. Gd – комплексы тексафиринов использовали для ФДТ и ЯМР-томографии, а также испытывали их in vivo в дозе 10 мг/кг веса мышей и in vitro на культуре клеток. Вещества селективно накапливались в опухоли, и через 7 дней ее облучали.
В выложенной заявке ФРГ [Niedball U., Gries H., Conrad J. At al. / Заявка ФРГ  3809671, кл. МПК С07D 487/22, выложена 28.09.89] металлокомплексы порфиринов с лантаноидами, синтезированные на основе производных тетрафенилпорфирина и содержащие различные органические основания, аминокислоты или амиды аминокислот, предлагаются для ЯМР, рентгеновской, фото- и радиодиагностики и терапии. 3809671, кл. МПК С07D 487/22, выложена 28.09.89] металлокомплексы порфиринов с лантаноидами, синтезированные на основе производных тетрафенилпорфирина и содержащие различные органические основания, аминокислоты или амиды аминокислот, предлагаются для ЯМР, рентгеновской, фото- и радиодиагностики и терапии.
 1621720, кл. МПК G01N 33/52, от 29.04.88], где в качестве контрастных веществ использованы иттербиевые комплексы 2,4-диметоксигематопорфирина IX, тетрасульфофенилпорфирина и 5,10,15,20-тетракис(4-карбоксифенил) порфирина. Недостатками этих комплексов являются относительно низкое время жизни люминесценции данных ИКП (не более 10 мкс), невысокая интенсивность люминенсценции и, как следствие, высокая доза (50 мг/кг веса) вводимого животным металлокомплекса порфирина. 1621720, кл. МПК G01N 33/52, от 29.04.88], где в качестве контрастных веществ использованы иттербиевые комплексы 2,4-диметоксигематопорфирина IX, тетрасульфофенилпорфирина и 5,10,15,20-тетракис(4-карбоксифенил) порфирина. Недостатками этих комплексов являются относительно низкое время жизни люминесценции данных ИКП (не более 10 мкс), невысокая интенсивность люминенсценции и, как следствие, высокая доза (50 мг/кг веса) вводимого животным металлокомплекса порфирина.
Техническим результатом изобретения является создание новых соединений, используемых в качестве флуоресцентных меток для диагностики злокачественных новообразований, которые позволяют увеличить времена жизни и интенсивность люминесценции ИКП, снизить дозы вводимого препарата при сохранении высоких значений коэффициента контраста (отношение содержания порфирина в опухоли к содержанию порфирина в соседней здоровой ткани).

Реализация данного изобретения подтверждается следующими примерами.
Пример 1.
Цинковый комплекс 5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил)пиразол-4-ил)порфирина.
1.5 г (5 ммоль) 1-N-(п-фторфенил)-3(о-хлорфенил)-4-пиразолкарбальдегида растворяли при перемешивании в 50 мл пропионовой кислоты. Нагревали реакционную смесь почти до кипения, добавляли 1 г ацетата цинка, затем 0.483 мл (5 ммоль) пиррола. Перемешивали при кипячении 3 ч. Затем реакционную смесь выливали в воду, нейтрализовали содой. Экстрагировали хлороформом, промывали водой, сушили над Na2SO4. После удаления растворителя цинковый комплекс очищали методом флэш-хроматографии на сухой колонке, элюировали хлороформом.
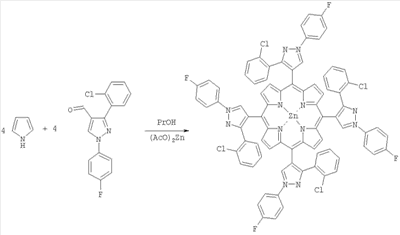
5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил)пиразол-4-ил)порфирин.
Цинковый комплекс 5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил)пиразол-4-ил)порфирина растворяли в ТГФ (тетрагидрофуран) при перемешивании, добавляли 5 мл концентрированной HCI, перемешивали 1.5 ч. Затем нейтрализовали водным аммиаком, промывали водой, сушили над Na2SO4, упаривали. Заливали 15 мл метанола, нерастворившийся осадок отфильтровывали, перекристаллизовывали из системы ТГФ/гептан. Выход 220 мг (12%). Электронный спектр,  макс, нм (10-3): 427.0 (290.9), 523.9 (17.86), 559.0 (11.0), 597.0 (5.98), 658.6 (7.65). Спектр 1H-ЯМР, ( макс, нм (10-3): 427.0 (290.9), 523.9 (17.86), 559.0 (11.0), 597.0 (5.98), 658.6 (7.65). Спектр 1H-ЯМР, ( , м.д.), (CDCl3): 9.15 (8H, с, , м.д.), (CDCl3): 9.15 (8H, с,  -Н), 8.75 (4Н, с, pyrazole-H), 6.55-8.14 (32H, м, Ar-H), -1.8 (2H, с, NH). Найдено: масс-спектр, m/z: 1392.706. Вычислено: для C80H46N12F4Cl4 м.м. 1393. -Н), 8.75 (4Н, с, pyrazole-H), 6.55-8.14 (32H, м, Ar-H), -1.8 (2H, с, NH). Найдено: масс-спектр, m/z: 1392.706. Вычислено: для C80H46N12F4Cl4 м.м. 1393.
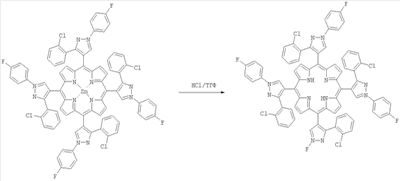
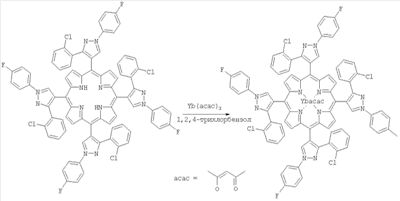
Иттербиевый комплекс 5,10,15,20-тетра(1N-(п-фторфенил)-3(о-хлорфенил) пиразол-4-ил)порфирина.
28 мг (0.02 ммоль) свободного основания порфирина и 30 (0.08 ммоль) мг ацетилацетоната иттербия суспендируют в 15 мл 1,2,4-трихлорбензола и кипятят в токе аргона 5 ч. После охлаждения реакционную массу пропускают через столбик оксида алюминия, тщательно промывают петролейным эфиром для удаления 1,2,4-трихлорбензола, а затем окрашенную зону элюируют при нагревании смесью хлороформ-изопропанол (3:1). Растворители удаляют при пониженном давлении и остаток хроматографируют на пластинках с силикагелем 5/40 мкм, отбирая менее подвижную малиновую зону иттербиевого комплекса. Выход 14.6 мг (42%). Электронный спектр поглощения,  макс., нм: 425, 557, 596. ИК-спектр, v, см-1: 1551 и 1594 (acac). макс., нм: 425, 557, 596. ИК-спектр, v, см-1: 1551 и 1594 (acac).
Пример 2.
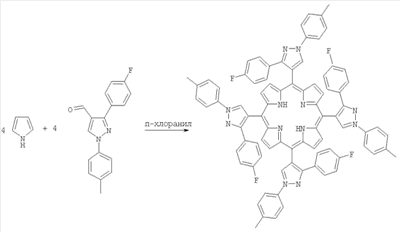
5,10,15,20-тетра(1-N-(п-метилфенил)-3(п-фторфенил)пиразол-4-ил)порфирин.
В 420 мл хлороформа растворяли 1.171 г (4.2 ммоль) 1-N-п-метилфенил-3(п-фторфенил)-4-пиразолкарбальдегида, 0.30 мл (4.2 ммоль) пиррола, 3.15 мл CH3OH при перемешивании. Реакционную смесь барботировали аргоном в течение всего времени реакции, добавляли 0.176 мл (1.40 ммоль) эфирата трехфтористого бора. Перемешивали 1 ч при комнатной температуре, затем 1 ч при кипячении. Добавляли 0.775 г (3.15 ммоль) п-хлоранила, перемешивали 1 ч при нагревании. После удаления растворителя порфирин очищали методом флэш-хроматографии на сухой колонке на оксиде алюминия, элюировали хлороформом. Выход 140 мг (10.2%). Электронный спектр,  макс, нм (отношение интенсивностей): 428.8 (0.53), 522.0 (0.048), 559.6 (0.03), 596.6 (0.02), 655.0 (0.01). Спектр 1H-ЯМР, (CDCl3, макс, нм (отношение интенсивностей): 428.8 (0.53), 522.0 (0.048), 559.6 (0.03), 596.6 (0.02), 655.0 (0.01). Спектр 1H-ЯМР, (CDCl3,  , м.д.): 9.02 (8Н, с, , м.д.): 9.02 (8Н, с,  -Н), 8.73 (4Н, с, pyrazole-H), 6.43-8.01 (32Н, м, Ar-Н), 2.03 (12Н, с, Me-Н), -1.8 (2Н, с, NH). Найдено: масс-спектр, m/z: 1311.879. Вычислено: для C84H58N12F4 м.м. 1312. -Н), 8.73 (4Н, с, pyrazole-H), 6.43-8.01 (32Н, м, Ar-Н), 2.03 (12Н, с, Me-Н), -1.8 (2Н, с, NH). Найдено: масс-спектр, m/z: 1311.879. Вычислено: для C84H58N12F4 м.м. 1312.
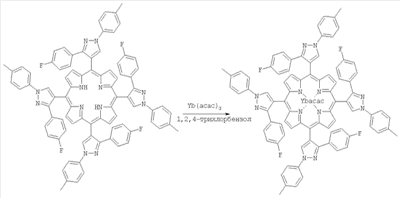
Иттербиевый комплекс 5,10,15,20-тетра(1-N-(п-метилфенил)-3(п-фторфенил)пиразол-4-ил)порфирина.
30 мг (0.023 ммоль) порфирина, 35 (0.09 ммоль) мг ацетилацетоната иттербия суспендируют в 20 мл 1,2,4-трихлорбензола и кипятят в токе азота 7 часов. Реакционную массу пропускают через столбик оксида алюминия, оставшийся трихлорбензол вымывают петролейным эфиром. Растворители упаривают на роторном испарителе и остаток хроматографируют на пластинках с силикагелем в хлороформе. Иттербиевый комплекс порфирина отделяют, элюируют с силикагеля и перекристаллизовывают из смеси хлороформ-метанол (1:7). Электронный спектр  макс, нм: 426, 520, 558, 597. ИК-спектр, v, см-1: 1550 и 1596 (асас). макс, нм: 426, 520, 558, 597. ИК-спектр, v, см-1: 1550 и 1596 (асас).
Пример 3.
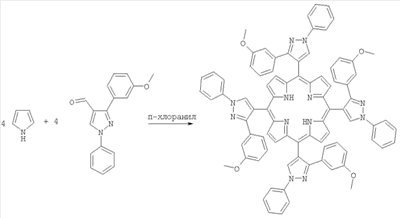
5,10,15,20-тетра(1-N-фенил-3(м-метоксифенил)пиразол-4-ил)порфирин.
В 750 мл хлороформа растворяли 2.08 г (7.5 ммоль) 1-N-фенил-3(м-метоксифенил)-4-пиразолкарбальдегида, 0.52 мл (7.5 ммоль) пиррола, 5.62 мл CH3OH при перемешивании. Реакционную смесь барботировали аргоном в течение всего времени реакции, добавляли 0.315 мл (2.5 ммоль) эфирата трехфтористого бора. Перемешивали 1 ч при комнатной температуре, затем 1 ч при кипячении. Добавляли 1.38 г (5.6 ммоль) п-хлоранила, перемешивали 1 ч при нагревании. После удаления растворителя порфирин очищали методом флэш-хроматографии на сухой колонке на оксиде алюминия, элюировали хлороформом. Перекристаллизовывали из системы ТГФ/гептан (1:2). Выход 410 мг (17%). Электронный спектр,  макс, нм (10-3): 428.0 (208.4), 522.1 (13.58), 558.4 (6.74), 595.7 (4.45), 652.4 (2.24). Спектр 1H-ЯМР, ( макс, нм (10-3): 428.0 (208.4), 522.1 (13.58), 558.4 (6.74), 595.7 (4.45), 652.4 (2.24). Спектр 1H-ЯМР, ( , м.д.), (CDCl3): 9.0 (8H, с, , м.д.), (CDCl3): 9.0 (8H, с,  -Н), 8.63 (4Н, с, pyrazole-H), 6.45-8.1 (36Н, м, Ar-Н), 3.0-3.3 (12Н, м, -OCH3), -1.8 (2Н, с, NH). -Н), 8.63 (4Н, с, pyrazole-H), 6.45-8.1 (36Н, м, Ar-Н), 3.0-3.3 (12Н, м, -OCH3), -1.8 (2Н, с, NH).
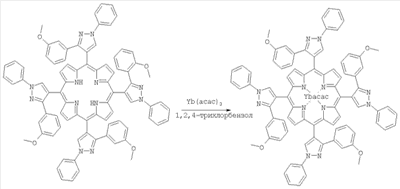
Иттербиевый комплекс 5,10,15,20-тетра(1-N-фенил-3(м-метоксифенил)пиразол-4-ил)порфирина.
25 мг (0.019 ммоль) порфирина, 35 (0.09 ммоль) мг ацетилацетоната иттербия суспендируют в 5 мл 1,2,4-трихлорбензола и кипятят в токе азота 7 часов. Реакционную массу пропускают через столбик оксида алюминия, оставшийся трихлорбензол вымывают петролейным эфиром. Растворители упаривают на роторном испарителе и остаток хроматографируют на пластинках с силикагелем в хлороформе. Иттербиевый комплекс порфирина отделяют, элюируют с силикагеля и перекристаллизовывают из смеси хлороформ-метанол (1:7). Электронный спектр  макс, нм: 431, 557, 594.6. ИК-спектр, v, см-1: 1551 и 1598 (асас). макс, нм: 431, 557, 594.6. ИК-спектр, v, см-1: 1551 и 1598 (асас).
Изучали спектры люминесценции Yb-комплексов тетрапиразолилпорфиринов в диметилсульфоксиде и определяют по кинетике затухания время жизни новых ИКП и сравнивали их с веществами, описанными в прототипе.
Спектр интенсивности люминесценции и кинетика ее затухания для Yb-комплекса 5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил) пиразол-4-ил)порфирина приведены на Фиг.1. и Фиг.2. Для сравнения там же представлены спектры люминесценции и кинетики затухания для ИКП, выбранных в качестве прототипа.
Как видно из Фиг.1, время жизни для Yb-комплекса 5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил)пиразол-4-ил)порфирина составляет около 20 мкс, что значительно превосходит времена жизни ИКП, выбранных в качестве прототипов (11 мкс для Yb-2,4-диметоксигематопорфирина IX и 8 мкс для Yb-комплекса 5,10,15,20-тетракис(4-карбоксифенил)порфирина).
Эффективность данных соединений как флуоресцентных меток подтверждается испытаниями на животных. В связи с тем, что производные тетрапиразолилпорфиринов являются гидрофобными соединениями, то для их солюбилизации использовали фосфатидилхолиновые липосомы. Для этого 2 мг металлокомплекса и 20 мг яичного лецитина в 3 мл хлороформа и 2 мл этанола упаривают досуха на роторном испарителе. Добавляли 1 мл 0.9% раствора хлорида натрия и озвучивали на ультразвуковой бане в течение 20 минут.
Экспериментальным животным (мышкам) с химически индуцированной опухолью вводили иттербиевые комплексы тетрапиразолилпорфиринов в хвостовую вену в дозе 5 мг/кг веса. Через 24 часа облучали лазером малигнизированные и нормальные ткани, проводили измерение сигнала люминесценции в области 975 нм, а затем рассчитывали коэффициент контрастности по отношению индекса люминесценции малигнизированных и нормальных тканей. Максимальный коэффициент контраста Ys составлял 49 через 24 час после введения препарата.
Преимущество предлагаемых тетрапиразолилпорфиринов по сравнению с соединениями, заявленными в прототипе, заключается в снижении дозы вводимых животным веществ, увеличении времени жизни люминесценции при сохранении высоких значений коэффициента контраста (табл.).
| Соединение |
Время жизни люминесценции (×10-6), с |
Вводимая доза, мг/кг |
Коэффициент контрастности |
| Yb-комплекс 5,10,15,20-тетра(1-N-(п-фторфенил)-3(о-хлорфенил)пиразол-4-ил)порфирина. |
20 |
5 |
49 |
| Yb-2,4-диметоксигематопорфирина IX |
11 |
50 |
48 |
Литература
 4. С.684-690. 4. С.684-690.
 3. С.364-367. 3. С.364-367.
3. Mody T.D., Galanter J. / Патент США  7112671, кл. МПК С07D 487/22, НКИ 540/145, опубл. 26.09.06. 7112671, кл. МПК С07D 487/22, НКИ 540/145, опубл. 26.09.06.
4. Sessler J.L, Gregory W.H., Mody T.D. / Патент США  5994535, кл. МПК С07D 487/22, НПК 540/472, опубл. 30.11.1999. 5994535, кл. МПК С07D 487/22, НПК 540/472, опубл. 30.11.1999.
5. Niedball U., Gries H., Conrad J. At al. / Заявка ФРГ  3809671, кл. МПК С07D 487/22, выложена 28.09.89. 3809671, кл. МПК С07D 487/22, выложена 28.09.89.
 1621720, кл. МПК G01N 33/52 от 29.04.88. 1621720, кл. МПК G01N 33/52 от 29.04.88.
 4. С.680-703. 4. С.680-703.
Формула изобретения
Yb-комплексы замещенных 5,10,15,20-тетрапиразолилпорфиринов
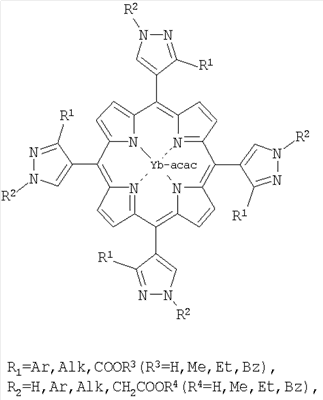
в качестве флуоресцентных меток для диагностики злокачественных новообразований.
РИСУНКИ
|
|