|
|
(21), (22) Заявка: 2008102156/04, 24.01.2008
(24) Дата начала отсчета срока действия патента:
24.01.2008
(46) Опубликовано: 27.10.2009
(56) Список документов, цитированных в отчете о
поиске:
WO 200609862 A1, 21.09.2006. WO 03055878 A1, 10.07.2003. CIUSTEA MIHAI et al. Identification of Non-Nucleoside DNA Synthesis Inhibitors of Vaccinia Virus by High-Throughput Screening. Journal of Medicinal Chemistry. 2008, 51(20), 6563-6570. RAGHAVENDRA M. et al. Microwave-assisted one-pot synthesis of some new furo[2,3-b]quinolines using potassiumcarbonate under solvent-free conditions. Canadian Journal of Chemistry, 2007, 85(12), 1041-1044. ВАСHIТЕ, ETIFY ABDEL-GHAFAR. Synthesis of new pyrazolo[3,4-b]quinolines, thieno[2,3-b]quinolines, and related condensed heterocyclic systems. Journal of the Chinese Chemical Society, 2001, 48(6B), 1175-1183. MEKHEIMER, RAMADAN A. et al. Fused quinoline heterocycles IV. First synthesis of four heterocyclic ring systems of 1H-5-thia-1,2,3,6-tetraazaacephenanthrylenes and 1H-5-thia-1,3,6-triazaacephenanthrylenes. Phosphorus, Sulfur and Silicon and the Related Elements, 2001, 175, 49-63. FATHY N.M. Synthesis of some thienoquinoline derivatives with expected pharmacological activity. Communications de la Faculte des Sciences de l’Universite d’Ankara. Series B: Chemistry and Chemical Engineering (1994). Volume Date 1991, 37(1-2), 1-8 (2008), 51(20), 6563-6570. RAGHAVENDRA M. et al. Microwave-assisted one-pot synthesis of some new furo[2,3-b]quinolines using potassium carbonate under solvent-free conditions. Canadian Journal of Chemistry. 2007, 85(12), 1041-1044. FATHY, N.M. et al. Synthesis of some thienoquinoline derivatives with expected pharmacological activity. Egyptian Journal of Pharmaceutical Sciences,1990, 31(1-4), 375-83. RAJ Т. TILAK et al. Synthesis of pyrimido[4′,5′-4,5]thieno[2,3-b]quinolm-4(3H)-ones” Journal of Chemical Research. Synopses, 1988, (2), 50. HULL ROY. Reactions of heterocycles with thiophosgene. V. 7-Chloro-1,2-dihydro-4-methoxy-2-thioxoquinoline-3-carboxaldehyde, a product from 7-chloro-4-methoxyquinoline. Journal of the Chemical Society, Perkin Transactions 1: Organic and Bio-Organic Chemistry (1972-1999), 1975, (22), 2271-80. HULL ROY. Reactions of heterocycles with thiophosgene. II. Chemistry of 3-formylqumoline-2(1H)-thione. Journal of the Chemical Society. Perkin Transactions 1: Organic and Bio-Organic Chemistry (1972-1999), 1973, (23), 2911-14. RU 2257385 C2, 27.07.2005.
Адрес для переписки:
141400, Московская обл., г. Химки, ул. Рабочая, 2а, корп.1, ЦВТ “ИИХР”, Н.М. Шмаковой
|
(72) Автор(ы):
Иващенко Александр Васильевич (US),
Иващенко Андрей Александрович (RU),
Кравченко Дмитрий Владимирович (RU)
(73) Патентообладатель(и):
Иващенко Андрей Александрович (RU),
АЛЛА ХЕМ, ЛЛС (US)
|
(54) ФУРО- И ТИЕНО[2,3-b]-ХИНОЛИН-2-КАРБОКСАМИДЫ, СПОСОБ ПОЛУЧЕНИЯ И ПРОТИВОТУБЕРКУЛЕЗНАЯ АКТИВНОСТЬ
(57) Реферат:
Данное изобретение относится к синтезу новых замещенных фуро[2,3-b]хинолин-2-карбоксамидов и замещенных тиено[2,3-b]хинолин-2-карбоксамидов или их рацематов, или их оптических изомеров, а также их фармацевтически приемлемых солей и/или гидратов общей формулы (I), которые обладают противотуберкулезной активностью. В соединении общей формулы (I)
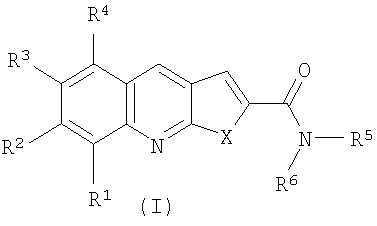
каждый из R1, R2, R3, R4 представляет собой заместитель циклической системы, выбранный из водорода, галогена, C1-С6-алкила; C1-С6-алкоксигруппы; Х представляет собой гетероатом, выбранный из кислорода или серы; R5 и R6 независимо друг от друга представляют собой заместители аминогруппы, выбранные из водорода, возможно замещенного C1-С6-алкила; возможно замещенного С3-С6-циклоалкила, который может быть аннелирован с бензольным кольцом; возможно замещенного фенила, который может быть аннелирован с диоксолом, диоксином, с группой -(СН2)n, где n=4-6, или с 5-6-членным возможно замещенным и возможно конденсированным азагетероциклилом; возможно замещенного насыщенного или ненасыщенного 5-6-членного гетероциклила, содержащего 1-2 гетероатома, выбранных из азота, кислорода, серы и возможно конденсированного с бензольным кольцом, или R5 и R6 вместе с атомом азота, с которым они связаны, образуют необязательно замещенный 5-6-членный азагетероцикл, возможно содержащий дополнительно гетероатом, выбранный из азота, и возможно аннелированный с бензольным кольцом или спироконденсированный с диоксолом, при этом заместители в указанном алкиле, циклоалкиле, фениле и гетероциклиле выбираются из атомов галогена, возможно замещенного C1-С6-алкила, СF3, возможно замещенного С3-С6-циклоалкила, возможно замещенного фенила, 5-6-членного гетероциклила, нитрогруппы, замещенной аминогруппы, алкилоксикарбонила, замещенного карбонила, аминокарбонила, алкилсульфанила. 7 н. и 2 з.п. ф-лы, 7 табл., 1 ил.
Текст описания приведен в факсимильном виде.                                                                         
Формула изобретения
1. Азагетероциклические соединения, представляющие собой замещенные фуро[2,3-b]хинолин-2-карбоксамиды и замещенные тиено[2,3-b]хинолин-2-карбоксамиды, или их рацематы, или их оптические изомеры, а также их фармацевтически приемлемые соли и/или гидраты общей формулы (I)

где каждый из R1, R2, R3, R4 представляет собой заместитель циклической системы, выбранный из водорода, галогена, C1-С6-алкила; C1-С6-алкоксигруппы;
Х представляет собой гетероатом, выбранный из кислорода или серы;
R5 и R6 независимо друг от друга представляют собой заместители аминогруппы, выбранные из водорода, возможно замещенного C1-С6-алкила;
возможно замещенного С3-С6-циклоалкила, который может быть аннелирован с бензольным кольцом;
возможно замещенного фенила, который может быть аннелирован с диоксолом, диоксином, с группой -(СН2)n, где n=4-6, или с 5-6-членным возможно замещенным и возможно конденсированным азагетероциклилом;
возможно замещенного насыщенного или ненасыщенного 5-6-членного гетероциклила, содержащего 1-2 гетероатома, выбранных из азота, кислорода, серы и возможно конденсированного с бензольным кольцом,
или R5 и R6 вместе с атомом азота, с которым они связаны, образуют необязательно замещенный 5-6-членный азагетероцикл, возможно содержащий дополнительно гетероатом, выбранный из азота, и возможно аннелированный с бензольным кольцом или спироконденсированный с диоксолом,
при этом заместители в указанном алкиле, циклоалкиле, фениле и гетероциклиле выбираются из атомов галогена, возможно замещенного C1-С6-алкила, CF3, возможно замещенного С3-С6-циклоалкила, возможно замещенного фенила, 5-6-членного гетероциклила, нитрогруппы, замещенной аминогруппы, алкилоксикарбонила, замещенного карбонила, аминокарбонила, алкилсульфанила; исключая:
соединения, в которых Х=O, R1=R2=R4=R5=R6=H, R3=H, СН3, ОСН3;
соединения, в которых X=S, R1=R2=R3=R4=R5=H, R6=H, 1-азабицикло[2.2.2]окт-3-ил;
соединения, в которых X=S, R1=R3=R4=R5=H, R2=CH3, R6=H, СН3, 2,5-диоксопирролидин-1-ил, 1,3-диоксоизоиндолин-2-ил, или R5 и R6 вместе с атомом азота, с которым они связаны, образуют 3,5-диметил-4,5-дигидро-1Н-пиразол-1-ил, 5-метил-1Н-пиразол-3(2Н)-оксо-2-ил;
соединения, в которых X=S, R1=R2=R4=R5=H, R3=трет-бутил, R6=H, (CH2)2NHBoc, (CH2)2NH2, (CH2)2NHCH3, (СН2)2N(СН3)2, (CH2)2CN, CH2CN, [1-(2,4-диметоксибензил)-2-оксо-азетидин-3-ил], 2-оксо-азетидин-3-ил, 2-амино-1-(S)-фенил-этил, 2(S)-амино-1-(3-аминофенил)этил, 2-амино-1(S)-{3-[(пиразин-2-карбонил)амино]фенил}этил, 2-амино-1(S)-{3-[(3-аминопиразин-2-карбонил)амино]фенил}этил, 2-амино-1(S)-{3-[(5-метил-изоксазол-3-карбонил)амино]фенил}этил;
и соединения, в которых X=S, R1=R2=R4=R5=H, R3=1-метил-циклопентил, R6=2-амино-1-(S)-{3-[(фуран-2-карбонил)амино]фенил}этил, 2-амино-1(S)-{3-[(1-метил-1Н-пиразол-3-карбонил)-амино]фенил}этил.
2. Соединения по п.1, представляющие собой замещенные фуро[2,3-b]хинолин-2-карбоксамиды и тиено[2,3-b]хинолин-2-карбоксамиды, содержащие пиперидиновый, пиперазиновый или пирролидиновый фрагмент, общей формулы II
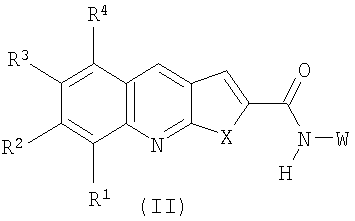
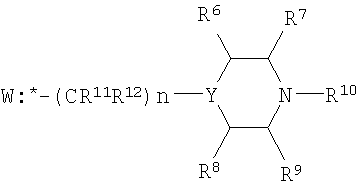 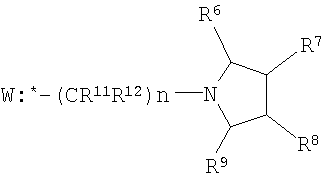
где R1, R2, R3, R4 и Х имеют вышеуказанное значение; W представляет собой замещенные пиперидин, пиперазин или пирролидин;
R6, R7, R8, R9 и R10 независимо друг от друга представляют собой водород, возможно замещенные C1-С6-алкил, С3-С6-циклоалкил, возможно замещенные фенил, этоксикарбонил, карбамоил, оксогруппу;
n – означает число -C(R11R12)- групп и принимает значения от 0 до 3;
R11, R12 представляют собой водород;
Y – представляет собой углерод или азот.
3. Соединения по п.1 или 2, представляющие собой замещенные N-((пиперидин-4-ил)метил)фуро[2,3-b]хинолин-2-карбоксамиды и замещенные N-((пиперидин-4-ил)метил)тиено[2,3-b]хинолин-2-карбоксамиды общей формулы III
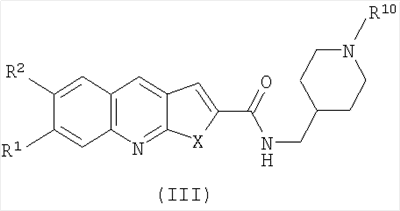
где R1, R2, R10 и Х имеют вышеуказанное значение.
4. Способ получения фуро[2,3-b]хинолин-2-карбоксамидов (Х=O) 3 и тиено[2,3-b]хинолин-2-карбоксамидов (X=S) 4 по любому из пп.1-3 взаимодействием замещенных карбоновых кислот 1 с подходящими аминами 2 в присутствии 1,1′-карбонилдиимидазола (КДИ) в среде органического растворителя
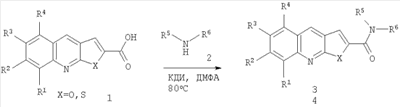
5. Активное начало для фармацевтических композиций и лекарственных средств, обладающее противотуберкулезной активностью и представляющее собой соединения общей формулы I по любому из пп.1, 2 или 3.
6. Фармацевтическая композиция, обладающая противотуберкулезной активностью, содержащая фармацевтически эффективное количество активного начала по п.5.
7. Способ получения фармацевтической композиции по п.6 смешением эффективного количества активного начала по п.5 с инертным наполнителем и/или растворителем.
8. Лекарственное средство в форме таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, для профилактики и лечения туберкулеза, включающее в свой состав активное начало по п.5 или фармацевтическую композицию по п.7.
9. Способ профилактики и лечения туберкулеза путем введения лекарственного средства по п.8.
РИСУНКИ
|
|