Патент на изобретение №2371441
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИАЛКИЛ(2,2,5,5-ТЕТРААЛКИЛ)-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОФУРАНОВ
(57) Реферат:
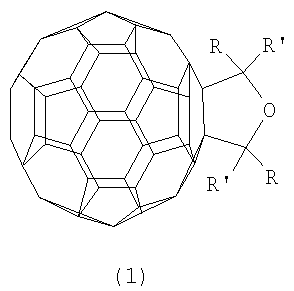
Изобретение относится к области органической химии, а именно к способу получения новых 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов общей формулы (1)
где R=Ме, R’=H; R=Pr, R’=H; R=R’=Me, заключающемуся во взаимодействии фуллерена С60 с диалкиловыми (диизоалкиловыми) эфирами общей формулы (RR’CH)2O, где R=Me, R’=H; R=Pr, R’=H, R=R’=Me в присутствии катализатора титанацендихлорида в мольном соотношении С60:эфир:Ср2ТiСl2=0.01:(5-15):(0.0015-0.0025) в среде толуола при температуре 140-160°С в течение 5-7 часов. Выход целевого продукта составляет 47-70%. Эти соединения могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами. 1 табл.
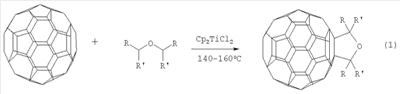
Предлагаемое изобретение относится к органической химии, конкретно к способу получения 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов общей формулы (I):
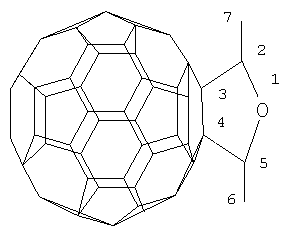
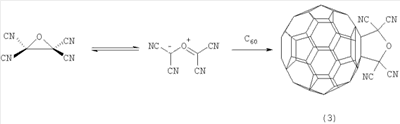
где R=Me, R’=H; R=Pr, R’=H; R=R’=Me. Функционально замещенные фуллерены могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами. Известен способ ([1] M.Ohno, A.Yashiro, S.Eguchi. Chem. Commun., 1996, 291) получения фуллеродигидрофурана формулы (2) с 27-60% выходом реакцией окислительного циклоприсоединения Известный способ не позволяет получать 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофураны (1). Известен способ ([2] N.Jagerovic, J.Elguero, J.-L.Aubagnac. J.Chem. Soc., Perkin Trans., 1996, 1, 499) получения стабильного тетрагидрофуранового аддукта фуллерена формулы (3) реакцией циклоприсоединения карбонилида, генерированного путем термического раскрытия цикла тетрацианооксирана, к С60 при температуре >100°С по схеме Известный способ не позволяет получать 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофураны (1). Таким образом, в литературе отсутствуют сведения по селективному синтезу 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов (1). Предлагается новый способ получения 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов общей формулы (1). Сущность способа заключается во взаимодействии фуллерена С60 с диалкиловыми (диизоалкиловыми) эфирами в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятыми в мольном соотношении С60:эфир:Ср2TiCl2=0.01:(5-15):(0.0015-0.0025), предпочтительно 0.01:10:0.0020, при температуре 140-160°С в течение 5-7 ч в растворе толуола. Выход 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов (1) составляет (по данным ВЭЖХ) 47-70%. В количестве 3-10% образуется продукт присоединения двух молекул эфира к фуллерену[60]. Реакция протекает по схеме R=Me, R’=H R=Pr, R’=H R=R’=Me. Диалкиловый (диизоалкиловый) эфир берут с избытком по отношению к фуллерену С60 с целью повышения выхода целевого продукта (1). Снижение количества эфира по отношению к С60 нецелесообразно, так как приводит к уменьшению выхода целевого продукта. 2,5-Диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофураны (1) образуются только с участием фуллерена[60] и диалкиловых (диизоалкиловых) эфиров. Проведение указанной реакции в присутствии катализатора титанацендихлорида Cp2TiCl2 больше 25 мол. % по отношению к С60 не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора титанацендихлорида Cp2TiCl2 менее 15 мол. % по отношению к С60 снижает выход продукта (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Изменение соотношения исходных реагентов в сторону значительного увеличения содержания эфира по отношению к фуллерену[60] приводит к присоединению дополнительных молекул исходного эфира к молекуле С60. Существенные отличия предлагаемого способа 1. Предлагаемый способ базируется на использовании в качестве исходных реагентов диалкиловых (диизоалкиловых) эфиров и катализатора Cp2TiCl2. В известном способе используется тетрацианооксиран. Предлагаемый способ, в отличие от известного, позволяет селективно получать 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофураны (1), синтез которых в литературе не описан. Способ поясняется следующими примерами ПРИМЕР 1. В металлический автоклав объемом 17 мл в атмосфере аргона помещают 0.01 ммоля фуллерена С60, 10 мл «сухого» толуола, 10 ммоль диэтилового эфира и 0.002 ммоль катализатора Cp2TiCl2, перемешивают 6 ч при температуре 150°С, получают 2,5-диметил-3,4-фуллеро[60]тетрагидрофуран общей формулы (1) с выходом 64% (по данным ВЭЖХ). В количестве 5% образуется продукт присоединения двух молекул эфира к фуллерену[60]. Спектр ЯМР13С 2,5-диметил-3,4-фуллеро[60]тетрагидрофурана (1) (
67.53 (С2,5), 75.23 (С3,4), 17.70 (С6,7). Сигналы углеродных атомов фуллеренового фрагмента располагаются в области 128-152 м.д. Другие примеры, подтверждающие способ, приведены в табл.1.
В качестве растворителя использовали толуол, т.к. в нем высокая растворимость фуллерена С60.
Формула изобретения
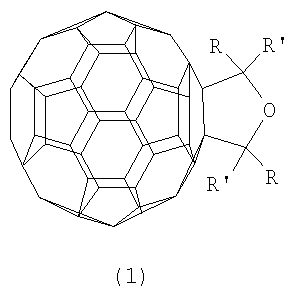
Способ получения 2,5-диалкил(2,2,5,5-тетраалкил)-3,4-фуллеро[60]тетрагидрофуранов общей формулы (1)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -кетоэфиров и
-кетоэфиров и 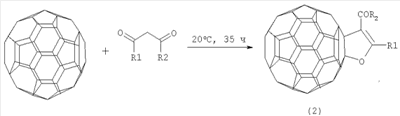
 , м.д.):
, м.д.):