|
|
(21), (22) Заявка: 2008105376/15, 12.02.2008
(24) Дата начала отсчета срока действия патента:
12.02.2008
(46) Опубликовано: 27.10.2009
(56) Список документов, цитированных в отчете о
поиске:
RU 2316477 C1, 10.02.2008. RU 2276657 C2, 20.05.2006. RU 95105013 A1, 27.12.1996. US 4551326 A, 05.11.1985. US 4385045 A, 24.05.1983. US 4405573 A, 20.09.1983.
Адрес для переписки:
392680, г.Тамбов, Моршанское ш., 19, ОАО “Корпорация “Росхимзащита”
|
(72) Автор(ы):
Ферапонтов Юрий Анатольевич (RU),
Ульянова Марина Александровна (RU),
Андреев Владислав Петрович (RU),
Рылов Юрий Борисович (RU)
(73) Патентообладатель(и):
Открытое акционерное общество “Корпорация “Росхимзащита” (ОАО “Корпорация “Росхимзащита”) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ФЕРРАТА (VI) КАЛИЯ
(57) Реферат:
Изобретение относится к получению феррата (VI) калия, который может быть использован как окислитель при обеззараживании сточных вод. Способ получения феррата (VI) калия включает взаимодействие надпероксида калия, оксида железа (III) и горючего, в качестве которого используют смесь элементарного железа и аморфного углерода. Для приготовления исходной шихты сначала смешивают оксид железа (III), элементарное железо и аморфный углерод, затем к полученной смеси добавляют надпероксид калия при следующих мольных соотношениях оксида железа (III) к указанным компонентам, моль/моль: Fe2O3/KO2=0,204-0,217, Fe2O3/C=0,45-0,80; Fe2O3/Fe=3,57-10,81. Взаимодействие исходных компонентов инициируют локальным разогревом шихты. Изобретение позволяет снизить расход надпероксида калия на единицу конечной продукции, повысить содержание основного вещества до 88 мас.% в продукте реакции. 1 ил., 1 табл.
Изобретение относится к способам получения феррата калия (K2FeO4). Феррат (VI) калия является одним из наиболее мощных известных окислителей (в кислой среде окислительный потенциал иона FeO4 2- 2- (2,2 В) выше окислительных потенциалов озона (2,07 В) и пероксида водорода (1,77 В)) и способен разлагать многие токсичные химические вещества до малотоксичных продуктов (окисляющее действие), а также вызывать гибель микроорганизмов (дезинфицирующее действие), что может быть использовано при обеззараживании и стерилизации сточных вод как отдельных промышленных объектов, так и больших мегаполисов. Следует особо отметить, что при разложении феррата (VI) калия в водной среде по реакции (1) (2,2 В) выше окислительных потенциалов озона (2,07 В) и пероксида водорода (1,77 В)) и способен разлагать многие токсичные химические вещества до малотоксичных продуктов (окисляющее действие), а также вызывать гибель микроорганизмов (дезинфицирующее действие), что может быть использовано при обеззараживании и стерилизации сточных вод как отдельных промышленных объектов, так и больших мегаполисов. Следует особо отметить, что при разложении феррата (VI) калия в водной среде по реакции (1)

наряду с атомарным кислородом образуется коллоидная система на основе гидроксида железа (III). Обладая хорошо развитой поверхностью, гидроксид железа (III) активно адсорбирует ионы тяжелых металлов, частицы суспензий и органические остатки, что может быть дополнительно использовано для очистки сточных вод промышленных предприятий.
Известен способ получения феррата калия [Заявка РФ  2006109693, C01G 49/00, опубликована 10.10.2007 г.], включающий взаимодействие надпероксида калия (KO2) и оксида железа (Fe2O3) в присутствии горючего. В качестве горючего используется углерод. Взаимодействие исходных компонентов инициируют локальным разогревом шихты до температуры порядка 500°С. Процесс протекает в режиме самораспространяющегося высокотемпературного синтеза (вид твердофазных химических процессов, когда энергия, необходимая для протекания основной эндотермической реакции, генерируется в процессе синтеза за счет протекания вспомогательной экзотермической реакции, называют реакциями самораспространяющегося высокотемпературного синтеза). 2006109693, C01G 49/00, опубликована 10.10.2007 г.], включающий взаимодействие надпероксида калия (KO2) и оксида железа (Fe2O3) в присутствии горючего. В качестве горючего используется углерод. Взаимодействие исходных компонентов инициируют локальным разогревом шихты до температуры порядка 500°С. Процесс протекает в режиме самораспространяющегося высокотемпературного синтеза (вид твердофазных химических процессов, когда энергия, необходимая для протекания основной эндотермической реакции, генерируется в процессе синтеза за счет протекания вспомогательной экзотермической реакции, называют реакциями самораспространяющегося высокотемпературного синтеза).
Данный способ имеет два существенных недостатка, жестко взаимосвязанных между собой: высокий расход исходного сырья (надпероксида калия) на получение единицы конечного продукта и низкое содержание основного вещества (не более 57% массовых) в продукте синтеза. Указанные недостатки обусловлены тем, что получение феррата калия из системы KO2-Fе2O3-C в режиме самораспространяющегося высокотемпературного синтеза возможно только при большом избытке надпероксида калия и горючего (что следует из приведенных примеров). Можно сделать предположение, что в данном случае лимитирующей стадией процесса синтеза феррата (VI) калия является реакция (2) между оксидом железа и надпероксидом калия:

которая протекает за счет энергии быстрой экзотермической реакции – горения углерода (3).

При этом для генерирования медленной эндотермической реакции (2) горючее (углерод) необходимо брать в значительно больших количествах по сравнению с величинами, рассчитанными на основании термохимических параметров процессов, протекающих в системе КО2-Fе2O3-С, т.е. значительная часть тепловой энергии, образующейся при сгорании углерода, рассеивается в окружающую среду. Причем кислород для горения углерода генерируется как за счет реакции (2), так и за счет термической диссоциации надпероксида калия. Из-за этого в продукте синтеза остается до 58% от первоначально взятого количества ионов калия, не связанных с ионом FeO4 2-. По этой причине данным способом принципиально невозможно получать феррат (VI) калия с высоким содержанием основного вещества. 2-. По этой причине данным способом принципиально невозможно получать феррат (VI) калия с высоким содержанием основного вещества.
Задачей изобретения является повышение экономичности процесса.
Технический результат заключается в снижении расхода исходного сырья (надпероксида калия) на единицу конечной продукции и повышение содержания основного вещества (феррата калия) в продукте синтеза.
Технический результат достигается тем, что в способе получения феррата (VI) калия путем взаимодействия надпероксида калия (KO2) и оксида железа (Fe2O3) в присутствии горючего в качестве горючего используют смесь углерода и элементарного железа при следующем мольном соотношении компонентов (моль оксида железа (III)/моль вещества):
| надпероксид калия (Fе2O3/КО2) |
0,204-0,217 |
| углерод (Fе2O3/С) |
0,45-0,80 |
| железо (Fе2O3/Fe) |
3,57-10,81 |
Способ осуществляют следующим образом. Вначале готовят шихту, для чего смешивают исходные компоненты – надпероксид калия, оксид железа (III) и горючее в указанных выше мольных соотношениях. В качестве горючего используют смесь элементарного железа и аморфный углерод. Оксид железа и горючее перед синтезом сушат до остаточной влажности не более 0.5% массовых. С целью избежания создания взрывоопасных мольных соотношений горючее (железо+углерод)-надпероксид калия смешение исходных компонентов осуществляют в две стадии. На первой стадии смешивают оксид железа и горючее. На второй стадии к полученной смеси добавляют надпероксид калия. Полученную таким образом шихту помещают в реактор. Исходная шихта может также прессоваться в таблетки, блоки любым известным способом (на гидравлическом прессе, на роторном таблеточном прессе, методом изостатического прессования и т.д.). В случае прессования исходной шихты в виде блоков они дробятся на любой дробилке, в результате чего получают продукт, имеющий полидисперсный состав. Гранулированный продукт помещают в реактор с помощью виброуплотнения.
Взаимодействие исходных компонентов инициируют локальным разогревом шихты до температуры порядка 500°С, что может быть осуществлено либо посредством контакта шихты с разогретой спиралью, ТЭНом и др., либо воздействием на шихту любого пиротехнического состава термитного типа (пусковая таблетка).
После инициирования в начальный момент протекает эндотермическая реакция между оксидом железа (III) и надпероксидом калия, в результате которой образуется феррат калия и кислород (2):

Выделившийся кислород вступает во взаимодействие с горючим по уравнениям реакций 3-4:


При этом выделяющаяся энергия (тепловая) обеспечивает дальнейшее протекание основной эндотермической реакции. Углерод при этом сгорает полностью без образования твердого остатка. Наличие в реакционной смеси элементарного железа способствует, во-первых, снижению скорости взаимодействия горючего (смеси железа и углерода) с кислородом и, во-вторых, увеличивает теплопроводность исходной шихты для синтеза феррата (VI) калия заявляемым способом. Суммарный эффект от двух перечисленных выше факторов обеспечивает оптимальное использование тепловой энергии окисления горючего для генерирования основной эндотермической реакции (2). За счет этого получение феррата (VI) калия из оксида железа (Fе2O3) и надпероксида калия (КО2) методом самораспространяющегося высокотемпературного синтеза возможно при использовании меньшего количества горючего и окислителя. Следует также отметить, что при горении элементарного железа в избытке кислорода образуется оксид железа (Fe2O3), который далее при взаимодействии с надпероксидом калия по уравнению реакции (2) образует феррат (VI) калия.
Перечисленные выше аспекты получения феррата (VI) калия заявляемым способом позволяют не только получать конечный продукт с высоким содержанием основного вещества, но и сократить расход исходных компонентов (надпероксида калия) на единицу конечной продукции.
Пример 1.
Смешивают 3200 г оксида железа (III), 198,6 г элементарного железа (Fе2O3/Fe=5,63) и 298,4 г углерода (Fе2O3/С=0,80). К полученной смеси добавляют 6532 г надпероксида калия (Fе2O3/КО2=0,217). Смешение производится обычным способом до получения однородного состава исходной шихты. Полученную шихту прессуют в таблетки диаметром примерно 9 мм. После этого таблетки на виброустановке загружают в реактор. Сверху слоя таблеток помещают пусковую таблетку. После этого осуществляют инициирование пусковой таблетки (например, нагревом электрической спиралью). Далее начинается непосредственно процесс высокотемпературного самораспространяющегося синтеза. Конечный продукт содержит 85% феррата калия.
Пример 2.
Смешивают 3200 г оксида железа (III), 313,94 г элементарного железа
(Fе2O3/Fe=3,57) и 418,58 г углерода (Fе2O3/С=0,57). К полученной смеси добавляют 6958 г надпероксида калия (Fе2O3/КО2=0,204). Смешение производится обычным способом до получения однородного состава исходной шихты. Полученную шихту помещают в реактор и подпрессовывают под давлением примерно 1 кг/см2. Инициирование высокотемпературного самораспространяющегося синтеза осуществляют локальным нагревом шихты электрической спиралью. Конечный продукт содержит 86% феррата калия.
Пример 3.
Смешиваются 3200 г оксида железа (III), 103,53 г элементарного железа (Fе2O3/Fе=10,81) и 517,66 г углерода (Fе2O3/С=0,46). К полученной смеси добавляют 6532 г надпероксида калия (Fе2O3/КО2=0,217). Далее как в примере 2. Конечный продукт содержит 88% феррата калия.
Пример 4.
Смешиваются 3200 г оксида железа (III), 215,40 г элементарного железа (Fе2O3/Fе=5,20) и 538,51 г углерода (Fе2O3/С=0,45). К полученной смеси добавляют 6816 г надпероксида калия (Fе2O3/КО2=0,208). Далее как в примере 2. Конечный продукт содержит 84% феррата калия.
В Таблице представлены данные о содержании K2FeO4 в продукте синтеза и нормах расхода исходного сырья (надпероксида калия) при получении феррата калия по заявляемому изобретению и аналогичные показатели при получении K2FeO4 по примеру 1 заявки РФ  2006109693. 2006109693.
| Таблица |
| Условия синтеза К2FеO4 |
Содержание K2FeO4 в продукте синтеза, % массовых |
Расход надпероксида калия при получении чистого K2FeO4, кг/кг |
| По примеру 1 |
85 |
0,97 |
| По примеру 2 |
86 |
1,02 |
| По примеру 3 |
88 |
0,94 |
| По примеру 4 |
84 |
1,03 |
По примеру 1 заявки РФ  2006109693 2006109693 |
51 |
2,24 |
Полученный заявляемым способом продукт был исследован методом качественного рентгено-фазового анализа. На чертеже представлена дифрактограмма образца феррата калия, полученного по примеру 3 (дифрактограммы образцов феррата калия, полученного по примерам 1-4 тождественны по своему характеру дифрактограмме образца феррата калия, полученного по примеру 3). Отсутствие на дифрактограмме дифракционного максимума при угле скольжения 2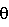 , равном 2,69°, свидетельствует о полном переходе в описанных в примере условиях железа из степени окисления Fe3+ в Fe6+. , равном 2,69°, свидетельствует о полном переходе в описанных в примере условиях железа из степени окисления Fe3+ в Fe6+.
Как видно из приведенных в Таблице данных, предложенный способ получения феррата калия обеспечивает более высокое содержание основного вещества в продукте реакции при более низких нормах расхода исходного сырья (надпероксида калия) на единицу конечной продукции нежели способ, описанный в заявке РФ  2006109693. 2006109693.
Формула изобретения
Способ получения феррата (VI) калия путем взаимодействия надпероксида калия, оксида железа (III) и горючего, отличающийся тем, что в качестве горючего используют смесь элементарного железа и аморфного углерода, причем для приготовления исходной шихты сначала смешивают оксид железа (III), элементарное железо и аморфный углерод, затем к полученной смеси добавляют надпероксид калия при следующих мольных соотношениях оксида железа (III) к указанным компонентам, моль/моль:
| Fe2O3/KO2 |
0,204-0,217 |
| Fe2O3/C |
0,45-0,80 |
| Fe2O3/Fe |
3,57-10,81 |
РИСУНКИ
|
|