|
|
(21), (22) Заявка: 2006127554/15, 22.12.2004
(24) Дата начала отсчета срока действия патента:
22.12.2004
(30) Конвенционный приоритет:
31.12.2003 US 60/533,858
(43) Дата публикации заявки: 10.02.2008
(46) Опубликовано: 20.10.2009
(56) Список документов, цитированных в отчете о
поиске:
WO 01/81405 A, 01.11.2001. EGRIE J.C. BROWNE J.K. Development and characterization of novel erythropoiesis stimulating protein (NESP). British J. of Cancer, 2001, v.84, pp 3-10. CHAMOW S.M., ASHKENAZI A. Immunoadhesins: principles and applications. Trends Biotechnol. 1996 Feb; 14(2), pp.52-60.
(85) Дата перевода заявки PCT на национальную фазу:
31.07.2006
(86) Заявка PCT:
EP 2004/014608 20041222
(87) Публикация PCT:
WO 2005/063808 20050714
Адрес для переписки:
101000, Москва, М.Златоустинский пер., 10, кв.15, “ЕВРОМАРКПАТ”, пат.пов. Н.В.Кузенковой
|
(72) Автор(ы):
ДЖИЛИС Стивен Д. (US),
ЛОДЕР Скотт (US),
КРЕСС Дороте (DE),
МАЛЕР Ханс-Кристиан (DE),
МЮЛЛЕР Роберт (DE)
(73) Патентообладатель(и):
МЕРК ПАТЕНТ ГМБХ (DE)
|
(54) Fc-ЭРИТРОПОЭТИН СЛИТЫЙ БЕЛОК С УЛУЧШЕННОЙ ФАРМАКОКИНЕТИКОЙ
(57) Реферат:
Изобретение относится к области медицины и касается Fc-эритропоэтин слитого белка с улучшенной фармакокинетикой. Сущность изобретения включает новые сиалилированные Fc-EPO слитые белки, предпочтительно включающие пару модификаций в Fc-части, а также в ЕРО части, которые имеют улучшенную фармакокинетику. В частности, Fc-EPO белки обладают длительным периодом полураспада в сыворотке крови и повышенной эффективностью in vivo. Fc-EPO слитые белки, синтезированные в клетках ВНК, обладают значительно более продолжительными периодами полураспада в сыворотке крови и повышенной эффективностью in vivo по сравнению с соответствующими Fc-EPO слитыми белками, полученными в других линиях клеток, таких как, например, клетки NS/0. Преимущество изобретения заключается в улучшении фармакокинетических свойств эритропоэтина. 8 н. и 15 з.п. ф-лы, 6 табл., 11 ил.
Текст описания приведен в факсимильном виде.                                                                         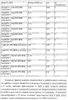     
Формула изобретения
1. Очищенный высоко сиалилированный димерный слитый белок, который существенно состоит из димерной Fc части, содержащей CH2 и CH3 домен IgG2 человека, шарнирный участок IgG человека, и человеческого эритропоэтина (ЕРО), где каждая цепь димерной Fc части является связанной посредством своего С-терминального конца непосредственно или с помощью линкерного пептида с N-терминальным концом молекулы ЕРО, при этом слитый белок обладает следующими свойствами:
(i) молекула ЕРО включает 15-28 остатков сиаловой кислоты;
(ii) участок Gln-Phe-Asn-Ser последовательности заменен Gln-Ala-Gln-Ser в пределах СН2 домена указанного IgG2, и
(iii) аминокислотная последовательность участка Leu-Ser-Leu-Ser вблизи С-терминального конца СН3 домена указанного IgG2 заменена Ala-Thr-Ala-Thr.
2. Димерный Fc-EPO слитый белок по п.1, в котором дополнительно C-терминальный остаток Lys СН3 домена заменен Ala.
3. Димерный Fc-EPO слитый белок по п.1, в котором шарнирный участок имеет происхождение от IgG1 человека.
4. Димерный Fc-EPO слитый белок по п.3, в котором указанный шарнирный участок IgG1 является модифицированным путем замены аминокислотного остатка Cys в пределах последовательности Pro-Lys-Ser-Cys-Asp-Lys шарнирного участка остатком Ser, образуя, таким образом, последовательность Pro-Lys-Ser-Ser-Asp-Lys в пределах шарнирного участка.
5. Димерный Fc-EPO слитый белок по п.1, в котором эритропоэтиновая часть включает, по крайней мере, одну из следующих аминокислотных замен:
(i) остаток, отличный от цистеина, в положении 29 молекулы ЕРО,
(ii) остаток, отличный от цистеина, в положении 33 молекулы ЕРО,
(iii) остаток цистеина в положении 88 молекулы ЕРО и
(iv) остаток цистеина в положении 139 молекулы ЕРО.
6. Димерный Fc-ЕРО слитый белок по п.5, в котором аминокислотный остаток, отличный от Cys, находится в положении 33 молекулы ЕРО вместо исходного остатка Cys, а остаток Cys находится в положении 88 молекулы ЕРО вместо исходного остатка Trp, что позволяет, таким образом, ЕРО части в пределах слитого белка образовывать Cys29-Cys88 дисульфидную связь.
7. Димерный Fc-EPO слитый белок по п.6, в котором аминокислотный остаток, отличный от Cys, находящийся в положении 33, представляет собой Pro.
8. Димерный Fc-EPO слитый белок по п.1, в котором ЕРО часть включает одну или более мутаций, выбранных из группы:
(i) Arg131 Glu131 Glu131
(ii) Arg139 Glu139 Glu139
(iii) His32 Gly32 Gly32
(iv) Ser34 Arg34 Arg34
(v) Pro90 Ala90. Ala90.
9. Димерный Fc-EPO слитый белок по п.1, в котором линкерный пептид включает сайт гликозилирования.
10. Димерный Fc-EPO слитый белок по п.9, в котором сайт гликозилирования включает аминокислотную последовательность Asn-Ala-Thr.
11. Димерный Fc-EPO слитый белок по п.1, в котором полная молекула IgG, включая шарнирный участок, имеет происхождение от IgG2.
12. Димерный Fc-EPO слитый белок по п.1, который дополнительно включает СН1 домен.
13. Димерный Fc-EPO слитый белок по п.1, в котором слитый белок содержит 20-22 остатка сиаловой кислоты.
14. Димерный Fc-ЕРО слитый белок по п.1, включающий последовательность:
EPKSSDKTHTCPPCPAPPVAGPSVFLPPPKPKDTLMISRTPEVTCVWDVSHEDPE
VQFNWYVDGVEVHNAKTKPREEQAQSTPRWSVLTWHQDWLNGKEYKCKVSN
KGLPAPIEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVE
WESNGQPE3STNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEA
LHNHYTQKSATATPGAAPPRLICDSRVLERYLLEAKEAENITTGCAEHCSLNENI
TVPDTKVNFYAWKRMEVGQQAVEVWQGLALLSEAVLRGQALLVNSSQPWEPL
QLHVDKAVSGLRSLTTLLRALGAQKEAISPPDAASAAPLRTITADTFRKLFRVYS
NFLRGKLKLYTGEACRTGDR (SEQ ID NO: 14).
15. Димерный Fc-ЕРО слитый белок по п.1, включающий последовательность:
EPKSSDKTHTCPPCPAPPVAGPSVFLPPPKPKDTLMISRTPEVTCVWDVSHEDPE
VQFNWYVDGVEVHNAKTKPREEQAQSTFRWSVLTWHQDWLNGKEYKCKVSN
KGLPAPIEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVE
WESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALH
NHYTQKSATATPGAAPPRLICDSRVLERYLLEAKEAENITTGCAEGPSLNENITV
PDTKVNFYAWKRMEVGQQAVEVWQGLALLSEAVLRGQALLWSSQPCEALQL
HVDKAVSGLRSLTTLLRALGAQKEAISPPDAASAAPLRTITADTFRKLFRVYSNF
LRGKLKLYTGEACRTGDR (SEQ ID NO: 15).
16. Молекула ДНК, кодирующая слитый белок по п.1.
17. Фармацевтическая композиция, приемлемая для лечения расстройств гематопоэза или гематопоэтической недостаточности у млекопитающего, включающая эффективное количество Fc-EPO слитого белка, охарактеризованного в п.1, необязательно вместе с фармацевтически приемлемым носителем, разбавителем или наполнителем.
18. Популяция очищенных высоко сиалилированных Fc-EPO слитых белков по п.1, приемлемых для введения млекопитающему, которую получают путем введения молекулы ДНК, кодирующей соответствующий Fc-EPO слитый белок, в клетку ВНК, экспрессии, изоляции и очистки популяции соответствующих Fc-EPO слитых белков, где указанная популяция имеет более длительный период полураспада в сыворотке крови по сравнению с популяцией соответствующих Fc-EPO слитых белков, синтезированных в клетках NS/0, PerC6 или 293.
19. Популяция очищенных Fc-EPO слитых белков по п.18, где указанная популяция слитых белков содержит в среднем 20-22 остатков сиаловой кислоты на очищенный Fc-EPO слитый белок.
20. Популяция очищенных Fc-EPO слитых белков по п.18 или 19, где ВНК клетка является адаптированной для роста в среде, не содержащей белка, или в суспензии.
21. Способ получения популяции высоко сиалилированных очищенных рекомбинантных Fc-EPO слитых белков по п.1, причем указанный способ включает следующие этапы:
(i) конструирование молекулы ДНК, кодирующей соответствующий Fc-EPO слитый белок;
(ii) трансформацию ВНК клетки с помощью указанной молекулы ДНК в среде, не содержащей белка, или в суспензии;
(iii) экспрессию популяции Fc-слитых белков, кодируемых указанной молекулой ДНК,
(iv) сбор, изоляцию и очистку указанной популяции Fc-EPO слитых белков.
22. Способ по п.21, в котором указанная синтезированная популяция слитых белков содержит в среднем 15-28 остатков сиаловой кислоты на очищенный Fc-EPO слитый белок.
23. Способ по п.21, в котором указанная синтезированная популяция слитых белков содержит в среднем 20-22 остатков сиаловой кислоты на очищенный Fc-EPO слитый белок.
РИСУНКИ
|
|