Патент на изобретение №2369618
|
||||||||||||||||||||||||||
(54) КОМПЛЕКСНАЯ СОЛЬ ОЛИГОХИТОЗОНИЯ И СПОСОБ ПОЛУЧЕНИЯ ЭТОЙ СОЛИ
(57) Реферат:
Комплексная соль олигомеров хитозана имеет средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: от 20 до 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; от 64 до 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; от 8 до 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков. Способ получения указанной комплексной соли включает образование раствора хитозана в водном растворе по меньшей мере одной органической кислоты, взятой в количестве от 23 до 115% от стехиометрии, введение в полученный раствор хитозана ферментов и осуществление ферментативного гидролиза раствора хитозана до достижения динамической вязкости реакционной смеси, равной от 1,60 до 1,80 сП·с образованием в растворе целевого продукта, который затем концентрируют и высушивают. 2 н. и 5 з.п. ф-лы.
Изобретение относится к технологии переработки природного хитозана, а точнее изобретение касается комплексной соли олигомеров хитозана и способа получения этой соли. Изобретение найдет применение при производстве продуктов функционального питания, биологически активных добавок к пище, фармацевтических препаратов для медицины и ветеринарии, косметических средств. Хитозан и олигомеры (олигосахариды) хитозана, обладающие мощным транспортным эффектом, способностью направленной доставки в организм человека самых различных полезных и жизненно необходимых веществ – витаминов, аминокислот, макро- и микроэлементов, представляют наибольший интерес для исследований их биологической активности и в настоящее время используются как основа для получения новых продуктов функционального питания, биологически активных добавок к пище, эффективных медицинских и ветеринарных препаратов, косметических средств и т.п. Наибольшей биологической активностью, в том числе выраженными бактерицидными и фунгицидными свойствами, анти-ВИЧ активностью, обладают самые низкомолекулярные олигомергомологи хитозана, содержащие от 2 до 8-12 повторяющихся звеньев – остатков D-глюкозамина, связанных гликозидными связями. Уникальные свойства продуктов питания, напитков, БАДов, медицинских и ветеринарных препаратов, косметических средств, содержащих олигомеры хитозана, сделали актуальной проблему разработки высокотехнологического способа их промышленного получения. Такой способ был разработан специалистами ЗАО «Био Технологии» (патент РФ Однако во многих случаях целесообразно производить и использовать не чистые олигомеры хитозана, а комплексные соединения, образуемые молекулами олигомергомологов с различными кислотами, прежде всего органическими, и другими веществами, содержащими ацильные группы. Такие соединения, например лактат олигохитозония, образуются за счет возникновения донорно-акцепторной связи между атомами азота аминогрупп пиранозных звеньев олигосахаридных цепей и катионами водорода, образованными при диссоциации молекул кислоты в растворах с последующим ионным взаимодействием протонированных аминогрупп и кислотных остатков. После сушки таких растворов получается кристаллическая соль, в молекулах которой комплексный катион олигохитозония связан с анионом кислотного остатка ионной связью. Целесообразность использования комплексных солей олигомеров хитозана при производстве продуктов питания, БАДов, фармацевтических, косметических средств связана с тем, что при квалифицированном выборе природы кислоты и доли связанных аминогрупп в повторяющихся звеньях олигомергомологов хитозана получается продукт, обладающий более высоким профилактическим и терапевтическим эффектом (за счет синергического эффекта олигомеров хитозана и органических кислот), улучшенными органолептическими показателями, лучшей растворимостью в воде и меньшей себестоимостью по сравнению с чистыми олигомерами хитозана. Наиболее близким по своей технической сущности является способ получения ионосвязанных производных олигосахарида хитозана ферментативной деполимеризацией хитозана в присутствии папаина и уксусной кислоты с последующей распылительной сушкой продукта (RU 2232775 С1, 20.07.2004). Полученный продукт затем подвергают попеременно двукратному растворению в воде и распылительной сушке, после чего полученный продукт растворяют в воде совместно с веществами, имеющими кислотные группы, выбранными из никотиновой кислоты, молочной кислоты, гидрохлорида глицина, L-карнитина гидрохлорида, глутаминовой кислоты, гамма-амино-бета-фенилмасляной кислоты гидрохлорида, аденозинфосфата, кокарбоксилазы, аспартама, гемфиброзила, гидрохлорида аминокапроновой кислоты, нимфлумовой кислоты, янтарной кислоты, аскорбиновой кислоты, витамина ВЗ, метионина или ацексамовой кислоты с последующим высушиванием полученного продукта. Указанный способ обеспечивает получение олигосахаридов хитозана, представляющих собой фракцию с числом “n” повторяющихся звеньев – остатков D-глюкозамина от 2 до 20, что свидетельствует о невысокой биологической активности продукта, так как наибольшей биологической активностью обладают олигомеры хитозана с n от 2 до 8-12. При этом названный способ имеет крайне низкую производительность, связанную с тем, что при распылительной сушке разбавленных водных растворов, содержащих 5-10% олигосахаридов хитозана и их производных, образуются порошки со значительной долей (величина которой обратно пропорциональна вязкости и концентрации раствора) мелких частиц размером до 5 мкм, что приводит к потерям сухих промежуточных и конечного продуктов в количестве от 35% (при работе с 10%-ным раствором олигосахаридов хитозана) до 40% (при работе с 5%-ным раствором олигосахаридов хитозана) на каждом из этапов распылительной сушки. Более того, при реализации названного способа необходимы высокие энергозатраты (при распылительной сушке растворов олигосахаридов хитозана и их производных, содержащих 90-95% влаги), что повышают себестоимость целевого продукта. Помимо сказанного, для указанного способа получения ионосвязанных производных олигосахарида хитозана характерна многоэтапность (нетехнологичность) процесса. Например, трехкратное проведение распылительной сушки 5-10%-ных растворов промежуточных продуктов и сушка 5-10%-ного раствора конечного продукта приводит к колоссальным потерям сухих продуктов (см. выше), огромным энергозатратам. Так, при работе с 5%-ными растворами (см. примеры 1, 2, 9, 13) суммарные потери при сушке промежуточных и конечного продуктов составляют около 87%, при работе с 10%-ными растворами суммарные потери составляют около 82%. Высокое содержание мелких частиц в конечном продукте снижает его качество, так как значительно затрудняет его дальнейшую переработку, в частности прессование, капсулирование, таблетирование, приготовление смесей с другими порошкообразными компонентами; при растворении в воде таких пылевидных порошков наблюдается комкование, связанное с агрегацией частиц с высокоразвитой поверхностью. Пылевидные частицы, содержащиеся в промежуточных и конечном продукте, при сушке не улавливаются рукавным фильтром и скруббером и попадают в атмосферу, создавая экологические проблемы. Таким образом, получаемый данным способом конечный продукт термически нестабилен и обладает недостаточными органолептическими показателями из-за наличия в нем ацетата олигохитозония (получаемый продукт представляет собой смесь олигомеров хитозана, комплексной соли олигомеров хитозана и органической кислоты и ацетата олигохитозония, причем содержание последнего в смеси составляет 2,4-3,8%). В основу заявляемого изобретения положена задача путем сокращения примесей и повышения содержания наиболее низкомолекулярных солей олигомеров хитозана в целевом продукте, получаемом в соответственно измененных условиях, создать такую комплексную соль олигомеров хитозана и такой способ получения этой соли, которые обеспечат более высокую биологическую активность целевого продукта с улучшенными термостабильностью и органолептическими свойствами. Технический эффект, который может быть достигнут при использовании заявляемой комплексной соли олигомеров хитозана, состоит в повышении эффективности продуктов функционального питания, биологически активных добавок к пище, медицинских и ветеринарных препаратов, косметических средств, полученных на основе таких солей. Поставленная задача достигается созданием комплексной соли олигомеров хитозана, содержащей комплексный катион олигомеров хитозана, связаный ионной связью по меньшей мере с одним анионом кислотного остатка, которая согласно изобретению имеет средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: от 20 до 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; от 64 до 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; от 8 до 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Благодаря изобретению создан продукт на основе самых низкомолекулярных олигомергомологов хитозана, содержащих от 2 до 12 повторяющихся звеньев, остатков D-глюкозамина, связанных гликозидными связями, имеющий повышенную биологическую активность, в том числе выраженные бактерицидные и фунгицидные свойства, анти-ВИЧ и антиопухолевую активность. Целесообразно указанную соль олигомеров хитозана получать способом, включающим образование раствора хитозана в водном растворе органической кислоты, введение в полученный раствор хитозана ферментов и осуществление ферментативного гидролиза раствора хитозана с образованием в растворе целевого продукта, высушивание целевого продукта, в котором согласно изобретению образование раствора хитозана осуществляют в водном растворе по меньшей мере одной органической кислоты, взятой в количестве от 23 до 115% от стехиометрии, а ферментативный гидролиз проводят до достижения динамической вязкости реакционной смеси, равной от 1,60 до 1,80 сП, и образования в растворе комплексной соли олигомеров хитозана, содержащей комплексный катион олигомеров хитозана, связанный ионной связью по меньшей мере с одним анионом кислотного остатка, имеющей средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: от 20 до 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; от 64 до 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; от 8 до 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Согласно изобретению полезно перед высушиванием осуществлять концентрирование реакционной смеси, содержащей целевой продукт, до содержания влаги 62-80 мас.%, что обеспечивает повышение качества и выхода целевого продукта. Согласно изобретению разумно в качестве органической кислоты использовать кислоту, обладающую биологической активностью, что обеспечивает дополнительное повышение биологической активности целевого продукта. Согласно изобретению полезно ферментативный гидролиз проводить при использовании в качестве фермента смеси хитозаназы и целлолюкса, взятых в массовом соотношении 1:(0,2-0,3) соответственно, что обеспечивает образование целевого продукта оптимального молекулярно-массового распределения, при этом согласно изобретению полезно ферментативный гидролиз проводить при содержании хитозаназы в количестве 1,8 единиц на 1 грамм хитозана, а целлолюкса в количестве 0,1-0,15% от массы хитозана. Согласно изобретению полезно в качестве фермента использовать фермент, иммобилизованный на инертном носителе, что обеспечивает повышение чистоты целевого продукта и возможность многократного использования фермента. Дальнейшие цели и преимущества заявляемого изобретения станут ясны из последующего подробного описания комплексной соли олигомеров хитозана и способа ее получения. Заявляемая комплексная соль олигомеров хитозана имеет следующую структурную формулу:
где R – органический радикал; n – целое число, равное от 2 до 20. Эта соль содержит комплексный катион олигомеров хитозана, связанный ионной связью по меньшей мере с одним анионом кислотного остатка, и согласно изобретению имеет средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: от 20 до 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; от 64 до 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; от 8 до 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Заявляемая комплексная соль олигомеров хитозана имеет как полностью связанные, так и частично связанные аминогруппы, что расширяет спектр ее биологически активного действия. Кроме того, благодаря преобладанию (до 92%) в составе заявляемой комплексной соли самых низкомолекулярных олигомергомологов хитозана, содержащих от 2 до 12 повторяющихся звеньев, остатков D-глюкозамина, связанных гликозидными связями, достигнуто повышение биологической активности комплексной соли, в том числе выраженных бактерицидных и фунгицидных свойств, анти-ВИЧ и антиопухолевой активности. Указанные характеристики заявляемой комплексной соли олигомеров хитозана обеспечивают повышение эффективности продуктов функционального питания, биологически активных добавок к пище, медицинских и ветеринарных препаратов, средств борьбы с заболеваниями сельскохозяйственных культур, косметических средств, полученных на основе таких солей. Соль с указанными характеристиками возможно получить следующим способом. Крабовый хитозан [поли- Ферментативный гидролиз проводят в присутствии, например, смеси хитозаназы и липаина (ферменты производства компании Lyven, Франция) в соотношении 1:(1-1,2) по массе, могут быть использованы хитозаназа или хитиназные комплексы на основе таких культур, как Streptomyces Kurssanovii, Streptomyces griseus при температуре 44-48°С. Предпочтительно использовать для гидролиза смесь хитозаназы и целлолюкса (производство «Сиббиофарм», Россия) в соотношении 1:(0,2-0,3) по массе соответственно. В процессе получения целевого продукта степень гидролиза контролируют путем отбора проб и измерений динамической вязкости раствора комплексной соли олигомеров хитозана на вискозиметре Брукфильда. Исследования показали целесообразность проведения гидролиза в условиях заявляемого способа при содержании в реакционной смеси хитозаназы в количестве 1,8 единиц на 1 грамм хитозана и целлолюкса в количестве 0,1-0,15% от массы хитозана, что обеспечивает выход комплексных солей олигомеров хитозана с указанным выше молекулярно-массовым распределением молекул олигомергомологов хитозана. Согласно изобретению ферментативный гидролиз проводят до достижения динамической вязкости реакционной смеси, равной от 1,60 до 1,80 сП. Благодаря выполнению вышеуказанных условий и соблюдения названных режимов технологии в реакционной массе получают раствор комплексной соли олигомеров хитозана и органической кислоты со следующим молекулярно-массовым распределением молекул олигомергомологов хитозана: от 20 до 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; от 64 до 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; от 8 до 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии (ГПХ) на жидкостном хроматографе Bio-Rad с рефрактометрическим детектором и системой компьютерной регистрации; колонка Tosohaas TSK 30 SW XL, в качестве растворителя и элюента используют фосфатный буфер (0,05 М, рН 3,7) с добавлением 0,5 М NaNO3. Найдено, что полученную реакционную массу, содержащую раствор комплексной соли олигомеров хитозана и органической кислоты – соли олигохитозония – перед проведением сушки целесообразно концентрировать до содержания влаги 62-80%. Кроме того, для уменьшения энергозатрат на этапе сушки вместо распылительной сушилки возможно использование сушилки с псевдокипящим слоем. Введение стадии концентрирования раствора комплексной соли олигомеров хитозана перед распылительной сушкой позволило – повысить производительность процесса за счет исключения потерь целевого продукта при снижении его себестоимости и энергозатрат (на 50-70%) на стадии распылительной сушки; – повысить чистоту биологически активного целевого продукта и получить комплексные соли олигомеров хитозана в виде порошков светло-желтого цвета оптимального гранулометрического состава, достаточно крупных (диаметр частиц 60-100 мкм) и однородных по размерам, что обеспечивает высокое качество продукта при его дальнейшем использовании в пищевой, косметической и фармацевтической промышленности, сельском хозяйстве. В результате проведенных исследований было определено оптимальное содержание влаги после концентрирования, которое составляет 62-80%. Отклонение от выбранного интервала в сторону увеличения содержания влаги приводит к существенным потерям целевого продукта и повышению энергозатрат при распылительной сушке. Отклонение в сторону уменьшения содержания влаги приводит к значительному повышению вязкости раствора и затрудняет проведение распылительной сушки. Для получения более узких по молекулярно-массовому распределению фракций комплексных солей олигомеров хитозана возможно проведение перед сушкой фракционирования раствора методом ультрафильтрации. Содержание основного вещества (комплексной соли олигомеров хитозана) в конечном продукте не менее 95%. Выход продукта в расчете на исходный хитозан 96%. Получаемые порошки комплексных солей олигомеров хитозана быстро растворимы в воде и физиологическом растворе, хорошо смешиваются с различными ингредиентами, более чистые и термостабильные, имеют улучшенные органолептические свойства (в частности, за счет отсутствия примеси ацетата олигохитозония), гранулометрические параметры, оптимальные для использования в пищевой и фармацевтической промышленности (размер частиц порошка 60-100 мкм) по сравнению с продуктом по прототипу. Нижеследующие примеры ни в коей мере не ограничивают объем патентных притязаний и приведены лишь с целью иллюстрировать заявляемый способ получения комплексных солей олигохитозония. Пример 1. Растворяют 50 кг крабового хитозана со степенью деацетилирования 95% в 1 м3 5,4%-ного водного раствора аскорбиновой кислоты (что составляет 105% от стехиометрии). Проводят ферментативный гидролиз в присутствии хитозаназы активностью 250 ед/г, взятой в количестве 1,8 ед. (7,2 мг) на 1 г хитозана, и целлолюкса-F активностью 1800 ед/г (2 мг на 1 г хитозана) при температуре 44°С в течение 20 часов до достижения динамической вязкости реакционной смеси, равной 1,68 сП, затем гидролизат концентрируют до содержания влаги 77% с использованием вакуумно-выпарной установки, обеспечивающей производительность по испаренной влаге 50 кг/час, при температуре 39°С и подвергают сушке на распылительной сушильной установке при скорости подачи раствора 30 л/час, температуре входящего теплоносителя 115°С, температуре на выходе из сушильной установки 65°С. В процессе гидролиза динамическую вязкость реакционной смеси контролируют на вискозиметре Брукфильда. Получена комплексная соль олигомеров хитозана и аскорбиновой кислоты (аскорбат олигохитозония) с полным связыванием аминогрупп в молекулах олигомеров хитозана, со средневязкостной молекулярной массой 1800 Да. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 48 Ионосвязанная аскорбиновая кислота – 52 Количество ионосвязанного продукта определялось методом потенциометрического титрования. По данным гель-проникающей хроматографии на колонке с акрилексом Р-2 (размер колонки 1100×35 мм) молекулярная масса продукта составляет 2000 Да. Выход продукта в расчете на исходный хитозан равен 96,0%. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 20% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 72% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 8% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Пример 2. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но при использовании аскорбиновой кислоты в количестве 105% от стехиометрии, гидролиз хитозана ведут с добавлением хитозаназы (1,8 единиц активности или 7,2 мг на 1 г хитозана) при температуре 46°С в течение 22 часов до достижения динамической вязкости реакционной смеси, равной 1,80 сП. Гидролизат концентрируют до содержания влаги 80% и сушат. Получен аскорбат олигохитозония с полным связыванием аминогрупп молекул олигомеров хитозана, со средневязкостной молекулярной массой 2100 Да. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 48 Ионосвязанная аскорбиновая кислота – 52 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2250 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 21% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 64% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 15% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 3. Растворяют 50 кг хитозана в 1 м3 2%-ного водного раствора янтарной кислоты (что составляет 115% от стехиометрии). Проводят гидролиз в присутствии хитозаназы активностью 250 eU/g (1,8 ед. или 7,2 мг на 1 г хитозана) и папаина активностью 36000 NFPU/mg (8,64 мг на 1 г хитозана) при температуре 48°С в течение 22 часов до достижения динамической вязкости реакционной смеси, равной 1,78 сП. Гидролизат концентрируют до содержания влаги 62% и подвергают распылительной сушке. Получают сукцинат олигохитозония с полным замещением аминогрупп молекул олигомеров хитозана, со средневязкостной молекулярной массой 2000 Да. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 71 Ионосвязанная янтарная кислота – 29 Количество ионосвязанного продукта определялось методом потенциометрического титрования. Данные гель-проникающей хроматографии дают значение молекулярной массы около 2200 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 22% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 70% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 8% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 95,8%. Пример 4. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но при использовании молочной кислоты гидролиз хитозана ведут в 1 м3 2,8%-ного водного раствора молочной кислоты (105% от стехиометрии) до достижения динамической вязкости реакционной смеси, равной 1,76 сП. После гидролиза и выпаривания раствора до содержания влаги 70% гидролизат подвергают распылительной сушке. Получен лактат олигохитозония со средневязкостной молекулярной массой 1950 Да, с полным замещением аминогрупп в молекулах олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 64 Ионосвязанная молочная кислота – 36 Количество ионосвязанного продукта определялось методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2150 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 23% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 66% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 11% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 5. Растворяют 50 кг крабового хитозана со степенью деацетилирования 95% в 1 м3 0,4%-ного водного раствора уксусной кислоты (23% от стехиометрии). Проводят ферментативный гидролиз в присутствии хитозаназы активностью 250 ед/г, взятой в количестве 1,8 ед. (7,2 мг) на 1 г хитозана, и целлолюкса-F, активностью 1800 ед/г (2 мг на 1 г хитозана) при температуре 44°С в течение 20 часов до достижения динамической вязкости реакционной смеси, равной 1,65 сП. В процессе гидролиза динамическую вязкость реакционной смеси контролируют на вискозиметре Брукфильда. Гидролизат концентрируют до содержания влаги 77% с использованием вакуумно-выпарной установки УВВ-50 (производительность по испаренной влаге 50 кг/час) при температуре 39°С и подвергают сушке на сушильной установке с псевдокипящим слоем (сушильная установка «в кипящем слое инертных тел» СИН-04, производительность 50 кг/час по упаренной влаге, скорость сушильного агента 4 м/сек). Получают комплексную соль олигомеров хитозана и уксусной кислоты (ацетат олигохитозония) с частичным (21,5%-ным) связыванием аминогрупп в молекулах олигомеров хитозана, со средневязкостной молекулярной массой 1700 Да. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 92,6 Ионосвязанная уксусная кислота – 7,4 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии на колонке с акрилексом Р-2 (размер колонки 1100×35 мм) молекулярная масса продукта составляет 1870 Да. Выход продукта в расчете на исходный хитозан равен 96,0%. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 66% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 9% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Пример 6. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют 1 м3 водного раствора смеси 2,7% аскорбиновой и 2,8% ацетилсалициловой кислот (103% от стехиометрии). Получают двойную комплексную соль олигомеров хитозана с аскорбиновой и ацетилсалициловой кислотами с полным связыванием аминогрупп в молекулах олигомеров хитозана, со средневязкостной молекулярной массой 2000 Да и полным замещением аминогрупп молекул олигомеров хитозана. Вязкость раствора составила 1,76 сП. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 47,6 Ионосвязанная аскорбиновая кислота – 34,6 Ионосвязанная ацетилсалициловая кислота – 17,8 Количество ионосвязанного продукта определялось методом потенциометрического титрования. По данным гель-проникающей хроматографии на колонке с акрилексом Р-2 (размер колонки 1100×35 мм) молекулярная масса продукта составляет 2200 Да. Выход продукта в расчете на исходный хитозан равен 96,0%. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 20% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 70% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 10% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Пример 7. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют раствор смеси 0,9% уксусной кислоты и 3,4% пантотеновой кислоты в 1 м3 (100% от стехиометрии) до достижения динамической вязкости реакционной смеси, равной 1,69 сП. После гидролиза и выпаривания раствора до содержания влаги 71% гидролизат подвергают распылительной сушке. Получают комплексную смешанную соль (ацетат-пантотеноат олигохитозония) со средневязкостной молекулярной массой 1900 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 54 Ионосвязанная уксусная кислота – 9,7 Ионносвязанная пантотеновая кислота – 36,3 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2100 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 64% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 11% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 8. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но при использовании для растворения хитозана водного раствора смеси 0,6% уксусной, 1,8% аскорбиновой и 0,67% янтарной кислот в 1 м3 (100% от стехиометрии). После гидролиза (вязкость раствора была равна 1,76 сП) и выпаривания раствора до содержания влаги 72% гидролизат подвергают распылительной сушке. Получают тройную комплексную соль (ацетат-аскорбат-сукцинат олигохитозония) со средневязкостной молекулярной массой 2000 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 57,5 Ионосвязанная уксусная кислота – 7 Ионносвязанная аскорбиновая кислота – 20 Ионосвязанная янтарная кислота – 15,5 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2180 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 20% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 69% (вязкость была равна 1) олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 11% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных частей; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 9. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют водный раствор смеси 2,7% аскорбиновой и 6,8% фолиевой кислот в 1 м3 (100% от стехиометрии). Получен раствор с вязкостью 1,60 сП. После гидролиза и выпаривания раствора до содержания влаги 70% гидролизат подвергают распылительной сушке. Получают комплексную соль со средневязкостной молекулярной массой 1600 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 53 Ионосвязанная аскорбиновая кислота – 28,5 Ионносвязанная фолиевая кислота – 18,5 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 1760 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 25% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 67% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 8% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 10. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют раствор 3,8% никотиновой кислоты в 1 м3 (105% от стехиометрии). Вязкость раствора после гидролиза равна 1,80 сП. После гидролиза и выпаривания раствора до содержания влаги 71% гидролизат подвергают распылительной сушке. Получают никотинат олигохитозония со средневязкостной молекулярной массой 2100 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 57 Ионосвязанная никотиновая кислота – 43 Количество ионосвязанного продукта определялось методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2250 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 20% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 64% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 16% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 11. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют водный раствор смеси 0,9% уксусной и 2,28% глутаминовой кислот в 1 м3 (100% от стехиометрии). Вязкость раствора после гидролиза равна 1,65 сП. После гидролиза и выпаривания раствора до содержания влаги 72% гидролизат подвергают распылительной сушке. Получают комплексную двойную соль (ацетат-глутаминат олигохитозония) со средневязкостной молекулярной массой 1700 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 61 Ионосвязанная уксусная кислота – 11 Ионосвязанная глутаминовая кислота – 28 Количество ионосвязанного продукта определялось методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 1850 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 23% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 67% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 10% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Пример 12. Получение комплексной соли олигомеров хитозана ведут аналогично указанному в примере 1, но для растворения хитозана используют водный раствор смеси 1,4% молочной кислоты и 4,6% аспартама в 1 м3 (100,3% от стехиометрии). Вязкость раствора после гидролиза равна 1,80 сП. После гидролиза и выпаривания раствора до содержания влаги 71% гидролизат подвергают распылительной сушке. Получают комплексную смешанную соль (лактат-аспарагинат-фенилаланинат олигохитозония) со средневязкостной молекулярной массой 2100 Да и полным замещением аминогрупп молекул олигомеров хитозана. Полученный продукт содержит, мас.%: Олигосахарид хитозана – 45,5 Ионосвязанная молочная кислота – 13 Ионосвязанный аспартам – 41,5 Количество ионосвязанного продукта определяют методом потенциометрического титрования. По данным гель-проникающей хроматографии молекулярная масса продукта составляет 2300 Да. Молекулярно-массовое распределение молекул олигомергомологов хитозана определяют методом гель-проникающей хроматографии с получением следующего результата: 21% олигомергомологов хитозана, содержащих от 2 до 6 повторяющихся D-глюкозаминных остатков; 64% олигомергомологов хитозана, содержащих от 7 до 12 повторяющихся D-глюкозаминных остатков; 15% олигомергомологов хитозана, содержащих от 13 до 20 повторяющихся D-глюкозаминных остатков; 0% олигомергомологов хитозана, содержащих более 20 повторяющихся D-глюкозаминных остатков. Выход продукта в расчете на исходный хитозан равен 96,0%. Таким образом, предложена новая комплексная соль олигомеров хитозана, имеющая заданное оптимальное молекулярно-массовое распределение молекул олигомергомологов хитозана, соответственно повышенную биологическую активность и чистоту, в виде порошков с оптимальным размером частиц (60-100 мкм), с повышенной термостабильностью, с улучшенными органолептическими свойствами. При этом предлагаемый способ получения такой комплексной соли олигомеров хитозана позволил повысить производительность процесса за счет исключения потерь целевого продукта (по прототипу они составляют 82-87%) при значительном снижении энергозатрат (на 60-80% по сравнению с прототипом) на стадии распылительной сушки, многократного уменьшения числа стадий процесса. Указанные преимущества изобретения позволяют реализовать в промышленных условиях экономически эффективную и экологически чистую технологию.
Формула изобретения
1. Комплексная соль олигомеров хитозана, содержащая комплексный катион олигомеров хитозана, связанный ионной связью по меньшей мере с одним анионом кислотного остатка, отличающаяся тем, что она имеет средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: 2. Способ получения комплексной соли олигомеров хитозана, включающий образование раствора хитозана в водном растворе органической кислоты, введение в полученный раствор хитозана ферментов и осуществление ферментативного гидролиза раствора хитозана с образованием в растворе целевого продукта, высушивание целевого продукта, отличающийся тем, что образование раствора хитозана осуществляют в водном растворе по меньшей мере одной органической кислоты, взятой в количестве от 23 до 115% от стехиометрии, а ферментативный гидролиз проводят до достижения динамической вязкости реакционной смеси, равной от 1,60 до 1,80 сП, и образования в растворе комплексной соли олигомеров хитозана, содержащей комплексный катион олигомеров хитозана, связанный ионной связью по меньшей мере с одним анионом кислотного остатка, имеющей средневязкостную молекулярную массу от 1600 до 2100 Да и следующее молекулярно-массовое распределение молекул олигомергомологов хитозана: 3. Способ по п.2, отличающийся тем, что перед высушиванием осуществляют концентрирование реакционной смеси, содержащей целевой продукт, до содержания влаги 62-80 мас.%. 4. Способ по п.2, отличающийся тем, что в качестве органической кислоты используют кислоту, обладающую биологической активностью. 5. Способ по п.2, отличающийся тем, что ферментативный гидролиз проводят при использовании в качестве фермента смеси хитозаназы и целлолюкса, взятых в массовом соотношении 1:(0,2-0,3) соответственно. 6. Способ по п.2 или 5, отличающийся тем, что ферментативный гидролиз проводят при содержании хитозаназы в количестве 1,8 единиц на 1 г хитозана, а целлолюкса в количестве 0,10-0,15% от массы хитозана. 7. Способ по п.2, отличающийся тем, что в качестве фермента используют фермент, иммобилизованный на инертном носителе.
|
||||||||||||||||||||||||||

 2316592) и успешно реализован в промышленном масштабе.
2316592) и успешно реализован в промышленном масштабе.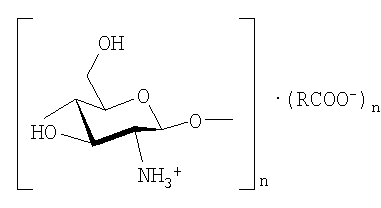
 -(1
-(1 4)-2-амино-2-деокси-D-глюкоза] со степенью деацетилирования 90-95% растворяют в водном растворе одной или более кислот, например аскорбиновой, лимонной, щавелевой, бензойной, малоновой, молочной, янтарной, ацетилсалициловой, сорбиновой, фумаровой, стеариновой, линолевой, циануровой, акриловой. Согласно изобретению образование раствора хитозана осуществляют в водном растворе по меньшей мере одной указанной кислоты, взятой в количестве от 23 до 115% от стехиометрии. Варьируя исходную концентрацию выбранной/выбранных кислот, можно менять степень замещения аминогрупп в молекулах олигомеров хитозана (степень кватернизации аминогрупп) в широких пределах. При использовании смеси двух или, например, трех и т.д. органических кислот конечный продукт представляет собой двойные (тройные и т.д.) комплексные соли олигомеров хитозана и двух (трех и т.д.) кислот.
4)-2-амино-2-деокси-D-глюкоза] со степенью деацетилирования 90-95% растворяют в водном растворе одной или более кислот, например аскорбиновой, лимонной, щавелевой, бензойной, малоновой, молочной, янтарной, ацетилсалициловой, сорбиновой, фумаровой, стеариновой, линолевой, циануровой, акриловой. Согласно изобретению образование раствора хитозана осуществляют в водном растворе по меньшей мере одной указанной кислоты, взятой в количестве от 23 до 115% от стехиометрии. Варьируя исходную концентрацию выбранной/выбранных кислот, можно менять степень замещения аминогрупп в молекулах олигомеров хитозана (степень кватернизации аминогрупп) в широких пределах. При использовании смеси двух или, например, трех и т.д. органических кислот конечный продукт представляет собой двойные (тройные и т.д.) комплексные соли олигомеров хитозана и двух (трех и т.д.) кислот.