|
|
(21), (22) Заявка: 2008126085/04, 26.06.2008
(24) Дата начала отсчета срока действия патента:
26.06.2008
(45) Опубликовано: 20.09.2009
(56) Список документов, цитированных в отчете о
поиске:
Милютин А.В. и др. Поиск биологически активных соединений в ряду  -ацетиламино- и -ацетиламино- и  -арилсульфониламиноэтиламидов ароилпировиноградных кислот. Химико-фармацевтический журнал. – 1996, т.30, -арилсульфониламиноэтиламидов ароилпировиноградных кислот. Химико-фармацевтический журнал. – 1996, т.30,  6, с.20-22. Андрейчиков Ю.С. и др. Кинетика декарбонилирования 5-арилфуран-2,3-дионов. Журнал органической химии. – 1978, т.XIV, вып.11,с.2436-2440. Гейн В.Л. и др. Синтез и противомикробная активность 5-ароил-(гетероил)метилен-2-имино-1,3-дифенил-тетрагидроимидазол-4-онов. – 2008, т.42, 6, с.20-22. Андрейчиков Ю.С. и др. Кинетика декарбонилирования 5-арилфуран-2,3-дионов. Журнал органической химии. – 1978, т.XIV, вып.11,с.2436-2440. Гейн В.Л. и др. Синтез и противомикробная активность 5-ароил-(гетероил)метилен-2-имино-1,3-дифенил-тетрагидроимидазол-4-онов. – 2008, т.42,  1, с.24-25. 1, с.24-25.
Адрес для переписки:
614990, г.Пермь, ул. Букирева, 15, ПГУ, А.А. Онорину
|
(72) Автор(ы):
Некрасов Денис Денисович (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Пермский государственный университет” (RU)
|
(54) 4-N-(4-АРИЛ-2,4-ДИОКСОБУТИРИЛ)АМИНОБЕНЗОЛСУЛЬФАМИДЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНУЮ, АНАЛЬГЕТИЧЕСКУЮ И АНТИМИКРОБНУЮ АКТИВНОСТИ
(57) Реферат:
4-N-(4-Арил-2,4-диоксобутирил)аминобензолсульфамиды общей формулы:
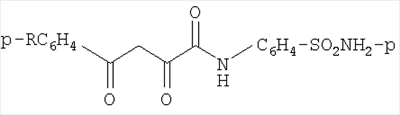
где R=Н, С2Н5O, Cl, проявляющие противовоспалительную, анальгетическую и антимикробную активности. 3 табл.
Изобретение относится к органической химии, а именно к ранее неизвестным сульфамидам 4-арил-2,4-диоксобутановых ароилпировиноградных кислот, проявляющих биологическую активность.
Из доступных заявителю источников известен способ получения близких по строению  -арилсульфониламиноэтиламидов ароилпировиноградных кислот, проявляющих слабую противовоспалительную и анальгетическую активность (А.В.Милютин, P.P.Махмудов, Ю.С.Андрейчиков, А.Ф.Голенева, Г.А.Тульбович, Т.И.Ковина. Химико-фармацевтический журнал. 1996. Т.30. -арилсульфониламиноэтиламидов ароилпировиноградных кислот, проявляющих слабую противовоспалительную и анальгетическую активность (А.В.Милютин, P.P.Махмудов, Ю.С.Андрейчиков, А.Ф.Голенева, Г.А.Тульбович, Т.И.Ковина. Химико-фармацевтический журнал. 1996. Т.30.  6. С.20-22). 6. С.20-22).

где R=H, Me, MeO, 2,4-Me, F, Br, Cl; Ar=Ph, C6H4Me-p.
Недостатком указанных соединений является слабый противовоспалительный и анальгетический эффект и отсутствие антимикробной активности.
Задачей настоящего изобретения является синтез 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамидов, свободных от указанного недостатка, и расширение арсенала средств воздействия на живой организм. Указанная задача решается 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамидами общей формулы:
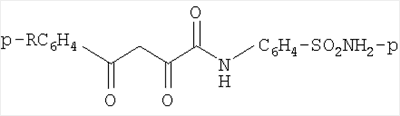
где R=H, С2Н5O, Cl,
проявляющими противовоспалительную, анальгетическую и антимикробную активность.
Синтез вышеуказанных соединений осуществляют взаимодействием 5-арил-2,3-дигидрофуран-2,3-дионов с п-аминобензолсульфамидом в диоксане при комнатной температуре в течение 30-60 минут с последующим выделением целевого продукта известными приемами.

где R=H, С2Н5O, Cl.
Реакция фурандиона с п-аминобензолсульфамидом протекает при комнатной температуре в растворе диоксана. Независимо от соотношения реагентов (1:1 или 2:1) образуются 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамиды. При избытке фурандиона в реакционной смеси присутствует вышеуказанный амид и непрореагировавший фурандион (по данным хроматограммы). Повышение температуры до 100°С на течение реакции не влияет, однако вместо избытка фурандиона на хроматограмме наблюдается известный 6-арил-3-ароил-4-гидрокси-2-пиранон (Ю.С.Андрейчиков, Ю.А.Налимова, А.П.Козлов, И.А.Русаков. Журнал органической химии. 1978. Т.14. Вып.11. С.2436-2440).
Ниже приведены примеры синтеза заявляемых соединений.
Пример 1. 4-N-(4-Фенил-2,4-диоксобутирил)аминобензолсульфамид
В раствор 0,01 моль фенилфурандиона в 20 мл безводного диоксана добавляется 0,01 моль n-аминобензолсульфамида и перемешивается на магнитной мешалке в течение одного часа. Растворитель упаривается, выделившийся осадок перекристаллизовывают из ДМФА.
Получают 2.84 г (85%) вещества. C16H14N2O5S. Т.пл. 218-220°С (ДМФА).
Вычислено, %: С=57.8; Н=4.2; N=8.4;
Найдено, %: С=57.6; Н=4.1; N=8.5.
Пример 2. 4-N-(4-п-этоксифенил-2,4-диоксобутирил)аминобензолсульфамид
В раствор 0,01 моль п-этоксифенилфурандиона в 20 мл безводного диоксана добавляется 0,01 моль n-аминобензолсульфамида и перемешивается на магнитной мешалке в течение 30 мин. Растворитель упаривается, выделившийся осадок перекристаллизовывают из ДМФА.
Получают 3.5 г (91%) вещества. C18H18N2O6S. Т.пл. 225-226°С (ДМФА).
Вычислено, %: С=57.3; Н=4.7; N=7.4;
Найдено, %: С=57.2; Н=4.5; N=7.5.
Пример 3. 4-N-(4-хлорфенил-2,4-диоксобутирил)аминобензолсульфамид
В раствор 0,01 моль п-хлорфенилфурандиона в 20 мл безводного диоксана добавляется 0,01 моль n-аминобензолсульфамида и перемешивается на магнитной мешалке 40 минут. Растворитель упаривается, выделившийся осадок перекристаллизовывают из ДМФА.
Получают 3.57 г (94%) вещества. C16H13N2O5SCl. Т.пл. 235-234°С (ДМФА).
Вычислено, %: С=52.4; Н=3.5; N=7.6;
Найдено, %: С=52.6; Н=3.4; N=7.5.
Структура полученных сульфамидов 1-3 доказана ИК- и ПМР-спектрами. В ИК-спектрах сульфамидов, снятых в вазелиновом масле, наблюдается полоса в области 1705-1710 см-1, соответствующая поглощению амидного карбонила. В области 1600-1620 см-1 присутствует широкая полоса валентных колебаний = С-Н двух бензольных колец и Н – хелатного цикла. В интервале 3200-3280 и 3300-3370 см-1 присутствуют пики связей = N-H и -NH2.
В ПМР-спектре сульфамидов, снятых в растворе дейтеродиметилсульфоксида в интервале 6,63-8,23 м.д., находятся сигналы протонов ароматических колец, на которые наложились сигналы -N-H и =С-Н групп. В области 10,76-10,93 м.д. находится широкая полоса группы -NH2. Отсутствие сигнала метиленовой группы свидетельствует о нахождении этих соединений в растворе ДМСО исключительно в енольной форме. Отсутствие сигнала енольного гидроксила в области 14-16 м.д., по-видимому, связано с обменом протонов растворителя. Енольный гидроксил в H-хелатном цикле обнаруживается качественной реакцией с хлоридом окисного железа (появляется характерное темно-фиолетовое окрашивание).
| Таблица 1 |
| 4-N-(4-Арил-2,4-диоксобутирил)аминобензолсульфамиды |
 |
% |
 |
v, см-1 |
 , м.д. , м.д. |
 |
 |
 |
 |
1600 (С6H5, С6Н4, С=O ОН ОН |
7,00-8,23 м |
 |
| H |
85 |
218-220 |
1710 (С=O амид) |
(11H, C6H5, C6H4, CH=, NH) |
1 |
 |
 |
 |
3260, 3370 (NH, NH2) |
10,83 ш.п. (2H, NH2) |
 |
 |
 |
 |
1600-1615 (2С6Н4, С=О ОН) ОН) |
1,23 т (3Н, СН3), 4,00 с (2Н, СН2) |
 |
| С2Н5O |
91 |
225-226 |
1705 (С=O амид) |
4,5 с (2Н, СН2), 6,63-8,13 м (10Н, |
2 |
 |
 |
 |
3230, 3300 (NH, NH2) |
2С6Н4, СН=,NH), 10,76 ш.п. (2H, NH2) |
 |
 |
 |
 |
1600 (2C6H6, C=O OH) OH) |
4,60 с (2Н, СН2), 7,06-8,23 м (10Н, |
 |
| Cl |
94 |
234-235 |
1700 (С=O амид) |
2С6Н4, СН=, NH), 10,93 ш.п. (2H, NH2) |
3 |
 |
 |
 |
3280, 3350 (NH, NH2) |
 |
 |
Эффективность заявляемых 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамидов подтверждается скринингом на анальгетическую активность по методу «горячей пластинки» (Н.В.Эдди, Д.Леймбах. Фармакология и токсикология. 311, 1960), противовоспалительной активности на модели «каррагенинового отека» {Методические рекомендции по экспериментальному изучению нестероидных противовоспалительных веществ. Фармкомитет, Москва, 1982). Чувствительность микроорганизмов к заявляемым соединениям определяли стандартным методом двукратных серийных разведений с оценкой активности по минимально действующей концентрации. Результаты биологической активности приведены в таблице 2 и 3.
| Таблица 2 |
| Противовоспалительная и анальгетическая ативность 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамидов |
| Соединение и препарат сравнения |
Токсичность ЛД50, мг/кг |
Доза, мг/кг |
Вид активности |
| Противовоспалительная |
Анальгетическая |
| Ингибирование отека через 4 ч, % |
Величина оборонительного рефлекса, сек |
| 1 |
1000 |
50 |
49 |
26,0 |
| 2 |
1000 |
50 |
60 |
27,8 |
| 3 |
1000 |
50 |
30 |
23,8 |
| Контроль (крахмальная слизь) |
 |
 |
0 |
11,2 |
| Вольтарен |
380 |
8 |
53,9 |
26,0 |
 -арилсульфониламиноэтиламиды ароилпировиноградных кислот -арилсульфониламиноэтиламиды ароилпировиноградных кислот |
>1000 |
50 |
18-43,4 |
17-24 |
| Таблица 3 |
| Противомикробная активность 4-N-(4-арил-2,4-диоксобутирил)аминобензолсульфамидов |
| Соединение и препарат сравнения |
Токсичность ЛД50, мг/кг |
Противомикробная активность мкг/мл |
| Е.coli |
St.aureus |
| 1 |
1000 |
1000 |
500 |
| 2 |
1000 |
500 |
500 |
| 3 |
1000 |
250 |
500 |
| Фурациллин |
 |
1000 |
500 |
Соединения 1-3 сопоставимы по токсичности с  -арилсульфониламиноэтиламидами ароилпировиноградных кислот. По анальгетической активности и противовоспалительному действию заявляемые соединения превосходят взятые за эталон сравнения -арилсульфониламиноэтиламидами ароилпировиноградных кислот. По анальгетической активности и противовоспалительному действию заявляемые соединения превосходят взятые за эталон сравнения  -арилсульфониламиноэтиламиды ароилпировиноградных кислот. Дополнительно к перечисленным активностям заявляемые соединения проявляют антимикробное действие по отношению к кишечной палочке и стафилококку, сопоставимое (соединение 1) или превосходящее (соединение 2 и 3) действие медицинского препарата фурациллин. -арилсульфониламиноэтиламиды ароилпировиноградных кислот. Дополнительно к перечисленным активностям заявляемые соединения проявляют антимикробное действие по отношению к кишечной палочке и стафилококку, сопоставимое (соединение 1) или превосходящее (соединение 2 и 3) действие медицинского препарата фурациллин.
Предлагаемые биологически активные соединения после клинической апробации найдут применение в практическом здравоохранении.
Формула изобретения
4-N-(4-Арил-2,4-диоксобутирил)аминобензолсульфамиды общей формулы
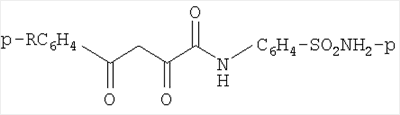
где R – Н, С2Н5О, Cl,
проявляющие противовоспалительную, анальгетическую и антимикробную активности.
|
|