Патент на изобретение №2365592
|
||||||||||||||||||||||||||||||||||
(54) (Z)-1′-R-6′,6′-ДИМЕТИЛ-3-(ФЕНИЛ(АРИЛАМИНО)МЕТИЛЕН)-6′,7′-ДИГИДРО-3Н-СПИРО[ФУРАН-2,3′-ИНДОЛ]-2′,4,4′,5(1’H,5’H)ТЕТРАОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
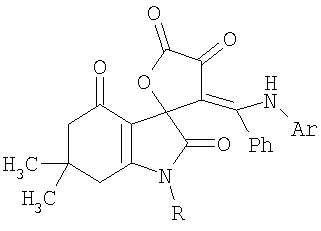
Изобретение относится к новым соединениям -(Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’Н,5’Н)-тетраонам формулы
где Ar = фенил, n-метоксифенил, n-толлил; R = аллил, бензил, фенил, n-толлил, n-метоксифенил, пиррол-3-ил)-2-оксоацетаты подвергают взаимодействию с N-замещенными 3-амино-5,5-диметилциклогекс-2-енонами в среде инертного апротонного растворителя с последующим выделением целевых продуктов. Процесс ведут при температуре 20-22°С. В качестве растворителя используют абсолютный хлороформ. Полученные соединения обладают анальгетической активностью. 2 н. и 2 з.п. ф-лы, 2 табл.
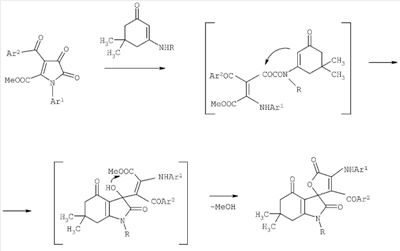
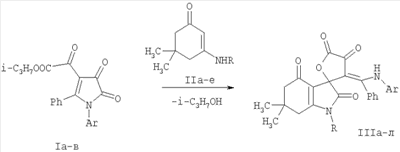
Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса спиро[фуран-2,3′-индолов] и к способу их получения, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем. К недостаткам данного способа относится невозможность получения (Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’H,5’H)-тетраонов. Задачей изобретения является разработка простого способа синтеза неописанных в литературе (Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3Н-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’Н,5’Н)-тетраонов. Поставленная задача осуществляется путем выдерживания при комнатной температуре изопропил 2-(1-арил-4,5-диоксо-2-фенил-4,5-дигидро-1Н-пиррол-3-ил)-2-оксоацетатов (Iа-в) с N-замещенными 3-амино-5,5-диметилциклогекс-2-енонами (IIa-е) по следующей схеме: где Ar=Ph (Ia, IIIa-e, IVa-e, Va-e), С6Н4OМе-4 (Iб, IIIж-к, IVж-к, Vж-к), С6Н4Ме-4 (Iв, IIIл, IVл, Vл); R=СН2СН=СН2 (IIa, IIIa, IVa, Va), CH2Ph (IIб, IIIб,ж,л, IVб,ж,л, Vб,ж,л), Ph (IIв, IIIв,з, IVв,з, Vв,з), С6Н4Ме-4 (IIг, IIIг, IVг, Vг), С6Н4OМе-4 (IIд, IIIд,и, IVд,и, Vд,и), Процесс ведут при температуре 20-22°С, а в качестве растворителей используют абсолютный хлороформ. Из патентной и технической литературы не были выявлены способы получения 1′-замещенных (Z)-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3Н-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’Н,5’Н)-тетраонов, имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты, растворители, в которых проходит реакция, и интервал температур, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень». Изобретение иллюстрируется следующими примерами. Пример 1. (Z)-1′-Аллил-6′,6′-диметил-3-(фенил(фениламино)метилен)-6′,7′-дигидpo-3H-спиpo[фypaн-2,3′-индол]-2′,4,4′,5(1’H,5’H)-тетраон (IIIa). Раствор 1.0 ммоль соединения (Ia) и 1.0 ммоль соединения (IIа) в 15 мл абсолютного хлороформа выдерживали при температуре 20°С в течение 8 ч (до исчезновения исходного пирролдиона по данным ТСХ), растворитель удалили, остаток затерли гексаном. Выход 72%. Т.пл. 148-149°С (разл., из этилацетата). Соединение (IIIa) C29H26N2O5. Найдено, %: С 74.13; Н 5.41; N 5.77. Вычислено, %: С 74.18; Н 5.43; N 5.81. Соединение (IIIa) – ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, труднорастворимое в обычных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях. В ИК спектре соединения (IIIa), снятого в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний NH группы при 3172 см-1, лактонной карбонильной группы при 1788 см-1, кетонной и лактамной карбонильных групп при 1753 см-1 и кетонной группы, вовлеченной в образование внутримолекулярной водородной связи при 1649 см-1. В спектре ПМР соединения (IIIa), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец присутствуют два синглета протонов двух метильных групп при 0.89 и 0.95 м.д., дублетные сигналы четырех неэквивалентных протонов метиленовых групп С5′H2 и С7′H2 в области 1.77-2.24 м.д. с характерными константами спин-спинового взаимодействия (J 16.8 и 18.4 Гц) и уширенный синглет протона группы NH в области 12.65 м.д. Пример 2. (Z)-1′-Бензил-6′,6′-диметил-3-(фенил(фениламино) метилен)-6,7′-дигидро-3Н-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’H,5’H)-тетраон (IIIб). Раствор 1.0 ммоль соединения (Iа) и 1.0 ммоль соединения (IIa) в 15 мл абсолютного хлороформа выдерживали при температуре 20°С в течение 8 ч (до исчезновения исходного пирролдиона по данным ТСХ), растворитель удалили, остаток затерли гексаном. Выход 77%. Т.пл. 152-153°С (из ацетона – этилацетата – ацетонитрила, 1:1:1). Соединение (IIIб) С33Н28N2O5 Найдено, %: С 74.36; Н 5.27; N 5.23. Вычислено, %: С 74.42; Н 5.30; N 5.26. Соединение (IIIб) – ярко-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, труднорастворимое в обычных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях. В ИК спектре соединения (IIIб), снятого в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний NH группы при 3183 см-1, лактонной карбонильной группы при 1781 см-1, кетонной и лактамной карбонильных групп при 1752 см-1 и кетонной группы, вовлеченной в образование внутримолекулярной водородной связи при 1651 см-1. В спектре ПМР соединения (IIIa), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец присутствуют два синглета протонов двух метильных групп при 0.81 и 0.90 м.д., дублетные сигналы четырех неэквивалентных протонов метиленовых групп С5′H2 и С7′ H2 в области 1.78-2.25 м.д. с характерными константами спин-спинового взаимодействия (J 16.0 и 18.5 Гц), два дублет протонов метиленовой группы бензильного заместителя при 4.33 и 4.70 с константой спин-спинового взаимодействия (J 16.0 Гц) и уширенный синглет протона группы NH в области 12.65 м.д. Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить неописанные в литературе (Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’H,5’H)-тетраоны (IIIa-л) с хорошими выходами, которые найдут применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств. Пример 3. Фармакологическое исследование (Z)-6′,6′-диметил-3-(фенил(4-метоксифенил)метилен)-1′-(нафтален-1 -ил)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’H,5’H)-тетраонов (IIIa,к) на наличие анальгетической активности. Анальгетическую активность соединений (IIIa,к) определяли методом «горячей пластинки» и на модели «уксусных корчей». Проведенные исследования показали (табл.1 и 2), что соединения (IIIa,к) обладают анальгетической активностью. Данные о фармакологической активности аналогов заявляемых соединений в доступной литературе отсутствуют.
Формула изобретения
1. (Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4’5(1’Н,5’Н)-тетраоны формулы 2. Способ получения (Z)-1′-R-6′,6′-диметил-3-(фенил(ариламино)метилен)-6′,7′-дигидро-3H-спиро[фуран-2,3′-индол]-2′,4,4′,5(1’Н,5’Н)тетраонов по п.1, отличающийся тем, что изопропил 2-(1-арил-4,5-диоксо-2-фенил-4,5-дигидро-1Н-пиррол-3-ил)-2-оксоацетаты подвергают взаимодействию с N-замещенными 3-амино-5,5-диметилциклогекс-2-енонами в среде инертного апротонного растворителя с последующим выделением целевых продуктов. 3. Способ по п.2, отличающийся тем, что процесс ведут при температуре 20-22°С. 4. Способ по п.2 или 3, отличающийся тем, что в качестве растворителя используют абсолютный хлороформ.
|
||||||||||||||||||||||||||||||||||

 126
126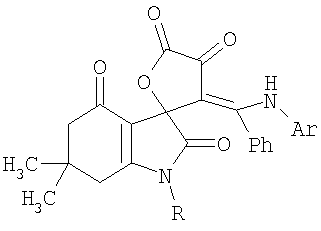
 -нафтил, а также к способу их получения, который заключается в том, что изопропил 2-(1-арил-4,5-диоксо-2-фенил-4,5-дигидро-1Н-
-нафтил, а также к способу их получения, который заключается в том, что изопропил 2-(1-арил-4,5-диоксо-2-фенил-4,5-дигидро-1Н-