|
|
(21), (22) Заявка: 2008118649/04, 12.05.2008
(24) Дата начала отсчета срока действия патента:
12.05.2008
(46) Опубликовано: 10.08.2009
(56) Список документов, цитированных в отчете о
поиске:
SU 482446, 30.08.1975. RU 2073009 С1, 10.02.1997. SU 1069403 А1, 15.04.1994.
Адрес для переписки:
630559, Новосибирская обл., Новосибирский р-н, р.п. Кольцово, 6, кв.122, а/я 173, патентоведу Ю.Н. Мистюрину
|
(72) Автор(ы):
Покровский Андрей Георгиевич (RU),
Салахутдинов Нариман Фаридович (RU),
Толстиков Генрих Александрович (RU)
(73) Патентообладатель(и):
Общество с ограниченной ответственностью “Сибфармакон” (ООО “Сибфармакон”) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ПЕНТАНИКОТИНАТА ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ, ЯВЛЯЮЩЕГОСЯ ИНГИБИТОРОМ РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА
(57) Реферат:
Изобретение относится к способу получения пентаникотината глицирризиновой кислоты без примесей путем взаимодействия глицирризиновой кислоты или ее аммонийной соли с химическим реагентом в растворителе с получением полиникатинатов глицирризиновой кислоты в виде осадка. В качестве химического реагента используют гидрохлорид хлорангидрида никотиновой кислоты, в качестве растворителя – пиридин, при соотношении реагентов гидрохлорида хлорангидрида никотиновой кислоты, пиридина и глицирризиновой кислоты соответственно (3-5):(26-27):1. Целевой продукт из полиникатинатов глицирризиновой кислоты выделяют методом препаративной высокоэффективной жидкостной хроматографии. Технический результат: выделение индивидуального пентаникотината глицерризиновой кислоты без примесей, который может использоваться в медицине, вирусологии, фармакологии, например в качестве ингибитора репродукции вируса иммунодефицита человека. 2 з.п. ф-лы, 6 табл.
Изобретение относится к биологически активным веществам, производным глицирризиновой кислоты, и может использоваться в медицине, вирусологии, фармакологии, например в качестве ингибитора репродукции вируса иммунодефицита человека.
Известно, что глицирризиновая кислота – основной ингредиент экстракта корней солодки голой (Glycyrrhiza glabra) и солодки уральской (Gl. Uralensis), обладает высокой биологической активностью и является высокоэффективным средством в лечении различных заболеваний. Так, она применяется при лечении вирусных гепатитов, входит в перечень препаратов (который насчитывает около 50 наименований), подавляющих репродукцию вируса иммунодефицита человека in vitro. Названная кислота оказывает противовирусное, противовоспалительное, противозудное и иммуномодулирующее действие, действует на разные типы ДНК и РНК вирусов in vitro и in vivo (Varicella zoster; Herpes simplex 1 и 2 типа; различные типы вируса папилломы человека, в т.ч. онкогенные), прерывает репликацию вирусов на ранних стадиях, вызывает выход вириона из капсида, тем самым не допуская его проникновения в клетки, что связано с селективным дозозависимым ингибированием фосфорилирующей киназы Р. Глицирризиновая кислота взаимодействует со структурами вируса (возможно, с белками), изменяя различные фазы вирусного цикла, что сопровождается необратимой инактивацией вирусных частиц, находящихся в свободном состоянии вне клеток, блокирует внедрение активных вирусных частиц внутрь клетки, нарушает способность вируса к индукции синтеза новых вирусных частиц, индуцирует образование интерферона, что является одним из компонентов противовирусного действия, инактивирует указанные вирусы в нетоксичных для нормально функционирующих клеток концентрациях. Мутантные штаммы вирусов, резистентные к ацикловиру и йодоуридину, также высокочувствительны к глицирризиновой кислоте, как и немутантные штаммы. Противовоспалительная активность глицирризиновой кислоты сочетается со стимулирующим влиянием на гуморальные и клеточные факторы иммунитета.
Производные глицирризиновой кислоты также, как и сама кислота, обладают высокой биологической активностью. В частности, моноаммониевая соль глицирризиновой кислоты (глицирам Г) или пента-О-никотинат глицирризиновой кислоты, 3-(b-D-2,3,4-три-о-никотинилглюкуронпиранозил)
1 2(a-D-3,4-ди-О-никотинилглюкуронпиранозил глицирретовой кислоты (ниглизин, НГ) используются для ингибирования репродукции вируса Марбург (Патент РФ  2088232, МПК А61К 31/70, опубл. 27.08.1997 г.). 2088232, МПК А61К 31/70, опубл. 27.08.1997 г.).
Известны способы получения пента-О-никотината глицирризиновой кислоты (авторское свидетельство СССР  482446, МПК С07С 173/00, опубл. 30.08.1975 и авторское свидетельство СССР 482446, МПК С07С 173/00, опубл. 30.08.1975 и авторское свидетельство СССР  1069403, МПК С07J 63/00, опубл. 30.04.1994 г.), в которых описаны различные способы получения пентаникотината глицирризиновой кислоты. В упомянутых авторских свидетельствах в качестве доказательств структуры образующегося вещества были использованы данные ИК-спектроскопии и элементного анализа. 1069403, МПК С07J 63/00, опубл. 30.04.1994 г.), в которых описаны различные способы получения пентаникотината глицирризиновой кислоты. В упомянутых авторских свидетельствах в качестве доказательств структуры образующегося вещества были использованы данные ИК-спектроскопии и элементного анализа.
Наиболее близким аналогом (прототипом) является способ получения пента-О-никотината глицирризиновой кислоты из глицирризиновой кислоты с использованием хлорангидрида никотиновой кислоты в среде азотистого основания (патент РФ  2073009, МПК С07J 63/00, опубл. 10.02.1997 г.). Глицирризиновую кислоту переводят в глицирам или трикалиевую соль и подвергают азеотропной сушке в смеси трибутиламина и бензола при 69-70°С в вакууме и хлорагидрид никотиновой кислоты используют в виде хлоргидрата при температуре 75-80°С в течение 3-4 ч при молярном соотношении реагентов 1:7.4-7.6 соответственно с последующей декантацией трибутиламина и обработкой реакционной смеси ацетоном при 50°С. 2073009, МПК С07J 63/00, опубл. 10.02.1997 г.). Глицирризиновую кислоту переводят в глицирам или трикалиевую соль и подвергают азеотропной сушке в смеси трибутиламина и бензола при 69-70°С в вакууме и хлорагидрид никотиновой кислоты используют в виде хлоргидрата при температуре 75-80°С в течение 3-4 ч при молярном соотношении реагентов 1:7.4-7.6 соответственно с последующей декантацией трибутиламина и обработкой реакционной смеси ацетоном при 50°С.
Однако в приведенных выше аналогах, в том числе и в прототипе, получают не чистое вещество, а пента-О-никотинат глицирризиновой кислоты с большим количеством примесей других никотинатов ГК.
Техническим результатом предлагаемого изобретения является создание такой технологии, которая обеспечивает выделение индивидуального пентаникотината глицирризиновой кислоты без примесей.
Указанный технический результат достигается тем, что в способе получения пентаникотината глицирризиновой кислоты путем взаимодействия глицирризиновой кислоты или ее аммонийной соли с химическим реагентом в растворителе с получением полиникатинатов глицирризиновой кислоты в виде осадка, согласно изобретению в качестве химического реагента используют гидрохлорид хлорангидрида никотиновой кислоты, в качестве растворителя – пиридин, при соотношении реагентов гидрохлорида хлорангидрида никотиновой кислоты, пиридина и глицирризиновой кислоты соответственно (3-5):(26-27):1, а целевой продукт из полиникатинатов глицирризиновой кислоты выделяют методом препаративной высокоэффективной жидкостной хроматографии по схеме, представленной ниже:
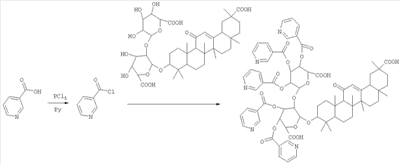
Препаративную высокоэффективную жидкостную хроматографию проводят путем растворения полиникатинатов глицирризиновой кислоты в этиловом спирте в соотношении 1:4 с последующим нанесением раствора на колонку и осуществления градиентного элюирования смесью 0.3 М раствора перхлората лития в воде и метанола в течение не более 15 минут. Целевой продукт в виде полиникатинатов глицирризиновой кислоты получают в количестве около 60 мас.%, а конечный продукт из полиникатинатов глицирризиновой кислоты методом высокоэффективной жидкостной хроматографии выделяют в количестве не менее 3 мас.%.
В результате проведенных исследований были подобраны аналитические условия, позволяющие надежно контролировать качественный состав реакционной смеси, включая исходные соединения, использующиеся растворители, промежуточные и конечные продукты реакций в условиях синтеза пентаникотината глицирризиновой кислоты, описанных в прототипах. Использование современных методик анализа позволило обнаружить, что реакционная смесь во всех случаях неоднородна и состоит из набора никотинатов глицирризиновой кислоты, содержащих в своей структуре как различное количество никотинатных остатков, так и являющихся изомерами замещения никотиновыми фрагментами гидроксильных групп глицирризиновой кислоты. В составе реакционной смеси присутствует и продукт полной этерификации исходного соединения – пентаникотинат глицирризиновой кислоты в количестве не более 4%. Варьирование условий реакции и оптимизация процесса по разным параметрам не приводят к преобладанию пентаникотината в реакционной смеси. Выделение целевого продукта было проведено с помощью препаративной высокоэффективной жидкостной хроматографии.
Пример 1. Анализ реакционных смесей
Вначале получают обзорные хроматограммы образцов реакционных смесей, выполненных методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на хроматографе «Милихром-А02». В табл.1 приведены условия хроматографирования.
Для идентификации получаемых продуктов были разработаны методики разделения реакционных смесей с использованием различных методов высокоэффективной жидкостной хроматографии и проведены препаративные разделения наработанных реакционных смесей. Выделенные продукты были охарактеризованы с использованием ЯМР-спектроскопии 1Н и 13C и ВЭЖХ-хроматомасс спектроскопии. На основании анализа молекулярных масс ионов, наблюдающихся в ВЭЖХ-хроматомасс спектре, показано, что реакционные смеси содержат набор полиникотинатов глицирризиновой кислоты, в том числе три- и тетраникотинаты, а также пентаникотинат глицирризиновой кислоты.
Таблица 1
Условия хроматографирования |
| Колонка |
Стальная, 75×2 мм, заполненная сорбентом LiChrospher RP-18 с размером частиц 5 мкм |
| Температура колонки |
35°С |
| Подвижная фаза (ПФ) |
А:0.3 М раствор перхлората лития в воде; В: метанол |
| Расход ПФ В от 0 до |
100 мкл/мин (элюент А 5 мин, градиент 100% за 15 мин, элюент В 5 мин) |
| Детектор |
Ультрафиолетовый, длина волны 260 нм |
| Время анализа |
25 мин |
Сравнением хроматограмм, полученных на ВЭЖХ-хроматомасс спектрометре с использованием УФ-детектора, данных ионмасс-детектора и соответствующих аналитических ВЭЖХ-хроматограмм, определены группы пиков в аналитических ВЭЖХ-хроматограммах, соответствующие различным полиникотинатам глицирризиновой кислоты, в том числе и пентаникотинату глицирризиновой кислоты.
Пример 2. Варианты синтеза пентаникотината глицирризиновой кислоты
Для отработки методики синтеза пентаникотината глицирризиновой кислоты были экспериментально исследованы возможные варианты синтеза полиникотинатов глицирризиновой кислоты, включающие в себя:
а) взаимодействие глицирризиновой кислоты (или ее аммонийной соли) с предварительно синтезированными по известным методикам ангидридом никотиновой кислоты или гидрохлоридом хлорангидрида никотиновой кислоты в различных растворителях (пиридин, N-метилпирролидон, триэтиламин и т.д.), в том числе в присутствии катализаторов;
б) взаимодействие глицирризиновой кислоты (или ее аммонийной соли) с полученным in situ гидрохлоридом хлорангидрида никотиновой кислоты в различных растворителях;
в) взаимодействие глицирризиновой кислоты (или ее аммонийной соли) с никотиновой кислотой в присутствии борсодержащих катализаторов;
г) взаимодействие активированной металлическим натрием аммонийной соли глицирризиновой кислоты с никотиновой кислотой;
д) взаимодействие глицирризиновой кислоты (или ее аммонийной соли) с никотиновой кислотой в условиях физического воздействия (микроволнового излучения).
На основании анализа полученных ВЭЖХ-хроматограмм определена наиболее перспективная методика синтеза полиникотинатов глицирризиновой кислоты – взаимодействие глицирризиновой кислоты (или ее аммонийной соли) с полученным in situ гидрохлоридом хлорангидрида никотиновой кислоты в пиридине.
Пример 3. Многофакторная оптимизация процесса (табл.2-4)
Варьируемые факторы: количество никотиновой кислоты, PCl5, пиридина, продолжительность и температура реакции.
Фиксированные факторы: количество глицирризиновой кислоты (10 г); температура и продолжительность первой стадии (синтез хлорангидрида никотиновой кислоты); обработка реакционной смеси.
Таблица 3
Матрица для пяти переменных факторов оптимизации |
| xl |
x2 |
x3 |
х4 |
x5 |
| 0.5 |
0.289 |
0.204 |
0.158 |
0.13 |
| -0.5 |
0.289 |
0.204 |
0.158 |
0.13 |
| 0 |
-0.578 |
0.204 |
0.158 |
0.13 |
| 0 |
0 |
-0.612 |
0.158 |
0.13 |
| 0 |
0 |
0 |
-0.632 |
0.13 |
| 0 |
0 |
0 |
0 |
-0.65 |
Рассчитываемый фактор в физической величине для исходной серии опытов:
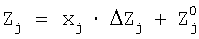 , где хj – коэффициент по матрице. , где хj – коэффициент по матрице.
По итогам первого этапа оптимизации определили наихудший опыт.
Рассчитываемый фактор в физической величине для следующего опыта: Zj=(2/n) Zji-Zi, где n – число факторов в матрице планирования, i – номер опыта, j – номер фактора, Zji-Zi, где n – число факторов в матрице планирования, i – номер опыта, j – номер фактора,  Zji – сумма значений i-x факторов без наихудшего опыта, Zi – значение i-го фактора в наихудшем опыте предыдущего симплекса. Zji – сумма значений i-x факторов без наихудшего опыта, Zi – значение i-го фактора в наихудшем опыте предыдущего симплекса.
Расчеты факторов каждого последующего опыта проводились после определения наихудшего опыта по этой же формуле.
Исходя из анализа полученных ВЭЖХ-хроматограмм и масс полученных продуктов выбраны условия реакции, подходящие для последующего масштабирования.
Пример 4. Синтез смеси никотинатов глицирризиновой кислоты
Двугорлую колбу емкостью 5 л, снабженную эффективной механической мешалкой, помещают в баню с глицерином с термометром. В колбу заливают 4.0 л пиридина, засыпают 500 г никотиновой кислоты и при перемешивании нагревают реакционную смесь до 30-35°С (здесь и далее указана температура бани), затем, не прекращая перемешивания, добавляют к образовавшейся суспензии 204.2 г пятихлористого фосфора. По окончании прибавления смесь нагревают до 80±3°С и перемешивают при этой температуре в течение 2 ч (примерно через 30-40 мин цвет реакционной смеси из светлого становится темно-коричневым). Далее добавляют при перемешивании 150 г глицирризиновой кислоты и выдерживают при 80±3°С в течение 4 ч 50 мин.
По окончании реакции убирают баню и дают остыть колбе до ~30-40°С, затем полученную суспензию разливают поровну в два стакана емкостью 5 л и добавляют в каждый стакан по ~1.0 л измельченного льда, приготовленного из дистиллированной воды, для перенесения оставшегося на стенках колбы осадка используют дистиллированную воду. Содержимое стаканов перемешивают и добавляют в них концентрированную соляную кислоту (~1.3 л в каждый стакан) до достижения слабокислого рН (~6), при этом наблюдается выпадение дополнительного количества осадка. Прибавление соляной кислоты сопровождается сильным разогревом реакционной массы. Оставляют стаканы на ночь для полного выпадения осадка. Выпавший в обоих стаканах коричневый осадок фильтруют. Объединенные с обоих стаканов осадки промывают дистиллированной водой (4×1 л). Вес светло-коричневого осадка составляет ~300 г.
Смешивают 2 л хлороформа и 0.4 л метанола (хлороформ: метанол = 5:1) и растворяют в этой смеси полученный ранее осадок. Растворение протекает достаточно медленно и требует выдержки в течение 1-2 ч при интенсивном перемешивании. Полученный раствор фильтруют, оставшийся осадок промывают 100 мл смеси хлороформа с метанолом в соотношении 5:1 (дважды по 50 мл), осадок (~10-15 г) выбросить. К фильтрату добавляют 2.3 л диэтилового эфира, при этом наблюдается интенсивное выпадение осадка. Полученную смесь перемешивают и оставляют на 1 ч для полного формирования осадка. Выпавший осадок фильтруют. Осадок промывают 150 мл диэтилового эфира (трижды по 50 мл), высушивают на фильтре. Вес осадка ~165 г. К полученному осадку добавляют 150 мл этилового спирта, перемешивают, фильтруют, высушивают на фильтре. Вес высушенного светло-коричневого осадка составляет ~150 г (выход ~60%).
Пример 5. Выделение пентаникотината глицирризиновой кислоты методом препаративной ВЭЖХ
Выделение целевого продукта из реакционной смеси проводят с использованием градиентной препаративной системы KNAUER на колонке 24×250 мм с Диасфер-С18, 10 мкм. Подвижная фаза – 0,3 М раствора перхлората лития в воде и метанол. Детекция проводилась с использованием прибора «Миллихром-А02». Реакционную смесь (полиникатинаты глицирризиновой кислоты) в количестве 5 г растворяют в этиловом спирте (20 мл) и наносят полученный раствор на колонку. Градиентное элюирование проводят смесью 0.3 М раствора перхлората лития в воде и метанола в течение 15 минут. Отбирают целевую фракцию, выходящую на 14,5 минуте. Из 5 г реакционной смеси было выделено 0,15 г (3%) пентаникотината глицирризиновой кислоты. Ниже приведена схема получения готового продукта:

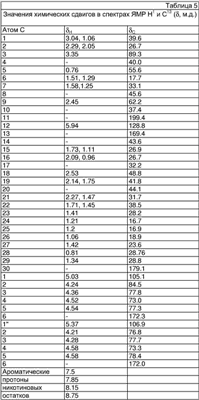
Спектры ЯМР 1Н и 13С записывали на спектрометрах АМ-400 и AV-300 фирмы Bruker с рабочими частотами 400.13 и 300.13 МГц для 1Н, 100.61 и 75.47 МГц для 13С, соответственно, для растворов веществ в CDC13 или в смеси CDCl3-CCl4 (~1:1 по объему). В качестве внутреннего стандарта использовали сигналы хлороформа ( Н 7.24 м.д., Н 7.24 м.д.,  С 76.90 м.д.). С 76.90 м.д.).
Пример 6. Исследование анти-ВИЧ активности пентаникотината глицирризиновой кислоты
В табл.6 приведены сравнительные данные по исследованию анти-ВИЧ активности на культуре клеток МТ-4 пентаникотината глицирризиновой кислоты и смеси никотинатов глицирризиновой кислоты.
| Таблица 6 |
| Данные анти-ВИЧ активности пентаникотината глицирризиновой кислоты |
| Соединение |
CD50, мкМ |
ID50, мкМ |
IS |
| Смесь никотинатов глицирризиновой кислоты |
2065 |
46,3 |
44,6 |
| Пентаникотинат глицирризиновой кислоты |
2040 |
15,1 |
57,0 |
Как видно из табл.6, пентаникотинат глицирризиновой кислоты обладает достаточно высокой анти-ВИЧ активностью.
Формула изобретения
1. Способ получения пентаникотината глицирризиновой кислоты путем взаимодействия глицирризиновой кислоты или ее аммонийной соли с химическим реагентом в растворителе с получением полиникатинатов глицирризиновой кислоты в виде осадка, отличающийся тем, что в качестве химического реагента используют гидрохлорид хлорангидрида никотиновой кислоты, в качестве растворителя – пиридин, при соотношении реагентов гидрохлорида хлорангидрида никотиновой кислоты, пиридина и глицирризиновой кислоты соответственно (3-5):(26-27):1, а целевой продукт из полиникатинатов глицирризиновой кислоты выделяют методом препаративной высокоэффективной жидкостной хроматографии по схеме, представленной ниже:
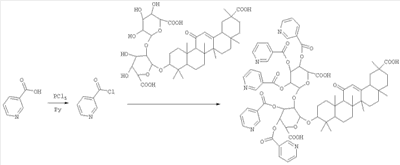
2. Способ получения пентаникотината глицирризиновой кислоты по п.1, отличающийся тем, что препаративную высокоэффективную жидкостную хроматографию проводят путем растворения полиникатинатов глицирризиновой кислоты в этиловом спирте в соотношении 1:4 с последующим нанесением раствора на колонку и осуществления градиентного элюирования смесью 0,3 М раствора перхлората лития в воде и метанола в течение не более 15 мин.
3. Способ получения пентаникотината глицирризиновой кислоты по п.1, отличающийся тем, что целевой продукт в виде полиникатинатов глицирризиновой кислоты получают в количестве около 60 мас.%, а конечный продукт из полиникатинатов глицирризиновой кислоты методом высокоэффективной жидкостной хроматографии выделяют в количестве не менее 3 мас.%.
|
|