Патент на изобретение №2360905
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СЕЛЕКТИВНЫЕ ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-4,7-ДИГИДРО-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ АДДИТИВНЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-5-МЕТИЛ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНОВ
(57) Реферат:
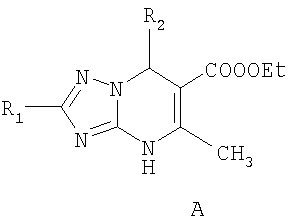
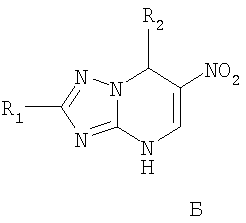
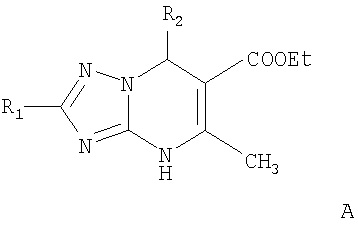
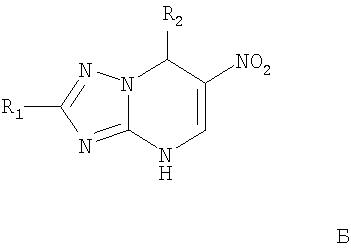
Изобретение относится к селективнм противотуберкулезным агентам, представляющим собой замещенные 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины общей формулы А или Б или фармацевтически приемлемые аддитивные натриевые или калиевые соли соединения Б
где в формуле A R1 = атом водорода; R2 = арил, выбранный из возможно замещенного фенила или гетерил, выбранный из тиенила, пиридила, индолила, пирролила, при этом замещенный фенил имеет 1-3 заместителя, выбранных из группы, включающей метокси-, нитро-, гидроксигруппу, а в формуле Б R1 = атом водорода, С1-С12алкил или С1-С12тиоалкил; R2 = арил, выбранный из возможно замещенного фенила или гетерила, выбранного из тиенила, пиридила, индолила, пирролила, при этом замещенный фенил имеет 1-3 заместителя, выбранных из группы, включающей метилендиоксигруппу, гидроксигруппу, нитро, бром, C1-С6алкил, C1-С6алкокси, а в замещенном гетериле заместитель выбирается из брома, C1-С6алкокси, C1-С6алкила. Изобретение также относится к способу получения соединений общей формулы А, включающий нагревание эквимолярных количеств арил- или гетероарилальдегида, ацетоуксусного эфира и аминотриазола в растворителя, такого как алифатический спирт, под воздействием ультразвука и к фармацевтической композиции. Предлагаемые агенты обладают более высокой активностью и более низкой токсичностью в сравнении с аналогами. 4 н.п. ф-лы, 8 табл.
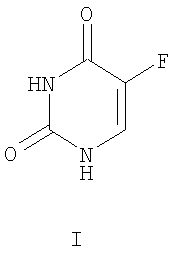
Настоящее изобретение относится к замещенным 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинам, способам их получения, а также к фармацевтически приемлемым аддитивным солям и фармацевтической композиции на основе замещенных 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов. Указанные соединения могут быть использованы в качестве противотуберкулезных агентов в первую очередь для лечения больных туберкулезом. Заявляемые в качестве селективных противотуберкулезных агентов соединения, их структура и способ получения описаны [Европейский патент Аналогом вышеуказанных веществ по строению является противоопухолевый препарат из класса замещенных дигидропиримидинов – 5-фторурацил I, который был использован для лечения экспериментального туберкулеза лабораторных животных [Патент РФ
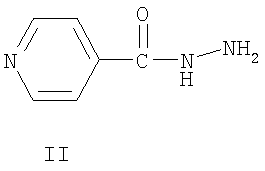
Однако 5-фторурацил токсичен, а его туберкулостатическая активность в опытах in vitro невысока (MIC=600 мкг/мл) [Патент РФ Аналог по назначению, изониазид формулы II является селективным противотуберкулезным препаратом, однако, недостатками этого препарата является его высокая токсичность и различные побочные эффекты при применении. Изониазид вызывает аллергию, негативно влияет на функцию желудочно-кишечного тракта, имеет побочное действие на нервную систему [М.Д.Машковский, Лекарственные средства, т.II, Харьков, Торгсин, 1998, с.332 и Фармакология и токсикология, 1987, 50, (4), с.87]. Отмечено широкое распространение устойчивых к изониазиду клинических штаммов микобактерий. Известен способ получения 7-арил(гетерил)-2-алкил-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов путем кипячения эквимолярных количеств 2-алкил-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина с ароматическим или гетероароматическим соединением в диоксане или спирте [Химия гетероциклических соединений, 1986, Описан способ получения соединений 7-арил(гетерил)-6-карбэтокси-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов кипячением в спирте ацетоуксусного эфира, 3-амино-1,2,4-триазола и ароматического или гетероароматического альдегида, с использованием промотирующего воздействия соляной кислоты [Изв. АН сер. хим. – 2003. – Задача изобретения – использование известных веществ в качестве селективных противотуберкулезных агентов, обладающих высокой активностью, специфично воздействующих на микроорганизм, и практически не воздействующих на макроорганизм, разработка эффективного способа их получения и фармацевтической композиции на их основе. Поставленная задача решается тем, что в качестве противотуберкулезных агентов используют замещенные 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины, объединенные общим изобретательским замыслом, представленные двумя группами соединений, которые отличаются заместителем в положении 6 (либо карбэтокси- либо нитрогруппа) и способом получения. Это замещенные 7-арил(гетерил)-6-карбэтокси-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины общей формулы А и замещенные 7-арил(гетерил)-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины общей формулы Б или их фармацевтически приемлемые натриевые или калиевые аддитивные соли
где R1 = атом водорода; R2 = арил, выбранный из возможно замещенного фенила или гетерил, выбранный из тиенила, пиридила, индолила, пирролила, при этом замещенный фенил имеет 1-3 заместителя, выбранных из группы, включающей нитро-, метокси-, гидроксигруппу
где R1 = атом водорода, С1-С12алкил или С1-С12тиоалкил; R2 = арил, выбранный из возможно замещенного фенила или гетерил, выбранный из тиенила, пиридила, индолила, пирролила, при этом замещенный фенил имеет 1-3 заместителя, выбранных из группы, включающей метилендиоксигруппу, гидроксигруппу, нитро, бром, C1-С6алкил, C1-С6алкокси, а в замещенном гетериле заместитель выбирается из брома, C1-С6алкокси, C1-С6алокси; С1-С6алкила. Для получения замещенных 7-арил(гетерил)-6-карбэтокси-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов формулы А используют новый, сонохимический способ, включающий нагревание эквимолярных количеств соответствующего арил- или гетерилальдегида, ацетоуксусного эфира и аминотриазола в среде растворителя, такого как алифатический спирт, отличающийся тем, что реакцию ведут под воздействием ультразвука. Указанный способ отличается от прототипа высокой селективностью процесса, что выражается в повышении выходов целевых продуктов с 56.2-67.2% до 85-90%. При этом 1Н ЯМР спектры технических продуктов содержат сигналы только целевого и исходных продуктов. Тогда как технические продукты, полученные по обычной методике (без ультразвукового воздействия), наряду с целевым 7-арил(гетерил)-6-карбэтокси-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидином содержат побочные продукты – 7-арил(гетерил)-5-гидрокси-6-карбэтокси-4,5,6,7-тетрагидро-1,2,4-триазоло[1,5-а]пиримидин и 5-арил(гетерил)-5,8-дигидро-6-карбэтокси-1,2,4-триазоло[4,3-а]пиримидин [Вестник УГТУ-УПИ. Серия химическая. 2005. Замещенные 7-арил(гетерил)-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины формулы Б получают способом, включающим кипячение эквимолярных количеств 2-алкил-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина с ароматическим или гетероароматическим соединением под воздействием ультразвука в среде растворителя, такого как алифатический спирт. При этом выходы целевых продуктов не стабильны и колеблются от 21.5 до 92%. Аддитивные соли 7-арил(гетерил)-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов формулы Б получают их взаимодействием с гидроксидом щелочного металла (натрия или калия) в этаноле. В отличие от аналогов по строению и терапевтическому действию указанные соединения представляют собой азолоаннелированные арил(гетерил) замещенные дигидропиримидины наличие туберкулостатической активности у которых не было очевидным. Туберкулостатическая активность и токсичность этих соединений по сравнению с ближайшими аналогами приведена в табл.1.
Значительная активность замещенных 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов при низкой токсичности может быть обусловлена их способностью к переносу через липофильные мембраны нейтральных молекул и заряженных частиц, в частности катионов металлов (табл.2), что по-видимому обеспечивает адресную доставку заявляемых соединений через клеточные мембраны возбудителя. С помощью QSAR расчетных методов проведена оценка проницаемости некоторых из заявляемых соединений (табл 3). Значения logP<5, что соответствует правилу Липински и означает, что данные вещества обладают приемлемой проницаемостью, чтобы рассматриваться в качестве потенциальных лекарств. Эти особенности строения и физико-химических свойств приводят к повышению активности указанных соединений (табл.4, 5). За счет своей специфичности к микобактериям они не оказывают подавляющего действия на нормальную микрофлору организма, практически не токсичны (табл.6, 7), обладают высоким терапевтическим эффектом (сравнимым с таковым для изониазида) при лечении экспериментальных животных (табл.8).
Исследование антимикобактериальной активности соединений формулы А и Б в опытах in vitro проводят бактериологически, методом вертикальной диффузии на плотной питательной среде Ливенштейна-Йенсена или “Новая”. В пробирку с засеянным тест-микробом по свободному краю на дно закапывают по 0,3 мл каждого разведения. Пробирки помещают в термостат в вертикальном положении и инкубируют при 37°С, результаты учитывают на 10-12 сутки. Антибактериальную активность замещенных соединений формулы А или Б изучают методом высевания растворов препарата в лунки. В чашку Петри с простым питательным агаром вносят тест-микроб. В лунку, расположенную посредине чашки Петри, вносят по 0,02 мл препарата в необходимых концентрациях. Результаты учитывают после 24-часовой инкубации в термостате при 37°С определением зоны задержки роста микроорганизмов по краям лунки. Изучение цитотоксичности соединений формулы А или Б проводят на клеточной культуре МТ-4 (перевиваемой линии клеток Т лимфоцитов человека). Токсичность различных концентраций соединений определяют по жизнеспособности клеток относительно контроля с использованием спектрофотометра при длине волны 540 нм, по полученным данным строят дозозависимые кривые и определяют концентрации, на 50% снижающие жизнеспособность клеток по сравнению с контролем (CD50). Исследование острой токсичности соединений формулы А или Б осуществляют по стандартной методике на белых мышах. Животные получают препарат per os в 10% растворе крахмала. Изучение терапевтического действия указанных соединений осуществляют на белых лабораторных мышах весом 18-23 г, зараженных внутривенно, в хвостовую вену в дозе 0.5 мг двухнедельной культуры (штамм Н37Rv) в 0.5 мл физ.раствора. Лечение начинают через неделю после заражения и проводят ежедневно в течение 8 недель. Исследуемые препараты, в том числе контрольный изониазид дают мышам в дозе 10 мг/кг веса. После забоя животных методом эвтаназии, проводят макро- и микроскопическое, а также гистологическое исследования, рассчитывают индекс поражения органов. Фармацевтическую композицию соединений на основе соединений формулы А или Б получают смешиванием фармацевтически приемлемого наполнителя и эффективного количества соединений формулы А или Б. В качестве наполнителя может быть использовано любое известное для этих целей твердое, жидкое или пластичное вещество.
Фармацевтическую композицию получают смешиванием фармацевтически приемлемого наполнителя и эффективного количества соединений формулы А или Б или фармацевтически приемлимых аддитивных солей соединений формулы Б. В качестве наполнителя может быть использовано любое известное для этих целей твердое, жидкое или пластичное вещество. Чистоту полученных соединений контролируют методом ТСХ, значения Rf определяют с использованием пластинок “Sorbfil” (Силикагель СТХ-1А, УФ) (Россия) или “Silufol-UV” (Чехословакия). Структуру полученных соединений доказывают данными элементного анализа (С,Н,N,O-анализатор фирмы Karlo Erba). ИК-спектры регистрируют на ИК-Фурье спектрометре «Spectrum One» фирмы «PerkinElmer» с помощью приставки диффузного отражения (Diffuse Reflectance Sampling Accessory (DRA)). Спектры ЯМР 1Н соединений записывают в ДМSO-d6 на приборе “Bruker-400” с рабочей частотой 400 мГц и ТМС в качестве внутреннего стандарта. Масс-спектры регистрируют на приборе «Varian MAT 311 – А» с комбинированным FD/EI источником в результате прямого введения пробы в область ионизации. Энергия ионизирующих электронов 70 эВ, ускоряющее напряжение 3 кВ. Температуры плавления определяют на микронагревательном столике «Boetius». Для проведения реакций под ультразвуковым воздействием используют ультразвуковой диспергатор марки УЗДН-2Т с частотой 22 кГц. Катионтранспортные свойства соединений изучают по общепринятой методике, заключающейся в исследовании переноса катиона из одной водной фазы в другую водную фазу через слой неполярного органического растворителя. Примеры конкретного выполнения. Пример 1 6-Этоксикарбонил-7-фенил-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы А, где R1 = атом водорода; R2 = фенил) К суспензии бензальдегида (10 ммолей), ацетоуксусного эфира (1.30 г, 10 ммоль) и 3-амино-1,2,4-триазола (0.83 г, 10 ммоль) в 10 мл этанола добавляют 0.5 мл, (10.0 ммоль) концентрированной НС1, опускают излучатель ультразвукового диспергатора, который включают на время, необходимое для завершения реакции (5 мин). Растворитель упаривают, остаток промывают ацетонитрилом. Выход 2.5 г (90%). Т.пл. 190-192°С. Спектр 1Н ЯМР (DMSO-d6): 1.04 (т, 3Н. СН3СН2, J=4.0); 2.42 (с, 3Н, Me); 3.94 (м, 2Н, СН3СН2); 6.27 (с, 1Н, С(7)Н); 7.26 (м, 5Н, Ph); 7.64 (с, 1Н, СН); 10.77 (с, 1Н, NH); ИК-спектр (DRA), Пример 2 6-Этоксикарбонил-7-(тиен-2-ил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы А, где R1 = атом водорода; R2 = тиен-2-ил) Получают аналогично примеру 1 из 10 ммолей 2-тиенилальдегида, ацетоуксусного эфира (1.30 г, 10 ммоль) и 3-амино-1,2,4-триазола (0.83 г, 10 ммоль) в присутствии (10.0 ммоль) винной кислоты. Выход 2.50 г (87%). Т.пл. 202-203°С. Спектр 1Н ЯМР (CDCl3): 1.18 (т, 3Н, СН3СН2, J=7.2); 2.58 (с, 3Н, Me); 4.14 (м, 2Н, СН3СН2); 6.75 (с, 1Н, СН); 7.65 (с, 1Н, С(7)Н); 7.01 (м, 3Н, тиазол); 10.32 (с, 1Н, NH); ИК-спектр (вазелиновое масло), Пример 3 6-Этоксикарбонил-7-(4-пиридил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы А, где R1 = атом водорода; R2 = 4-пиридил) Получают аналогично примеру 1 из 10 ммолей 4-пиридинальдегида, ацетоуксусного эфира (1.30 г, 10 ммоль) и 3-амино-1,2,4-триазола (0.83 г, 10 ммоль). Очищают кристаллизацией из смеси метанол-вода (1:2). Выход 2.55 г (90%). Т.пл. 178-180°С. Спектр 1Н ЯМР (DMSO-d6): 1.15 (т, 3Н, СН3СН2, J=4.0); 2.42 (с, 3 Н, Me); 3.94 (кв, 2Н, СН3СН2, J-4.0); 6.27 (с, 1Н, С(7)Н); 7.24 (д, 2Н, Ру); 8.54 (д, 2Н, Ру); 7.64 (с, 1Н, СН); 10.42 (с, 1Н, NH); ИК-спектр, Пример 4 6-Этоксикарбонил-7-(2-нитрофенил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы А, где R1 = атом водорода; R2 = 2-нитрофенил) Получают аналогично примеру 1 из 10 ммолей 2-нитробензальдегида, ацетоуксусного эфира (1.30 г, 10 ммоль) и 3-амино-1,2,4-триазола (0.83 г, 10 ммоль). Выход 2.83 г (85%). Т.пл. 240-242°С. Спектр 1Н ЯМР (DMSO-d6): 1.05 (т, 3Н, СН3СН2, J-=7.2); 1.63 (с, 3Н, Me); 4.04 (м, 2Н, СН3CH2); 7.51 (с, 1Н, CH-Ph); 7.75 (м, 4Н, Ph); 7.60 (с, 1Н, СН); 10.83 (с, 1Н, NH); ИК-спектр, (вазелиновое масло), Пример 5 6-Этоксикарбонил-7-(3,5-диметокси-4-гидроксифенил)-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы А, где R1 = атом водорода; R2 = 3,5-диметокси-4-гидроксифенил) Получают аналогично примеру 1 из 10 ммолей 3,5-диметокси-4-гидроксибензальдегида, ацетоуксусного эфира (1.30 г, 10 ммоль) и 3-амино-1,2,4-триазола (0.83 г, 10 ммоль). Очищают кристаллизацией из смеси метанол-вода (1:2). Выход 1.44 г (87%). Т.пл. 175-177°С. Спектр 1H ЯМР (DMSO-d6): 1.05 (т, 3Н, СН3СН2, J=7.0); 2.41 (с, 3Н, Me); 3.68 (с, 3Н, ОМе); 4.06-4.11(м, 2Н, СН3CH2); 6.18 (с, 1Н, С(7)Н); 6.39-6.47 (м, 2Н, Ph); 7.66 (с, 1Н, С(2)Н); 8.41(с, 1Н, ОН); 10.70 (с, 1Н, NH); ИК-спектр (вазелиновое масло), Пример 6 2-Октилтио-6-нитро-7-(индол-2-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1 = 2-октилтио-группа; R2 = индол-2-ил) В смесь 150 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина с 57 мг индола в 5 мл бутанола опускают излучатель ультразвукового диспергатора, который включают на время, необходимое для завершения реакции (5-10 мин). Раствор охлаждают, отфильтровывают осадок и промывают гексаном. Выход 190 мг (92%). Т.пл. 208-210°С. Спектр 1Н ЯМР (DMSO-d6): 11.92 (уш.с., NH), 11.13 (с., NH), 8.36 (с., Н5), 7.37 (д., 1Н, СН,.7=2.4 Гц), 7.34 (д., 1Н, Ar, J=8 Гц), 7.29 (д., 1Н, Ar, J=8 Гц), 7.07-7.03 (м., 1Н, Ar), 6.97-6.93 (м., 1Н, Ar), 6.83 (с., Н7), 2.90 (т., 2Н, СН2), 1.58-1.50 (м., 2Н), 1.28-1.21 (м., 10 Н), 0.87 (т., 3Н, СН3). Найдено (%): С, 59.09; Н, 6.21; N, 19.75. C21H26N6SO2. Вычислено (%): С, 59.15; Н, 6.10; N, 19.72. Пример 7 2-Октилтио-6-нитро-7-(3,5-диметил-4-гидроксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=3,5-диметил-4-гидроксифенил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 122 мг 2,6-диметилфенола. Выход: 200 мг (45%), т.пл. 112-114°. Вычислено (%): С, 58.47; Н, 6.73; Н, 16.24. C21H29N5O3S. Найдено (%): С, 58.21; Н 6.80; N, 16.40. Спектр 1Н ЯМР (DMSO-d6): 11.83 (с, NH), 8.34 (с, Н5), 8.21 (с, ОН), 6.80 (с, 2Н), 6.23 (с, Н7), 2.95 – 2.92 (м, 2Н, СН2), 2.13 (с, 6Н, 2СН3), 1.62-1.54 (м, 2Н, СН2), 1.32-1.24 (м, 10Н, 5СН2), 0.87 (т, 3Н). Пример 8 2-Октилтио-6-нитро-7-(3,4-дигидроксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=3,4-дигидроксифенил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 122 мг 1,2-дигидроксибензола. Выход: 90 мг (21.5%), т.пл. 135-138°. Вычислено (%): С, 54.42; Н, 5.97; N, 16.71. C19H25N5O4S. Найдено (%): С, 54.68; Н, 6.11; N, 16.80. Спектр 1Н ЯМР (DMSO-d6): 11.93 (с, 1Н, NH); 9.02 (с, 2Н, 2ОН), 8.50 (с, Н5), 6.71-6.59 (м, 3Н, Ar), 6.45 (с, Н7), 2.90 (т, 2Н, СН2), 1.59-1.62 (м, 2Н, СН2), 1.27-1.23 (м,10Н, 5СН2), 0.88 (т, 3Н, СН3). Пример 9 2-Октилтио-6-нитро-7-(5-броминдолил-3-ил)-4,7-дигидро-1,2,4-триазоло [1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=5-бромоиндолил-3-ил) Получают аналогично Примеру 6 из 200 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 127 мг 5-броминдола. Выход: 180 мг (55%), т.пл. 166-169°. Вычислено (%):С, 49.90; Н, 4.95; N, 16.63. C21H25N6O2SBr. Найдено (%): С, 49.92; Н, 5.00; N, 16.60. Спектр 1Н ЯМР (DMSO-d6): 11.94 (с, NH), 11.34 (с, NH), 8.40 (с, Н5), 7.54 (д, 1Н, Ar), 7.38 (д, 1Н, Ar), 7.29 (д, 1Н, Ar), 7.16-7.13 (дд, 1Н, Ar), 6.84 (с, Н7), 2.92 (т, 2Н, СН2), 1.57-1.51 (м, 2Н, СН2), 1.27-1.21 (м, 10Н, 5СН2), 0.87 (т, 3Н, СН3). Пример 10 2-Октилтио-6-нитро-7-(тиен-2-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=тиен-2-ил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 80 мкл тиофена. Выход:120 мг (30.5%), т.пл. 135-137°. Вычислено (%): С, 51.89; Н, 5.89; N, 17.80. C17H23N5O2S2. Найдено (%): С, 51.56; Н, 6.00; N, 17.78. Спектр 1Н ЯМР (DMSO-d6): 11.90 (с, NH), 8.44 (с, Н5), 6.60-6.58 (м, 1Н, Ar), 6.45 (с, Н7), 5.98-5.90 (м, 2Н, Ar), 3.00-2.96 (м, 2Н, СН2), 1.60-1.54 (м, 2Н, СН2), 1.30-1.23 (м, 10Н, 5СН2), 0.85 (т, 3Н, СН3). Пример 11 2-Октилтио-6-нитро-7-(3,4-метилендиоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=3,4-метилендиоксифенил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 80 мг 3,4-метилендиоксибензола. Выход 293 мг (68%). т.пл. 128-130°С. Найдено (%):С, 55.54; Н, 5.90; N, 16.38. C20H25N5SO4. Вычислено (%): С, 55.67; Н, 5.84; N, 16.23. Спектр Н1 ЯМР (DMSO-d6): 12.00 (c, NH), 8.64 (с, Н5), 7.25 (д, 1Н, J=8.0 Hz), 6.70-6.68 (м, 2Н), 5.22 (с, Н7), 4.03 (с, CH2), 2.95-2.91 (м, 2Н), 1.54-1.42 (м, 2Н), 1.27-1.14 (м, 10Н), 0.80 (т, 3Н). Пример 12 2-Октилтио-6-нитро-7-(5-метоксииндол-3-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=5-метоксииндол-3-ил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 81 мг 5-метоксииндола. Выход 447 мг (76%). т.пл 104-106°С. Найдено (%):С, 57.78; Н, 6.03; N, 18.48. С22Н28N6SO3. Вычислено (%): С, 57.89; Н, 6.14; N, 18.42. Спектр Н1 ЯМР (DMSO-d6): 12.00 (с, NH), 11.07 (с, NH), 8.48 (с, Н5), 7.42 (д, 1Н, J=2.4 Hz), 7.25 (д, 1Н, J=8.0 Hz), 6.86 (с, Н7), 6.75-6.71 (м, 2Н), 3.70 (с, 3Н), 2.95-2.91 (м, 2Н), 1.54-1.46 (м, 2Н), 1.26-1.16 (м, 10Н), 0.84 (т, 3Н). Пример 13 2-Октилтио-6-нитро-7-(пиррол-2-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=2-октилтио-группа; R2=пиррол-2-ил) Получают аналогично Примеру 6 из 309 мг 2-октилтио-6-нитро-1,2,4-триазоло[1,5-а]пиримидина и 70 мкл пиррола. Выход: 260 мг (53.2%), т.пл. 186-188°. Вычислено (%): С, 54.26; Н, 6.38; N, 22.34. C17H24N6O2S. Найдено (%): С, 54.21; Н, 6.32; N, 22.30. Спектр 1Н ЯМР (DMSO-d6): 11.91 (с, NH), 11.12 (с, NH), 8.40 (с, Н5), 6.66-6.65 (м, 1Н, Ar), 6.58 (с, Н7), 5.97-5.90 (м, 2Н, Ar), 3.00-2.96 (м, 2Н, СН2), 1.59-1.54 (м, 2Н, СН2), 1.31-1.22 (м, 10Н, 5CH2), 0.85 (т, 3Н, СН3). Пример 14 6-Нитро-7-(2-гидрокси-3,5-ди-трет-бутилфенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин (Соединение формулы Б, где R1=Н; R2=2-гидрокси-3,5-ди-трет-бутилфенил) Получают аналогично Примеру 6 из 211 мг 7-этокси-6-нитротриазолопиримидина и 206 мг 2,4-ди-трет-бутилфенола. Выход: 225 мг (54%), т.пл. 240-242°С. Найдено (%): С, 61,44; Н, 6,78; N, 18,86. C19H25N5O3. Вычислено (%): С, 61,37; Н, 6,81; Н, 19,10. Спектр 1Н ЯМР (DMSO-d6): 12.01 (уш.с, 1Н, NH); 8.57 (с, 1Н, Н1′); 8.55 (с, 1Н, ОН); 7.84 (с, 1Н, Н2); 7.17 (д, 1Н, H7 J=2A Hz); 7.08 (с, 1Н, Н5′); 6.81 (д, 1Н, Н5, J=2.06 Hz); 1.37-1.24 (м, 9Н); 1.19-1.08 (м, 9Н). Пример 15 2-Метил-6-нитро-7-(2,4-ди-трет-бутилфенил)-4,7-дигидро-1,2,4-триазоло[1,5-а] пиримидин (Соединение формулы Б, где R1=метил; R2=2,4-ди-трет-бутилфенил) Получают аналогично Примеру 6 из 200 мг 2-метил-6-нитротриазолопиримидина и 206 мг 2,4-ди-трет-бутилфенола. Выход: 170 мг (42%), т.пл. 257-259°С. Найдено (%): С, 61,95; Н, 7,03; N, 18,24. С30Н27N5O3. Вычислено (%): С, 62,32; Н, 7,06; N, 18,17. Спектр 1Н ЯМР (DMSO-d6): 11.9 (уш.с, 1Н, NH); 8.66 (с, 1Н, Н1′); 8.56 (с, 1Н, ОН); 7.17 (д, 1Н, Н7, J=2.3 Hz); 6.97 (с, 1Н, Н5′); 6.79 (д, 1Н, Н5′ J=2.3 Hz); 2.01 (с, 3Н, СН3); 1.24 (с, 18Н). Пример 16 2-октилтио-6-нитро-7-(индол-3-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина натриевая соль (Соединение формулы Б, где R1=2-октилтио-группа; R2=индол-3-ил) 100 мг 2-октилтио-6-нитро-7-(индол-3-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а] пиримидина растворяют в 3 мл этанолоного раствора NaOH и оставляют на 2 часа, затем осадок фильтруют, промывают этанолом и сушат на воздухе. Выход: 90 мг (85%), т.пл. 204-206°. Вычислено (%): С, 56.25; Н, 5.58; N, 18.75. C21H27N6O2SNa. Найдено (%): С, 56.45; Н, 5.70; N, 18.83. Спектр 1Н ЯМР (DMSO-d6): 11.13 (с, 1Н, NH), 8.32 (с, 1Н, Н5), 7.34-7.28 (м, 3Н, Ar), 7.07-7.03 (м, 1Н, Ar), 6.97-6.94 (м, 1Н, Ar), 6.83 (с, Н7), 2.90 (т, 2Н, СН2), 1.56-1.50 (м, 2Н, СН3), 1.27-1.21 (м, 10Н, 5СН2), 0.85 (т, 3Н, СН3). Пример 17 Фармкомпозиция на основе 6-этоксикарбонил-7-фенил-5-метил-4,7-дигидро-1,2,4-триазоло[1,5-а] пиримидина для исследования терапевтического эффекта 20 мг субстанции растирают в ступке и постепенно добавляют небольшими порциями 3 мл 0.1%-ного крахмального раствора до получения однородной суспензии. Полученную композицию используют для лечения экспериментальных животных (белые мыши) путем ее ежедневного, внутрижелудочного введения каждой мыши в дозе 10 мг/кг. Пример 18 Фармкомпозиция на основе 6-нитро-7-(индол-3-ил)-4,7-дигидро-1,2,4-триазоло[1,5-а] пиримидина калиевой соли для исследования острой токсичности 100 мг субстанции растирают в ступке и постепенно добавляют небольшими порциями 5-10 мл 10%-ного крахмального клейстера до получения однородной суспензии. Полученную композицию используют для исследования острой токсичности путем однократного внутрижелудочного введения экспериментальным животным (белые мыши) в дозе от 75 до 5000 мг/кг.
Формула изобретения
1. Селективный противотуберкулезный агент, представляющий собой замещенные 7-арил(гетерил)-4,7-дигидро-6-карбэтокси-1,2,4-триазоло[1,5-а]пиримидины общей формулы А 2. Селективный противотуберкулезный агент, представляющий собой замещенные 7-арил(гетерил)-4,7-дигидро-6-нитро-1,2,4-триазоло[1,5-а]пиримидины общей формулы Б или их фармацевтически приемлемые аддитивные натриевые или калиевые соли 3. Способ получения соединений общей формулы А по п.1, включающий нагревание эквимолярных количеств арил- или гетероарилальдегида,ацетоуксусного эфира и аминотриазола в растворителя, такого как алифатический спирт, отличающийся тем, что реакцию ведут под воздействием ультразвука. 4. Фармацевтическая композиция, обладающая антимикобактериальной активностью, содержащая активное начало и фармацевтически приемлемый наполнитель, отличающаяся тем, что в качестве активного начала она содержит замещенные 7-арил(гетерил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидины общей формулы А по п.1 или формулы Б по п.2 или аддитивные соли соединений общей формулы Б по п.2 в эффективном количестве.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 8, c.1677-1678. РУСИНОВ В.Л. и др. & laquo. Нитроазины. XIV. *Амбитентностьариламинов в реакциях с 6-нитроанизоло[1,5-а]пиримидинами. ЖОрх, 1991, 27(5), с.1100-1105.
8, c.1677-1678. РУСИНОВ В.Л. и др. & laquo. Нитроазины. XIV. *Амбитентностьариламинов в реакциях с 6-нитроанизоло[1,5-а]пиримидинами. ЖОрх, 1991, 27(5), с.1100-1105.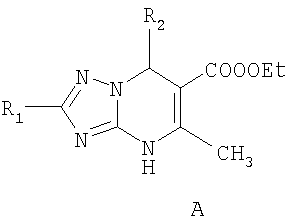
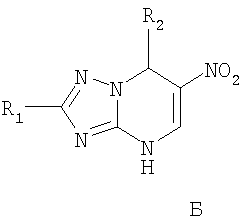
 ) и токсичность замещенных 7-арил(гетерил)-4,7-дигидро-1,2,4-три-азоло[1,5-а]пиримидинов (мыши) в сравнении с аналогами
) и токсичность замещенных 7-арил(гетерил)-4,7-дигидро-1,2,4-три-азоло[1,5-а]пиримидинов (мыши) в сравнении с аналогами