Патент на изобретение №2359975
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ АРАБИНОГАЛАКТАНОВ
(57) Реферат:
Изобретение относится к новым производным арабиногалактана, которые могут быть использованы в медицине, фармакологии. Описывается способ получения модифицированных арабиногалактанов окислением его первичных гидроксигрупп системой 2,2,6,6-тетраметилпиперидиний-1-оксил радикал-NaBr-NaClO-H2O при рН 10,2 до карбоксильных и последующей конъюгации карбоксигрупп окисленного арабиногалактана с аминосодержащими соединениями в присутствии конденсирующего агента 1-этил-3-[3-(диметиламино)пропил]карбодиимида в водной среде при комнатной температуре и рН 4,7-4,8. В качестве аминосодержащих соединений используют ряд фармакологически значимых аминов: п- и о-аминофенолы, 5- и 4-аминосалициловые, антраниловую и n-аминобензойную кислоты, этиловый эфир п-аминобензойной кислоты (анестезин), (3-диэтиламиноэтиловый эфир n-аминобензойной кислоты (новокаин), 1-фенил-2,3-диметил-4-аминопиразолон-5 (4-аминоантипирин), гидразид изоникотиновой кислоты (изониазид), сульфаниламидные препараты, такие как n-аминобензолсульфамид (стрептоцид), n-аминобензолсульфацетамид-натрий (сульфацил-натрий), 2-аминоэтансульфоновую кислоту (таурин), природные а-аминокислоты (глицин, лизин и др.), диамины (гидразин, этилендиамин) и дигидразиды (дигидразид адипиновой кислоты). Получают производные арабиногалактана, которые могут быть использованы в медицине и фармакологии. Конверсия карбоксигрупп в амидные окисленного арабиногалактана достигает 90-95%. 1 ил., 1 табл.
Изобретение относится к области химии, в частности к способу получения новых веществ – производных арабиногалактана, которые могут быть использованы в медицине, фармакологии.
Молекулы арабиногалактана состоят из основной цепи (1 3CN с поли-L-лизином был получен графт-сополимер арабиногалактана реакцией восстановительного аминирования между остатком восстанавливающего сахара в конце цепи арабиногалактана и Другие графт-сополимеры арабиногалактана получают привитой сополимеризацией с акриламидом и с последующей обработкой диметиламином и формальдегидом по реакции Манниха. Такие сополимеры применяют для улучшения обезвоживания и повышения прочности бумаги [Авт. св. Известны эфиры арабиногалактанов с коричной кислотой или ее производными, содержащими алкильные, аллильные, CN, Hal или NH2-группы; во многих случаях были модифицированы не менее 50% гидроксигрупп арабиногалактана [Заявка JP 60219202]. По гидроксильным группам арабиногалактанов получены конъюгаты с тиофенкарбоновыми кислотами (они могут быть полезны в качестве носителей, адсорбентов или смол [Заявка JP 60219201]) и некоторыми жирными кислотами (пальмитиновой, стеариновой и деканоевой) [Заявка US 2001036933]. Водорастворимые биосовместимые арабиногалактаны с липофильными заместителями могут применяться в качестве адьювантов, ингибиторов клеточной адгезии, инфекции или воспаления. Ряд производных арабиногалактана, проявляющих аффинность к асиалогликопротеиновым рецепторам, синтезирован с целью получения соединений с противовирусными, противовоспалительными, радиопротекторными свойствами [Пат. WO 9325239]. Арабиногалактан сначала был модифицирован гидразином или этилендиамином или конъюгирован с поли-L-лизином. По полученным свободным аминогруппам при помощи 1-этил-3-[3-(диметиламино)пропил]карбодиимида (КДИ) были присоединены антивирусные агенты аденозин-5′-монофосфат и аденин арабинозид-5′-монофосфат, а также противовоспалительный агент пепстатин. Фосфатные группы в фосфорилированном арабиногалактане были этерифицированы в присутствии КДИ S-2-(3-аминопропиламино)этилтиофосфорной кислотой, обладающей радиопротекторными свойствами [Пат. WO 9325239]. В природе встречаются кислые формы арабиногалактанов, содержащие в своем составе небольшой процент уроновых кислот. Арабиногалактаны с карбоксифункцией получают и синтетическим путем – этерификацией гидроксигрупп янтарным или глутаровым ангидридом или обработкой арабиногалактана диангидридом диэтилентриаминопентауксусной (DTPA) кислоты. Содержание карбоксигрупп в гемисукцинате арабиногалактана составило 1.96 милли-экв/г продукта, в эфире арабиногалактана с DTPA – 0.117 милли-экв/г. Карбоксиметил- и карбоксиэтиларабиногалактаны, полученные по реакции с бромуксусной и 2-бромпропионовой кислотами, содержали 5.2 и 1.3 милли-экв карбоксигрупп на грамм конечного продукта [Пат. WO 9325239].
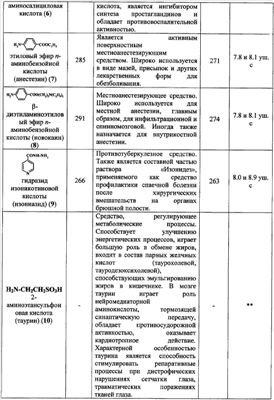
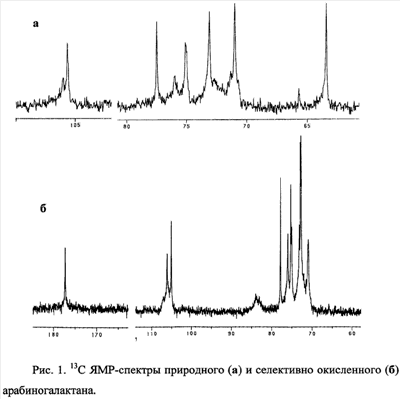
Селективным способом окисления первичной гидроксигруппы в полисахаридах (гиалуроновой кислоте, целлюлозе, хитине) является окисление системой 2,2,6,6-тетраметилпиперидиний-1-оксил радикал (ТЕМПО)-NaBr-NaClO-H2 Наиболее близким к предлагаемому изобретению является способ получения конъюгатов альгиновой кислоты с содержащими аминогруппу соединениями, в присутствии КДИ при комнатной температуре в водной среде (рН 4.7-4.8) [Пат. РФ Задачей предлагаемого изобретения является получение модифицированных арабиногалактанов. Это достигается следующим образом. Первичные гидроксигруппы арабиногалактана из лиственницы селективно окисляют до карбоксильных в системе 2,2,6,6-тетраметилпиперидиний-1-оксил радикал (ТЕМПО)-NaBr-NaClO-H2O (рН 10.2). Таким образом получают арабиногалактан, содержащий карбоксильные группы (АГ-СООН), которые затем в присутствии конденсирующего реагента КДИ вовлекают в реакцию с соединениями, содержащими первичную аминогруппу (RNH2). Реакцию проводят в водной среде (рН 4.7-4.8) при комнатной температуре в течение 20-30 мин при соотношении реагентов АГ-COOH:RNH2:КДИ = 1:2:1.5 или АГ-COOH:RNH2:КДИ = 1:5:1.5, если в качестве RNH2 используются Следует отметить, что по способу, предлагаемому в работе Jiang В. et al., гиалуроновая кислота была окислена по первичным гидроксигруппам не больше чем на ~80%. Арабиногалактан был окислен по первичным гидроксигруппам на 100%, что составляет 5.1 милли-экв карбоксигрупп на 1 г продукта АГ-СООН (в виде натриевой соли). Другими способами, приведенными в описании уровня техники, такой результат не получен. Высокое содержание уроновых кислот в структуре модифицированного арабиногалактана позволяет увеличить фармакологическую нагрузку на макромолекулу, что достигается эффективной карбодиимидной конъюгацией карбоксигрупп с аминами. Предлагаемое изобретение иллюстрируется следующими примерами. Пример 1. 2ОН-групп до карбоксильных подтверждается данными ИК-(по появлению интенсивного пика при 1600 см-1 для карбоксилат-аниона) и 13С ЯМР-спектроскопии. В 13С ЯМР-спектре окисленного арабиногалактана (АГ-СООН) в области 176-178 м.д. наблюдается появление группы сигналов, отвечающих атомам углерода карбоксильных групп окисленных остатков арабинозы и галактозы (арабинуроновой и галактуроновой кислот соответственно). При этом сигналы атомов углерода СН2ОН-групп в области 62-63 м.д. отсутствуют, что также свидетельствует о полной трансформации первичных гидроксигрупп арабиногалактана в карбоксильные (рис.1). б) К смеси 60 мг (~0.3 ммоль) АГ-СООН и 66.5 мг (0.6 ммоль) n-аминофенола (1) в 10 мл Н2О добавляют 0.1 н. NaOH (или, если требуется, 0.1 н. HCl) до рН 4.7-4.8, затем при интенсивном перемешивании и температуре 20-22°С вносят 86.3 мг (0.45 ммоль) карбодиимида (соотношение реагентов Ar-COOH:RNH2:КДИ=1:2:1.5), поддерживая рН 4.7-4.8 титрованием 0.1 н. НС1. Через 0.5 ч к охлажденной до 0°С реакционной смеси последовательно добавляют 0.1 н. NaOH (до рН 7-8), 2-3 мл насыщенного раствора NaCl и 30 мл охлажденного метанола. Выпавший осадок отделяют центрифугированием, растворяют в 10 мл 6% NaCl, добавляют 30 мл метанола. Вновь выпавший осадок центрифугируют, промывают метанолом (10×3 мл), затем эфиром (10×3 мл) и сушат при температуре Конверсию карбоксильных групп АГ-СООН в амидные определяют по данным 1Н-ЯМР-спектроскопии, используя интегральные интенсивности характеристических сигналов протонов остатков соответствующих аминов по отношению к внутреннему стандарту – интенсивности сигналов всех протонов исследуемого образца в области 3.25-4.50 м.д. Спектры 1Н-ЯМР регистрировали для растворов в D2O на спектрометре Bruker АМХ-300 (рабочая частота для 1Н-ЯМР-300.13 МГц), в качестве внутреннего стандарта использовали натриевую соль 3-(триметилсилил)-1-пропансульфоновой кислоты. УФ-спектры получали на спектрофотометре Specord M-40. Контроль рН растворов проводили с помощью рН-метра «рН-340». Примеры 2-13. Окисление арабиногалактана и реакцию полученного АГ-СООН с соответствующим амином (2-13) и очистку продуктов проводят аналогично примеру 1. Конверсия карбоксигрупп в амидные окисленного арабиногалактана достигает 90-95%. Примеры 14, 15. Окисление арабиногалактана и реакцию АГ-СООН с глицином (14), D,L-лизином (15) проводят аналогично примеру 1, но при соотношении реагентов АГ-СООН:RNH2:КДИ=1:5:1.5; при данном соотношении конверсия карбоксигрупп в амидные окисленного арабиногалактана достигает 90-95%. Очистку целевых конъюгатов проводят аналогично примеру 1. Некоторые спектральные характеристики конъюгатов (в сравнении с аминами) приведены в таблице.
Формула изобретения
Способ получения модифицированных арабиногалактанов, характеризующийся тем, что арабиногалактан окисляют в системе 2,2,6,6-тетраметилпиперидиний-1-оксил радикал-NaBr-NaClO-Н2О, рН 10.2, с получением содержащего карбоксильные группы арабиногалактана (АГ-СООН), который затем в водной среде при комнатной температуре, рН 4.7-4.8, в присутствии конденсирующего агента 1-этил-3-[3-(диметиламино)пропил]карбодиимида (КДИ) подвергают взаимодействию с содержащими первичную аминогруппу соединениями общей формулы RNH2, где
|
||||||||||||||||||||||||||

 1. С.27-37]. Лиственница западная (Larix occidentalis) и сибирская {Larix sibirica) являются коммерчески значимыми источниками арабиногалактана, который применяется в качестве эмульсификатора или стабилизатора при изготовлении некоторых пищевых продуктов. Высокомолекулярный арабиногалактан рекомендуется для применения в качестве иммуностимулирующего средства, активизирующего макрофаги [Заявка WO 2006082707], а в комплексе с солями железа – при железодефицитных анемиях [Пат. RU 2208440].
1. С.27-37]. Лиственница западная (Larix occidentalis) и сибирская {Larix sibirica) являются коммерчески значимыми источниками арабиногалактана, который применяется в качестве эмульсификатора или стабилизатора при изготовлении некоторых пищевых продуктов. Высокомолекулярный арабиногалактан рекомендуется для применения в качестве иммуностимулирующего средства, активизирующего макрофаги [Заявка WO 2006082707], а в комплексе с солями железа – при железодефицитных анемиях [Пат. RU 2208440]. 3) – связанных остатков D-галактозы с состоящими из L-арабинозы и D-галактозы (1
3) – связанных остатков D-галактозы с состоящими из L-арабинозы и D-галактозы (1
 -аминокислоты и их производные. В качестве аминосодержащих соединений используют фармакозначимые n- (1) и о-аминофенолы (2), n-аминобензойную (3) антраниловую (4), 4- (5) и 5-аминосалициловые (6) кислоты, этиловый эфир n-аминобензойной кислоты (анестезин) (7),
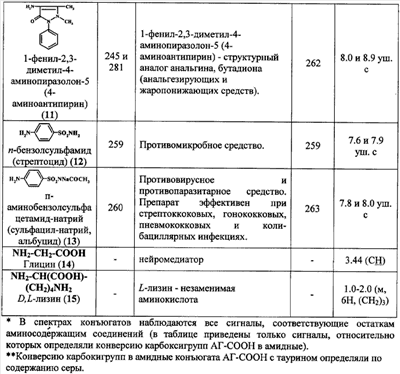
-аминокислоты и их производные. В качестве аминосодержащих соединений используют фармакозначимые n- (1) и о-аминофенолы (2), n-аминобензойную (3) антраниловую (4), 4- (5) и 5-аминосалициловые (6) кислоты, этиловый эфир n-аминобензойной кислоты (анестезин) (7),  -диэтиламиноэтиловый эфир n-аминобензойной кислоты (новокаин) (8), гидразид изоникотиновой кислоты (изониазид) (9), 2-аминоэтансульфоновую кислоту (таурин) (10), 1-фенил-2,3-диметил-4-аминопиразолон-5 (4-аминоантипирин) (11), а также сульфаниламидные препараты, содержащие свободную аминогруппу, такие как n-аминобензолсульфамид (стрептоцид) (12), n-аминобензолсульфацетамид-натрий (сульфацил-натрий) (13). Могут быть использованы и другие амины:
-диэтиламиноэтиловый эфир n-аминобензойной кислоты (новокаин) (8), гидразид изоникотиновой кислоты (изониазид) (9), 2-аминоэтансульфоновую кислоту (таурин) (10), 1-фенил-2,3-диметил-4-аминопиразолон-5 (4-аминоантипирин) (11), а также сульфаниламидные препараты, содержащие свободную аминогруппу, такие как n-аминобензолсульфамид (стрептоцид) (12), n-аминобензолсульфацетамид-натрий (сульфацил-натрий) (13). Могут быть использованы и другие амины: 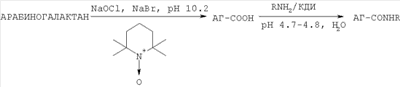
 60°С и пониженном давлении. Получают ~60 мг конъюгата в виде белого порошка. Конверсия карбоксигрупп в амидные в конъюгате с n-аминофенолом ~100%.
60°С и пониженном давлении. Получают ~60 мг конъюгата в виде белого порошка. Конверсия карбоксигрупп в амидные в конъюгате с n-аминофенолом ~100%.