Патент на изобретение №2359676
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ КОРРЕКЦИИ ПОСТЭВАКУАТОРНОГО СИНДРОМА У БОЛЬНЫХ С НАПРЯЖЕННЫМ ЗЛОКАЧЕСТВЕННЫМ АСЦИТОМ
(57) Реферат:
Изобретение относится к медицине, а именно к онкологии, хирургии и интенсивной терапии, и может быть использовано в качестве коррекции постэвакуаторного синдрома у больных с напряженным асцитом вследствие карциноматоза брюшины. Для этого пациенту производят удаление асцитической жидкости. Затем полученную асцитическую жидкость концентрируют и фильтруют с помощью гемодиализного фильтра, а затем концентрат фильтруют с помощью плазмофильтра. К полученному фильтрату добавляют гипохлорит натрия для окисления, цефазолин 2,0 г/л и преднизолон 90 мг/л с последующей реинфузией жидкости пациенту. Способ позволяет осуществлять эффективную коррекцию гиповолемических и гипопротеинемических расстройств у больных с данной патологией за счет введения аутоасцитической жидкости с максимально повышеной концентрацией белка с неизменным соотношением его фракций, сниженной концентрацией молекул средней массы и максимально удаленными атипичными клетками. 3 табл.
Изобретение относится к области медицины, в частности к абдоминальной хирургии и онкологии, и может быть использовано как адьювантный метод лечения больных с запущенными формами онкологических заболеваний органов брюшной полости, осложненных карциноматозом брюшины и напряженным малигнизированным асцитом.
Недостатками указанного способа являются отсутствие лечебной коррекции неизбежно развивающейся гиповолемии и гипопротеинемии, что ведет к значительному снижению качества жизни данной категории больных. Недостатком этого способа является высокая цена лекарственного средства. Цель изобретения – повысить эффективность лечения и качество жизни больных с карциноматозом брюшины и напряженным малигнизированным асцитом. Цель достигается путем экстракорпоральной концентрации, фильтрации и реинфузии асцитической жидкости, причем используют два вида специальных фильтров (гемодиализный и плазмофильтр) и в состав фильтрата добавляют гипохлорит натрия, цефазолин 2,0 г/л и преднизолон, в дозе 90 мг/л. Способ коррекции постэвакуаторного синдрома у больных с напряженным злокачественным асцитом состоит из четырех этапов и реализуется следующим образом. 1 этап. Этап забора асцитической жидкости. В асептических условиях под местной анестезией больному с напряженным асцитом выполняется лапароцентез общепринятым способом. Асцитическая жидкость эвакуируется в стерильную емкость. Помимо этого эвакуированная жидкость направляется на цитологическое, клиническое, бактериологическое и биохимическое исследования. 2 этап. Этап фильтрации с концентрированием асцитической жидкости заключается в концентрации забранной асцитической жидкости посредством гемодиализного фильтра. Асцитическая жидкость при помощи роликового насоса по системе магистралей поступает в гемодиализный фильтр, где происходит ее фильтрация и концентрирование. При этом концентрат поступает обратно в стерильную емкость, а безбелковый водный фильтрат в отдельный контейнер. Таким образом, к завершению этапа фильтрации происходит концентрирование асцитической жидкости в заданное количество раз. Однако полученный раствор остается с сохраненным клеточным составом, в котором присутствуют клетки крови, а также атипичные клетки. Поэтому нами предложено использование плазмофильтра, способного задерживать все клетки крови. 3 этап. Этап клеточной фильтрации асцитической жидкости заключается в фильтрации асцитической жидкости от клеток крови и атипичных клеток с помощью плазмофильтра. Полученный концентрат после второго этапа при помощи роликового насоса по системе магистралей поступает в плазмофильтр, где происходит его фильтрация. Клетки оседают в фильтре, а отфильтрованная жидкость поступает во вторую стерильную емкость. 4 этап. Этап качественной коррекции асцитической жидкости заключается в добавлении в полученный фильтрат окислителя (гипохлорит натрия), антибиотика (цефазолин) и глюкокортикоида (преднизолон). Добавление гипохлорита натрия позволяет снизить содержание в фильтрате молекул средней массы, провоспалительных цитокинов и других продуктов раковой интоксикации. Применение антибиотика снижает вероятность бактериального инфицирования, а введение глюкокортикоида предотвращает развитие возможных пирогенных реакций. Авторами установлено, после первого этапа фильтрации с заданными параметрами концентрация общего белка повышалась в заданное количество раз. Количество белка в удаляемой жидкости было низким и составляло примерно 5 г/л, что доказывает эффективность работы гемодиализного фильтра. Изменений в соотношениях фракций белков после всех этапов фильтрации выявлено не было. Изменения содержания в асцитической жидкости уровней креатинина, билирубина и мочевины были незначительны. При цитологическом исследовании асцитической жидкости до фильтрации, а также после второго этапа – фильтрации асцитической жидкости наблюдалось одинаковое большое количество эозинофилов, лимфоидных элементов, лейкоцитов, клеток мезотелия с реактивными изменениями, а также атипичные клетки. После третьего этапа, клеточной фильтрации, их количество в асцитической жидкости значительно уменьшалось до единичных клеток, что говорит об эффективности использования плазмофильтра. При бактериологическом исследовании как до фильтрации, так и после обоих этапов фильтрации роста микрофлоры выявлено не было. После четвертого этапа добавления в асцитическую жидкость окислителя, антибиотика и глюкокортикоида отмечалось снижение в асцитической жидкости концентрации молекул средней массы. Аллергических, пирогенных реакций и инфекционных осложнений у больных не наблюдалось. Таким образом, разработанный способ позволяет в стерильных условиях концентрировать асцитическую жидкость, повышая белковый состав в заданное количество раз с неизмененным соотношением фракций белка. Отфильтровывание атипичных клеток делает эту методику безопасной в отношении гематогенной генерализации опухоли, а удаление из концентрированной асцитической жидкости клеток крови, снижение концентрации молекул средней массы и добавление глюкокортикоида предотвращает возможные пирогенные реакции. Клиническая апробация и оценка эффективности реинфузии асцитической жидкости. Характеристика больных. Характеристика больных контрольной и основной групп в зависимости от локализации первичной опухоли, пола и возраста пациентов представлена в таблице 1. После выполнения лапароцентеза и эвакуации асцитической жидкости с целью коррекции развивавшегося постэвакуаторного синдрома больным основной группы проводили корректирующую инфузионную терапию, включавшую парентеральное введение плазмозамещающих растворов, назначали анальгетики. В качестве плазмозаменителей использовались кристаллоиды (0,9% раствор натрия хлорида) и коллоидные растворы (концентрированная асцитическая жидкость больного с добавлением гипохлорита натрия для окисления, цефазолина 2.0 г/л и преднизолона 90 мг/л) в объеме 400 и 500 мл в сутки соответственно. Длительность курса проводимой терапии составила 3 суток. Больным контрольной группы проводилась симптоматическая терапия (анальгетики).
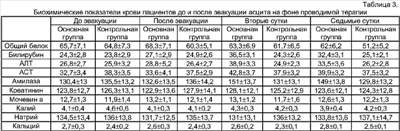
Основные гемодинамические параметры, показатели диуреза, содержания гемоглобина, эритроцитов и тромбоцитов в основной и контрольной группах больных представлены в таблице 2. Как видно из таблицы 1, до и непосредственно после эвакуации асцитической жидкости показатели гемодинамики, общего анализа крови и диуреза в основной и контрольной группах были практически одинаковыми. Во вторые сутки в контрольной группе у больных отмечались выраженные расстройства гемодинамики, вплоть до гиповолемического шока, гемоконцентрация, снижение диуреза. К седьмым суткам выраженность возникших нарушений несколько снизилась. Однако по-прежнему в сравнении с основной группой сохранялись гипотония и некоторое снижение диуреза. В основной группе на фоне проводимой инфузионной терапии в объеме 500 мл концентрата асцитической жидкости и 800 мл физиологического раствора в течение первых трех суток подобных изменений измеряемых показателей не отмечалось или они были менее выражены. Характеристика биохимических показателей крови основной и контрольной групп представлена в таблице 3. Как видно из таблицы 3, в контрольной группе больных в биохимическом анализе крови отмечалось постепенное снижение содержания общего белка с достижением минимального значения к седьмым суткам. В основной группе на фоне проводимой реинфузии концентрированной асцитической жидкости значимой гипопротеинемии не отмечалось. В то же время выявлялось некоторое увеличение общего билирубина и трансаминаз, вероятно обусловленное их повышенным содержанием в реинфузируемой жидкости. Аллергических, гиперпиретических реакций и инфекционных осложнений при проведении метода не было. Таким образом, проведение в постэвакуаторный период инфузионной терапии с использованием в качестве коллоидного плазмозамещающего раствора концентрированной асцитической жидкости позволяет предотвратить неизбежно возникающие после эвакуации асцита клинические проявления гиповолемии и развитие гипопротеинемии, максимально нарастающей к концу первой недели после выполнения лапароцентеза.
Формула изобретения
Способ коррекции гиповолемических и гипопротеинемических расстройств, развивающихся после эвакуации напряженного асцита у больных с карциноматозом брюшины, включающий удаление асцитической жидкости, ее концентрирование, фильтрацию и последующую реинфузию, отличающийся тем, что вначале полученную асцитическую жидкость концентрируют и фильтруют с помощью гемодиализного фильтра, а затем концентрат фильтруют с помощью плазмофильтра, к полученному фильтрату добавляют гипохлорит натрия для окисления, цефазолин 2,0 г/л и преднизолон 90 мг/л.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||