Патент на изобретение №2358974
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ ИМИДАЗО-ПИРИДИНА, ОБЛАДАЮЩИЕ СРОДСТВОМ К РЕЦЕПТОРУ МЕЛАНОКОРТИНА
(57) Реферат:
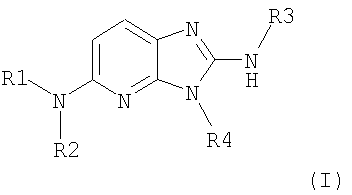
Описываются новые производные имидазо-пиридина общей формулы I
в рацемической, энантиомерной форме или в виде любой комбинации этих форм и их фармацевтически приемлемые соли. Значения радикалов R1-R4 приведены в описании. Данные соединения обладают сродством к рецептору меланокортина, что позволяет их использовать при получении лекарственных средств для лечения нарушений, связанных с массой тела, расстройств психики, боли, нарушений половой активности. Описывается также фармацевтическая композиция, содержащая новые соединения, и способ их получения. 4 н. и 1 з.п. ф-лы, 1 табл.
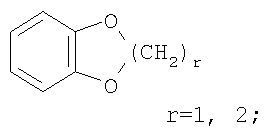
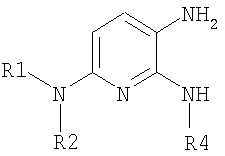
Объектом настоящего изобретения являются новые производные имидазо-пиридина. Эти продукты обладают высоким сродством к некоторым подтипам рецепторов меланокортинов, в частности к рецепторам МС4. Они представляют особый интерес для лечения патологических состояний и заболеваний, в которых участвует один или несколько рецепторов меланокортинов. Изобретение также относится к фармацевтическим композициям, содержащим указанные продукты, и к их применению для получения лекарственного средства. Меланокортины представляют собой группу пептидов, происходящих от одного предшественника, проопиомеланокортина (РОМС), и структурно близких друг к другу: адренокортикотропного гормона (АСТН), гормона, стимулирующего Действие меланокортинов опосредовано семейством особых мембранных рецепторов, имеющих семь трансмембранных доменов и связанных с белками G. На сегодняшний день клонировано и охарактеризовано пять подтипов рецепторов, названных МС1-МС5. Эти рецепторы различаются распределением в тканях и сродством к различным меланокортинам, причем рецепторы МС2 распознают только АСТН. Стимуляция рецепторов меланокортинов активирует аденилатциклазу и продукцию циклического АМФ. Хотя специфическая функциональная роль каждого из этих рецепторов выяснена не до конца, лечение патологических расстройств или заболеваний может быть связано со сродством к некоторым подтипам рецепторов. Так, активация рецепторов МС1 связана с лечением воспалений, тогда как их блокировка связана с лечением рака кожи. Лечение нарушений питания связано с рецепторами МС3 и МС4, лечение ожирения – за счет агонистов и лечение кахексии и анорексии – за счет антагонистов. Другими показаниями, связанными с активацией рецепторов МС3 и МС4 являются нарушения половой активности, невропатические боли, тревожные состояния, депрессия и наркомания. Активация рецепторов МС5 связана с лечением угрей и дерматозов. Усилия исследователей направлены, таким образом, на поиск непептидных низкомолекулярных соединений, обладающих биодоступностью при пероральном введении, которые являлись бы мощными агонистами или антагонистами рецепторов меланокортина. Заявитель обнаружил, что новые соединения общей формулы (I), приведенной ниже, обладают высоким сродством к рецепторам меланокортинов. Они действуют преимущественно на рецепторы МС4. Указанные соединения, являющиеся агонистами или антагонистами рецепторов меланокортинов, могут быть использованы для лечения патологических состояний или заболеваний обмена веществ, нервной системы или дерматологических, в которых участвуют один или несколько рецепторов меланокортинов, таких как, например, воспалительные состояния, нарушения энергетического гомеостаза, усвоения пищи, нарушения массы тела (ожирение, кахексия, анорексия), расстройства половой активности (нарушения эрекции), боль, в частности невропатическая боль. Можно также назвать психические расстройства (тревожные состояния, депрессия), наркоманию, кожные заболевания (угри, дерматозы, рак кожи, меланомы). Эти соединения также могут быть использованы для стимуляции регенерации нервов. Таким образом, объектом изобретения являются соединения общей формулы(I) в рацемической, энантиомерной форме или в виде любой комбинации этих форм, в которой: R1 и R2 обозначают, независимо, атом водорода; (C1-C8)алкил, который может быть замещен гидроксилом; (C2-C6)алкенил; бициклоалкил; или радикал формулы -(CH2)n-Х1 или -X-(CH2)n’-X’1; X обозначает -C(O)- или -C(S)-NH-; X1 обозначает (C1-C6)алкоксил, (C3-C7)циклоалкил, адамантил, гетероциклоалкил, арил или гетероарил, причем (C3-C7)циклоалкил, гетероциклоалкил, арил и гетероарил могут быть замещены одним или несколькими одинаковыми или разными заместителями, выбранными из -(CH2)n1-V1-Y1, галогена, нитрогруппы и цианогруппы; V1 обозначает -O-, -S- или ковалентную связь; Y1 обозначает (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами, или арил; n и n’ обозначают целое число от 0 до 6 и n1 – целое число от 0 до 2 (при условии, что когда n равно 0, тогда X1 не обозначает радикал алкоксил); X’1 обозначает атом водорода, (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами, (C3-C7)циклоалкил; или арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, цианогруппы, (C1-C6)алкилкарбонила, (C1-C6)алкила, который может быть замещен одним или несколькими одинаковыми или разными галогенами, и (C1-C6)алкоксила, который может быть замещен одним или несколькими одинаковыми или разными галогенами; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетеробициклоалкил или гетероциклоалкил, которые могут быть замещены одним или несколькими одинаковыми или разными заместителями, выбранными из гидроксила, (C1-C6)алкила, который может быть замещен гидроксилом, (C1-C6)алкоксикарбонила, -(CH2)n”-A, -C(O)-NV1‘Y1‘ и гетероциклоалкила; или R1 и R2 вместе образуют радикал формулы: V1‘ и Y1‘обозначают, независимо, атом водорода или (C1-C6)алкил; A обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, цианогруппы, (C1-C6)алкила, который может быть замещен одним или несколькими одинаковыми или разными галогенами, и (C1-C6)алкоксила, который может быть замещен одним или несколькими одинаковыми или разными галогенами; n” обозначает целое число от 0 до 2; R3 обозначает -Z3, -C(RZ3)(R’Z3)-Z3, -C(RZ3)(R’Z3)-(CH2)p-Z3 или -C(O)-Z’3; RZ3 и R’Z3 обозначают, независимо, атом водорода или (C1-C6)алкил; Z3 обозначает Z3a, Z3b, Z3c, Z3d, или Z3e; Z3a обозначает (C1-C6)алкил или (C2-C6)алкенил; Z3b обозначает (C1-C6)алкоксил, (C1-C6)алкилтио, (C1-C6)алкиламино или ди((C1-C6)алкил)амино; Z3c обозначает арил или гетероарил; причем арил и гетероарил могут быть замещены одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, цианогруппы, нитрогруппы, азидной группы, окси-радикала или -(CH2)p’-V3-Y3; V3 обозначает -O-, -S-, -C(O)-, -C(O)-O-, -O(CO)-, -SO2-, -SO2NH-, -NR’3-SO2-, -NR’3-, -NR’3-C(O)-, -C(O)-NR’3-, -NH-C(O)-NR’3– или ковалентную связь; Y3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, (C1-C6)алкила и (C1-C6)алкоксила; или арил-(C1-C6)-алкил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, (C1-C6)алкила и (C1-C6)алкоксила; Z3d обозначает (C1-C6)алкоксикарбонил, аминокарбонил, (C1-C6)алкиламинокарбонил, ди((C1-C6)алкил)аминокарбонил; Z3e обозначает (C1-C6)алкил-C(O)-NH-, (C3-C7)циклоалкил, гетероциклоалкил или радикал формулы причем (C3-C7)циклоалкил и гетероциклоалкил могут быть замещены одним или несколькими окси-радикалами или одинаковыми или разными (C1-C6)алкилами, Z’3 обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы и -(CH2)p”-V’3-Y’3; V’3 обозначает -O-, -C(O)-, -C(O)-O-, -C(O)-NR’3-, -NR’3-C(O)-, -NH-C(O)-NR’3 или ковалентную связь; Y’3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; R’3 обозначает атом водорода, (C1-C6)алкил или (C1-C6)алкоксил; p, p’ и p” обозначают, независимо, целое число от 0 до 6; R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом или аралкилом; гетероарил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода, (C1-C8)алкил; (C2-C6)алкенил; (C3-C7)циклоалкил, который может быть замещен одним или несколькими одинаковыми или разными (C1-C6)алкильными заместителями; циклогексен; гетероарил; арил, который может быть замещен одним или несколькими одинаковыми или разными радикалами, выбранными из -(CH2)s”-V4-Y4, галогена и нитрогруппы; V4 обозначает -O-, -S-, -NH-C(O)-, -NV4‘- или ковалентную связь; Y4 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; V4‘ обозначает атом водорода или (C1-C6)алкил; s” обозначает целое число от 0 до 4; или Z4 обозначает радикал формулы s и s’ обозначают, независимо, целое число от 0 до 6; или фармацевтически приемлемая соль этого соединения. В приведенных выше определениях выражение «галоген» обозначает фтор, хлор, бром или иод, предпочтительно хлор, фтор или бром. Выражение «алкил» (если не уточняется) предпочтительно обозначает алкил, содержащий от 1 до 6 атомов углерода, прямой или разветвленный, такой как метил, этил, пропил, изопропил, бутил, изобутил, втор.-бутил и трет.-бутил, пентил или амил, изопентил, неопентил, 2,2-диметил-пропил, гексил, изогексил или 1,2,2-триметил-пропил. Термин (C1-C8)алкил обозначает алкил, содержащий от 1 до 8 атомов углерода, прямой или разветвленный, такой как определенные выше, а также гептил, октил, 1,1,2,2-тетраметилпропил, 1,1,3,3-тетраметил-бутил. Под выражением «алкил, замещенный гидроксилом» следует понимать любую прямую или разветвленную алкильную цепь, содержащую гидроксил, расположенный по длине цепи; так, в случае цепи, содержащей 3 атома углерода и гидроксильный радикал, в качестве примера можно привести HO-(CH2)3-, CH3-CH(ОН)-CH2– и CH3-CH2-CH(OH)-. Под алкенилом, если не уточняется, понимают прямой или разветвленный алкил, содержащий от 1 до 6 атомов углерода и по меньшей мере одну ненасыщенную (двойную) связь, такой как, например, винил, аллил, пропенил, бутенил или пентенил. Термин «алкоксил» обозначает радикалы, в которых алкил является таким, как определено выше, такие как, например, метокси, этокси, пропилокси или изопропилокси, а прямой, вторичный или третичный бутокси, пентилокси. Термин «алкоксикарбонил» обозначает предпочтительно радикалы, в которых алкоксил является таким, как определено выше, например метоксикарбонил, этоксикарбонил. Термин «(C3-C7)циклоалкил» обозначает насыщенную углеродную моноциклическую систему, содержащую от 3 до 7 атомов углерода, предпочтительно циклопропильный, циклобутильный, циклопентильный, циклогексильный или циклогептильный циклы. Выражение «гетероциклоалкил» обозначает насыщенную моноциклическую или бициклическую конденсированную систему, содержащую от 2 до 9 атомов углерода и по меньшей мере один гетероатом. Этот радикал может содержать несколько одинаковых или разных гетероатомов. Предпочтительно гетероатомы выбирают из кислорода, серы или азота. В качестве примера гетероциклоалкила можно назвать циклы, содержащие по меньшей мере один атом азота, такие как пирролидин, имидазолидин, пиразолидин, изотиазолидин, тиазолидин, изоксазолидин, оксазолидин, пиперидин, пиперазин, азепан (азациклогептан), азациклооктан, диазепан, морфолин, декагидроизохинолин (или декагидрохинолин), а также циклы, не содержащие азот, такие как тетрагидрофуран или тетрагидротиофен. В качестве иллюстрации циклоалкила или гетероциклоалкила, замещенных окси-радикалом, можно назвать, например, пирролидинон и имидазолидинон. Термин «бициклоалкил» обозначает неконденсированную насыщенную бициклическую углеводородную систему, содержащую от 5 до 9 атомов углерода, такую как бициклогептан, например бицикло[2,2,1]гептан, или бицикло-октан, например бицикло[2,2,2]октан или бицикло [3,2,1]октан. Термин «гетеробициклоалкил» обозначает неконденсированную насыщенную бициклическую углеводородную систему, содержащую от 5 до 8 атомов углерода и по меньшей мере один гетероатом, выбранный из азота, кислорода или серы. В качестве примера гетеробициклоалкила можно назвать азабициклогептан и азабициклооктан, такие как 7-аза-бицикло[2,2,1]гептан, 2-аза-бицикло [2,2,2]октан или 6-аза-бицикло[3,2,1]октан. Выражение «арил» обозначает ароматический радикал, состоящий из одного цикла или нескольких конденсированных циклов, например фенил, нафтил, флуоренил или антрил. Выражение «гетероарил» обозначает ароматический радикал, состоящий из одного цикла или нескольких конденсированных циклов, где по меньшей мере один цикл содержит один или несколько одинаковых или разных гетероатомов, выбранных из серы, азота или кислорода. В качестве примера гетероарила можно назвать радикалы, содержащие по меньшей мере один атом азота, такие как пирролил, имидазолил, пиразолил, изотиазолил, тиазолил, изоксазолил, оксазолил, триазолил, тиадиазолил, пиридил, пиразинил, пиримидил, хинолил, изохинолил, хиноксалинил, индолил, дигидроиндолил, бензоксадиазолил, карбазолил, феноксазинил, а также радикалы, не содержащие атомов азота, такие как тиенил, бензотиенил, фурил, бензофурил, дибензофурил, дигидробензофурил, дибензотиенил, тиоксантенил или пиранил. Термин «аралкил (арилалкил)» предпочтительно обозначает радикалы, в которых арил и алкил являются такими, как определено выше, например бензил или фенетил. В качестве иллюстрации арила или гетероарила, замещенных окси-радикалом, можно назвать, например, флуоренон, акридон, ксантенон, бензотиенил-дион, антрахинон, тиоксантен, бензокумарин. Также в настоящей заявке радикал (CH2)i (целое число i может обозначать n, n’, n”, n1, p, p’, p”, s, s’ и s”, как они определены выше) обозначает прямую или разветвленную углеводородную цепь, содержащую i атомов углерода. Так, радикал -(CH2)3– может обозначать -CH2-CH2-CH2-, но также -CH(CH3)-CH2-, -CH2-CH(CH3)- или – C(CH3)2-. Также согласно настоящей заявке, когда какой-либо радикал имеет формулу -B-D-E, где D обозначает, например, -C(O)-NH-, это означает, что атом углерода в -C(O)-NH- связан с В, а атом азота – с E. Предпочтительно изобретение относится к соединению формулы I, определенной выше, отличающемуся тем, что R1 и R2 обозначают, независимо, атом водорода, (C1-C8) алкил, бициклоалкил или радикал формулы -(CH2)n-X1 или -X-(CH2)n’-X’1; X обозначает -C(O)- или -C(S)-NH-; X1 обозначает (C1-C6)алкоксил, (C3-C7)циклоалкил, который может быть замещен (C1-C6)алкилом, или гетероарил; X’1 обозначает атом водорода, (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами, (C3-C7)циклоалкил или арил, который может быть замещен (C1-C6)алкилкарбонилом; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетеробициклоалкил или гетероциклоалкил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из (C1-C6)алкила, (C1-C6)алкоксикарбонила и -(CH2)n”-A; A обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена и (C1-C6)алкила; n” обозначает целое число от 0 до 1; R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода, (C1-C8)алкил или арил, который может быть замещен одним или несколькими одинаковыми или разными радикалами, выбранными из -(CH2)s”-V4-Y4; V4 обозначает -O-; Y4 обозначает (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; s” обозначает целое число от 0 до 4; s и s’ обозначают, независимо, целое число от 1 до 4; или соль; или фармацевтически приемлемой соли этого соединения, и, в частности, соединение I отвечает по меньшей мере одной из следующих характеристик: циклоалкил выбран из циклопропила, циклобутила и циклогексила; бициклоалкил представляет собой бицикло[2,2,1]гептан; гетеробициклоалкил представляет собой 7-аза-бицикло [2,2,1]гептан; арил представляет собой фенил; гетероарил представляет собой фурил; гетероциклоалкил выбран из пиперидина, морфолина и пиперазина; или является фармацевтически приемлемой солью этого соединения. Также очень предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R1 и R2 обозначают, независимо, атом водорода, (C1-C8)алкил или радикал формулы -(CH2)n-X1 или -X-(CH2)n’-X’1; X обозначает -C(O)-; X1 обозначает (C3-C7)циклоалкил; X’1 обозначает атом водорода или (C3-C7)циклоалкил; n обозначает 0 или 1; n’ обозначает целое число от 0 до 5; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетероциклоалкил, который может быть замещен одним или несколькими одинаковыми или разными (C1-C6)алкильными заместителями; и, в частности, (C3-C7)циклоалкил, обозначаемый X1 и X’1, выбирают из циклопропила, циклобутила и циклогексила; и гетероциклоалкил, который образуют вместе R1 и R2, представляет собой пиперидиновый цикл; или к фармацевтически приемлемой соли этого соединения. Также очень предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода или (C1-C8)алкил; s и s’ обозначают, независимо, целое число от 2 до 4; и, в частности, гетероциклоалкил, обозначаемый R’4, выбирают из пиперидина и морфолина; или к фармацевтически приемлемой соли этого соединения. Также предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R3 обозначает -C(O)-Z’3; Z’3 обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена и -(CH2)p”-V’3-Y’3; V’3 обозначает -O- или ковалентную связь; Y’3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; p” обозначает целое число от 0 до 2; или к фармацевтически приемлемой соли этого соединения. Также предпочтительно изобретение относится к соединению формулы I как она определена выше, отличающемуся тем, что R3 обозначает -Z3, -C(RZ3)(R’Z3)-Z3 или -C(RZ3)(R’Z3)-(CH2)p-Z3; или к фармацевтически приемлемой соли этого соединения. Также очень предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R3 обозначает -Z3 и Z3 обозначает Z3b, Z3c или Z3e; и предпочтительно Z3 обозначает Z3c и Z3c обозначает арил, и, в частности, Z3c обозначает фенил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы или -(CH2)p’-V3-Y3; V3 обозначает -O-, -S-, -C(O)-, -C(O)-O-, -SO2NH-, -NR’3-C(O)-, -C(O)-NR’3– или ковалентную связь; R’3 обозначает атом водорода; Y3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; и, в частности, Z3c обозначает фенил, замещенный одним или несколькими одинаковыми или разными заместителями формулы -(CH2)p’-V3-Y3; V3 обозначает -C(O)-, -C(O)-O- или -C(O)-NR’3-; R’3 обозначает атом водорода; Y3 обозначает атом водорода или (C1-C6)алкил; или к фармацевтически приемлемой соли этого соединения. Также очень предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R3 обозначает -C(RZ3)(R’Z3)-Z3 и Z3 обозначает Z3d или Z3e; или к фармацевтически приемлемой соли этого соединения. Также очень предпочтительно изобретение относится к соединению формулы I, как она определена выше, отличающемуся тем, что R3 обозначает -C(RZ3)(R’Z3)-(CH2)p-Z3 и Z3 обозначает Z3с, Z3d или Z3e, и, в частности, Z3 обозначает Z3d или Z3e; Z3d обозначает (C1-C6)алкоксикарбонил или аминокарбонил; Z3e обозначает (C1-C6)алкил-C(O)-NH-, гетероциклоалкил, который может быть замещен окси-радикалом, или радикал формулы или к фармацевтически приемлемой соли этого соединения. В настоящей заявке, символ ->* соответствует месту присоединения радикала. Если место присоединения на радикале не показано, это означает, что присоединение происходит по одному из свободных мест на этом радикале, по которому оно возможно. В соответствии с определениями вариативных групп R1, R2, R3 и R4 соединения по изобретению могут быть получены в жидкой фазе согласно различным процедурам от А до Е, описанным ниже. А. Получение согласно реакционной схеме A: Как описано на схеме А, 2,6-дихлор-3-нитропиридин может быть обработан первичным амином в присутствии органического основания, такого как третичный амин, или неорганического основания, такого как карбонат калия или цезия, в апротонном неполярном растворителе, таком как толуол, при температуре, близкой к 20°C, в течение 3-18 часов с получением соединения (1). Хлорсодержащее производное (1) может вступать в реакцию с первичным или вторичным амином в присутствии органического основания, такого как третичный амин, или неорганического основания, такого как карбонат калия или цезия, в апротонном полярном растворителе, таком как ацетонитрил, диметилформамид или НМРА, при температуре 20-70°C в течение 2-18 часов с получением соединения (2). Нитрогруппу соединения (2) восстанавливают каталитическим гидрированием в присутствии 10% палладия на угле в инертном растворителе, таком как метанол, этанол, этилацетат, или в смеси этих растворителей при температуре 18-25°C в течение 2-8 часов с получением дианилина (3). Производное (3) затем обрабатывают изотиоцианатом в присутствии агента сочетания, на смоле в качестве носителя или без носителя, такого как диизопропилкарбодиимид или дициклогексилкарбодиимид, или N-циклогексилкарбодиимид-N-метилполистирольная смола, в инертном растворителе, таком как тетрагидрофуран, метиленхлорид или хлороформ, при температуре 20-70°C в течение 2-72 часов с получением производного (4). В альтернативном варианте производное (3) может быть обработано изотиоцианатом в инертном растворителе, таком как тетрагидрофуран, метиленхлорид, хлороформ или этанол, при температуре 20-80°C в течение 1-16 часов, после чего полученный тиокарбамид может быть обработана желтым оксидом ртути (II) в присутствии каталитического количества серы в полярном растворителе, таком как метанол или этанол, в течение 2-24 часов при температуре 20-80°C с получением (4). Пример A1: гидрохлорид 4-{[3-(3-аминопропил)-5-(диизобутиламино)-3H-имидазо[4,5-b]пиридин-2-ил]амино}-N-метилбензамида Стадия 1: трет.-бутил 3-[(6-хлор-3-нитропиридин-2-ил)амино]пропилкарбамат К 2,6-дихлор-3-нитропиридину (8 г, 1 экв.) в растворе в толуоле (150 мл) последовательно добавляют карбонат калия (5,4 г, 1,2 экв.) и трет.-бутил-N(2-аминопропил)карбамат (6,8 г, 1 экв.). После 6 часов перемешивания при температуре, близкой к 20°C, смесь концентрируют при пониженном давлении при 40°C, затем добавляют воду (80 мл) и дихлорметан (200 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного твердого вещества, осуществляемой путем флэш-хроматографии на силикагеле (элюент: гептан/этилацетат 7:3), получают целевое соединение в виде твердого вещества желтого цвета (11,4 г; выход 92%). SM/CL: MM рассчитанная=330,7; m/z=331,1 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 2: трет.-бутил 3-{[6-(диизобутиламино)-3-нитропиридин-2-ил]амино}пропилкарбамат К раствору трет.-бутил 3-[(6-хлор-3-нитропиридин-2-ил)амино]пропилкарбамата (2 г, 1 экв.) в ацетонитриле (100 мл) последовательно добавляют карбонат калия (1,31 г, 1,5 экв.) и диизобутиламин (981 мг, 1,2 экв.). Смесь нагревают с обратным холодильником в течение 5 часов, затем охлаждают до комнатной температуры и концентрируют при пониженном давлении при 40°C. Остаток помещают в дихлорметан (200 мл) и воду (90 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного остатка, осуществляемой путем флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 7:3 – 1:1), получают целевое соединение в виде масла желтого цвета (2,46 г; выход 95%). SM/CL: MM рассчитанная=437,6; m/z=438,3 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 3: трет.-бутил 3-[5-(диизобутиламино)-2-({4-[(метиламино)карбонил]фенил}амино)-3H-имидазо[4,5-b]пиридин-3-ил]пропилкарбамат В гемолизную пробирку, помещенную в автоклав, вводят трет.-бутил-3-{[6-(диизобутиламино)-3-нитропиридин-2-ил]амино}пропилкарбамат (63 мг) в растворе в смеси этилацетат/этанол 3:1 (1,5 мл), и 10% палладий на угле (7 мг). После 3 часов перемешивания в атмосфере водорода (3 бар) при температуре приблизительно 20°C смесь отфильтровывают через целит в гемолизную пробирку, содержащую раствор 4-изотиоцианато-N-метилбензамид (43 мг, 1,2 экв.) в тетрагидрофуране (1 мл). К полученному таким образом фильтрату добавляют N-циклогексилкарбодиимид-N-метил-полистирольную смолу (Novabiochem; загрузка 1,9 ммоль/г; 237 мг, 3 экв.). Смесь нагревают с обратным холодильником в течение 18 часов, охлаждают до комнатной температуры, затем фильтруют через стеклянный фильтр и концентрируют фильтрат при пониженном давлении при 40°C. В результате очистки остатка путем флэш-хроматографии на силикагеле (элюент: гептан/этилацетат от 1:1 до 100% этилацетата) получают целевое соединение (53 мг; выход 65%). SM/CL: MM рассчитанная=551,7; m/z=552,3 (MH+) ЯМР(1H, 400 МГц, ДМСО-d6): Стадия 4: гидрохлорид 4-{[3-(3-аминопропил)-5-(диизобутиламино)-3H-имидазо[4,5-b]пиридин-2-ил]амино}-N-метилбензамид К раствору трет.-бутил 3-[5-(диизобутиламино)-2-({4-[(метиламино)карбонил]фенил}амино)-3H-имидазо[4,5-b]пиридин-3-ил]пропилкарбамата (51 мг) в этилацетате (0,5 мл) добавляют раствор соляной кислоты в простом эфире (1н., 2 мл). После 2 часов перемешивания при температуре, близкой к 20°C, смесь фильтруют и полученное твердое вещество промывают простым этиловым эфиром и высушивают (50 мг; выход 95%). SM/CL: MM рассчитанная=451,6; m/z=452,3 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Пример A2: гидрохлорид 1-(4-{[5-(дибутиламино)-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-2-ил]амино}фенил)-этанона Стадия 1: 6-хлор-3-нитро-N-(3-пиперидин-1-илпропил) пиридин-2-амин К 2,6-дихлор-3-нитропиридин (500 мг, 1 экв.) в растворе в толуоле (10 мл) последовательно добавляют карбонат калия (540 мг, 1,5 экв.) и 3-пиперидино-пропиламин (420 мг, 1 экв.). После 2 часов перемешивания при температуре, близкой к 20°C, смесь концентрируют при пониженном давлении при 40°C, затем добавляют воду (20 мл) и дихлорметан (70 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного твердого вещества, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 3:7 до 100% этилацетата), получают целевое соединение в виде твердого вещества желтого цвета (473 мг; 61% выход). SM/CL: MM рассчитанная=298,8; m/z=299,1 (MH+) ЯМР (1H,400 МГц, ДМСО-d6): Стадия 2: N6,N6-дибутил-3-нитро-N2-(3-пиперидин-1-илпропил)пиридин-2,6-диамин К раствору 6-хлор-3-нитро-N-(3-пиперидин-1-илпропил)пиридин-2-амина (59 мг, 1 экв.) в ацетонитриле (3 мл) последовательно добавляют карбонат калия (54 мг, 2 экв.) и раствор дибутиламина (30 мг, 1,2 экв.) в ацетонитриле (2 мл). Смесь нагревают с обратным холодильником в течение 15 часов затем охлаждают до комнатной температуры и концентрируют при пониженном давлении при 40°C. Остаток помещают в дихлорметан (200 мл) и воду (90 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4 затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 1:1 до 100% этилацетата), получают целевое соединение (73 мг; выход 95%). SM/CL: MM рассчитанная=391,6; m/z=392,2 (MH+) Стадия 3: гидрохлорид 1-(4-{[5-(дибутиламино)-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-2-ил]амино}фенил)этанон В гемолизную пробирку, помещенную в автоклав, добавляют N6,N6-дибутил-3-нитро-N2-(3-пиперидин-1-илпропил)пиридин-2,6-диамин (70 мг) в растворе в смеси этилацетат/метанол 3:1 (2 мл) и палладий на угле 10% (7 мг). После 3 часов перемешивания в атмосфере водорода (3 бар) при температуре приблизительно 20°C смесь фильтруют через целит в гемолизную пробирку, содержащую раствор 4-изотиоцианато-N-метилбензамид (43 мг, 1,2 экв.) в тетрагидрофуране (1 мл). К полученному таким образом фильтрату добавляют N-циклогексилкарбодиимид-N-метил-полистирольную смолу (Novabiochem; загрузка 1,9 ммоль/г; 284 мг, 3 экв.). Смесь нагревают с обратным холодильником в течение 18 часов, охлаждают до комнатной температуры, затем фильтруют через стеклянный фильтр и фильтрат концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент: от 100% дихлорметана до дихлорметан/метанол 9:1), получают целевое соединение в виде основания. Соль соответствующего гидрохлорида образуют добавлением раствора 1н. соляной кислоты в простом этиловом эфире. Полученный осадок фильтруют и высушивают, получая целевое соединение (72 мг). SM/CL: MM рассчитанная=504,7; m/z=505,2 (MH+) ЯМР (lH, 400 МГц, ДМСО-d6): Получение изотиоцианатов, не выпускаемых промышленно: Первичный амин может быть превращен в изотиоцианат обработкой тиофосгеном в присутствии третичного основания, такого как триэтиламин, в апротонном растворителе, таком как дихлорметан или тетрагидрофуран, при температуре 0-20°C в течение 0,3-2 часов, или, в альтернативном варианте, обработкой дисульфидом углерода и циклогексилкарбодиимидом на носителе в виде смолы или без носителя в апротонном растворителе, таком как дихлорметан или тетрагидрофуран, при температуре 0-70°C в течение 0,3-15 часов. Получение 4-изотиоцианато-N-метилбензамида: К охлажденному до 0°C раствору 4-амино-N-метилбензамида (2 г, 1 экв.) и триэтиламина (5,6 мл, 3 экв.) в тетрагидрофуране (260 мл) по каплям добавляют тиофосген (1,13 мл, 1,1 экв.). Смесь перемешивают 30 мин при 0°C, затем удаляют холодную баню и продолжают перемешивание в течение еще 30 мин. В смесь добавляют воду (100 мл) и простой диэтиловый эфир (250 мл). После декантации и экстракции органические фазы объединяют, промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. Полученное твердое вещество перекристаллизуют в смеси дихлорметан/петролейный эфир (2,2 г; выход 86%). ЯМР (1Н, 400 МГц, ДМСО-d6): 2,77(д, 3Н), 7,51(АВ, 2Н), 7,88(АВ, 2Н), 8,52(м, 1Н). Согласно процедуре, аналогичной той, которая была описана для N-(4-изотиоцианатофенил)ацетамида, могут быть получены следующие изотиоцианаты: Получение N-(4-изотиоцианатофенил)-N’-метоксикарбамида: К охлажденному до 0°C раствору трет.-бутил-4-аминофенилкарбамата (1,04 г) в безводном дихлорметане (100 мл) добавляют карбонилдиимидазол (CDI) (1,62 г, 2 экв.). Температуру смеси доводят до 20°C и перемешивают при этой температуре в течение 15 часов. К охлажденной до 0°C реакционной среде последовательно добавляют триэтиламин (7 мл, 10 экв.), затем гидрохлорид O-метилгидроксиламина (4,2 г, 10 экв.). После 3 часов перемешивания при температуре, близкой к 20°C, к смеси добавляют воду, насыщенную гидрокарбонатом натрия и хлороформом. После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C, получая трет.-бутил-4-{[(метоксиамино)карбонил]амино}фенилкарбамат (1,33 г). Через суспензию этого производного в этилацетате пропускают ток газообразной соляной кислоты до полного завершения реакции. Полученный осадок фильтруют, затем промывают простым диэтиловым эфиром и высушивают, получая гидрохлорид N-(4-аминофенил)-N’-метоксикарбамида (1 г). К охлажденному до 0°C раствору гидрохлорида N-(4-аминофенил)-N-метоксикарбамида (1 г) и триэтиламина (3,2 мл, 5 экв.) в тетрагидрофуране (90 мл) по каплям добавляют тиофосген (0,38 мл, 1,1 экв.). Смесь перемешивают 15 мин при 0°C, затем добавляют воду и простой диэтиловый эфир. После декантации и экстракции органические фазы объединяют, промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 7:3 до 3:7), получают целевое соединение (630 мг ; выход 62%). ЯМР (1H, 400 МГц, ДМСО-d6): Получение ацил-изотиоцианатов, не выпускаемых промышленно: Ацил-изотиоцианаты могут быть получены, исходя из хлоргидридов соответствующих кислот, путем обработки тиоцианатом калия в апротонном растворителе, таком как ацетонитрил, при температуре 0-60°C в течение 0,2-5 часов. Метил-4-изотиоцианатокарбонилбензоат: К раствору метил-4-хлоркарбонилбензоата (2 г) в ацетонитриле (30 мл) добавляют тиоцианат калия (1,08 г, 1,1 экв.). После 1 часа перемешивания при приблизительно 20°C смесь фильтруют и фильтрат концентрируют при пониженном давлении при 40°C. Полученное твердое вещество очищают с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 1:1), получая целевое соединение (2,1 г; выход 95%). ЯМР (1H, 400 МГц, ДМСО-d6): Согласно процедуре, аналогичной той, которая была описана для метил-4-изотиоцианатокарбонилбензоата, могут быть получены следующие изотиоцианаты: Согласно реакционной схеме A и аналогично процедуре, описанной в отношении синтеза гидрохлорида 4-{[3-(3-аминопропил)-5-(диизобутиламино)-3H-имидазо[4,5-b]пиридин-2-ил]амино}-N-метилбензамида или гидрохлорида 1-(4-{[5-(дибутиламино)-3-(3-пиперидин-1-илпропил)-3Н-имидазо[4,5-b]пиридин-2-ил]амино}фенил)этанона, могут быть получены следующие соединения: в которых R1R2N обозначает один из следующих радикалов: R3 обозначает один из следующих радикалов:
1 или несколько заместителей, выбранных из: и R4 обозначает один из следующих радикалов: В. Получение согласно реакционной схеме B: Как описано в схеме В, производное (5), полученное согласно реакционной схеме А, может быть обработано органической или неорганической кислотой, такой как трифторуксусная кислота или соляная кислота (водная или в газообразной форме), в апротонном растворителе, таком как дихлорметан, простой диэтиловый эфир или этилацетат, при температуре 0-20°C в течение 0,5-5 часов с получением амина (6). Амин (6) может реагировать с альдегидом в протонном или апротонном растворителе, таком как дихлорметан, тетрагидрофуран или метанол, в течение 1-15 часов при температуре 0-50°C. Затем полученный имин восстанавливают in situ с помощью восстановителя на смоле в качестве носителя или без носителя предпочтительно с помощью триацетоксиборгидрида натрия, цианоборгидрида натрия или боргидрида на носителе (смоле), в присутствии или в отсутствие кислоты, такой как уксусная кислота, при температуре от 20 до 50°C в течение периода времени от 0,2 до 5 часов, с получением соединения (7). Вторичный амин (7) может в случае необходимости быть подвергнут второму восстанавливающему аминированию в тех же операционных условиях, как было описано перед этим для получения третичного амина (7′). Пример B1: 3-{2-[(4-метоксибензил)амино]этил}-N5,N5-бис(3-метилбутил)-N2-(3,4,5-триметоксифенил)-3H-имидазо[4,5-b]пиридин-2,5-диамин Стадия 1: трет.-бутил-2-[(6-хлор-3-нитропиридин-2-ил)амино]этилкарбамат К 2,6-дихлор-3-нитропиридину (10,2 г, 1 экв.) в растворе в толуоле (200 мл) последовательно добавляют карбонат калия (8,3 г, 1,2 экв.) и трет.-бутил-N(2-аминоэтил)карбамат (8 г, 1 экв.). После 4 часов перемешивания при температуре, близкой к 20°C, смесь концентрируют при пониженном давлении при 40°C, затем добавляют воду (130 мл) и дихлорметан (250 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного твердого вещества, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 7:3), получают целевое соединение в виде твердого вещества желтого цвета (12,5 г; выход 79%). SM/CL: MM рассчитанная=316,7; m/z=317,1 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 2: трет.-бутил-2-({6-[бис(3-метилбутил)амино]-3-нитропиридин-2-ил}амино)этилкарбамат К раствору трет.-бутил 2-[(6-хлор-3-нитропиридин-2-ил)амино]этилкарбамата (316 мг, 1 экв.) в ацетонитриле (10 мл) последовательно добавляют карбонат калия (207 мг, 1,5 экв.) и диизоамиламин (188 мг, 1,2 экв.). Смесь нагревают с обратным холодильником в течение 5 часов, затем охлаждают до комнатной температуры и концентрируют при пониженном давлении при 40°C. Остаток помещают в дихлорметан (50 мл) и воду (15 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 9:1 до 7:3), получают целевое соединение (430 мг; выход 98%). SM/CL: MM рассчитанная=437,6; m/z=438,3 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 4: трет.-бутил-2-{5-[бис(3-метилбутил)амино]-2-[(3,4,5-триметоксифенил)амино]-3N-имидазо[4,5-b]пиридин-3-ил}этилкарбамат В автоклав помещают трет.-бутил-2-({6-[бис(3-метилбутил)амино]-3-нитропиридин-2-ил}амино)этилкарбамат (400 мг, 1 экв.) в растворе в смеси этилацетат/этанол 2:1 (60 мл) и палладий на угле 10% (40 мг). После 5 часов перемешивания в атмосфере водорода (3 бар) при температуре приблизительно 20°C смесь фильтруют через целит в сосуд, содержащий 3,4,5-триметоксифенил-изотиоцианат (248 мг, 1,2 экв.). Фильтрат концентрируют при пониженном давлении при 40°C, затем остаток разбавляют тетрагидрофураном (50 мл) и добавляют N-циклогексилкарбодиимид-N-метил-полистирольную смолу (Novabiochem; загрузка 1,9 ммоль/г; 1,92 г, 4 экв.). Смесь нагревают с обратным холодильником в течение 8 часов, затем охлаждают до комнатной температуры и фильтруют через стеклянный фильтр. Фильтрат концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 9:1 до 6:4), получают целевое соединение (324 мг; выход 59%). SM/CL: MM рассчитанная=598,8; m/z=599,4 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 5: 3-(2-аминоэтил)-N5,N5-бис(3-метилбутил)-N2-(3,4,5-триметоксифенил)-3H-имидазо[4,5-b]пиридин-2,5-диамин К раствору трет.-бутил-2-{5-[бис(3-метилбутил)амино]-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамата (300 мг) в этилацетате (6 мл) добавляют раствор соляной кислоты в диоксане (4н., 3 мл). После 4 часов перемешивания при температуре, близкой к 20°C, смесь фильтруют. Полученное твердое вещество промывают простым диэтиловым эфиром. Полученный таким образом гидрохлорид помещают в дихлорметан и воду, насыщенную гидрокарбонатом натрия. После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C, получая целевое соединение в виде свободного основания (237 мг, выход 95%). SM/CL: MM рассчитанная=498,7; m/z=499,3 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 6: 3-{2-[(4-метоксибензил)амино]этил}-N5,N5-бис(3-метилбутил)-N2-(3,4,5-триметоксифенил)-3H-имидазо[4,5-b]пиридин-2,5-диамин Раствор 3-(2-аминоэтил)-N5,N5-бис(3-метилбутил)-N2-(3,4,5-триметоксифенил)-3H-имидазо[4,5-b]пиридин-2,5-диамина (83 мг, 1 экв.) и п-анизальдегида (25 мг, 1 экв.) в дихлорметане (1,5 мл) перемешивают 6 часов при температуре, близкой к 20°C. Смесь разбавляют метанолом (2 мл), затем добавляют триацетоксиборгидрид натрия (70 мг, 2 экв). После 0,5 часа перемешивания при температуре, близкой к 20°C, к смеси добавляют дихлорметан (20 мл) и воду, насыщенную гидрокарбонатом натрия (10 мл). После декантации и экстракции, объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 1:1 до 2:8), получают целевое соединение(70 мг, выход 68%). SM/CL: MM рассчитанная=618,8; m/z=619,4 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): C. Получение согласно реакционной схеме C: Соединения (7), в которых s=3, могут быть также получены согласно следующей схеме С: Как описано в схеме С, производное (8), полученное согласно реакционной схеме А, может быть обработано либо органической кислотой, такой как тозилат пиридиния или п-толуолсульфоновая кислота, в апротонном растворителе, таком как ацетон, в присутствии воды, при температуре 20-70°C в течение 2-12 часов, либо неорганической кислотой, такой как водная соляная кислота, в апротонном растворителе, таком как тетрагидрофуран, при температуре 0-20°C в течение 6-18 часов, с получением соединения (9). Альдегид (9) может быть затем обработан амином в протонном или апротонном растворителе, таком как дихлорметан, тетрагидрофуран или метанол, в течение 1-18 часов при температуре 20°C. Затем полученный имин восстанавливают in situ с помощью восстановителя, предпочтительно с помощью триацетоксиборгидрида натрия или цианоборгидрида натрия, в присутствии или в отсутствие кислоты, такой как уксусная кислота, при температуре от 20 до 50°C в течение периода времени от 0,2 до 6 часов, с получением соединения (10). Вторичный амин (10) может в случае необходимости быть подвергнут второму восстанавливающему аминированию в тех же операционных условиях, как было описано перед этим для получения третичного амина (10′). Согласно реакционной схеме B или C могут быть получены следующие соединения: в которой R1R2N обозначает один из следующих радикалов: R3 обозначает один из следующих радикалов: и R4 обозначает один из следующих радикалов: D. Получение согласно реакционной схеме D: Как описано в схеме D, хлорсодержащее производное (1), полученное согласно реакционной схеме А, может быть превращено в анилин (11), путем обработки трифторацетамидом в присутствии неорганического основания, такого как карбонат цезия или калия, и катализатора фазового переноса, такого как тетрабутиламмонийбромид, в апротонном полярном растворителе, таком как диметилформамид, при температуре 80-110°C в течение 2-6 часов. Анилин (11) может быть защищен в форме трифторацетамида путем обработки трифторуксусным ангидридом в присутствии третичного амина, такого как триэтиламин или пиридин, в апротонном растворителе, таком как дихлорметан, при температуре 0-20°C в течение 0,2-2 часов с получением соединения (12). Нитропроизводное (12) восстанавливают каталитическим гидрированием в присутствии 10% палладия на угле в инертном растворителе, таком как метанол, этанол, этилацетат, или в смеси этих растворителей, при температуре 18-25°C в течение 2-8 часов, получая дианилин (13). Производное (13) затем обрабатывают изотиоцианатом в присутствии агента сочетания на смоле в качестве носителя или без носителя, такого как диизопропилкарбодиимид или дициклогексилкарбодиимид, или N-циклогексилкарбодиимид-N-метилполистирольная смола, в инертном растворителе, таком как тетрагидрофуран, метиленхлорид или хлороформ, при температуре 20-70°C в течение 2-72 часов, получая производное (14). Трифторацетамид (14) гидролизуют в присутствии карбоната калия или натрия в протонном полярном растворителе, таком как метанол или этанол, в присутствии воды при температуре 50-80°C в течение 8-32 часов, получая анилин (15). Анилин (15) может вступать в реакцию с хлорангидридом кислоты в апротонном растворителе, таком как дихлорметан или тетрагидрофуран, в присутствии основания, такого как третичный амин на смоле в качестве носителя или без носителя, например триэтиламин или морфолинометилполистирольная смола, при температуре 0-40°C в течение 0,3-2 часов с получением амида (16). Анилин (15) может также вступать в реакцию с изотиоцианатом в апротонном растворителе, таком как тетрагидрофуран, при температуре 20-70°C в течение 5-24 часов с получением тиокарбамида (17). Пример D1: гидрохлорид N-{3-(2-аминоэтил)-2-[(3,4,5-триметоксифенил)амино]-3Н-имидазо[4,5-b]пиридин-5-ил}-2-пропилпентанамида Стадия 1: трет.-бутил-2[(6-амино-3-нитропиридин-2-ил)амино]этилкарбамат К раствору трет.-бутил-2[(6-хлор-3-нитропиридин-2-ил)амино]этилкарбамата, полученного согласно примеру В1 (2 г, 1 экв.) в диметилформамиде (100 мл), последовательно добавляют карбонат калия (0,87 мг, 1 экв.), тетрабутиламмонийбромид (0,2 г, 0,1 экв.) и трифторацетамид (1,4 г, 2 экв.). Смесь нагревают в течение 4 часов при 100°C, затем охлаждают до комнатной температуры и фильтруют через стеклянный фильтр. Фильтрат концентрируют при пониженном давлении при 40°C, затем к полученному остатку добавляют воду (40 мл) и дихлорметан (100 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного твердого вещества, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат 6:4), получают целевое соединение (1,21 г; выход 64%). SM/CL: MM рассчитанная=297,3; m/z=298,2 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 2: трет.-бутил-2-({3-нитро-6-[(трифторацетил)амино]пиридин-2-ил}амино)этилкарбамат К охлажденному до 0°C раствору трет.-бутил-2-[(6-амино-3-нитропиридин-2-ил)амино]этилкарбамата (840 мг, 1 экв.) в дихлорметане (25 мл) последовательно добавляют триэтиламин (0,59 мл), затем трифторуксусный ангидрид (0,56 мл). После 1 часа перемешивания при 0°C к смеси добавляют воду (10 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. Полученное твердое вещество желтого цвета перекристаллизуют в смеси дихлорметан/гептан и промывают простым диэтиловым эфиром (910 мг; выход 81%). ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 3: трет.-бутил 2-({3-амино-6-[(трифторацетил)амино]пиридин-2-ил}амино)этилкарбамат В автоклав загружают трет.-бутил-2-({3-нитро-6-[(трифторацетил)амино]пиридин-2-ил}амино)этилкарбамат (900 мг) в растворе в смеси этилацетат/этанол 2:1 (120 мл) и палладий на угле 10% (130 мг). После 15 часов перемешивания в атмосфере водорода (3 бар) при температуре приблизительно 20°C катализатор удаляют фильтрацией через целит и фильтрат концентрируют при пониженном давлении при 40°C, получая целевое соединение (820 мг; выход 98%). SM/CL: MM рассчитанная=363,3; m/z=364,2 (MH+) ЯМР (lH, 400 МГц, ДМСО-d6): Стадия 4: трет.-бутил-2-{5-[(трифторацетил)амино]-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамат К раствору трет.-бутил-2-({3-амино-6-[(трифторацетил)амино]пиридин-2-ил}амино)этилкарбамата (800 мг, 1 экв.) в тетрагидрофуране (50 мл) последовательно добавляют 3,4,5-триметоксифенилизотиоцианат (600 мг, 1,2 экв.) и N-циклогексилкарбодиимид-N-метил-полистирольную смолу (Novabiochem; загрузка 1,9 ммоль/г; 4,6 г, 4 экв.). Смесь нагревают с обратным холодильником в течение 24 часов, затем охлаждают до комнатной температуры и фильтруют через стеклянный фильтр. Фильтрат концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 6:4 до 3:7), получают целевое соединение в виде твердого вещества кремового цвета (750 мг; выход 62%). SM/CL: MM рассчитанная=554,5; m/z=555,2 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 5: трет.-бутил-2-{5-амино-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамат К трет.-бутил-2-{5-[(трифторацетил)амино]-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамату (470 мг, 1 экв.) в метаноле (32 мл) и воде (2 мл) добавляют карбонат калия (1,17 г, 10 экв.). Смесь нагревают с обратным холодильником в течение 26 часов, затем охлаждают до комнатной температуры и концентрируют при пониженном давлении при 40°C. Остаток дополняют водой (15 мл) и дихлорметаном (50 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C, получая целевое соединение (379 мг; выход 97%). SM/CL: MM рассчитанная=458,5; m/z=459,2 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 6: трет.-бутил-2-{5-[(2-пропилпентаноил)амино]-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамат К раствору трет.-бутил-2-{5-амино-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамата (37 мг, 1 экв.) в дихлорметане (2 мл) последовательно добавляют морфолинометилполистирол (Novabiochem; загрузка 3,64 ммоль/г; 33 мг, 1,5 экв.) и 2-пропилпентаноилхлорид (15 мг, 1,2 экв.). Смесь перемешивают 1 час при температуре, близкой к 20°C, затем фильтруют через стеклянный фильтр. Фильтрат концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 4:6 до 3:7), получают целевое соединение (34 мг; выход 73%). SM/CL: MM рассчитанная=584,7; m/z=585,3 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 7: гидрохлорид N-{3-(2-аминоэтил)-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-5-ил}-2-пропил-пентанамид К раствору трет.-бутил-2-{5-[(2-пропилпентаноил)амино]-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамата (30 мг) в этилацетате (1 мл) добавляют раствор соляной кислоты в диоксане (4н., 1 мл). После 1 часа перемешивания при температуре, близкой к 20°C, смесь концентрируют при пониженном давлении при 40°C. Полученное твердое вещество промывают простым этиловым эфиром и высушивают (29 мг, выход 97%). SM/CL: MM рассчитанная=485,2; m/z=484,6 (MH+) ЯМР (lH, 400 МГц, ДМСО-d6): Пример D2: N-{3-(2-аминоэтил)-2-[(3,4,5-триметокси-фенил)амино]-3H-имидазо[4,5-b]пиридин-5-ил}-N’-(втор.-бутил)тиокарбамид Стадия 1: трет.-бутил-2-{5-{[(втор.-бутил-амино)карбонотиоил]амино}-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b] пиридин-3-ил}этилкарбамат Раствор трет.-бутил-2-{5-амино-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамата, полученного согласно примеру Dl (37 мг, 1 экв.), и втор.-бутилизотиоцианата (20 мг, 2 экв.) в тетрагидрофуране (3 мл) нагревают с обратным холодильником в течение 17 часов, затем охлаждают до комнатной температуры и при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент:гептан/этилацетат от 4:6 до 3:7), получают целевое соединение (30 мг; выход 65%). SM/CL: MM рассчитанная=573,7; m/z=574,2 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 2: гидрохлорид N-{3-(2-аминоэтил)-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-5-ил}-N’-(втор.-бутил)тиокарбамида К раствору трет.-бутил-2-{5-{[(втор.-бутиламино)карбонотиоил]амино}-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-3-ил}этилкарбамата (22 мг) в этилацетате (1 мл) добавляют раствор соляной кислоты в диоксане (4н., 0,7 мл). После 1 часа перемешивания при температуре, близкой к 20°C, смесь концентрируют при пониженном давлении при 40°C. Полученное твердое вещество промывают простым этиловым эфиром и высушивают (20 мг, выход 91%). SM/CL: MM рассчитанная=473,6; m/z=474,2 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Согласно реакционной схеме D и следуя процедуре, описанной для гидрохлорида N-{3-(2-аминоэтил)-2-[(3,4,5-триметоксифенил)амино]-3H-имидазо[4,5-b]пиридин-5-ил}-2-пропилпентанамида, могут быть получены следующие соединения: в которых RlR2N обозначает один из следующих радикалов: R3 обозначает один из следующих радикалов: и R4 обозначает один из следующих радикалов: E. Получение согласно реакционной схеме E: Как описано в схеме E, хлорсодержащее производное (1), полученное согласно реакционной схеме A, может вступать в реакцию с первичным амином в присутствии органического основания, такого как третичный амин, или неорганического основания, такого как карбонат калия или цезия, в апротонном полярном растворителе, таком как ацетонитрил, диметилформамид или HMPA, при температуре 20-70°C в течение 2-18 часов, с получением соединения (18). Нитрогруппу соединения (18) восстанавливают каталитическим гидрированием в присутствии 10% палладия на угле в инертном растворителе, таком как метанол, этанол, этилацетат, или в смеси этих растворителей, при температуре 18-25°C в течение 2-8 часов, получая дианилин (19). Производное (19) затем обрабатывают изотиоцианатом в присутствии агента сочетания на смоле в качестве носителя или без носителя, такого как диизопропилкарбодиимид, или дициклогексилкарбодиимид, или N-циклогексилкарбодиимид-N-метил полистирольная смола, в инертном растворителе, таком как тетрагидрофуран, метиленхлорид или хлороформ, при температуре 20-70°C в течение 2-72 часов, получая производное (20). В альтернативном варианте производное (19) может быть обработано изотиоцианатом в инертном растворителе, таком как тетрагидрофуран, метиленхлорид, хлороформ или этанол, при температуре 20-80°C в течение 1-16 часов, затем полученный тиокарбамид может быть обработан желтым оксидом ртути (II) в присутствии каталитического количества серы в полярном растворителе, таком как метанол или этанол, в течение 2-24 часов при температуре 20-80°C, с получением соединения (20). Производное (20) может вступать в реакцию с хлорангидридом кислоты в апротонном растворителе, таком как дихлорметан или тетрагидрофуран, в присутствии основания, такого как третичный амин на смоле в качестве носителя или без носителя, такого как триэтиламин или морфолинометилполистирольная смола, при температуре 0-40°C в течение 0,3-2 часов с получением амида (21). Анилин (20) может также вступать в реакцию с изотиоцианатом в апротонном растворителе, таком как тетрагидрофуран, при температуре 20-70°C в течение 5-48 часов, с получением тиокарбамида (22). Пример E1: Гидрохлорид N-[2-[(4-ацетилфенил)амино]-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-5-ил]-N-бутилбутанамид Стадия 1: N6-бутил-3-нитро-N2-(3-пиперидин-1-илпропил)пиридин-2,6-диамин К раствору 6-хлор-3-нитро-N-(3-пиперидин-1-илпропил)пиридин-2-амина (1 г, 1 экв.; получен согласно примеру A2) в ацетонитриле (80 мл) последовательно добавляют карбонат калия (930 мг, 2 экв.) и раствор 1-бутиламина (300 мг, 1,2 экв.) в ацетонитриле (2 мл). Смесь нагревают с обратным холодильником в течение 15 часов, затем охлаждают до комнатной температуры и концентрируют при пониженном давлении при 40°C. Остаток помещают в дихлорметан (200 мл) и воду (90 мл). После декантации и экстракции объединенные органические фазы промывают рассолом, высушивают над Na2SO4, затем концентрируют при пониженном давлении при 40°C. В результате очистки полученного остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент: гептан/этилацетат от 9:1 до 100% этилацетата), получают целевое соединение (1,1 г; выход 98%). SM/CL: MM рассчитанная=335,4; m/z=336,4 (MH+) ЯМР (1H, 400 МГц, ДМСО-d6): Стадия 2: 1-(4-{[5-(бутиламино)-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-2-ил]амино}фенил)этанон В автоклав помещают N6-бутил-3-нитро-N2-(3-пиперидин-1-илпропил)пиридин-2,6-диамин (500 мг) в растворе в смеси этилацетат/этанол 3:1 (10 мл) и палладий на угле 10% (50 мг). После 3 часов перемешивания в атмосфере водорода (3 бар) при температуре приблизительно 20°C смесь фильтруют через целит в сосуд, содержащий раствор 4-ацетилфенил-изотиоцианата (270 мг, 1 экв.) в тетрагидрофуране (10 мл). К полученному таким образом фильтрату добавляют N-циклогексилкарбодиимид-N-метил- полистирольную смолу (Novabiochem; загрузка 1,9 ммоль/г; 2,63 г, 3 экв.). Смесь нагревают с обратным холодильником в течение 15 часов, охлаждают до комнатной температуры, затем фильтруют через стеклянный фильтр и фильтрат концентрируют при пониженном давлении при 40°C. В результате очистки остатка, осуществляемой с помощью флэш-хроматографии на силикагеле (элюент: от 100% дихлорметан до дихлорметан/метанол 9:1), получают целевое соединение (230 мг; выход 34%). SM/CL: MM рассчитанная=448,6; m/z=449,3 (MH+) Стадия 3: Гидрохлорид N-[2-[(4-ацетилфенил)амино]-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-5-ил]-N-бутилбутанамид К раствору 1-(4-{[5-(бутиламино)-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-2-ил]амино}фенил)этанона (54 мг) в безводном дихлорметане (1 мл) последовательно добавляют морфолинометиловую смолу (Novabiochem, загрузка=3,5 ммоль/г; 69 мг, 2 экв.) и бутирилхлорид (17 мг). После 30 минут перемешивания до комнатной температуры добавляют аминометилполистирольную смолу для улавливания избытка хлорангидрида кислоты. После 2 часов перемешивания при комнатной температуре смесь фильтруют и концентрируют при пониженном давлении при 40°C. Соль соответствующего гидрохлорида получают добавлением 1н. соляной кислоты в простом этиловом эфире. Полученный осадок фильтруют и высушивают, получая целевое соединение (68 мг). SM/CL: MM рассчитанная=518,7; m/z=519,4 (MH+) Согласно реакционной схеме E и в соответствии с процедурой, описанной для гидрохлорида N-[2-[(4-ацетилфенил)амино]-3-(3-пиперидин-1-илпропил)-3H-имидазо[4,5-b]пиридин-5-ил]-N-бутилбутанамида, могут быть получены следующие соединения: в которых R1R2N обозначает один из следующих радикалов: R3 обозначает один из следующих радикалов: и R4 обозначает один из следующих радикалов: Также объектом настоящего изобретения является способ получения соединения формулы (I), как она определена выше, отличающийся тем, что соединение общей формулы: в которой R1, R2, R4 имеют указанные выше значения, обрабатывают изотиоцианатом общей формулы R3N=C=S, в которой R3 имеет указанное выше значение, в присутствии агента сочетания или желтого оксида ртути (II) в присутствии серы в течение периода времени от 3 до 48 часов в протонном или апротонном растворителе при температуре от 50 до 80°C. Агент сочетания может находиться на носителе, как N-метилциклогексилкарбодиимид-N-метил полистирольная смола, или не иметь носителя, как диизопропилкарбодиимид, диэтилкарбодиимид или дициклогексилкарбодиимид. Можно использовать протонный растворитель, такой как метанол или этанол, или апротонный растворитель, такой как тетрагидрофуран или ацетонитрил. Также объектом изобретения является соединение общей формулы (II) в рацемической, энантиомерной форме или в виде любой комбинации этих форм и в которой: R1 и R2 обозначают, независимо, атом водорода, (C1-C8) алкил, который может быть замещен гидроксилом; (C2-C6)алкенилалкенил, бициклоалкил или радикал формулы -(СН2)n-X1 или -X-(CH2)n’-X’1; X обозначает -C(O)- или -C(S)-NH-; X1 обозначает (C1-C6)алкоксил, (C3-C7)циклоалкил, адамантил, гетероциклоалкил, арил или гетероарил, причем (C3-C7)циклоалкил, гетероциклоалкил, арил и гетероарил могут быть замещены одним или несколькими одинаковыми или разными заместителями, выбранными из -(CH2)n1-V1-Y1, галогена, нитрогруппы и цианогруппы; V1 обозначает -O-, -S- или ковалентную связь; Y1 обозначает (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами, или арил; n и n’ обозначают целое число от 0 до 6, а n1 – целое число от 0 до 2 (при условии, что когда n равно 0, тогда X1 не обозначает радикал алкоксил); X’1 обозначает атом водорода; (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; (C3-C7)циклоалкил; или арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, цианогруппы, (C1-C6)алкила, который может быть замещен одним или несколькими одинаковыми или разными галогенами, и (C1-C6)алкоксила, который может быть замещен одним или несколькими одинаковыми или разными галогенами; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетеробициклоалкил или гетероциклоалкил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из гидроксила, (C1-C6)алкила, (C1-C6)гидроксиалкила, (C1-C6)алкоксикарбонила, -(CH2)n”-A, -C(O)-NV1‘Y1‘ и гетероциклоалкила; или R1 и R2 вместе образуют радикал формулы: V1‘ и Y1‘ обозначают, независимо, атом водорода или (C1-C6)алкил; A обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, цианогруппы, (C1-C6)алкила, который может быть замещен одним или несколькими одинаковыми или разными галогенами, и (C1-C6)алкоксила, который может быть замещен одним или несколькими одинаковыми или разными галогенами; n” обозначает целое число от 0 до 2; R3 обозначает -(CH2)p-Z3 или -C(O)-Z’3; Z3 обозначает (C1-C6) алкил, (C2-C6)алкенилалкенил, (C1-C6)алкоксил, (C1-C6)алкоксикарбонил, (C1-C6)алкиламинокарбонил, (C3-C7)циклоалкил, гетероциклоалкил, арил или гетероарил, причем (C3-C7)циклоалкил и гетероциклоалкил могут быть замещены одним или несколькими одинаковыми или разными (C1-C6)алкилами, арил может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы, азидной группы или -(CH2)p’-V3-Y3; V3 обозначает -O-, -S-, -C(O)-, -C(O)-O-, -NH-C(O)-, -C(O)-NR’3-, -NH-C(O)-NR’3-, -NH-C(O)-NR’3-O- (в качестве иллюстрации предпочтительного варианта, не представленного в примерах) или ковалентную связь; Y3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; или Z3 обозначает радикал формулы Z’3 обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы и -(CH2)p”-V’3- Y’3; V’3 обозначает -O-, -C(O)-, -C(O)-O-, -C(O)-NR’3-, -NH-C(O)-, -NH-C(O)-NR’3- или ковалентную связь; Y’3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; R’3 обозначает атом водорода, (C1-C6)алкил или (C1-C6)алкоксил; p, p’ и p” обозначают, независимо, целое число от 0 до 4; R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом или аралкилом; гетероарил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода, (C1-C8)алкил, (C2-C6)алкенилалкенил; (C3-C7)циклоалкил, который может быть замещен одним или несколькими одинаковыми или разными (C1-C6)алкильными заместителями; циклогексен; гетероарил, арил, который может быть замещен одним или несколькими одинаковыми или разными радикалами, выбранными из -(CH2)s”-V4-Y4, галогена и нитрогруппы; V4 обозначает -O-, -S-, -NH-C(O)-, -NV4′- или ковалентную связь; Y4 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; V4′ обозначает атом водорода или (C1-C6)алкил; s” обозначает целое число от 0 до 4; или Z4 обозначает радикал формулы s и s’ обозначают, независимо, целое число от 0 до 6; или фармацевтически приемлемая соль этого соединения. Предпочтительно изобретение относится к соединениям формулы II, определенной выше, и в которой R1 и R2 обозначают, независимо, атом водорода, (C1-C8)алкил, бициклоалкил или радикал формулы -(СН2)n-Xl или -X-(CH2)n’-X’1; X обозначает -C(O)- или -C(S)-NH-; X1 обозначает (C1-C6)алкоксил, (C3-C7)циклоалкил или гетероарил, X’1 обозначает атом водорода; (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; (C3-C7)циклоалкил или арил; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетеробициклоалкил или гетероциклоалкил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из (C1-C6)алкила, (C1-C6)алкоксикарбонила и -(CH2)n”-A; A обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена и (C1-C6)алкила; n” обозначает целое число от 0 до 3; R3 обозначает -(CH2)p-Z3 или -C(O)-Z’3; Z3 обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена, нитрогруппы и -(CH2)p’-V3-Y3; V3 обозначает -O-, -S-, -C(O)-, -C(O)-O-, -NH-C(O)-, -C(O)-NR’3- или ковалентную связь; Y3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; или Z3 обозначает радикал формулы Z’3 обозначает арил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из галогена и -(CH2)p”-V’3- Y’3; V’3 обозначает -O- или ковалентную связь; Y’3 обозначает атом водорода или (C1-C6)алкил; R’3 обозначает атом водорода; p, p’ и p” обозначают, независимо, целое число от 0 до 4; R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода, (C1-C8)алкил или арил, который может быть замещен одним или несколькими одинаковыми или разными радикалами, выбранными из -(CH2)s”-V4-Y4; V4 обозначает -O-; Y4 обозначает (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; s” обозначает целое число от 0 до 4; s и s’ обозначают, независимо, целое число от 0 до 6; или фармацевтически приемлемая соль этого соединения, и, в частности, циклоалкил выбирают из циклопропила и циклогексила; и/или бициклоалкил представляет собой бицикло[2,2,1]гептан, и/или гетероарил представляет собой фурил, и/или арил представляет собой фенил, и/или гетеробициклоалкил представляет собой 7-аза-бицикло[2,2,1]-гептан, и/или гетероциклоалкил выбирают из пиперидина и пиперазина. Также очень предпочтительно изобретение относится к соединениям формулы II, определенной выше, и в которой R1 и R2 обозначают, независимо, атом водорода, (C1-C8)алкил или радикал формулы -(СН2)n-Xl; X1 обозначает (C3-C7) циклоалкил, в частности циклопропил или циклогексил; или R1 и R2 образуют вместе с атомом азота, с которым они связаны, гетероциклоалкил, который может быть замещен одним или несколькими одинаковыми или разными (С1-С6)алкильными заместителями; и/или R3 обозначает -(CH2)p-Z3; Z3 обозначает (C1-C6) алкоксикарбонил, (C1-C6)алкиламинокарбонил или фенил, который может быть замещен одним или несколькими одинаковыми или разными заместителями, выбранными из нитрогруппы и -(CH2)p’-V3-Y3; V3 обозначает -O-, -C(O)-, -C(O)-O-, -NH-C(O)-, -C(O)-NR’3, -NH-C(O)-NR’3-, -NH-C(O)-NR’3-O-; Y3 обозначает атом водорода или (C1-C6)алкил, который может быть замещен одним или несколькими одинаковыми или разными галогенами; R’3 обозначает атом водорода; р и p’ обозначают, независимо, целое число от 0 до 4; и/или R4 обозначает радикал формулы -(CH2)s-R’4; R’4 обозначает гетероциклоалкил, содержащий по меньшей мере один атом азота и который может быть замещен (C1-C6)алкилом; или радикал формулы -NW4W’4; W4 обозначает атом водорода или (C1-C8)алкил; W’4 обозначает радикал формулы -(CH2)s’-Z4; Z4 обозначает атом водорода, (C1-C8)алкил, (C3-C7)циклоалкил; s и s’ обозначают, независимо, целое число от 0 до 6; и, в частности, циклоалкил выбирают из циклопропила и циклогексила и/или гетероциклоалкил выбирают из пирролидина, пиперидина, морфолина, пиперазина; или к фармацевтически приемлемой соли этого соединения. Соединения I и II по изобретению обладают интересными фармакологическими свойствами. Так, обнаружено, что соединения I по настоящему изобретению обладают высоким сродством к некоторым подтипам рецепторов меланокортинов, в частности к рецепторам МС4. Соединения согласно настоящему изобретению могут, таким образом, быть использованы для различных терапевтических применений. Предпочтительно они могут быть использованы для лечения патологических состояний или заболеваний, в которых участвуют один или несколько рецепторов меланокортинов, таких как состояния воспаления, нарушения, связанные с массой тела (ожирение, кахексия, анорексия), нарушения половой активности (нарушения эрекции), боль, а также расстройства психики (тревожные состояния, депрессия), наркомания, кожные заболевания (акне, дерматозы, меланомы). Далее, в экспериментальной части, имеется демонстрация фармакологических свойств соединений по изобретению. Объектом настоящей заявки также являются фармацевтические композиции, содержащие в качестве действующего начала по меньшей мере один продукт формулы I, как она определена выше, а также фармацевтически приемлемые соли указанного продукта формулы I, в комбинации с фармацевтически приемлемым носителем. Под фармацевтически приемлемой солью понимают, в частности, соли присоединения с неорганическими кислотами, такие как гидрохлорид, гидробромид, гидроиодид, сульфат, фосфат, дифосфат и нитрат, или с органическими кислотами, такие как ацетат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, п-толуолсульфонат, памоат и стеарат. В рамки настоящего изобретения также входят, при условии их применимости, соли, образованные с основаниями, такие как гидроксид натрия или калия. В отношении других примеров фармацевтически приемлемых солей можно обратиться к “Salt selection for basic drugs”, Int.J. Pharm.(1986), 33,201-217. Объектом настоящей заявки также является применение соединений согласно настоящему изобретению для получения лекарственного средства для лечения нарушений, связанных с массой тела, таких как ожирение, кахексия, в частности кахексия раковых патологий, кахексия СПИДа, кахексия лиц пожилого возраста, сердечная кахексия, почечная кахексия, кахексия ревматоидного артрита, и анорексия, для лечения боли, в частности невропатической боли, лечения расстройств психики, таких как тревожные состояния и депрессия, лечения нарушений половой активности, таких как нарушения эрекции. Фармацевтическая композиция может находиться в твердой форме, например в форме порошков, гранул, таблеток, желатиновых капсул или суппозиториев. Подходящими твердыми носителями могут быть, например, фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза натрия, поливинилпирролидин и воск. Фармацевтические композиции, содержащие соединение по изобретению, могут также находиться в жидкой форме, например в форме растворов, эмульсий, суспензий или сиропов. Подходящими жидкими носителями могут быть, например, вода, органические растворители, такие как глицерин или гликоли, а также их смеси в различных пропорциях в воде, с добавлением фармацевтически приемлемых масел или жиров. Жидкие стерильные композиции могут быть использованы для внутримышечных, внутрибрюшинных или подкожных инъекций, а также стерильные композиции могут вводиться внутривенно. Все технические и научные термины, используемые в настоящем тексте, имеют значения, известные специалисту. Кроме того, все патенты (или заявки на патент), а также другие библиографические источники включены в настоящий текст путем ссылки. Экспериментальная часть: Соединения по изобретению, полученные согласно процедурам, описанным выше в примерах А, В, С, D и Е, сведены в нижеследующую таблицу. Соединения охарактеризовывались по их времени удержания (tr) и молекулярному пику, определяемому масс-спектрометрией (МН+). Для масс-спектрометрии использовали простой четырехполюсный масс-спектрометр (Micromass, модель Platform), оснащенный источником electrospray, с разрешением 0,8 Да при точке минимума 50%. Калибровку проводят ежемесячно между массами 80 и 1000 Да с помощью калибрующей смеси иодида натрия и иодида рубидия в растворе в смеси изопропанол/вода (1/1 об.). Для жидкостной хроматографии используют систему Waters, включающую рядный дегазатор, четырехкомпонентный насос Waters 600, планшетный инъектор Gilson 233 и УФ-детектор Waters PAD 996. Использовали следующие условия элюирования: Элюент A вода + 0,04% трифторуксусной кислоты B ацетонитрил
Расход: 1 мл/мин Впрыск:10 мкл Колонка: Uptisphere ODS 3 мкм 75*4,6 мм i.d Эти примеры представлены для демонстрации вышеописанных процедур и ни в коем случае не должны рассматриваться как ограничивающие рамки изобретения. Фармакологическое исследование Сродство соединений согласно настоящему изобретению к различным подтипам рецепторов меланокортинов было измерено согласно процедурам, аналогичным тем, которые описаны далее в отношении рецепторов МС4. Исследование сродства соединений к рецепторам МС4 меланокортинов: Сродство соединений по изобретению к рецепторам МС4 определяли на основании измерения ингибирования связывания [l25I]-[Nle4, D-Phe7]- Клетки CHO-K1, стабильно экспрессирующие человеческие рецепторы МС4, культивируют в среде RPMI 1640, содержащей 10% зародышевой телячьей сыворотки, 2 мМ глутамина, 100 ед./мл пенициллина, 0,1 мг/мл стрептомицина и 0,5 мг/мл G418. Клетки собирают с помощью 0,5 мМ ЭДТУ и центрифугируют при 500 g в течение 5 мин при 4°C. Осадок ресуспендируют в солевой среде с фосфатным буфером (PBS) и центрифугируют при 500 g в течение 5 мин при 4°C. Осадок ресуспендируют в буферной среде Tris 50 мМ, рН 7,4 и центрифугируют при 500 g в течение 5 мин при 4°C. Клетки лизируют обработкой ультразвуком и центрифугируют при 39000 g в течение 10 мин при 4°C. Осадок ресуспендируют в буферной среде Tris 50 мМ, рН 7,4 и центрифугируют при 50000 g в течение 10 мин при 4°C. Мембраны, полученные в этом последнем осадке, хранят при -80°C. Измерение конкурентного ингибирования связывания [l25I]-[Nle4, D-Phe7]- Связанный [l25I]-[Nle4, D-Phe7]- Специфическое связывание получают путем вычитания неспецифического связывания (определяемого в присутствии 0,1 мкМ Nle4, D-Phe7– Агонистическую или антагонистическую активность соединений согласно настоящему изобретению в отношении рецепторов МС4 определяли путем измерения продукции циклического АМФ клетками СНО-К1, трансфицированными рецепторами МС4. Измерение продукции внутриклеточного циклического АМФ с помощью рецепторов МС4: Клетки СНО-К1, экспрессирующие рецепторы МС4 меланокортинов, культивируют на 384-лунковых планшетах в среде RPMI 1640 с 10% зародышевой телячьей сыворотки и 0,5 мг/мл G418. Клетки промывали дважды, используя 50 мкл среды RPMI, содержащей 0,2% BSA и 0,5 мМ 3-изобутил-1-метилксантина (IBMX). Для измерения агонистического действия соединения клетки инкубировали в течение 5 мин при 37°C в присутствии 0,5 мМ IBMX, затем стимулировали продукцию циклического АМФ путем добавления соединения в концентрациях от 1 пМ до 10 мкМ дважды в течение 20 мин при 37°C. Антагонистическое действие соединения измеряли путем одновременного добавления Nle4,D-Phe7– Реакционную среду удаляли и добавляли 80 мкл лизирующего буфера. Уровень внутриклеточного циклического АМФ измеряли с помощью конкурентного теста с использованием флуоресцентного циклического АМФ (CatchPoint, Molecular Devices).
Формула изобретения
1. Соединение общей формулы (I) 2. Соединение по п.1, отличающееся тем, что 3. Соединение по п.2, отличающееся тем, что оно отвечает по меньшей мере одной из следующих характеристик: 4. Соединение по п.1, отличающееся тем, что 5. Соединение по п.4, отличающееся тем, что (С3-С7)циклоалкил, обозначаемый X1 и Х’1 выбирают из циклопропила, циклобутила и циклогексила; и гетероциклоалкил, который образуют вместе R1 и R2, представляет собой пиперидиновый цикл; или фармацевтически приемлемая соль этого соединения. 6. Соединение по п.1, отличающееся тем, что 7. Соединение по п.6, отличающееся тем, что гетероциклоалкил, обозначаемый R’4, выбирают из: пиперидина и морфолина; или фармацевтически приемлемая соль этого соединения. 8. Соединение по п.1, отличающееся тем, что R3 обозначает -C(O)-Z’3; 9. Соединение по п.1, отличающееся тем, что R3 обозначает -Z3 или -C(RZ3)(R’Z3)-(CH2)p-Z3; или фармацевтически приемлемая соль этого соединения. 10. Соединение по п.9, отличающееся тем, что R3 обозначает -Z3; или фармацевтически приемлемая соль этого соединения. 11. Соединение по п.10, отличающееся тем, что Z3 обозначает арил; или фармацевтически приемлемая соль этого соединения. 12. Соединение по п.11, отличающееся тем, что Z3 обозначает фенил, замещенный одним или несколькими одинаковыми или разными заместителями, выбранными из: галогена, нитрогруппы или -(СН2)p’-V3-Y3; 13. Соединение по п.11, отличающееся тем, что Z3 обозначает фенил, замещенный одним или несколькими одинаковыми или разными заместителями формулы 14. Соединение по п.9, отличающееся тем, что R3 обозначает 15. Соединение по п.14, отличающееся тем, что Z3 обозначает (С1-С6)алкоксикарбонил, аминокарбонил; (С1-С6)алкил-С(O)-NH-, гетероциклоалкил, который может быть замещен окси-радикалом, или радикал формулы 16. Способ получения соединения формулы (I) по одному из пп.1-15, отличающийся тем, что соединение общей формулы: 17. Фармацевтическая композиция, обладающая сродством к рецептору меланокортина МС4, содержащая в качестве действующего начала по меньшей мере одно соединение по одному из пп.1-15 в комбинации с фармацевтически приемлемым носителем. 18. Применение соединения по одному из пп.1-15 для получения лекарственного средства для лечения нарушений, связанных с массой тела, расстройств психики, боли, нарушений половой активности. 19. Применение соединения по п.18 для получения лекарственного средства для лечения нарушений, связанных с массой тела, таких как ожирение, кахексия и, в частности кахексия раковых патологий, кахексия СПИДа, кахексия лиц пожилого возраста, сердечная кахексия, почечная кахексия, кахексия ревматоидного артрита, и анорексия. 20. Применение соединения по п.18 для получения лекарственного средства для лечения расстройств психики, таких как тревожные состояния и депрессия. 21. Применение соединения по п.18 для получения лекарственного средства для лечения боли и, в частности невропатической боли.
PD4A – Изменение наименования обладателя патента СССР или патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Адрес для переписки:
Извещение опубликовано: 27.04.2010 БИ: 12/2010
|
||||||||||||||||||||||||||

 -меланоциты (
-меланоциты ( – MSH и
– MSH и  -MSH (Eipper B.A. et Mains R.E., Endocr. Rev. 1980, 1, 1-27). Меланокортины осуществляют большое число физиологических функций. Они стимулируют синтез стероидов в коре надпочечников и синтез эумеланина в меланоцитах. Они регулируют усвоение питательных веществ, энергетический метаболизм, половую функцию, регенерацию нейронов, кровяное давление и частоту сердечных сокращений, а также восприятие боли, познавательную функцию, внимание и память. Меланокортины также обладают противовоспалительными и жаропонижающими свойствами и регулируют секрецию многих эндокринных или экзокринных желез, таких как сальные, слезные, молочные железы, предстательная железа и поджелудочная железа (Wikberg S.E. et al. Pharmacol. Res. 2000, 42, 393-420; Abdel-Malek Z.A., Cell. Mol. Life. Sci. 2001, 58, 434-441).
-MSH (Eipper B.A. et Mains R.E., Endocr. Rev. 1980, 1, 1-27). Меланокортины осуществляют большое число физиологических функций. Они стимулируют синтез стероидов в коре надпочечников и синтез эумеланина в меланоцитах. Они регулируют усвоение питательных веществ, энергетический метаболизм, половую функцию, регенерацию нейронов, кровяное давление и частоту сердечных сокращений, а также восприятие боли, познавательную функцию, внимание и память. Меланокортины также обладают противовоспалительными и жаропонижающими свойствами и регулируют секрецию многих эндокринных или экзокринных желез, таких как сальные, слезные, молочные железы, предстательная железа и поджелудочная железа (Wikberg S.E. et al. Pharmacol. Res. 2000, 42, 393-420; Abdel-Malek Z.A., Cell. Mol. Life. Sci. 2001, 58, 434-441).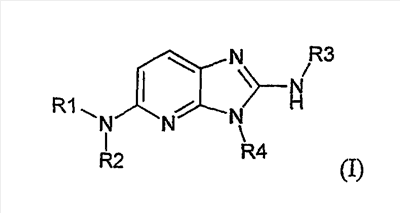
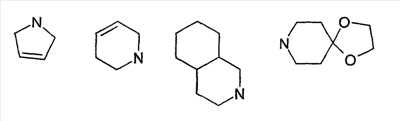
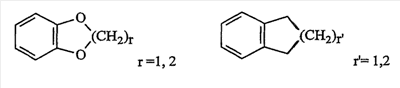
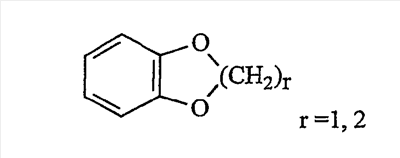
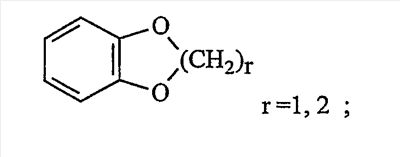
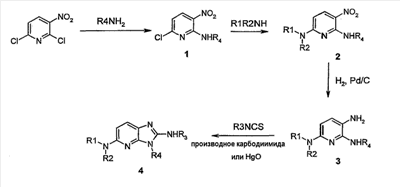
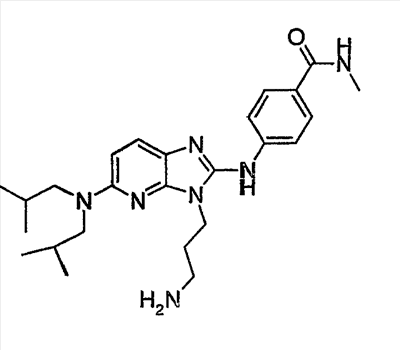
 1,36(с, 9H), 1,68(м, 2H), 2,99(дд, 2H), 3,51(дд, 2H), 6,76(д, 1H), 6,86(т, 1H), 8,41(д, 1H), 8,75(т, 1H).
1,36(с, 9H), 1,68(м, 2H), 2,99(дд, 2H), 3,51(дд, 2H), 6,76(д, 1H), 6,86(т, 1H), 8,41(д, 1H), 8,75(т, 1H).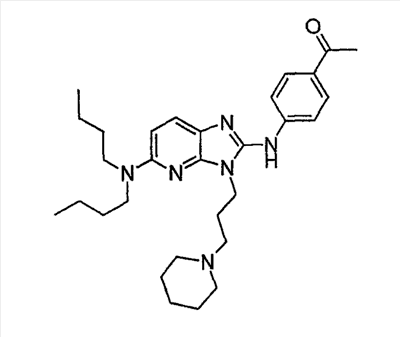
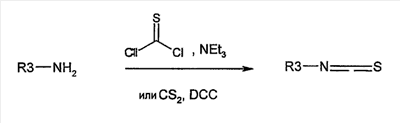
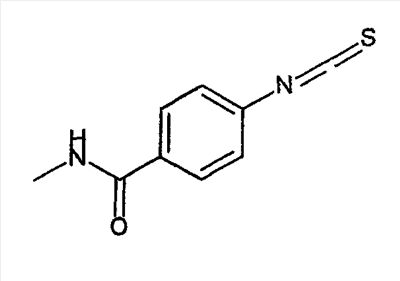
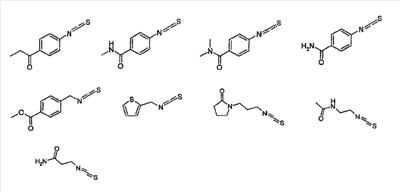
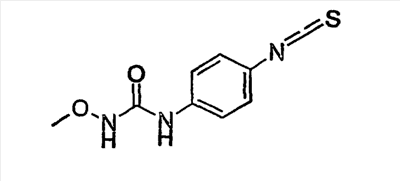

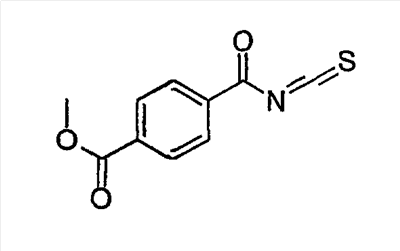
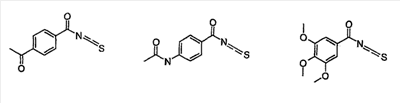
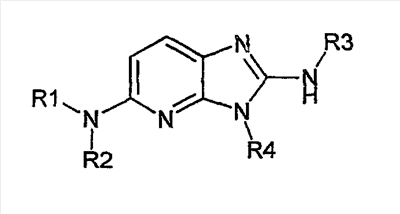
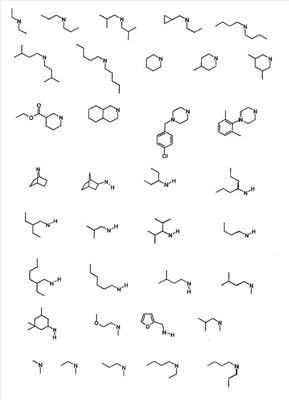
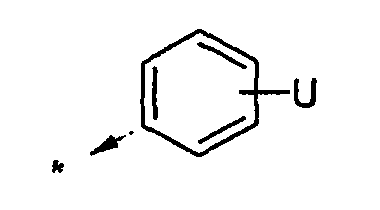
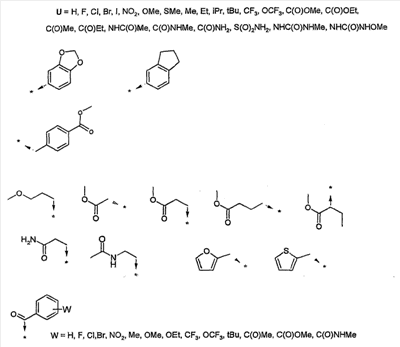
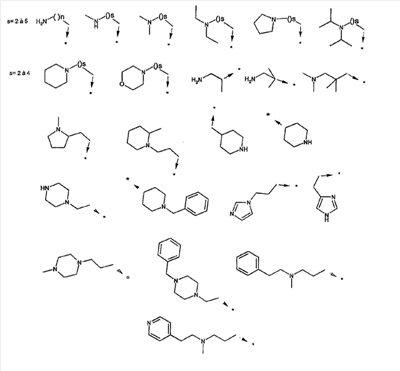
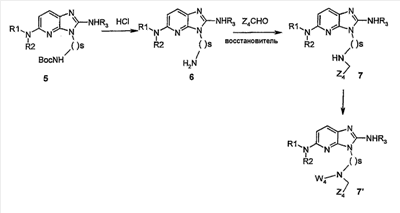
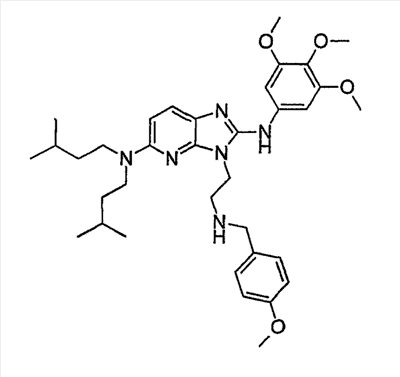

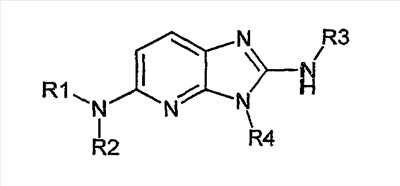
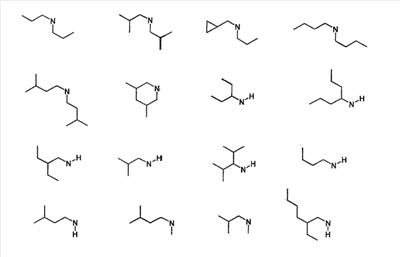
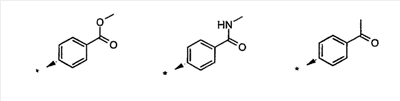
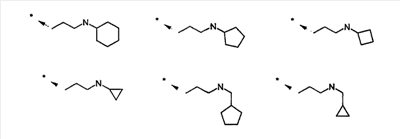
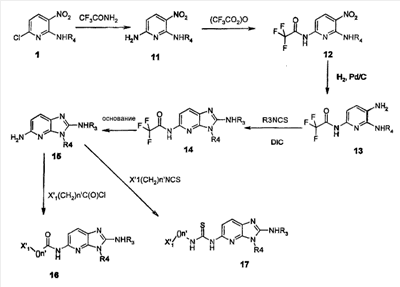
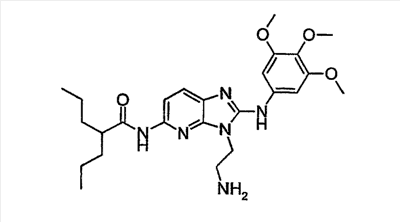
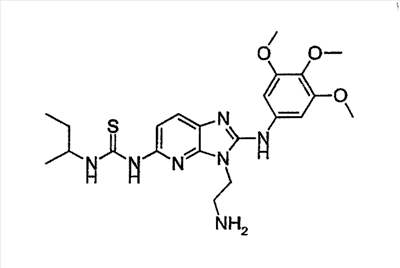
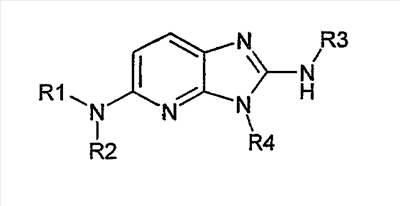
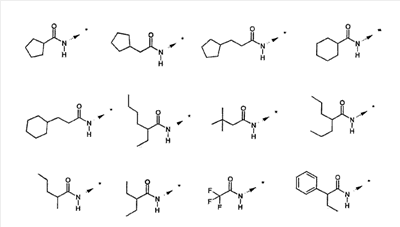
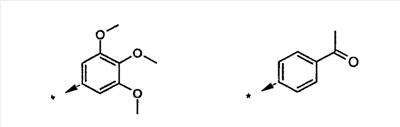

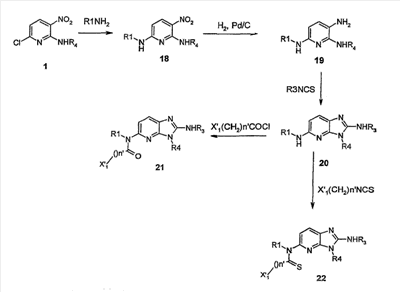
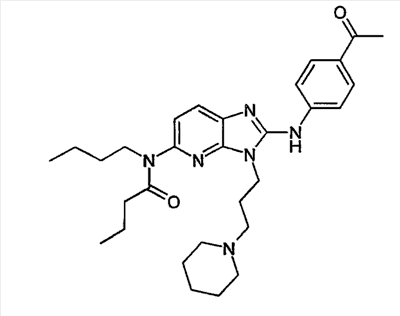
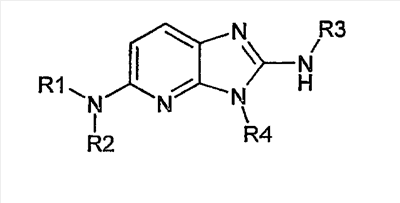
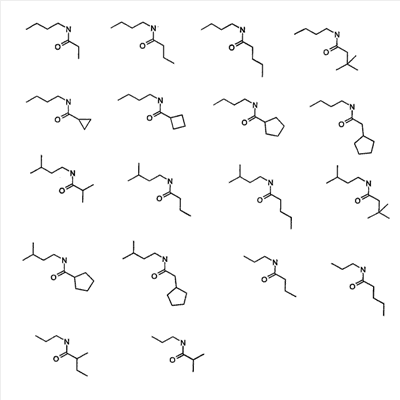
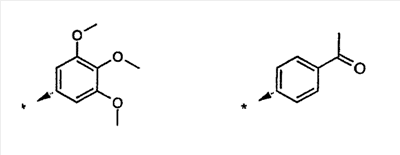

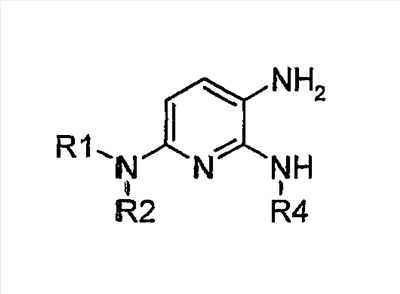
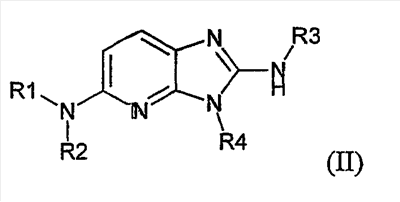
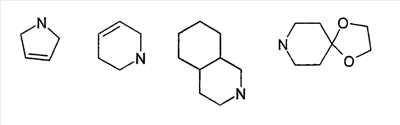
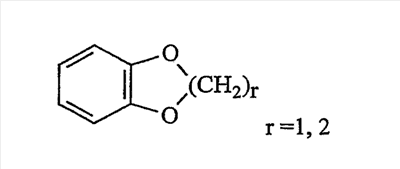
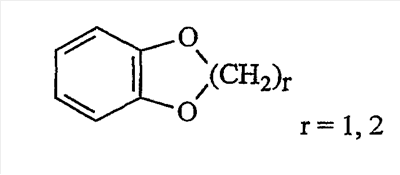
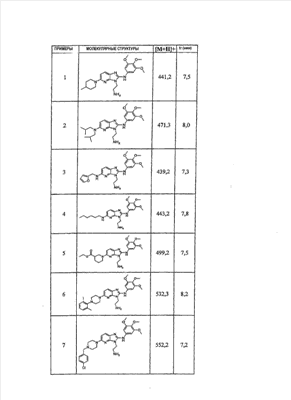
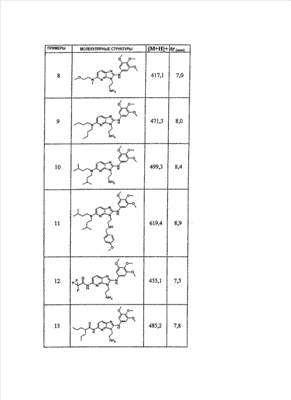
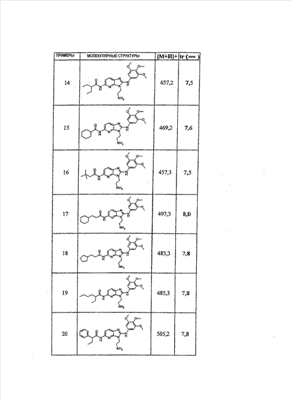
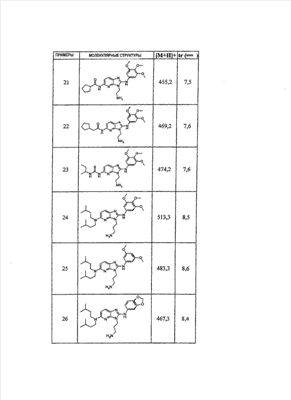
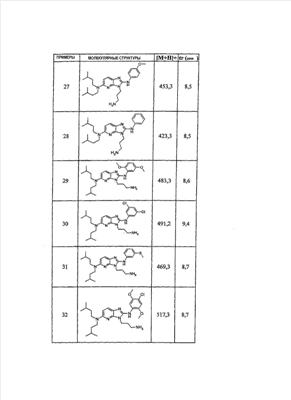
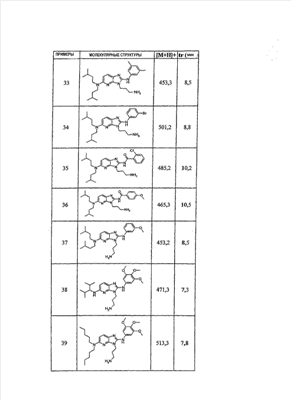
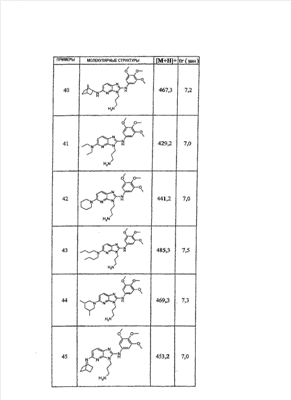
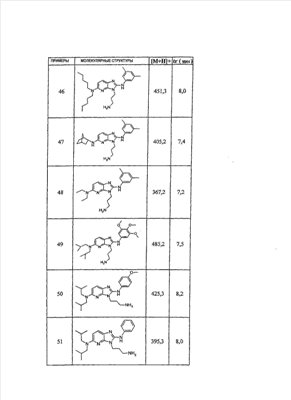
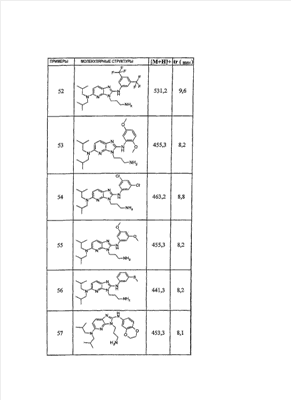
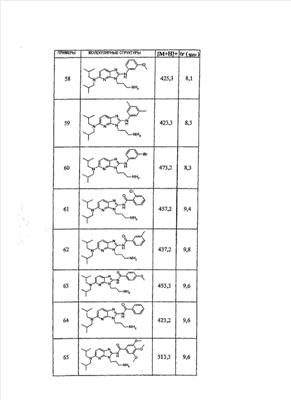
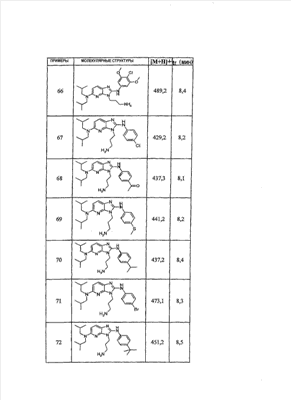
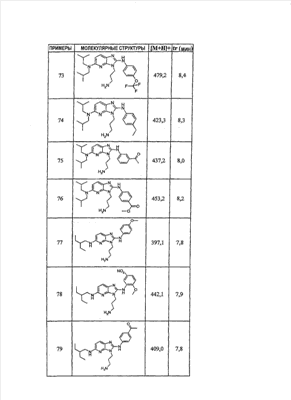
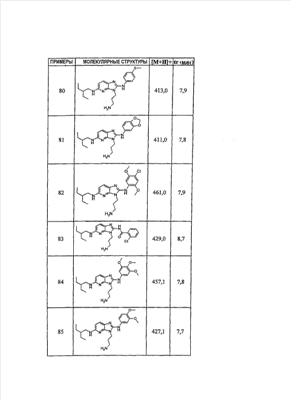
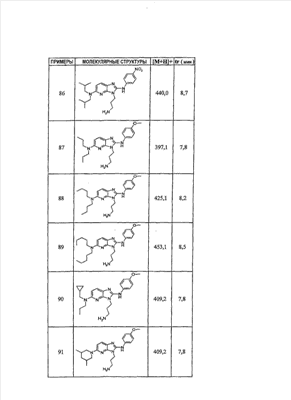
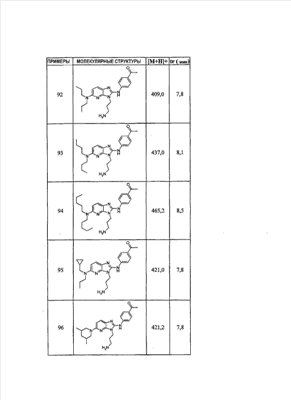
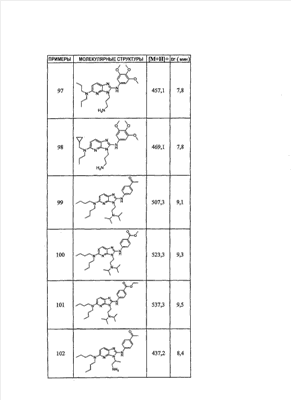
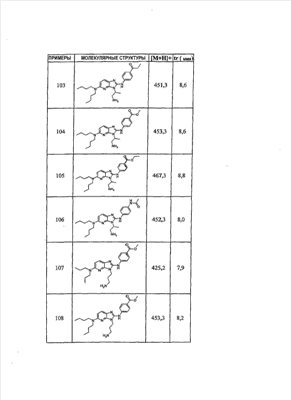
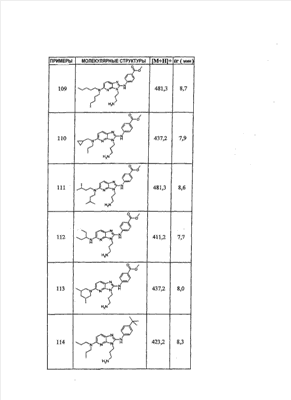
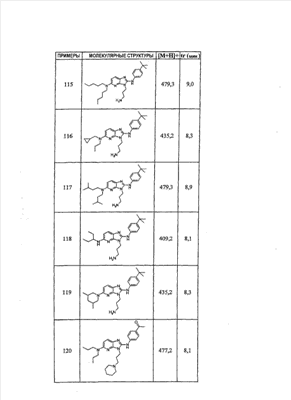
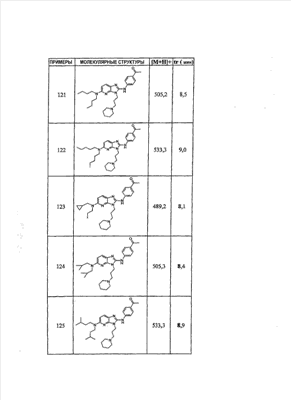
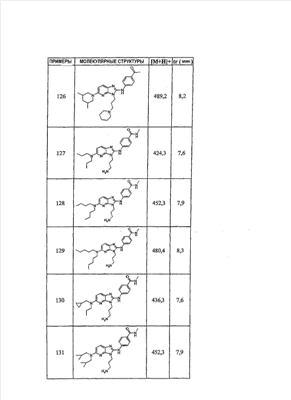
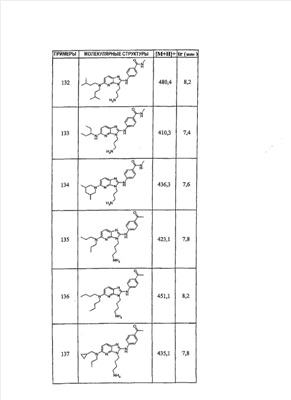
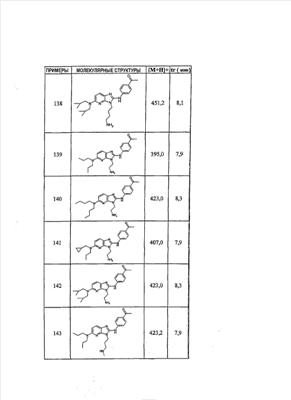
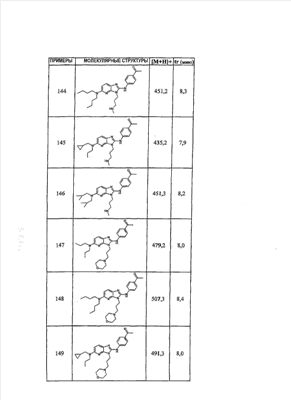
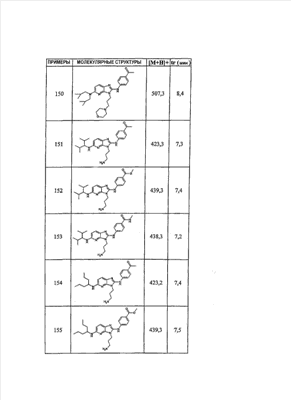
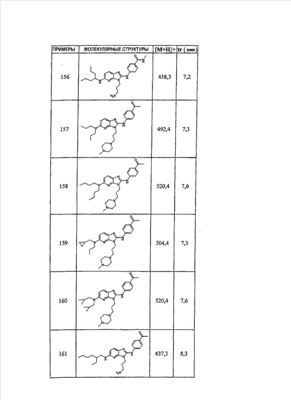
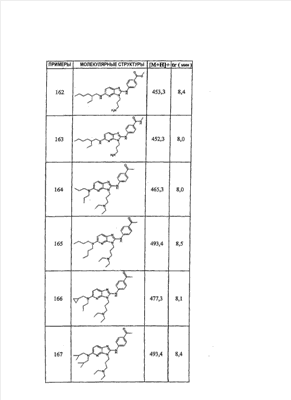
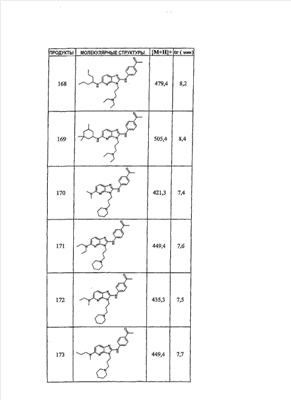
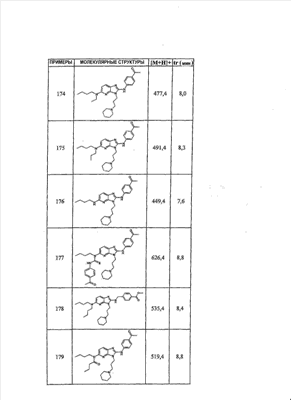
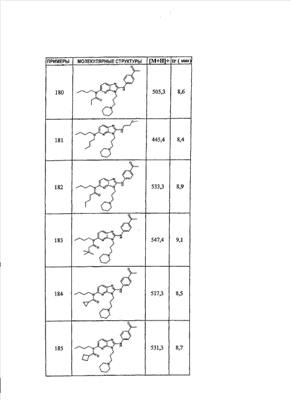
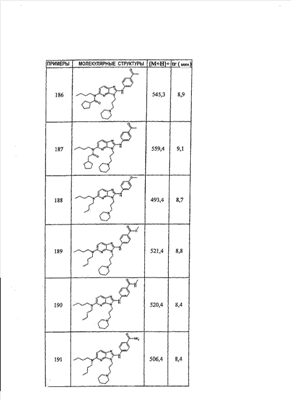
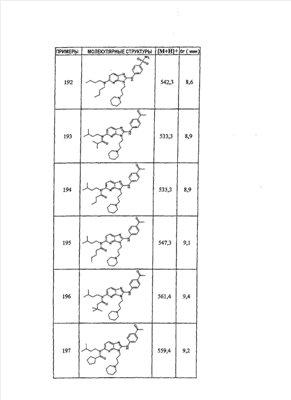
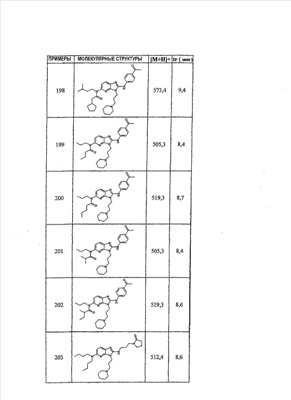
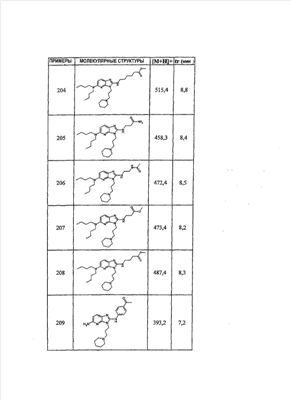
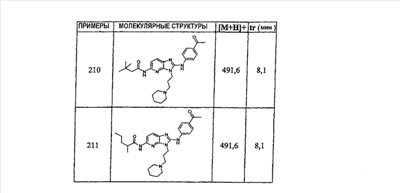
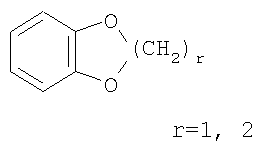
 ”-V4-Y4;
”-V4-Y4;