Патент на изобретение №2358008
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ШТАММ STREPTOMYCES GRISEOCARNEUS SUBSP. BLEOMYCINI ВКПМ-S1086 – ПРОДУЦЕНТ БЛЕОМИЦЕТИНА И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА БЛЕОМИЦЕТИНА
(57) Реферат:
Изобретение относится к новому штамму-продуценту антибиотика блеомицетина и его использованию в биосинтезе противоопухолевого антибиотика блеомицетина гидрохлорида, используемого при лечении плоскоклеточного рака. Штамм-продуцент Streptomyces griseocarneus subsp. bleomycini ВКПМ-S1086 получен в результате индуцированного мутагенеза с последующим отбором вариантов на селективных средах, содержащих стрептомицин и ванкомицин. Полученный штамм 10007 депонирован в ВКПМ под номером S1086 и продуцирует блеомицетин в 1,8 раз больше, чем исходный штамм. Антибиотик блеомицетин получают из культуральной жидкости продуцента с использованием карбоксильного катионита КБ-2 и очисткой на нейтральном гидрофобном сорбенте “Стиросорб MN-200». Фильтрация раствора антибиотика на колонке с сорбентом “Стиросорб MN-200» позволяет сорбировать примеси и не сорбировать антибиотик, повышает до 70% выход антибиотика с содержанием активного вещества до 97%. Использование на этой стадии воды позволяет получать высокоочищенные бессолевые препараты блеомицетина гидрохлорида. Использование изобретения позволяет повысить выход антибиотика до 70% с содержанием активного вещества до 97%. 2 н.п. ф-лы, 1 табл.
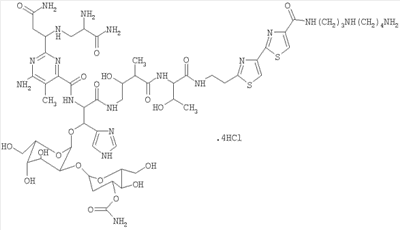
Изобретение относится к медицинской промышленности и касается нового штамма-продуцента противоопухолевого антибиотика блеомицетина, широко используемого в терапии плоскоклеточного рака. Блеомицетина гидрохлорид. Мол. Масса = 1586,4. Противоопухолевый антибиотик блеомицетин (в зарубежных фармакопеях не описан) является представителем группы антибиотиков-гликопептидов, к которой относится применяемый в медицинской практике антибиотик блеомицин (Bleocin, Nippon Kayaku, Japan и Blenoxan, Bristol Mayer’s, USA). В отличие от блеомицина, блеомицетин является монокомпонентным препаратом, представленным блеомицином А5. Зарубежные препараты являются смесью нескольких компонентов, главными из которых являются блеомицины А2 и В2. Блеомицетин отличается от многокомпонентных зарубежных аналогов пониженной легочной токсичностью. Известен штамм Streptoverticillium subsp. bleomycini (ИНА-1706) – продуцент антибиотика блеомицетина [1]. Недостатком данного штамма является низкий уровень содержания антибиотика в культуральной жидкости (не более 70 мкг блеомицетина в 1 мл культуральной жидкости). Сущность изобретения состоит в том, что получен новый штамм-продуцент блеомицетина в результате двухступенчатого мутагенного воздействия метилнитрозогуанидина и гамма-лучей 60Со на исходный штамм Полученный новый штамм депонирован в коллекции культур ФГУП ГосНИИгенетика под номером ВКМП-S1086. Штамм ВКМП-S1086 обладает повышенной продуктивностью блеомицетина (120 мкг в 1 мл культуральной жидкости) и характеризуется следующими культурально-морфологическими и физиологическими признаками. Культурально-морфологические и физиологические признаки штамма ВКМП-S1086. Температура 37°С; длительность выращивания (7-21) сутки. Споровый посевной материал с десятидневной культуры штамма, выращенного на овсяном агаре. Цвет определен по таблице Бондарева и Праузера (табл.1): Микробиологические признаки. Гифы воздушного мицелия прямые или извилистые, цепочки спор прямые, расположены мутовчато, поверхность спор гладкая. Физиолого-биохимические свойства. Аэроб растет при (24-37°С; оптимум 37°С, желатину разжижает. Молоко пептонизирует. Сахарозу инвертирует. Крахмал гидролизует. На клетчатке не растет. Восстанавливает нитраты до нитритов. Меланоидные пигменты не образует при росте на среде Треснера с лимонно-кислым железом. Отношение к углеводам: хорошо использует глюкозу, фруктозу, инозит; умеренно – лактозу, арабинозу, рафинозу, слабо – сахарозу, рамнозу, ксилозу, не использует маннит, галактозу и целлюлозу. Антагонистические свойства. При испытании методом штриха на глюкозо-нитратном агаре Штамм ВКПМ-S1086 поясняется следующим примером. Пример 1. Споровым материалом с мицелием культуры Streptomyces griseocarneus subsp. bleomycini ВКПМ-S1086, выращенной в течение (7-10) суток на овсяной агаровой среде, засевают питательную среду (100 мл в колбах Эрленмейера, объемом 750 мл) и выращивают (18-24) часа при 37°С на качалке при (220-240) об/мин. Состав посевной среды, %:
Выросшим мицелием в количестве (3-5) % засевают питательную среду (100 мл в колбах Эрленмейера, объемом 750 мл) следующего состава, %:
Ферментацию проводят на качалке при (200-220) об/мин, 28°С в течение 144 ч. Антибиотическую активность культуральной жидкости определяют методом тонкослойной хроматографии с биологическим проявлением по Bacillus subtilis ATCC 6633. Содержание блеомицетина (блеомицина А5) в культуральной жидкости продуцента к концу ферментации составляет 120 мкг/мл. Преимуществом заявленного штамма по сравнению с прототипом является более высокое содержание антибиотика блеомицетина в культуральной жидкости, а именно в штамме-прототипе 70 мкг/мл, в заявленном штамме 120 мкг/мл. Известен способ получения блеомицетина на основе штамма ИНА-1706. Этот способ основан на выделении блеомицетина из нативного раствора с рН 5,5 на катионите КБ-2 (Na+) с последующей промывкой смолы 0,5 М раствором уксусной кислоты и десорбцией антибиотика 0,25 н.раствором соляной кислоты. Дальнейшая очистка проводится методом хроматографии на колонке с катионитом КБ-2 (Na+), используя для вытеснения 0,15 М водный буферный раствор уксуснокислого аммония с рН 6,5, с последующим выделением блеомицина А5 из буферного раствора сорбцией на КБ-2, элюцией 0,25 н. раствором HCl и осаждением блеомицетина (блеомицина А5) ацетоном из водно-метанольного раствора при рН (4,0-4,5). Известный способ имеет ряд недостатков – это невысокий выход (не более 50%-ов) целевого продукта, кроме того, известный способ не позволяет полностью освободиться от минорных, содержащихся в следовых количествах компонентов – блеомицинов группы В, а также от окрашенных примесей. Сущность изобретения состоит в том, что блеомицетин выделяют из культуральной жидкости, полученной в результате биосинтеза штамма-продуцента ВКПМ-S1086, сорбцией на карбоксильной смоле КБ-2 в солевой форме. Смолу промывают 0,5 М раствором уксусной кислоты и антибиотик десорбируют 0,25 н. раствором соляной кислоты. После повторной сорбции на карбоксильном катионите КБ-2 в солевой форме блеомицетин элюируют 0,15 молярным водным буферным раствором уксуснокислого аммония с рН 6,5. Обессоленный обрабатывают сорбентом «Стиросорб MN-200» в статических условиях из расчета не менее 5 мл адсорбента на 1 г антибиотика и оставляют не менее чем на 1 час при частом перемешивании для установления равновесия. Раствор отделяют от адсорбента. Адсорбент многократно промывают небольшими порциями воды. Промывку адсорбента прекращают, когда поглощение при Первые, наиболее концентрированные промывки присоединяют к общему раствору, последующие используют для промывки обеззоливающих смол. Обеззоленный раствор антибиотика при рН=(6,0-7,0) упаривают в вакууме при температуре не более 45°С, остаток растворяют в 90% метаноле, устанавливают рН в пределах (3,7-4,4) добавлением раствора HCl и осаждают 7-кратным объемом ацетона. Общий выход блеомицетина не менее 70%. На «Стиросорбе MN-200» адсорбируются преимущественно блеомицины группы «В» (В-2, В-4) и окрашенные примеси, блеомицин А-5 (блеомицетин) практически не адсорбируется. Способ поясняется следующим примером: Пример 2. Блеомицетин выделяют из культуральной жидкости, полученной в результате биосинтеза штамма-продуцента ВКПМ-S1086, сорбцией на карбоксильной смоле КБ-2 в солевой форме. Смолу промывают 0,5 М раствором уксусной кислоты и антибиотик десорбируют 0,25 н. раствором соляной кислоты. После повторной сорбции на карбоксильном катионите КБ-2 в солевой форме блеомицетин элюируют 0,15 молярным водным буферным раствором уксуснокислого аммония с рН 6,5. Элюат обрабатывают сорбентом «Стиросорб MN-200» в статических условиях из расчета не менее 5 мл адсорбента на 1 г антибиотика и оставляют не менее чем на 1 час при частом перемешивании для установления равновесия. Раствор отделяют от адсорбента. Адсорбент многократно промывают небольшими порциями воды, оставляя каждую из них в контакте с адсорбентом на (10-20) мин. Промывку адсорбента прекращают, когда поглощение в растворе снизится до 2% от исходного. При обработке «Стиросорбом MN-200» рН раствора не изменяется (рН=6,0). Для удаления минеральных катионов (блеомицетин осаждают при рН 3,7-4,4) раствор пропускают через столб катионита КУ-2-20 в [H+] (Кнаб.=1,5) из расчета 3 г антибиотика (30000 ед. поглощения) на 1 г смолы (1,5 мл). Смолу промывают водой. Вытекающий с колонки раствор имеет рН Общий выход блеомицетина не менее 70%. Блеомицетин (блеомицин А5), полученный на основе биосинтеза нового мутантного штамма Streptomyces griseocarneus subsp. bleomycini ВКПМ-1086, представляет собой белый порошок, хорошо растворимый в воде, метаноле, ограниченно – в этаноле и нерастворим в других органических растворителях. По физико-химическим свойствам, антибактериальной и противоопухолевой активности и токсичности полностью соответствует требованиям ФС. Брутто-формула: C57H89N19O21S2.4HCl. Мол. масса 1586,4 а.е.м. УФ-спектр: Мол. масса основания (метод MALDI-MS)=1441 (М+2Н) и 1463 (M+Na++H); ИК-спектр (KBr), Использование нового сорбента «Стиросорба MN-200» считаем существенным, поскольку именно он приводит к повышению выхода целевого продукта и улучшению его качества. Высокая антибиотическая активность нового штамма Streptomyces griseocarneus subsp. bleomycini ВКПМ-S1086 (в 1,8 раза превышающая активность штамма прототипа ИНА
Источники информации 1. Зенкова В.А. и др. Антибиотики,
Формула изобретения
1. Штамм Streptomyces griseocarneus subsp. bleomycini ВКПМ-S1086 – продуцент антибиотика блеомицетина. 2. Способ получения антибиотика блеомицетина путем биосинтеза штамма-продуцента, сорбции антибиотика из нативного раствора, элюции антибиотика с последующим его выделением, концентрацией и осаждением, отличающийся тем, что в качестве продуцента используют штамм Streptomyces griseocarneus subsp. bleomycini ВКПМ-S1086, сорбцию примесей проводят на сорбенте “Стиросорб MN-200”, раствор антибиотика обеззоливают, концентрируют и осаждают ацетоном в форме гидрохлорида.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 28.04.2009
Извещение опубликовано: 27.06.2010 БИ: 18/2010
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 1706 с последующим отбором мутантов на средах, содержащих акридиновые красители в субингибирующих рост концентрациях.
1706 с последующим отбором мутантов на средах, содержащих акридиновые красители в субингибирующих рост концентрациях. max=290 нм в растворе снизится до 2% от исходного.
max=290 нм в растворе снизится до 2% от исходного. 4,0. Его нейтрализуют небольшим количеством анионита ЭДЭ-10П [ОН–] до рН=(6,0-7,0) и упаривают в вакууме (при 45°С). Остаток растворяют в 90% метаноле из расчета 100 мг (100 ед. поглощения) в 1 мл, устанавливают рН в пределах (3,7-4,4) добавлением раствора HCl и осаждают 7-кратным объемом ацетона. Потери антибиотика на КУ-2-20 и анионите ЭДЭ-10П составляют не более (2-3)%.
4,0. Его нейтрализуют небольшим количеством анионита ЭДЭ-10П [ОН–] до рН=(6,0-7,0) и упаривают в вакууме (при 45°С). Остаток растворяют в 90% метаноле из расчета 100 мг (100 ед. поглощения) в 1 мл, устанавливают рН в пределах (3,7-4,4) добавлением раствора HCl и осаждают 7-кратным объемом ацетона. Потери антибиотика на КУ-2-20 и анионите ЭДЭ-10П составляют не более (2-3)%. 1 см) 290 (108);
1 см) 290 (108);