|
|
(21), (22) Заявка: 2007143151/15, 21.11.2007
(24) Дата начала отсчета срока действия патента:
21.11.2007
(46) Опубликовано: 10.06.2009
(56) Список документов, цитированных в отчете о
поиске:
SU 810615 А1, 10.03.1981. SU 13300075 А1, 15.08.1987. RU 2225848 С2, 20.03.2004. US 2007/0114682 А1, 24.05.2007. JP 2001129305 А, 15.05.2001.
Адрес для переписки:
367015, Республика Дагестан, г.Махачкала, пр. имама Шамиля, 70, ГОУ ВПО ДГТУ, отдел интеллектуальной собственности
|
(72) Автор(ы):
Ахмедов Ганапи Янгиевич (RU)
(73) Патентообладатель(и):
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ “ДАГЕСТАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ” (ДГТУ) (RU)
|
(54) СПОСОБ СТАБИЛИЗАЦИОННОЙ ОБРАБОТКИ ВОДЫ
(57) Реферат:
Изобретение относится к области очистки природных вод, преимущественно геотермальных, и может быть использовано, например, в теплоэнергетике и теплоснабжении. Способ стабилизационной обработки геотермальной воды заключается в ее дегазации с последующим использованием образовавшихся кристаллов карбоната кальция в качестве затравки. Перед дегазацией парциальное давление углекислого газа в обрабатываемой воде доводят до равновесного значения путем замещения на другой газ – азот. При этом исходное давление в воде перед ее дегазацией сохраняют. Способ обеспечивает повышение эффективности стабилизационной обработки воды за счет более глубокой очистки ее от растворенного в ней карбоната кальция. 2 ил., 1 табл.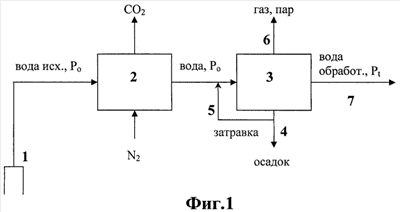
Изобретение относится к области обработки природных вод при их использовании для выработки электроэнергии, теплоснабжения, а также в различных отраслях промышленности и в сельском хозяйстве.
Известны способы предотвращения карбонатных отложений с помощью введения в обрабатываемую воду кристаллической затравки с добавлением поверхностно-активных веществ [1].
Недостатками их являются загрязнение водоемов поверхностно-активными веществами, а также необходимость расходования химических реагентов.
Наиболее близким к описываемому изобретению по технической сущности и достигаемому результату является способ предотвращения карбонатных отложений в геотермальной воде, заключающийся в ее дегазации с последующим использованием образовавшихся кристаллов карбоната кальция в качестве затравки [2].
Недостаток данного изобретения заключается в невысокой эффективности очистки воды от карбоната кальция. Это связано с недостаточной степенью удаления углекислого газа из обрабатываемой воды после дегазации и невысоким значением перепада парциального давления углекислого газа в воде от равновесного до конечного значения.
Техническим решением предлагаемого изобретения является повышение эффективности стабилизационной обработки воды, заключающееся в более глубокой очистке ее от растворенного в ней карбоната кальция.
Техническое решение достигается тем, что в способе стабилизационной обработки геотермальной воды, заключающейся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, перед дегазацией при сохранении исходного давления в воде парциальное давление углекислого газа в ней доводят до равновесного значения путем замещения части растворенного углекислого газа азотом.
Схема реализации предлагаемого способа стабилизационной обработки воды дается на примере геотермальной воды скважины  3Т г.Кизляра Республики Дагестан. Вода скважины содержит ионы, мг/л: Na+ – 2260; Са2+ – 160; Mg2+ – 40; Cl– – 3550; HCO3 3Т г.Кизляра Республики Дагестан. Вода скважины содержит ионы, мг/л: Na+ – 2260; Са2+ – 160; Mg2+ – 40; Cl– – 3550; HCO3 – – 390; SO4 – – 390; SO4 2- – 150. Газосодержание – 1,2 м3/м3, в процентном отношении – СО2 – 18%, N2+СН4 – 82%. pH 6,55. 2- – 150. Газосодержание – 1,2 м3/м3, в процентном отношении – СО2 – 18%, N2+СН4 – 82%. pH 6,55.
На фиг.1 – блок-схема реализации способа, на фиг.2 – кривые, соответствующие реальным (1) и возможным (2) значениям равновесного давления и температуры воды скважины 3Т, при которых вода стабильна.
Геотермальная вода из скважины 1 поступает в конвертор 2 с исходным давлением Рo; где осуществляется замена части углекислого газа, растворенного в воде, на азот с таким расчетом, что парциальное давление углекислого газа на выходе из конвертора 2 устанавливается на величине, близкой к равновесному, то есть из воды еще не выделяется твердая фаза карбоната кальция. При этом исходное давление Рo в воде сохраняется. Далее вода с давлением Рo поступает в кристаллизатор-отстойник 3, где происходит ее дегазация при резком падении давления от исходного Рo до конечного Pt значения. Нарушается карбонатно-кальциевое равновесие и в толще воды выделяется большое количество твердой фазы карбоната кальция. Образовавшийся осадок из нижней части кристаллизатора-отстойника 3 выводится наружу по линии 4, а часть его по линии 5 подается обратно в кристаллизатор-отстойник 3 в качестве затравки. Выделившиеся при дегазации пар и газ по линии 6 поступают к соответствующему потребителю, а обработанная (стабильная) вода подается по линии 7 для нужд горячего тепловодоснабжения.
Обычно на практике при осуществлении дегазации (фиг.2) перепад давления  Р от исходного Рo до конечного Pt значения состоит из двух составляющих: Р от исходного Рo до конечного Pt значения состоит из двух составляющих:
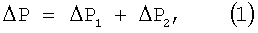
где  Р1=Po-Ps – перепад давления от исходного Рo до равновесного Ps значения, при котором еще не выделяется твердая фаза карбоната кальция; Р1=Po-Ps – перепад давления от исходного Рo до равновесного Ps значения, при котором еще не выделяется твердая фаза карбоната кальция;  Р2=Ps-Pt – перепад давления от равновесного Ps до конечного Рt значения. При замещении части углекислого газа в воде на азот значение Ps смещается в сторону исходного давления Рo и перепад давления Р2=Ps-Pt – перепад давления от равновесного Ps до конечного Рt значения. При замещении части углекислого газа в воде на азот значение Ps смещается в сторону исходного давления Рo и перепад давления
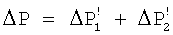 , ,
где 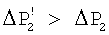 . .
При этом скорость кристаллизации карбоната кальция в присутствии кристаллической затравки определяется согласно исследованиям [3-5]:
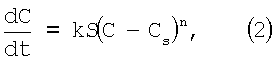
где k – коэффициент пропорциональности; n – константа поверхностной реакции (n=1÷2); S – площадь поверхности кристаллической затравки; С-Cs – пересыщение раствора воды по карбонату кальция. Как видно из (2), чем больше С-Cs, тем больше скорость кристаллизации, а пересыщение раствора С-Cs, в свою очередь, прямо пропорционально второй составляющей  Р2 (или Р2 (или 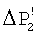 ). Поэтому, чем больше ). Поэтому, чем больше  Р2 (или Р2 (или 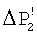 ) при дегазации, тем эффективнее идет процесс кристаллизации карбоната кальция на затравке. На фиг.2 показана разница в величинах ) при дегазации, тем эффективнее идет процесс кристаллизации карбоната кальция на затравке. На фиг.2 показана разница в величинах  Р2 и Р2 и 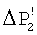 при подаче воды на дегазацию без замещения СО2 на азот (кривая 1) и с замещением (кривая 2) соответственно. при подаче воды на дегазацию без замещения СО2 на азот (кривая 1) и с замещением (кривая 2) соответственно.
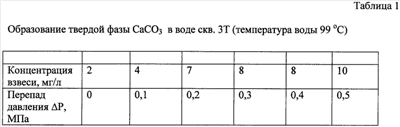
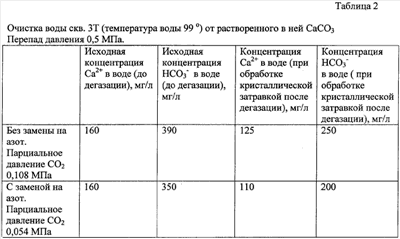
В работе [6] показано образование твердой фазы карбоната кальция в воде скважины 3Т в виде частиц взвеси сразу после дегазации ее при различных перепадах давления в системе (см. табл.1). При большом перепаде 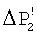 и большой поверхности, образующейся при этом, кристаллической затравки скорость кристаллизации карбоната кальция из раствора возрастает, то есть имеет место так называемое явление массовой кристаллизации. А многократное использование кристаллической затравки для обработки воды приводит к более глубокой очистке воды от растворенного в ней карбоната кальция. Результаты опытов по очистке геотермальной воды скв. и большой поверхности, образующейся при этом, кристаллической затравки скорость кристаллизации карбоната кальция из раствора возрастает, то есть имеет место так называемое явление массовой кристаллизации. А многократное использование кристаллической затравки для обработки воды приводит к более глубокой очистке воды от растворенного в ней карбоната кальция. Результаты опытов по очистке геотермальной воды скв.  3Т г.Кизляра от растворенного в ней карбоната кальция при замене части углекислого газа на азот и использовании кристаллической затравки для ее обработки показаны в таблице 2. Как видно из таблицы 2, при замене 50% углекислого газа на азот перед дегазацией концентрация ионов Са2+ в воде после дегазации и обработки ее кристаллической затравкой снижается до уровня 110 мг/л против 125 мг/л без замены СО2 на азот, что свидетельствует о более глубокой очистке воды от растворенного в ней карбоната кальция. 3Т г.Кизляра от растворенного в ней карбоната кальция при замене части углекислого газа на азот и использовании кристаллической затравки для ее обработки показаны в таблице 2. Как видно из таблицы 2, при замене 50% углекислого газа на азот перед дегазацией концентрация ионов Са2+ в воде после дегазации и обработки ее кристаллической затравкой снижается до уровня 110 мг/л против 125 мг/л без замены СО2 на азот, что свидетельствует о более глубокой очистке воды от растворенного в ней карбоната кальция.
Технически замена СО2 на азот была осуществлена следующим образом. В емкости из нержавеющей стали объемом 1,2 м3 исходное давление Рo=0,6 МПа. Парциальное давление СО2 при этом составляло 0,18×0,6 МПа = 0,108 МПа. Снизили Рo до 0,3 МПа. Это – давление, при котором еще не выделяется твердая фаза карбоната кальция из раствора воды скв. 3Т. Далее с помощью насоса закачали в емкость воздух (в воздухе 78% азота и 21% О2) до достижения исходного значения Рo=0,6 МПа. Парциальное давление СО2 при этом составило 0,09×0,6 МПа = 0,054 МПа.
Таким образом, в способе стабилизационной обработки геотермальной воды, заключающейся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, замещение части углекислого газа на азот с сохранением исходного давления в воде перед ее дегазацией позволяет повысить эффективность стабилизационной обработки воды, заключающейся в более глубокой очистке ее от растворенного в ней карбоната кальция.
Источники информации
1. Авторское свидетельство СССР  307070, кл. С02В 5/00, 1971. 307070, кл. С02В 5/00, 1971.
2. Авторское свидетельство СССР  810615, кл. C02F 5/00, 1981. 810615, кл. C02F 5/00, 1981.
Формула изобретения
Способ стабилизационной обработки геотермальной воды, заключающийся в ее дегазации при снижении исходного давления с последующим возвратом образовавшихся кристаллов карбоната кальция в исходную воду и использованием в качестве затравки, отличающийся тем, что перед дегазацией при сохранении исходного давления в воде парциальное давление углекислого газа в ней доводят до равновесного значения путем замещения части растворенного углекислого газа азотом.
РИСУНКИ
|
|