Патент на изобретение №2356629
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ГИДРОДЕОКСИГЕНАЦИИ ЖИРНЫХ КИСЛОТ, ИХ ЭФИРОВ И ТРИГЛИЦЕРИДОВ
(57) Реферат:
Изобретение относится к области получения углеводородов путем каталитической гидродеоксигенации животных жиров, растительных масел, эфиров жирных кислот, свободных жирных кислот и разработки катализатора для этого процесса. Описан катализатор гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим, по крайней мере, благородный металл в количестве не более 5.0 мас.% или содержит, по крайней мере, никель, или медь, или железо, или их комбинацию в восстановленной форме в количестве не более 54.7 мас.% и, по крайней мере, переходные металлы, отличающиеся от перечисленных выше, в оксидной форме в количестве не более 40 мас.%, носитель – остальное. Описаны три варианта способа приготовления катализатора. Процесс гидродеоксигенации осуществляют с использованием описанного выше катализатора при давлении водорода менее 3,0 МПа, температуре 250-340°С. Технический результат – высокая активность несульфидированных катализаторов и мягкие условия осуществления процесса. 5 н. и 5 з.п. ф-лы, 2 табл.
Изобретение относится к области получения углеводородов путем каталитической гидродеоксигенации животных жиров, растительных масел, эфиров жирных кислот, свободных жирных кислот и разработки катализатора для этого процесса. Известно, что растительные масла и животные жиры (триглицериды жирных кислот) в последнее время рассматриваются как возобновляемый частичный заменитель традиционного моторного топлива (дизельного и бензинового топлива). Однако напрямую триглицериды не используются в качестве компонентов моторных топлив, а подвергаются переэтерификации метанолом в присутствии кислот или щелочей, которые выступают в роли катализаторов, с получением метиловых эфиров соответствующих жирных кислот, так называемого биодизеля. Биодизель может использоваться в качестве добавки к стандартному дизельному топливу не более 15-20 мас.% без потери эксплуатационных характеристик двигателя и его модернизации. По своим эксплуатационным свойствам биодизель уступает дизельным фракциям в связи с высоким содержанием кислорода в его составе, что снижает его калорийность на 15-20%, стабильность и делает его в два раза более вязким, чем обычный дизель. В связи с этим возникает острая необходимость дальнейшей его переработки с целью удаления кислорода. Крупнейшие компании Европы и США интенсивно работают в направлении получения стандартного дизельного топлива из биодизеля. Работы направлены на проведение деоксигенации биодизеля в присутствии стандартных сульфидированных катализаторов нефтепереработки на основе Ni-Mo, Co-Mo, нанесенных на Al2О3 [O.I.Senol, E.-M.Ryymin, T.-R.Vilijava, A.O.I.Krause, Reaction of methyl heptanoate hydrodeoxygenation on sulphided catalysts, J. Mol. Cat. A: Chem., 268 (2007), 1-8; M.Ferrari, В.Delmon, P.Grange, Influence of the active phase loading in carbon supported molybdenum-cobalt catalysts for hydrodeoxygenation reactions, Micropor. Mesopor. Mat., 56 (2002), 279-290; E.Laurent, В.Delmon, Study of the hydrodeoxygenation of carbonyl, carboxylic and guaiacyi groups over sulfided СоМо/Al2О3 and NiMo/Al2O3 catalysts, Appl. Catal. A, 109 (1994), 777-96; O.I.Senol, T.-R.Vilijava, A.O.I.Krause, Hydrodeoxygenation of methyl esters on sulphide СоМо/Al2О3 and NiMo/Al2O3 catalysts, Catalysis Today, 100 (2005), 331-335]. Эти катализаторы имеют невысокую активность и селективность по выходу дизельных фракций и быстро дезактивируются с падением содержания серы в катализаторе, поскольку в отличие от нефти исходное содержание серы в растительных маслах минимально. Для поддержания постоянной активности сульфидированных катализаторов необходимо постоянно добавлять в реакционную зону Н2S либо сероорганику. При выполнении данного условия и давлении водорода 1.5-2,0 МПа и 275-300°С удается достигнуть степени конверсии эфира 100% и степени деоксигенации – 100%. В качестве исходных субстратов при этом в основном используются насыщенные метилгептаноат, диэтилдеканодиат, этилдеканоат, которые имеют более высокую реакционную способность в реакции гидродеоксигенации, чем более высококипящие производные жирных кислот – компонентов растительных масел и животных жиров. Для селективного гидрирования жиров и растительных масел используют другой тип катализаторов в несульфидированной форме. Продукты гидрирования жиров широко используют в пищевой и химической промышленности. В основном используют нанесенные Ni-содержащие катализаторы. Так, например, в [US 3896053, B01J 11/22, 22.07.1975] используется Ni, Co, Cu – Al2О3 катализаторы, приготовленные методом соосаждения соответствующих карбонатов переходных металлов и гидроксида алюминия. После прокалки катализаторы восстанавливались в атмосфере водорода и использовались в селективном гидрировании жиров и растительных масел при 100-140°С и атмосферном давлении водорода. После 1 ч гидрирования удается получить смеси продуктов с йодным числом 37-40. Известен способ гидрирования масла в присутствии Ni-Cu-катализатора, нанесенного методом соосаждения на различные носители: SiO2, Al2O3, TiO2, MgO, Cr2О3 [US 3743662, С11С 3/12, 03.07.1973]. Восстановленный при 600°С катализатор при содержании 1 мас.% в масле показывает максимальную активность в гидрировании двойных связей триглицеридов жирных кислот при 200°С и 0,5 МПа H2. Известен способ селективного гидрирования свободных жирных C12-C20 кислот в присутствии Ni-Cu-Cr-катализатора при 0,25-0,7 МПа и 180-260°С [US 4133822, C11C 3/12]. Йодное число получаемого продукта гидрирования достигает 40 после 3 ч гидрирования. Приведенные катализаторы гидрирования селективно гидрируют непредельные углеводородные радикалы жиров и растительных масел без восстановления кислородсодержащих эфирных групп и тем более без гидрокрекинга триглицеридов с образованием насыщенных алканов. Известны пропиточные катализаторы 15-25 мас.% Ni/Al2O3 или 15-25 мас.% Со/Al2O3 и Cu-Cr-Ni-катализатор H14279 Degussa, которые позволяют гидрировать смесь альдегидов, эфиров (на примере изотридеканил формиата) карбоновых кислот до спиртов при 2-3 МПа H2 и 160-190°С в жидкой фазе [US 2007/0027346 A1, C07C 29/14]. Гидрирование смеси идет только до спиртов без образования соответствующих алканов. Известен способ получения углеводородов термолизом растительных масел в присутствии алюмосиликатов или катализаторов, содержащих оксиды переходных металлов IIA, IIIA, IVA, VIA, VIIA или VIIIA при температурах 300-700°С [GB 1524781, C10G 3/00, 13.09.1978; US 5233109, C07C 1/00, 03.08.1993]. В результате крекинга из триглицеридов жирных кислот образуется смесь углеводородов, в основном олефинового ряда, кислород удаляется в виде CO2 и Н2О, а катализатор быстро коксуется, и требуется его регенерация отжигом. Образование насыщенных алканов дизельного ряда непосредственно из триглицеридов жирных кислот возможно в присутствие традиционных сульфидированных катализаторов гидрокрекинга – СоМо/Al2О3 и NiMo/Al2О3 при повышенных температуре 350-450°С и давлении Н2 – 4,8-15,2 МПа [US 4992605, C10L 1/04, 12.02.1991; US 5705722, C07C 1/00, 06.01.1998]. Так, например, при гидрообработке пальмового масла при 360°С, 5,5 МПа Н2 и LHSV=1,18 ч-1 выход жидких продуктов составляет 91 мас.%, в том числе 8,7 мас.%. Н2О. В органической фракции основным продуктом является фракция C15-C18 углеводородов (71 мас.%) с температурой кипения 210-343°С. Выход углеводородов с температурой кипения более 343°С составляет 9,5 мас.%. Данные по содержанию серы и стабильности сульфидированных катализаторов не приводятся. Тем не менее, известно, что используемые сульфидированные катализаторы гидрокрекинга склонны восстанавливаться в восстановительной среде, а восстановленная форма катализатора способствует в свою очередь образованию кокса, что в свою очередь приводит к дезактивации катализатора. В связи с этим актуальным является разработка несульфидированных катализаторов гидродеоксигенации кислородорганических соединений типа свободных жирных кислот, их сложных эфиров и триглицеридов, которые являются компонентами жиров и растительных масел. Наиболее близким к заявленному по технической сущности и достигаемому эффекту является способ получения углеводородов путем каталитического декарбоксилирования жирных карбоновых кислот, их эфиров и триглицеридов [WO 2006119357, С07С 7/148, 09.11.2006]. Вышеуказанные соединения являются производными или компонентами широкого спектра растительных масел и животных жиров. Процесс деоксигенации проводится при 250-380°С при повышенном давлении до 5,0 МПа в жидкой фазе в инертной или водородной атмосфере. В качестве растворителя предпочтительно использовать продукты деоксигенации исходного сырья – парафины с температурой кипения 150-350°С. В качестве катализатора используется как минимум один металл VIII группы Периодической системы в восстановленной форме, нанесенный на Al2О3, SiO2, Cr2O3, MgO2, TiO2 или С. При приготовлении катализатора декарбоксилирования предпочтительно наносить Pd или Pt в количестве 2-8 мас.%. методом пропитки на углеродный носитель. В случае Ni-катализатора предпочтительно наносить 10-30 мас.%. Продуктом деоксигенации является смесь линейных углеводородов, в основном линейных парафинов с температурой кипения 180-350°С, что соответствует остаткам исходных жирных кислот без одного атома углерода. Наибольшей активностью в декарбоксилировании стеариновой кислоты обладает 5% Pd/C, который позволяет достигать степени конверсии кислоты 100% с селективностью образования гептадекана 97% за 1.5 ч при 300°С, 0,8 МПа Не и массовом соотношении кислота/катализатор=4,5. Этиловый эфир стеариновой кислоты полностью превращается в алканы в присутствии 5%Pd/C только при 360°С и давлении 2,9 МПа. Для превращения триглицерида стеариновой кислоты используют 5% Pd/C со следующими реакционными параметрами: 360°С и 4,2 МПа газовой смеси (5 об.% Н2 – 95 об.% Ar). При этом конверсия триглицерида после 6 часов составляет 99%, а выход С17-углеводородов составляет не менее 85%. После дезактивации катализаторы на углеродных носителях не поддаются регенерации и утилизируются. Другие указанные катализаторы на основе металлов VIII группы обладают гораздо более низкой активностью в процессе декарбоксилирования карбоновых кислот. Данные по их активности в реакциях декарбоксилирования эфиров и триглицеридов жирных кислот не приводятся. Недостатком известных катализаторов гидродеоксигенации является то, что данные катализаторы нестабильны при деоксигенации алифатических оксисоединений и не обладают достаточной активностью для их промышленного применения в данных процессах. Кроме того, применяемые в прототипе катализаторы дороги из-за достаточно высокого процента нанесения благородного металла и небольшого соотношения субстрат/катализатор. Изобретение решает задачу создания несульфидированного катализатора для процесса гидродеоксигенации животных жиров, растительных масел, эфиров жирных кислот, свободных жирных кислот с целью получения углеводородов, не содержащие кислород, при более мягких условиях процесса (пониженные температура и давление водорода) и с пониженным содержанием в катализаторе благородного металла либо без него. Задача решается катализатором гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим благородный металл в количестве не более 5 мас.%, или никель, или медь, или железо, или их комбинацию в восстановленной форме в количестве не более 55 мас.%, переходные металлы, отличающиеся от перечисленных выше, в оксидной форме в количестве не более 40 мас.% и носитель. Благородный металл выбирают из группы: Rh, Ru, Pt, Pd. Переходный металл в несульфидной оксидной форме выбирают из группы: Со2О3, ZrO2, CeO2, TiO2, Cr2O3, MoO2, WO2, V2O5, MnO2. Носитель выбирают из группы: Композитный катализатор в активированном состоянии содержит либо благородный металл не более 5 мас.%, либо переходные металлы не более 55 мас.% в восстановленном состоянии, которые отвечают за активацию водорода, и не более 40 мас.% оксида переходного металла с переменной валентностью, отвечающего за активацию кислородсодержащего органического соединения. Поверхность носителя, выбранного из группы: Задача также решается способом приготовления катализатора гидродеоксигенации, который готовят как минимум тремя способами. Первый вариант – методом многократной пропитки по влагоемкости следующим образом: подготовленный носитель высушивают при 100-120°С, пропитывают водорастворимьми солями соответствующих переходных металлов, высушивают при 100-120°С, прокаливают при 400-550°С до образования соответствующих оксидов. Процедуру пропитки повторяют требуемое количество раз. В случае нанесения нескольких компонентов пропитку каждого компонента проводят либо последовательно, либо одновременно с другими компонентами. Нанесение соли благородного металла при необходимости проводят пропиткой по влагоемкости в последнюю очередь. Второй вариант – методом последовательного или одновременного осаждения гидрооксидов или карбонатов переходных металлов в присутствие носителя следующим образом: растворы водорастворимых солей переходных металлов подщелачивают гидрооксидами или карбонатами щелочных металлов или аммиаком в присутствии носителя или без него. Образовавшийся осадок старят при температуре 20-90°С в течение 10-48 ч в маточном растворе. Осадок отфильтровывают и отмывают до нейтральной среды. После высушивания полученный композит прокаливают до 500-550°С. Благородный металл при необходимости наносят методом пропитки по влагоемкости на сформированный ранее композит. Третий вариант – методом совместного сплавления/разложения нитратов переходных металлов следующим образом: твердые кристаллогидраты нитратов соответствующих переходных металлов смешивают со стабилизирующими добавками типа нитрат циркония, церия, алюминия или гидроксида алюминия, выступающими в качестве носителя. Смесь нагревают до температуры плавления смеси. Далее температуру в течение 2-3 ч повышают до 300-350°С и выдерживают при конечной температуре 2-4 ч. Приготовленные по каждому из описанных выше трех вариантов способа катализаторы перед целевым процессом активируют путем нагревания в токе водородсодержащего газа до температуры процесса и выдерживания при конечной температуре в течение 2 ч. Задача решается также способом проведения процесса гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот (олеиновая и декановая), их эфиров (этилкапрат) и триглицеридов (рапсовое масло), при температуре 250-350°С и давлении водорода 1,0-3,0 МПа с объемной скоростью (LHSV) кислородорганической жидкости (КЖ), равной 0,3-2,0 мл КЖ/мл кат/ч, в присутствии катализатора, описанного выше. Технический результат заключается в высокой активности заявляемых несульфидированных катализаторов, которые позволяют проводить процесс гидродеоксигенации кислородсодержащих алифатических соединений при более низких температуре и давлении водорода, чем в присутствии катализаторов на основе благородных металлов, указанных в прототипе. Процесс гидродеоксигенации проводят в реакторах следующего типа: – проточный с неподвижным слоем катализатора и газообразном состоянии исходных реагентов и продуктов реакции; – трехфазный реактор с неподвижным слоем катализатора и нисходящим прямотоком фаз; – автоклав с интенсивным перемешиванием катализатора в жидкой фазе кислородорганического компонента. Анализ продуктов гидродеоксигенации в газовой и жидкой фазах осуществляют методом газовой хроматографии на газовых хроматографах «Хромос-1100» с использованием капиллярных колонок ZB-1, неподвижная фаза 100% диметилполисилоксан 30 м × 0.32 мм × 0,25 мкм; ZB-5, неподвижная фаза 5% фенил + 95% диметилполисилоксан 30 м × 0.32 мм × 0,25 мкм; ZB-FFAP неподвижная фаза нитротерефталевая кислота, модифицированная полиэтиленгликолем, 30 м × 0.32 мм × 0,5 мкм, а также насадочной угольной колонке. Степень деоксигенации (HDO) определяют следующим образом:
Сущность изобретения иллюстрируется следующими примерами и таблицами. Пример 1. (1 вариант приготовления катализатора). Углеродный или оксидный носитель, выбранный из ряда: Катализатор в количестве 10 мл испытывают в проточном реакторе при давлении водорода 1,0 МПа, температуре 300°С, токе H2 3 л/ч и Ar 3 л/ч в реакции гидродеоксигенации этилкапрата (C9H19COOC2H5) с объемной скоростью подачи этилкапрата (LHSV) 0,3 ч-1. Активность катализатора и степень деоксигенации этилкапрата приведены в таблице 1.
Пример 2. (1 вариант приготовления катализатора). Углеродный или оксидный носитель, выбранный из ряда: Катализатор в количестве 5 мл испытывают в проточном реакторе при давлении водорода 1,0 МПа, температуре 270-310°С, LHSV=0,3 ч-1, токе H2 3 л/ч и Ar 3 л/ч в реакции гидродеоксигенации этилкапрата. Активность катализатора и степень деоксигенации этилкапрата приведены в таблице 2.
Пример 3. (2 вариант приготовления катализатора). К раствору, содержащему 100 г гексагидрата оксид-нитрата циркония, 140 г гексагидрата нитрата никеля и 38 г тригидрата нитрата меди, добавляют при перемешивании раствор, содержащий 80 г NaOH, до достижения рН 7. Далее выпавший осадок старят в течение 24 ч в маточном растворе, после чего отфильтровывают и отмывают дистиллированной водой. После высушивания при 150°С полученный композит прокаливают при 500°С в течение 5 ч. Полученный композит содержит, мас.%: Ni – 37.5, Cu – 12.5, ZrO2 – 50. Перед тестированием в реакции гидродеоксигенации катализатор восстанавливают в токе водорода при давлении 1,0 МПа и температуре 300°С. Катализатор в количестве 5 мл испытывают в проточном реакторе при давлении водорода 1,0 МПа, температуре 260°С, токе Н2 3 л/ч и Ar 3 л/ч в реакции гидродеоксигенации этилкапрата, который подается с объемной скоростью 0,75 ч-1. Степень конверсии этилкапрата составляет 100%, выход деоксигенированных продуктов составляет 99% с селективностью (мол.%): нонан – 90; октан – 7; гексан – 3. Пример 4. (2 вариант приготовления катализатора). К раствору, содержащему 75 г гексагидрата нитрата никеля и 23 г тригидрата нитрата меди, добавляют в качестве стабилизирующего носителя 24,5 г оксида церия (II) и при перемешивании раствор, содержащий 40 г NaOH, до достижения рН 8. Далее выпавший осадок старят в течение 36 ч в маточном растворе, после чего отфильтровывают и отмывают дистиллированной водой. После высушивания при 120°С полученный композит прокаливают при 550°С в течение 3 ч. Полученный композит содержит, мас.%: Ni – 37.5, Cu – 12.5, СеО2 – 50. Катализатор восстанавливают, как в примере 3, при температуре 320°С и испытывают в реакции гидродеоксигенации в проточном реакторе при давлении водорода 1,5 МПа, температуре 250°С, токе Н2 3 л/ч и Ar 3 л/ч. При объемной скорости подачи этилкапрата (LHSV) 1,0 ч-1 степень конверсии этилкапрата достигает 90% и степень деоксигенации 98% с селективностью (мол.%): декан – 25, нонан – 45; октан – 20; гексан – 10. Пример 5. (2 вариант приготовления катализатора). К раствору, содержащему 50 г гексагидрата нитрата церия, добавляют в качестве стабилизирующего носителя 23 г оксида титана (IV) и при перемешивании раствор, содержащий 30 г NaOH, до достижения рН 8. Осаждение гидроксида церия, сушка и прокаливание композита проводят, как в примере 4. Далее к полученному композиту добавляют раствор, содержащий 75 г гексагидрата нитрата никеля и 23 г тригидрата нитрата меди, и при перемешивании раствор, содержащий 83 г Na2CO3. Далее выпавший осадок старят в течение 24 ч в маточном растворе, после чего дальнейшую обработку проводят, как в примере 4. Полученный композит содержит, мас.%: Ni – 25.05, Cu – 8.35, СеО2 – 33.3, TiO2 – 33.3. Катализатор восстанавливают, как в примере 3, при температуре 325°С и испытывают в реакции гидродеоксигенации в проточном реакторе при давлении водорода 1,5 МПа, температуре 250°С, токе H2 3 л/ч и Ar 3 л/ч. При объемной скорости подачи этилкапрата (LHSV) 0,5 ч-1 степень конверсии этилкапрата достигает 99% и степень деоксигенации 98% с селективностью (мол.%): нонан – 55; октан – 31; гептан – 4; гексан – 10. Пример 6. (3 вариант приготовления катализатора). 50 г гексагидрата нитрата церия, 75 г гексагидрата нитрата никеля и 23 г тригидрата нитрата меди механически смешивают. Смесь нагревают до температуры плавления смеси. Далее смесь нагревают до 320°С со скоростью 2°С/мин и выдерживают при конечной температуре 2 ч. Полученный композит содержит, мас.%: Ni – 37.5, Cu – 12.5, CeO2 – 50. Удельная поверхность катализатора по БЭТ – 8 м2/г. Катализатор восстанавливают, как в примере 3, и испытывают в реакции гидродеоксигенации олеиновой кислоты в проточном реакторе при давлении водорода 1,5 МПа, температуре 300°С, токе Н2 10 л/ч и Ar 10 л/ч. При объемной скорости подачи олеиновой кислоты (LHSV) 0,4 ч-1 степень ее конверсии достигает 90% и степень деоксигенации 90% с селективностью (% мол.): гептан – 2,7, октан – 5,0, нонан – 9,9, декан – 5,4, ундекан – 15,9, додекан – 3,7, тридекан – 5,1, тетрадекан – 4,5, пентадекан – 9,2, гексадекан – 6,1, гептадекан – 30,5, остальное – 2,0. Пример 7. (3 вариант приготовления катализатора). 100 г гексагидрата оксид-нитрата циркония, 140 г гексагидрата нитрата никеля и 38 г тригидрата нитрата меди механически смешивают. Смесь нагревают до температуры плавления смеси. Далее смесь нагревают до 350°С со скоростью 3°С/мин и выдерживают при конечной температуре 3 ч. Полученный композит содержит, мас.%: Ni – 37.5, Cu – 12.5, ZrO2 – 50. Удельная поверхность катализатора по БЭТ – 12 м2/г. Катализатор восстанавливают, как в примере 3, при температуре 350°С и испытывают в реакции гидродеоксигенации олеиновой кислоты в проточном реакторе при давлении водорода 1,5 МПа, температуре 290°С, токе Н2 10 л/ч и Ar 3 л/ч. При объемной скорости подачи олеиновой кислоты (LHSV) 0,5 ч-1 степень ее конверсии достигает 85% и степень деоксигенации 83% с селективностью (мол.%): нонан – 9,5, декан – 9,5, ундекан – 15,9, додекан – 5,7, тридекан – 6,1, тетрадекан – 3,5, гексадекан – 6,0, гептадекан – 41,5, остальное – 3,0. Пример 8. (3 вариант приготовления катализатора). Отличается от примера 7 тем, что 63 г нитрата алюминия механически смешивают с 140 г гексагидрата нитрата никеля и 38 г тригидрата нитрата меди, смесь нагревают до 300°С. Полученный композит содержит, мас.%: Ni – 41, Cu – 13.7, Al2О3 – 45,3. Удельная поверхность катализатора по БЭТ – 15 м2/г. Катализатор восстанавливают, как в примере 3, при температуре 325°С и испытывают в реакции гидродеоксигенации декановой кислоты в проточном реакторе при давлении водорода 1,0 МПа, температуре 270°С, токе Н2 3 л/ч и Ar 3 л/ч. При объемной скорости подачи декановой кислоты (LHSV) 0,75 ч-1 степень конверсии декановой кислоты достигает 100% и степень деоксигенации 96% с селективностью (мол.%): нонан – 85; октан – 14; остальное – 1. Пример 9. (3 вариант приготовления катализатора). Отличается от примера 8 тем, что 23,4 г гидроксида алюминия механически смешивают с 140 г гексагидрата нитрата никеля и 38 г тригидрата нитрата меди, смесь нагревают до 300°С. Полученный композит содержит, мас.%: Ni – 41, Cu – 13.7, Al2О3 – 45,3. Удельная поверхность катализатора по БЭТ – 18 м2/г. Катализатор испытывают в реакции гидродеоксигенации декановой кислоты в проточном реакторе при давлении водорода 1,5 МПа, температуре 300°С, токе Н2 3 л/ч и Ar 3 л/ч. При объемной скорости подачи декановой кислоты (LHSV) 0,5 ч-1 степень конверсии декановой кислоты достигает 94% и степень деоксигенации 90% с селективностью (мол.%): нонан – 87; октан – 11; остальное – 2. Пример 10. Катализатор из примера 5 испытывают в реакции гидродеоксигенации рапсового масла (в основном смесь триглицеридов эруковой, олеиновой, линолевой и линоленовой кислот) в автоклаве объемом 300 мл при 3,0 МПа водорода и температуре 340°С. Соотношение объемов рапсового масла и катализатора составляет 10:1. После 5 часов проба жидкой фазы отбирается и анализируется. Объемное соотношение Н2/рапсовое масло = 1000 (в перерасчете на нормальные условия). В результате выход газообразных продуктов составляет 5 мас.% от исходного рапсового масла, воды – 11% и 84% насыщенных углеводородов состава C15-C21. Как видно из приведенных примеров, предлагаемые катализаторы позволяют проводить процесс гидродеоксигенации кислородсодержащих алифатических соединений, в первую очередь карбоновых кислот и их сложных эфиров и триглицеридов растительного происхождения, при более мягких условиях – давлении водорода до 3,0 МПа и температуры 250-340°С. Другим преимуществом заявляемых каталитических систем является то, что катализаторы не содержат либо содержат в небольших количествах соединения благородных металлов, что позволяет снизить стоимость катализатора и повысить рентабельность производства компонентов моторных топлив из растительных масел. Приводимые выше катализаторы имеют выраженную гидрирующую способность, что позволяет использовать их в процессах гидрирования в химической промышленности.
Формула изобретения
1. Катализатор гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим переходные металлы и носитель, отличающийся тем, что катализатор содержит, по крайней мере, благородный металл в количестве не более 5,0 мас.% или содержит, по крайней мере, никель или медь, или железо, или их комбинацию в восстановленной форме в количестве не более 54,7 мас.% и, по крайней мере, переходные металлы, отличающиеся от перечисленных выше, в оксидной форме в количестве не более 40 мас.%. 2. Катализатор по п.1, отличающийся тем, что благородный металл выбирают из группы: Rh, Ru, Pt, Pd. 3. Катализатор по п.1, отличающийся тем, что переходный металл в несульфидной оксидной форме выбирают из группы: CO2O3, ZrO2, CeO2, TiO2, Cr2O3, МоО2, WO2, V2O5, MnO2. 4. Катализатор по п.1, отличающийся тем, что носитель выбирают из группы: 5. Способ приготовления катализатора гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим переходные металлы, нанесенные на носитель методом пропитки носителя растворами соединений металлов с последующей сушкой и терморазложением соединений металлов, отличающийся тем, что при нанесении нескольких компонентов пропитку каждого компонента проводят либо последовательно, либо одновременно с другими компонентами, нанесение соли благородного металла при необходимости проводят пропиткой по влагоемкости в последнюю очередь, терморазложение соединений металлов проводят после каждой пропитки либо в инертной среде при температуре 400-550°С с последующим восстановлением водородом при температуре 300-350°С, либо в кислородной среде при температуре 400-550°С с последующим восстановлением водородом, либо непосредственно в среде водорода при температуре 300-350°С, при этом получают катализатор по п.1. 6. Способ по п.5, отличающийся тем, что носитель выбирают из группы: 7. Способ приготовления катализатора гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим переходные металлы, включает сушку, терморазложение до соответствующих оксидов, отличающийся тем, что катализатор формируют последовательным или одновременным осаждением гидрооксидов или карбонатов переходных металлов в присутствии стабилизирующего носителя с последующим старением в маточном растворе, фильтрацией и восстановлением водородом при температуре 300-350°С, при этом получают катализатор по п.1. 8. Способ по п.7, отличающийся тем, что стабилизирующий носитель выбирают из группы: ZrO2, СеО2, TiO2, углеродный материал. 9. Способ приготовления катализатора гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов, который является сложным композитом, содержащим переходные металлы, отличающийся тем, что катализатор формируют совместным сплавлением/разложением кристаллогидратов нитратов переходных металлов совместно со стабилизирующими добавками типа нитрат циркония, церия, алюминия или гидроксида алюминия при нагреве до температуры 300-350°С на воздухе с последующим восстановлением водородом при температуре 300-350°С, при этом получают катализатор по п.1. 10. Процесс гидродеоксигенации кислородсодержащих алифатических соединений типа карбоновых кислот, их эфиров и триглицеридов с использованием катализатора, отличающийся тем, что процесс проводят при давлении водорода менее 3,0 МПа, температуре 250-340°С в присутствии катализатора по любому из пп.1-4 или приготовленный по любому из пп.5-9.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -,
-, 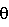 -,
-,  -Al2O3, SiO2, зауглероженный SiO2, углеродный носитель, ZrO2, CeO2, TiO2.
-Al2O3, SiO2, зауглероженный SiO2, углеродный носитель, ZrO2, CeO2, TiO2.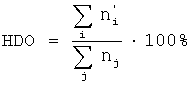 , где
, где 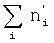 – суммарное количество молей не содержащих кислород продуктов реакции,
– суммарное количество молей не содержащих кислород продуктов реакции, 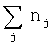 – суммарное количество молей всех продуктов реакции.
– суммарное количество молей всех продуктов реакции. -,
-, 